贫瘦煤Na2CO3溶液催化热解特性研究
王翠兰 金永传 赵 泽 赵 歌 臧志飞 梁 杰
(中国矿业大学(北京)化学与环境工程学院,10083 北京)
0 引 言
煤炭地下气化是将煤炭在地下煤层中进行有控制的燃烧,通过煤的化学作用和热作用产生H2,CO和CH4等可燃气体的过程,是集建井、采煤、转化工艺为一体的新一代化学采煤技术[1-4],该过程一般被分为煤热解和煤焦气化两个阶段。煤炭热解是在隔绝空气的情况下煤炭受热,发生化学变化和物理变化后失重的过程,大多数学者认为该过程机理的本质是自由基机理[5]。煤炭热解主要有两个变化阶段,首先是大分子结构(芳香类化合物和脂肪烃碳链)破坏解聚成自由基,这些自由基以新的状态进行排列并进行反应缩聚,最终形成挥发分。贫瘦煤煤化程度高,热解活性低,在热解过程中,添加催化剂可以降低热解反应的活化能,减少能量消耗,增加煤热解中有效气体组分[6]。
梁新星等[7-8]研究了煤炭地下催化气化工艺,采用10%(质量分数,下同)Ca(OH)2和10% Ca(OH)2+4%Na2CO3的水溶液随气化剂喷入地下气化模型实验炉,结果表明,煤气中的H2和CO稍有增加,但随气化剂带入的催化剂与煤层接触面较小,催化效果不明显。罗明等[9]实验对比发现K2CO3,Na2CO3,Ca(NO3)2,KCl和K2SO4这五种金属催化剂都可以有效降低煤热解温度,提高热解速率,且这五种催化剂的作用强度依次降低。吴洁等[10]研究发现,在热解过程中碱金属能使煤的结构更为紧密,阻止煤内部自身的一些大分子逸出,强化了半焦生成的过程,在此过程中碱金属催化剂可以促进含氧官能团分解,增加烷烃产率。已报道的文献多采用碱金属钾盐和碱土金属钙盐作为煤热解的催化剂,但对钠盐催化剂的报道相对较鲜见。
因在地下催化气化过程中催化剂无法回收,必须采用活性适中、价格低廉、对地下环境无太大影响的催化剂,一般采用碱金属作为催化剂,因固态催化剂无法进入煤层,地下气化只能选择液态催化剂,又因气化剂喷入法的催化效果不明显,故本实验以质量分数为8%的Na2CO3溶液作为催化剂,采用高压压入法使煤块充分负载催化剂。
1 实验内容
1.1 煤样
本实验煤样采用陕西王斜矿生产的贫瘦煤。提前选取规则规整、煤质均匀的煤块,用切割机和直尺切割成尺寸为1 cm正方体的实验煤样,擦干净煤块表面上的粉末后进行煤质分析(见表1和表2)。

表1 煤样的元素分析和工业分析(%*)Table 1 Proximate and ultimate analyses of samples(%*)

表2 煤样的煤灰分析(%*)Table 2 Coal ash analysis of samples(%*)
1.2 实验设备
实验所用设备主要采用负载催化剂的高压反应釜和实验室自己研发的用于测量煤样最终失重率的热重分析仪。高压反应釜由釜体、釜盖、安全装置和压力表等部件组成。高压反应釜装置如图1所示。

1.3 实验方案
1.3.1 常规热解实验
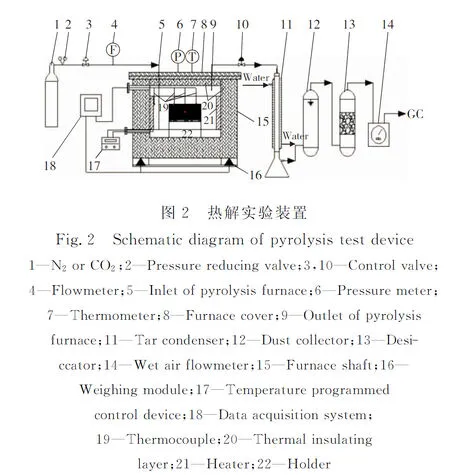
常规热解实验在常压和不同热解气氛(CO2和N2)下进行,将煤样装进热重分析仪(见图2)后,首先在不加热时通入气化剂一段时间将热解炉原有空气排出,并检查装置连接是否严密。打开程序升温控制仪,调节电流为10 mA,使热重分析仪温度逐步升高至800 ℃,恒温1 h。热解实验时,收集反应产物进行动力学分析,并将煤样在N2和CO2两种气氛下热解时产生的热解气体通过SWG200-1型烟气分析仪(德国,MRU公司)测定气体组分。
1.3.2 催化热解实验
催化剂为8%(质量分数)的Na2CO3溶液,通过浸渍法把催化剂负载到已制备好的尺寸为1 cm正方体的贫瘦煤煤块当中。具体的操作步骤为:将一定质量的无水Na2CO3溶解于对应质量的超纯水当中,配制成质量分数为8%的Na2CO3溶液,将配制好的Na2CO3溶液和尺寸为1 cm的正方体煤块放置在烧杯中,使溶液将煤块完全浸没,再放入高压反应釜中,将高压反应釜密封。然后向高压反应釜通入N2,并分别加压至1.0 MPa,1.5 MPa,2.0 MPa和2.5 MPa,达到需要压力后使釜内压力保持24 h,使得煤块充分负载催化剂。将经过负载处理的煤块分别记为Ⅰ,Ⅱ,Ⅲ和Ⅳ,并把煤样放置在干燥箱内干燥24 h。24 h后将煤块取出,通过称重得到负载过催化剂的煤块质量,进而分别计算出催化剂的负载量,各种煤块负载催化剂质量如表3所示。
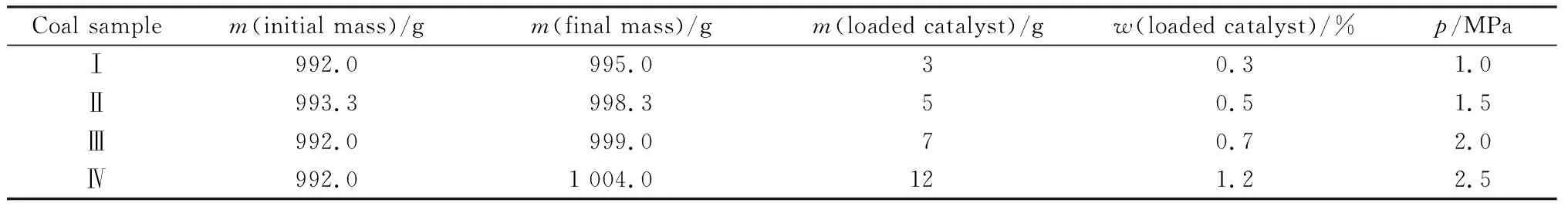
表3 煤样负载催化剂的质量Table 3 Catalyst quality loaded by coal samples
催化剂负载操作结束后,分别将负载过催化剂的煤块Ⅰ,Ⅱ,Ⅲ和Ⅳ放入热重分析仪中,通入N2作为载气,设置加热终温为800 ℃,在常压下进行热解实验,煤块内部升温速率控制曲线如图3所示,并用热电偶记录相关温度数据。热解系统可以得到贫瘦煤的内外温度变化情况以及TG-DTG曲线,通过对其分析得到煤的催化热解特性。催化热解时产生的热解气体由气袋收集后通过烟气分析仪测定,得到热解气体的组分随温度的变化趋势。
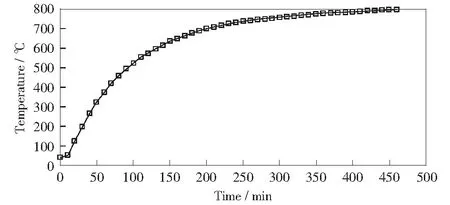
图3 在终温800 ℃ N2气氛下煤样的升温曲线Fig.3 Heating curve of samples in N2 atmosphere at final temperature 800 ℃
2 结果与讨论
2.1 原煤的常规热解反应
2.1.1 原煤的常规热解失重曲线
常压下,实验终温为800 ℃,分别以N2和CO2作为气化剂进行热解反应,得到的TG曲线如图4所示。

图4 在终温800 ℃ CO2和N2气氛下煤样的TG-DTG曲线Fig.4 TG-DTG curves of samples in CO2 and N2atmosphere at final temperature 800 ℃a—TG;b—DTG

2.1.2 原煤常规热解气体组分随温度的变化趋势
在800 ℃终温下,将煤样在N2和CO2两种气氛下热解时产生的热解气体通过烟气分析仪测定。热解气体体积分数随温度的变化曲线如图5所示。
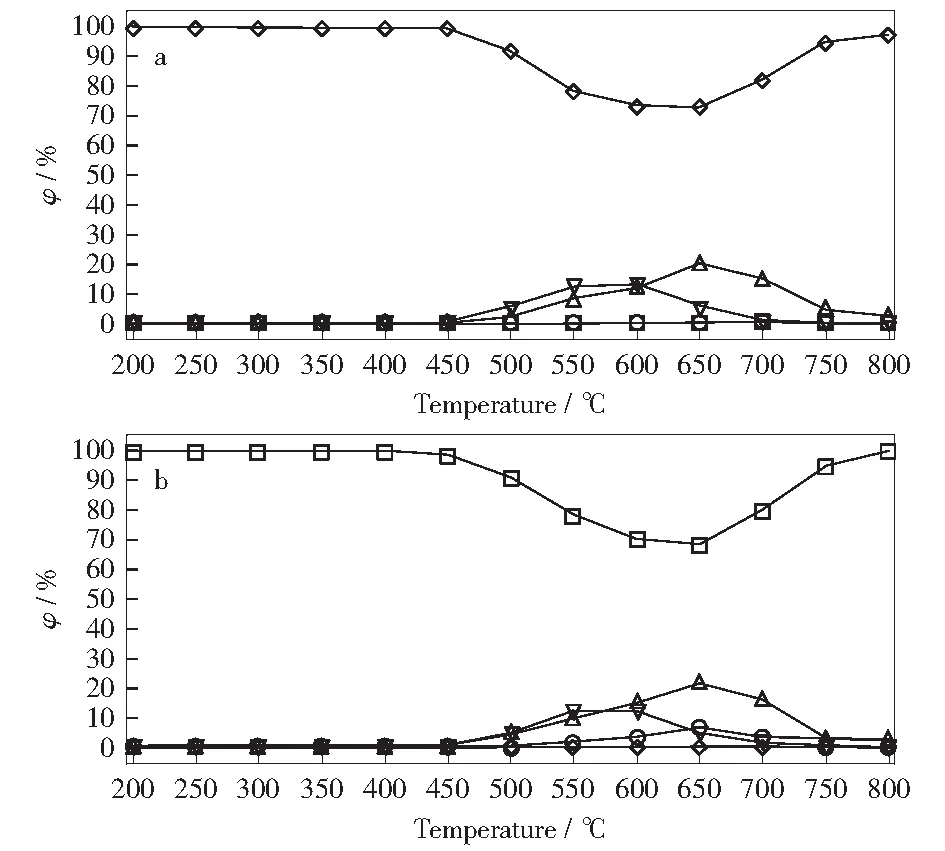
图5 在终温800 ℃ N2和CO2气氛下热解气体体积分数随温度的变化曲线Fig.5 Curves of volume fraction of pyrolysis gas changing with temperature in N2 and CO2 atmosphere at final temperature 800 ℃a—N2;b—CO2□—CO2;○—CO;△—H2;▽—CH4;◇—N2
由图5可知,气体组分中甲烷气体的产生过程主要分为三个阶段:第一阶段是温度在450 ℃以下,这个阶段产生甲烷的体积分数很少,这是由于在此阶段产生的甲烷气体主要是由煤样原本所吸附的甲烷气体经过加热从煤中逸出而得到的;第二阶段为450 ℃~600 ℃,在这个温度区间内产生的甲烷气体组分体积分数先逐渐增加,并在温度为600 ℃时达到最高峰;在温度为600 ℃之后,伴随着反应的进行,热解产生的甲烷气体组分随之减少,这是由于煤样中包含甲基的官能团随着反应进行而减少。在煤样进行热解时,热解反应产生甲烷气体的体积分数在N2气氛下较在CO2气氛下体积分数相对要大一些,产生此现象的主要原因是在高温环境下,CO2气体会与煤样中的C元素发生还原反应,吸收很多热量,从而使煤炭中生成的甲基键在CO2气氛下相比在N2气氛下煤炭中生成的甲基键要少一些。
煤样发生热解反应时在CO2气氛下较在N2气氛下产生氢气的体积分数要相对大一些,并且氢气气体组分在温度为450 ℃时才开始被检测出,在温度为650 ℃时热解产生氢气的体积分数达到最大值。热解反应产生氢气的体积分数较高可以表明,本实验所用贫瘦煤样中含有比较多的芳香族结构的官能团。
在CO2气氛下热解产生CO气体的体积分数较在N2气氛下热解产生CO气体的体积分数大一些,且温度较高时在CO2气氛下产生CO气体的体积分数明显增加,一定程度说明了热解反应生成CO气体需要较高的温度(超过600 ℃)。综上所述,在以CO2作为热解反应的气氛时,必须保持比较高的热解温度才能进一步提高热解反应产生CO气体的体积分数。
2.1.3 原煤的常规热解动力学分析
煤样在第一阶段进行热解反应时,由于温度较低基本没有发生反应。由煤样失重的TG曲线可以看出,最开始时失重TG曲线比较平缓,而当温度不断上升到一定点后,煤样开始快速失重,进行热解反应,而达到终温反应结束时,其TG曲线基本不再变化,此时的失重可以忽略不计。针对终温为800 ℃的热解反应,动力学分析数据处理时选取了煤样开始发生失重至反应结束这一温度区间的部分(即选择温度为350 ℃~800 ℃)研究动力学参数,主要分析第二阶段中温反应区和第三阶段高温反应区。因此,动力学参数处理分成第Ⅰ阶段(350 ℃~650 ℃)和第Ⅱ阶段(650 ℃~800 ℃)。
学者们通过丰富的理论假设和实际实验,提出了很多用于分析煤炭热解的动力学模型,包括均相模型、修正体积模型和混合模型等。本实验采用混合模型[15-18]对王斜矿贫瘦煤的热解进行反应动力学研究。混合模型模拟煤气化过程既结合了相关参数的实际意义和理论联系,也考虑了相关经验。其反应速率表达式如式(1)~式(3)所示:

(1)
(2)
ln ((dx/dt)/(1-x)m)=ln (A/β)-E/RT
(3)
式中:x为煤样转化率;t为时间,s;k为速率常数;m为反应级数,m=2;β为升温速率,K/min;E为活化能,kJ/mol;R为气体摩尔常数,8.314 J/(mol·K);T为热力学温度,K;A为频率因子,s-1。
在800 ℃下,煤样在N2和CO2两种气氛下热解的反应动力学参数如表4所示。
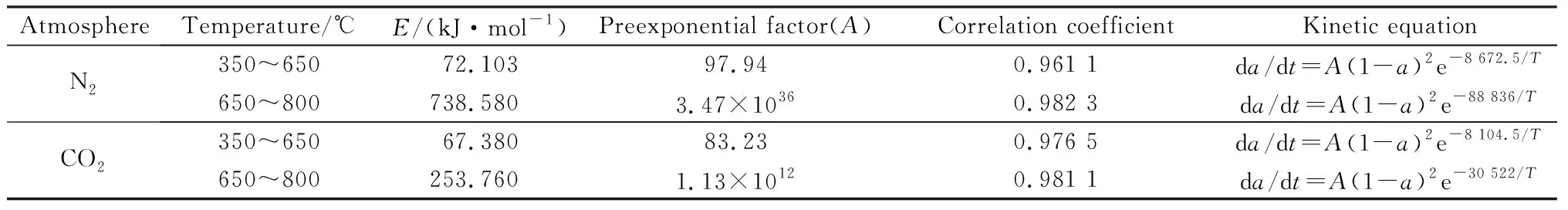
表4 在800 ℃下煤样的动力学参数Table 4 Kinetic parameters of samples at 800 ℃
由表4可知,煤样在实验终温为800 ℃的环境下分别通入N2和CO2两种气体进行热解,当在第Ⅰ阶段中温反应区时,CO2气氛下煤样的反应活化能(E)和指前因子(A)与在N2气氛下煤样的反应活化能(E)和指前因子(A)大小基本相同,并且都保持在较低水平上。而在第Ⅱ阶段高温反应区时,在N2气氛下煤样发生热解的反应活化能(E)和指前因子A较在CO2气氛下煤样的反应活化能(E)和指前因子(A)要大。
由于进行热解实验的煤颗粒尺寸为1 cm的正方体,颗粒表面温度与中心温度会有一定差别,颗粒中心的热解组分经过扩散到达颗粒表面。因此,大颗粒煤热解过程存在热质逆向传递的影响,所得到的动力参数是宏观动力学参数,一般适用于粒径与实验粒径相当的煤颗粒热解。
2.2 负载催化剂煤样的热解反应
2.2.1 煤样的催化热解失重曲线
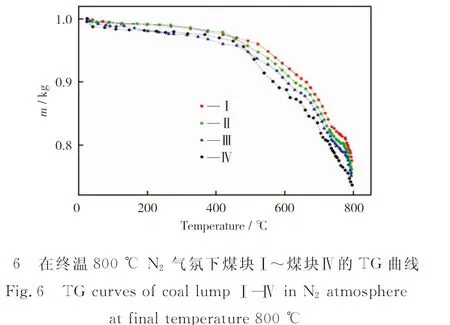
在终温800 ℃,N2气氛下,负载催化剂煤块Ⅰ~煤块Ⅳ的TG曲线如图6所示。由图6可知,在500 ℃左右煤块Ⅰ热解开始出现大幅失重现象,且煤块Ⅰ最终的失重率比原煤热解的失重率大1%,煤块Ⅰ的热解失重率为23%。煤块Ⅱ热解开始出现大幅度失重现象的温度在450 ℃左右,并且煤块Ⅱ的最终失重率比煤块Ⅰ的热解失重率大1%,煤块Ⅱ的热解失重率为24%。煤块Ⅲ的最终失重率比煤块Ⅱ的热解失重率大1%,煤块Ⅲ的热解失重率为25%。煤块Ⅳ的最终失重率比煤块Ⅲ的热解失重率要大2%,煤块Ⅳ的热解失重率为27%。负载过催化剂的煤样较原煤发生热解反应后最终的失重率要大1%~5%,且随着催化剂负载量的增加热解反应最终失重率也随之有所增加。
2.2.2 煤样的催化热解气体组分随温度的变化趋势
负载催化剂的煤块Ⅰ~煤块Ⅳ热解时热解气体体积分数随着温度的变化如图7所示。

图7 热解气体体积分数随煤块热解温度的变化曲线Fig.7 Curves of volume fraction of pyrolysis gas changing with coal pyrolysis temperaturea—Ⅰ;b—Ⅱ;c—Ⅲ;d—Ⅳ□—CO2;○—CO;△—H2;▽—CH4;◇—N2
由图7可知,同原煤相比,负载催化剂煤样发生热解反应产生的热解气体CH4的体积分数相差不大,煤块Ⅳ较其他煤样相比产生的CH4较多一些,产生气体组分中氢气的体积分数有明显增加,且氢气产生的温度也有所延后,产生气体组分中一氧化碳的体积分数有明显的增加。这是因为Na2CO3改变了煤的热解途径,促进氨基、酯和醚氧键的形成,通过水解/醇解反应生成更多的苯酚和醇类,促进了化学脱水反应发生,形成更多的烯烃化合物,通过强化脱羰和脱羧反应使CO的体积分数增加[19]。
2.2.3 煤样的催化热解动力学分析
在800 ℃终温N2气氛下煤块Ⅰ~煤块Ⅳ进行热解的反应动力学参数如表5所示。

表5 煤块Ⅰ~煤块Ⅳ热解动力学参数表Table 5 Pyrolysis kinetics parameters of coal lumpⅠ-Ⅳ
由表5可知,负载过催化剂的实验煤样的反应活化能和指前因子较原煤都相对低一些,根据负载催化剂质量的不同,反应活化能降低22%~76%。反应活化能越低表示发生反应需要的能量也越低,进而表明煤块在负载催化剂后发生热解反应的难度降低,这说明质量分数为8%的Na2CO3对煤样的热解反应有一定的催化作用。
图8所示为不同煤块在中高温区的反应活化能。由图8可以看出,原煤、煤块Ⅰ、煤块Ⅱ、煤块Ⅲ、煤块Ⅳ发生热解反应时在中温反应区的反应活化能分别为72.103 kJ/mol,56.050 kJ/mol,49.385 kJ/mol,44.310 kJ/mol,28.600 kJ/mol,而在高温反应区的反应活化能依次为738.58 kJ/mol,228.67 kJ/mol,225.34 kJ/mol,222.42 kJ/mol,177.15 kJ/mol。煤样热解的反应活化能由大到小依次为原煤、煤块Ⅰ、煤块Ⅱ、煤块Ⅲ、煤块Ⅳ。这说明催化剂对于煤样的热解反应过程具有催化作用,煤块负载催化剂的质量越多,催化效果也越强,煤样相对越容易进行热解反应。这是因为,碱金属化合物参与了煤炭反应,使其表面的碳骨架结构发生变化,碳氢键的键合力增强,碳键间的相互作用力减弱,降低了化学反应发生的难度,降低活化能,催化作用得以实现[20-21]。

图8 不同煤样在中高温区的反应活化能Fig.8 Activation energy of different coal samples in middle and high temperature zone
2.3 催化热解产物的测定
煤在高温热解后生成的液体产物中最主要的部分就是焦油,无催化剂时焦油产率平均质量分数为4.5%,有催化剂时焦油产率平均质量分数为3.8%。焦油主要包含苯、酚、烃三种物质。通过GCMS-2010测定实验煤样在常规热解及催化热解反应后生成的焦油成分的质量分数,结果见图9。

图9 负载不同量催化剂煤样热解焦油各组分的质量分数Fig.9 Mass fraction of each component of pyrolysis tar of coal samples loading different amounts of catalyst
由图9可以看出,负载过催化剂的煤样在进行热解后,产生的焦油中苯系物的质量分数增加,由常规热解的78.6%分别增加至煤块Ⅰ的81.21%、煤块Ⅱ的82.66%,煤块Ⅲ的84.78%和煤块Ⅳ的86.21%。而焦油中烃类的质量分数由16.41%变为煤块Ⅰ的5.48%、煤块Ⅱ的4.21%、煤块Ⅲ的9.78%和煤块Ⅳ的11.67%。焦油中酚类的质量分数由4.99%变为煤块Ⅰ的13.31%、煤块Ⅱ的13.13%、煤块Ⅲ的5.44%和煤块Ⅳ的2.12%。原因可能是,煤样负载的催化剂抑制了烃类物质的产生,但这种抑制作用也在随着煤样负载催化剂质量的增加而减弱。
3 结 论
1) 常规热解时,相同的终温条件下煤样在CO2气氛下的失重率较在N2气氛下的失重率大3%~5%,且反应活化能也相对较小。
2) 同原煤相比,负载催化剂煤样发生热解反应产生的热解气体CH4的体积分数相差不大,煤块Ⅳ较其他煤样CH4的体积分数要大一些;气体组分中氢气的体积分数有明显增加,且产生氢气的起始温度也有所延后;气体组分中一氧化碳的体积分数有明显增加。
3) 当煤样负载催化剂量比较少时,负载了催化剂的煤样热解产生的焦油中烃类的质量分数会有所降低,但当煤样负载催化剂的质量逐渐增加时,对煤块热解过程产生的焦油中烃类成分的抑制作用在减弱。
4) 负载催化剂的煤样发生热解反应后最终的失重率较原煤的失重率大1%~5%,说明质量分数为8%的Na2CO3催化剂对贫瘦煤热解反应有较为明显的催化效果,且催化效果随着负载催化剂质量增加而有所提高,具体表现为煤样热解反应活化能由大到小依次为原煤、煤块Ⅰ、煤块Ⅱ、煤块Ⅲ、煤块Ⅳ。

