sCD40L对高脂血症大鼠勃起功能的影响①
董龙信,陈大印,刘 莹,宋明欣,郭玉刚
(佳木斯大学附属第一医院泌尿外科,黑龙江 佳木斯 154003)
我们在ED的理解中,许多病理生理学的进展是通过使用动物模型而取得的。动物模型的研究可能助于阐明这些变化产生不同的阴茎血流动力学的基本机制。本研究采用高脂血症相关ED大鼠模型,探讨高脂血症内sCD40L及NOS变化对ED的影响。
高脂血症(hyperlipidemia,HLP)是一种代谢紊乱,其在心血管风险中起着重要作用。HLP被认为是引起ED重要的危险因素之一,HLP的严重程度与ED的患病率呈线性增加[1]。血液中脂质水平升高是对人体是有害的,因为脂质暴露在氧气中会进行氧化过程,这是一种连锁反应,有助于产生活性氧(ROS)。由于活性氧的产生而导致的氧化应激(OS)增加,似乎在高脂血症相关性ED中起着重要作用[2]。sCD40L(可溶性CD40配体)作为一种跨膜蛋白,在结构上与TNF-α相关,并在多种细胞类型中表达,包括B细胞、上皮细胞、成纤维细胞、内皮细胞(ECs)和血小板。CD40L和sCD40L的表现出促炎性和促凝作用,是炎症反应中细胞信息通道的关键介质[3]。sCD40L通过其受体CD40连接到循环单核细胞,从而促进它们与血管内皮细胞的黏附。在一些内皮细胞障碍相关疾病中,sCD40L水平升高,激活CD40 / CD40L通路可不断加剧炎症反应。NOS存在于平滑肌和内皮细胞上,在阴茎动脉血管平滑肌和海绵体窦平滑肌的松弛过程中起重要作用。本研究着重于高脂血症阴茎组织sCD40L含量的变化及其对内皮细胞的影响,然后探讨了其影响NOS活性是否导致勃起功能障碍的机制之一,为勃起功能障碍的诊断和治疗提供一个新的思路。
1 材料与方法
1.1 动物和实验设计
所有实验程序及过程遵守新冠肺炎防护政策,均遵循佳木斯大学动物管理条例,经黑龙江动物保护与利用委员会批准。雄性Wistar大鼠30只(8周龄,体重270~330g),置于标准温度(23±1)℃、湿度(60±10)%和12h的光/暗周期下保持温度。我们将大鼠随机分为两组:正常饮食组(A组)、高脂饮食组(B组)。
高脂饲料中胆固醇2%,猪油9%,蛋黄粉11%,胆酸钠1%和77%基础饲料混合配制而成,建立高脂血症动物模型,连续8周。对照组大鼠同时接受基础饲料喂养。
主要仪器设备:血清全自动生化检测仪;水合氯醛;sCD40L试剂盒、阴茎海绵体测压设备。大鼠sCD40L酶联免疫吸附测定(ELISA)试剂盒;盐酸阿扑吗啡注射液;NOS试剂盒。
血液检查:造模成功后分别于高脂饲料喂养的第2周及第4周末,采血测定TC、TG、LDL-C、HDL-C的含量,以检测血脂水平。
病理检查:在第2周和第4周结束时,动物被处死并解剖。取阴部动脉约1.5cm,进行病理检查、HE染色、光镜观察。
1.2 指标检测和方法
(1)阿扑吗啡(APO)实验:分别在第2周和第4周结束时,在A组和B组大鼠颈后皮下用80μg/kg剂量注射APO,观察半小时,记录大鼠勃起次数。(2)sCD40L含量及NOS活性浓度的测定:用免疫组织化学染色结果观察sCD40L表达,用酶联免疫吸附试验(ELISA)检测sCD40L含量及NOS活性。
1.3 统计学方法
2 结果
2.1 高脂血症大鼠模型的建立
正常饮食组(A组)动脉内膜内皮连完整,结构层次清晰,血管管腔无狭窄,无粥样斑块形成。见图1;高脂血症组(B组)动脉内皮完整性受损,结构层次欠清晰,管腔狭窄,内膜下形成斑块,斑块内有胆固醇晶体及炎性细胞浸润,见图2。
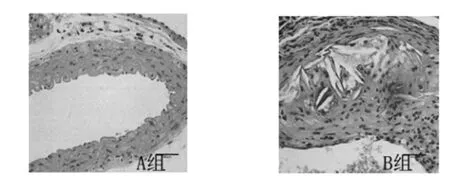
图1 A组阴部动脉壁组织结构(×100) 图2 B组阴部动脉壁组织结构(×100)
2.2 两组血脂情况
见表1。
表1 A组和B组的血脂情况
2.3 阿扑吗啡实验结果
见表2。

表2 A组和B组大鼠阴茎勃起次数、勃起率情况
2.4 大鼠阴茎组织内sCD40L的检测
sCD40L阳性染色呈蓝色颗粒状,主要位于血管内皮细胞,如图3~5。图像分析结果:与A组相比,B组海绵体细胞含量明显增加。

图3 A组染色(×400) 图4 B组2周染色(×400) 图5 B组4周染色(×400)
2.5 正常饮食组和高脂血症组大鼠阴茎组织中sCD40L含量、NOS活性浓度
见表3。

表3 两组sCD40L、NOS活性浓度
2.6 大鼠阴茎组织中sCD40L含量与NOS活性浓度的相关性分析
NOS活性浓度r值 -0.832(P<0.05)。通过分析数据得知大鼠海绵体sCD40L含量与NOS活性呈负相关。
3 讨论
HLP是一种常见的疾病,随着社会的不断进步,该类患者逐步呈现年轻化趋势,临床中可以发现在一些患者中可发生ED。ED是指在性交过程中持续性的、无法达到和维持足以使人满意的性行为的勃起,并伴有相应的生活及心理障碍。随着年龄的增长,ED变得更加常见,有研究表明至少有1200万年龄在40~79岁的美国人患有ED。其发生原因有很多,如神经源性、血管疾病、糖尿病、血管疾病、药物滥用以及睾酮缺乏有关[4],但高脂饮食的HLP是一种慢性疾病,可降低血流灌注压,改变动脉血流动力学,被认为是最重要的危险因素之一,该类疾病引起ED的原因主要是由于后期其导致脂质沉积,纤维组织增生,动脉内膜蜕变和钙化,动脉壁增厚变硬,导致阴茎海绵体供养动脉管腔不断狭窄,血流减少。
CD40作为受体并没有内在的信号转导能力。这是通过招募肿瘤坏死因子受体相关因子而发生的,值得注意的是, CD40L也以可溶性形式出现 sCD40L,从其膜结合的对应物中分离出来。在被激活的血小板和T细胞分泌后,可溶性分子保留了结合和激活上述受体的能力。在一些研究中, sCD40L是心血管事件的一个强有力的预测因子,sCD40L是一种血小板衍生配体,在粥样硬化发病机制和血栓形成并发症中发挥重要作用,驱动其他细胞因子、趋化因子、黏附分子、细胞外基质降解酶和细胞生存介质的表达,是炎症反应中细胞信息通道的关键介质[5]。sCD40L水平已被提出作为动脉粥样硬化血栓形成的生物标志物。与内皮细胞表面CD40结合,促进内皮细胞分泌ROS,使内皮细胞功能障碍。
阴茎勃起活动的关键过程是海绵体平滑肌松弛。这使得流向海绵体的血流增多,海绵体充满压迫了静脉,静脉流出减少。NO是参与阴茎勃起的主要神经递质[6]。
本实验研究发现HLP导致sCD40L增加,进而引起阴茎海绵体NOS活性及勃起率明显降低,血脂越高,NOS的下降越明显,勃起次数减少,炎症反应加剧,内皮细胞不断分泌活性氧,活性氧含量不断增加,一氧化氮产生减少,内皮细胞损伤,导师ED。这表明HLP在ED的发病机理中起着重要的作用,目前对sCD40L的研究领域有限,我们后续需进一步研究sCD40L表达调控的机制、是否受其他因素调控。

