硅酸钠对空气电池中镁阳极腐蚀行为及放电性能的影响研究
刘战祥,罗红秦,陈宇威,屈钧娥,2,王海人
(1.湖北大学材料科学与工程学院, 湖北 武汉 430062; 2.中国地质大学(武汉)纳米矿物材料及应用教育部工程研究中心, 湖北 武汉 430078)
0 引言
随着人类社会的高速发展,能源消耗急增,资源日趋短缺,因而亟需开发各种新的能源形式来满足人类发展的需要.金属空气电池作为一种特殊类型的燃料电池,其成本相对低廉、对环境友好、无污染、且可充分利用储量丰富的铝、镁、锌等金属资源,被作为一种新的能源方式而受到关注[1-2].
镁地壳资源丰富,是近年来受到关注的一类可用于空气电池阳极的材料.镁空气电池目前尚未大面积商业推广主要受限于镁活泼性太强,易自腐蚀,从而大大降低了电池的放电性能[3].有研究表明对镁进行合金化以及热处理,或者采用缓蚀型电解液添加剂均可在一定程度上抑制镁阳极的自腐蚀而提高电极的放电效率,从而改善电池的放电性能[4-12].通过电解液添加剂来减缓自腐蚀的方法相对来说更为简单高效,操作性更强,具有重要研究意义.如癸基葡萄糖苷、水溶性石墨烯、8-羟基喹啉、硝酸铈等电解质添加剂对以镁及其合金作为阳极的空气电池放电性能均有一定程度上的改善作用[8-11].
硅酸钠被发现对碱性含Cl-溶液中的AZ91D镁合金有显著的缓蚀作用[13-14],但有关硅酸钠应用于纯镁空气电池作为添加剂的研究少有报道.本研究以空气电池中纯镁阳极为研究对象,探讨硅酸钠对其在中性NaCl介质中腐蚀行为以及放电性能的影响规律及相关机制,结果表明硅酸钠是一种潜在可应用于镁空气电池提高放电效率的电解质添加剂.
1 实验部分
1.1 实验材料99.9% 纯度的工业纯镁箔片,使用SiC砂纸逐级打磨至1200#,用蒸馏水和酒精清洗后置于干燥器中备用,实验所用到的电解质溶液为25 ℃环境下3.5%NaCl溶液.
1.2 实验工程使用Corrtest 350电化学工作站在三电极体系中进行腐蚀电化学测试,镁为工作电极(1 cm2,WE),饱和甘汞电极(CE)为参比电极,Pt为对电极(CE). 极化曲线测试中,电位扫描范围为:Ecorr- 0.5 V ~Ecorr+ 0.5 V,扫描速率为1 mV/s;交流阻抗测试中,交流扰动振幅为5 mV,测试频率范围为10-1~105Hz,采用ZSimpWin 软件对阻抗数据进行拟合.采用武汉蓝电电池测试系统对所组装的镁空气电池进行放电测试,阴极为市售空气电池阴极材料,阳极为纯镁电极,测试电解质中添加缓蚀剂前后的放电电压-时间曲线,试样腐蚀形貌及表面元素由JSM6510LV型SEM-EDS观察测试获得.
2 结果与讨论
2.1 极化曲线镁在含有不同浓度Na2SiO3的NaCl溶液中测得的动电位极化曲线如图1所示,拟合得到的相关电化学参数如表1所示,可见随着硅酸钠的浓度增加,拟合得到的自腐蚀电流密度逐渐减小,当Na2SiO3浓度增加到0.01 mol/L时,电流密度由空白的426.63 μA·cm-2降低至45.05 μA·cm-2,缓蚀效率达到89.44%.这是因为随着硅酸钠溶液浓度升高,硅酸钠单体会聚合形成二聚物、三聚物、低聚物甚至多聚物的硅酸盐,不同类型的硅酸根阴离子与Mg2+结合生成的硅酸盐沉淀,其再进一步与Mg(OH)2膜结合,形成保护膜沉积于镁表面,从而大大降低了镁的腐蚀速率[13].此后,随着溶液中硅酸钠的继续增加,缓蚀效率增加幅度并不明显,因此0.01 mol·L-1硅酸钠的添加量是较为经济和理想的缓蚀浓度.

图1 镁电极在空白及含有Na2SiO3 的NaCl溶液中测得的动电位极化曲线

表1 Na2SiO3对NaCl电解液中镁电极极化曲线电化学参数的影响
2.2 电化学交流阻抗分析图2(a)为镁电极在空白及含有Na2SiO3的NaCl溶液中测得的Nyquist图.采用图2(b)所示等效电路图对EIS图谱进行拟合,其中RS为溶液电阻;Rct为电荷转移电阻,CPEdl为对应于双电层电容的常相位角元件;Rf为包括腐蚀产物及缓蚀剂反应物的表面膜层对应的膜电阻,相应于膜电容的常相位角原件为CPEf.n1和n2分别为对应于CPEdl和CPEf界面的弥散常数.由Nyquist图可见在低频区出现了感抗弧,这与电解质中活性物种在电极表面的吸附过程有关[15].由于镁在3.5%NaCl溶液中的腐蚀速度较快,低频区的感抗数据较为弥散,因此在拟合模型中未考虑感抗元件,仅对容抗弧部分进行拟合,得到的电化学参数如表2所示.

图2 镁电极在空白及含有Na2SiO3 的NaCl溶液中测得的Nyquist图(a)及相应的拟合等效电路(b)
由表2数据可见纯镁在电解液中的电荷转移电阻Rct和膜层电阻Rf均随着硅酸钠添加剂浓度的提高而增大,并且呈现与极化曲线一致的规律:当硅酸钠浓度达到0.01 mol·L-1浓度后,阻抗的增加幅度明显减缓.同时随着硅酸钠浓度增加,对应于膜层的双电层电容值明显减小,说明硅酸添加后,镁表面生成了硅酸镁保护膜,保护膜层的厚度增加,对镁起到了更好的保护作用,从而显著减缓了腐蚀.

表2 Na2SiO3对NaCl电解液中镁电极EIS拟合电化学参数的影响
2.3 浸泡腐蚀实验图3是镁阳极在空白与含有0.01 mol·L-1硅酸钠3.5%NaCl溶液中浸泡1 h后表面测得的形貌图以及EDS能谱图.可见,在空白组溶液中浸泡后的镁样品,其表面堆积了大量的 Mg(OH)2腐蚀产物;而加入了硅酸钠添加剂后,镁样品的腐蚀程度明显降低,镁基体表面打磨时留下的沟槽结构仍清晰可见,只有少部分面积遭受了较为严重的腐蚀.能谱分析结果表明添加有硅酸钠的溶液中,镁表面检测到硅元素的存在,有硅酸镁保护膜生成从而抑制了镁的腐蚀.
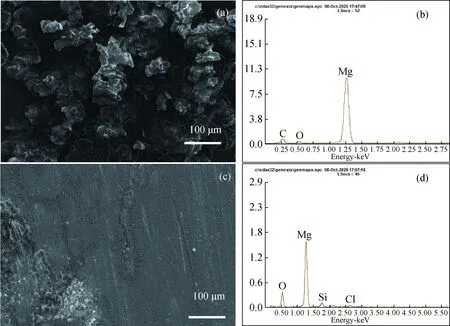
图3 镁电极于不同介质中浸泡1 h后测得的SEM形貌及表面元素EDS分析(a, b) 3.5% NaCl;(c, d) 3.5% NaCl+0.01 mol/L Na2SiO3
2.4 镁空气电池放电性能测试图4为镁空气电池测得的放电曲线.可以看到,随着放电电流从2 mA/cm2增加到4 mA/cm2,电池的输出电压呈现下降的趋势,这与大电流密度下,电极表面生成的腐蚀产物膜更厚,从而增加了电极表面电阻有关.在电池电解液中加入了0.01 mol/L Na2SiO3添加剂后,电池的输出电压略有降低(降低幅度小于50 mV),但放电平台区显著延长,2 mA/cm2以及4 mA/cm2放电电流密度下,放电平台时间分别增加了约11 h和6 h,同时平台区的电压也更为稳定. 本实验中添加有硅酸钠的电解质中镁空气电池的放电时间(2 mA/cm2,25.5 h)明显大于Deyab等[8]报道的相同电解质及纯镁阳极条件下添加十烷基葡糖苷后电池的放电时间(2 mA/cm2,15 h),说明硅酸钠是一种优异的镁空气电池电解质添加剂.

图4 不同放电电流密度下于3.5% NaCl以及3.5% NaCl+0.01 mol/L Na2SiO3电解质中测得的镁空气电池的放电曲线(a)2 mA/cm2;(b)4 mA/cm2
图5为在以镁为工作电极,铂为对电极,饱和甘汞电极为参比电极的三电极体系中,于4 mA/cm2恒电流极化条件下对镁进行恒电流阳极极化1 h后,取出样品并去除腐蚀产物后测得的SEM形貌图.相对于自然腐蚀状态(图3),在恒电流极化条件下,镁表面溶解程度显著增加.极化条件下镁在空白NaCl溶液中遭受的腐蚀更为严重,镁基体表面凹凸不平,而添加有0.01 mol/L Na2SiO3的NaCl溶液中得到的镁表面基体相对平整,腐蚀程度显著减轻,即在电池放电状态下,Na2SiO3添加剂也可以通过形成的硅酸镁/氢氧化镁复合保护膜而显著抑制镁阳极的自腐蚀,从而达到了大大提高镁阳极放电效率的效果.

图5 镁阳极于4 mA/cm2电流密度下、恒电流阳极极化1 h并去除腐蚀产物后测得的表面形貌(a):3.5% NaCl,1 h;(b)3.5% NaCl+0.01 mol/L NaSiO3 ,1 h
3 结论
Na2SiO3添加剂对中性NaCl介质中工业纯镁的腐蚀有明显的抑制效果,随着Na2SiO3的添加浓度从0.001 mol/L逐渐增加至0.01 mol/L,缓蚀效率由36.17%逐渐增加至90.5%,此后继续增大浓度,缓蚀效率并无显著增加.EDX分析证实溶液中的硅酸根与镁离子反应生成硅酸镁,与腐蚀产物氢氧化镁一起沉积于镁表面保护基体,从而抑制镁的自腐蚀析氢反应.
取0.01 mol/L的添加浓度,研究了Na2SiO3添加剂对空气电池中纯镁阳极的放电行为,结果表明Na2SiO3加入后放电电压虽然有所正移(正移幅度<50 mV),但可通过抑制镁的自腐蚀溶解,明显延长电池放电时间,2 mA/cm2以及4 mA/cm2放电电流密度下,放电平台时间分别增加了约11 h和6 h.

