利奈唑胺和万古霉素治疗MRSA引起的复杂皮肤和软组织感染的效果比较
袁慧姣 韩波
辽宁中医药大学附属医院检验科,沈阳 110032
过去20年中,广泛使用的广谱抗菌剂产生了严重的选择压力,导致临床上出现了诸多多耐药的革兰阳性菌感染病例。院内肺炎(nosocomial pneumonia,NP)和复杂皮肤和软组织感染(complex skin and soft tissue infections,cSSTIs)是最常见的感染。其中cSSTIs通常涉及深度软组织,需要静脉注射抗生素治疗,手术干预或两者兼而有之[1-4]。而金黄色葡萄球菌,尤其是耐甲氧西林金黄色葡萄球菌(methicillin-resistantStaphylococcusaureus,MRSA)是这些感染的主要原因[5-6]。
一直以来,万古霉素或替考拉宁等糖肽类药物是用于治疗MRSA感染患者的常见选择。尽管目前大多数菌株仍是万古霉素敏感株,但万古霉素中间体金黄色葡萄球菌(vancomycin-intermediateStaphylococcus aureus,VISA)菌株早已不鲜见。自2002年以来,国外已报道了多种耐万古霉素金黄色葡萄球菌(vancomycin-resistantStaphylococcus aureus,VRSA)菌株[7-9]。万古霉素治疗还存在其他局限性,如组织渗透力差,葡萄球菌中最小抑制浓度(MIC)增加等[10-11]。全球范围内菌株耐药性的增长趋势以及治疗抗生素引起的感染的高成本强调了对用于治疗革兰阳性感染新药剂的需求。利奈唑胺是第1个恶唑烷酮抗生素,能够抑制革兰阳性菌蛋白质合成的起始阶段[12]。临床试验证明,利奈唑胺在革兰阳性菌引起的cSSTIs[13]和NP[14]治疗中具有良好的耐受性和有效性。
本研究旨在评估利奈唑胺治疗因MRSA引起的cSSTIs患者的疗效和安全性。选择万古霉素作为比较,因为它是革兰阳性生物体感染的全球标准治疗药物。
1 资料与方法
1.1 一般资料 选取2017年3月至2018年3月本院治疗并发生cSSTIs的患者,共98例,最小年龄22岁,最大年龄55岁,年龄(45.35±8.1)岁。将所有患者采用随机数字表法分为利奈唑胺组与万古霉素组。利奈唑胺组患者49例,男性25例、女性24例,年龄(43.25±4.90)岁;万古霉素组患者49例,男性27例、女性22例,年龄(43.15±5.25)岁。纳入标准:(1)年龄大于18岁,小于65岁;(2)患者及其家属均知情并同意。排除标准:(1)孕产妇或哺乳期妇女;(2)对研究方案中任一药物过敏者;(3)肾功能不全者;(4)革兰阴性菌、真菌或分枝杆菌感染者。本研究经本院医学伦理委员会审核并批准。
1.2 治疗方法 每天对患者进行伤口检查并用生理盐水冲洗,使用康惠尔增强型透明贴[康乐保公司,国食药监械(进)字2008第2661180号],在治疗初期,检查和换药至少1次/d,可酌情增加次数。利奈唑胺组患者接受静脉注射利奈唑胺(Pfizer Pharmaceuticals LLC公司,H20160609)600 mg/次,2次/d,每次间隔12 h;万古霉素组患者接受静脉注射万古霉素[VIANEXS.A(PLANTC)公司,H20160456],根据患者体质量每次用量15 mg/kg,2次/d,每次间隔12 h。根据患者临床症状进行治疗7~14 d,并在停药后7 d随访。
1.3 检测指标 监测患者临床症状及不良反应并详细记录,于治疗前后采集血、痰、胸腹腔积液或伤口分泌物标本进行微生物学培养和药敏试验,用以排除革兰阴性菌、真菌或分枝杆菌感染者,统计治疗后的细菌清除率,细菌清除评价标准根据《抗菌药物临床应用指导原则(2015年版)》[15],将治疗结果分为无效、进步、显效和痊愈4个等级,根据显效和痊愈例数计算有效率。采用双抗体夹心-酶联免疫吸附测定(ELISA)检测患者血清白细胞介素-6(IL-6)、白细胞介素-1β(IL-1β)和肿瘤坏死因子-α(TNF-α)水平,采用流式细胞术检测患者外周血辅助性T细胞17(Th17)细胞比例。统计患者住院时间与静脉注射时间。
1.4 统计学方法 统计分析使用SPSS22.0专业软件进行,符合正态分布的计量数据以均数±标准差表示,组间比较采用独立样本t检验,组内比较采用配对t检验;计数数据采用百分率表示,采用χ2检验,P<0.05表示差异有统计学意义。
2 结 果
2.1 临床疗效 在停药时(使用最后1剂药物后24 h),利奈唑胺组的细菌清除率显著高于万古霉素组,但在随访时(停药后第7天)两组的细菌清除率相当,见表1。在停药时和随访时,利奈唑胺组患者与万古霉素组患者临床治愈率比较,差异均无统计学意义(均P>0.05),见表2。
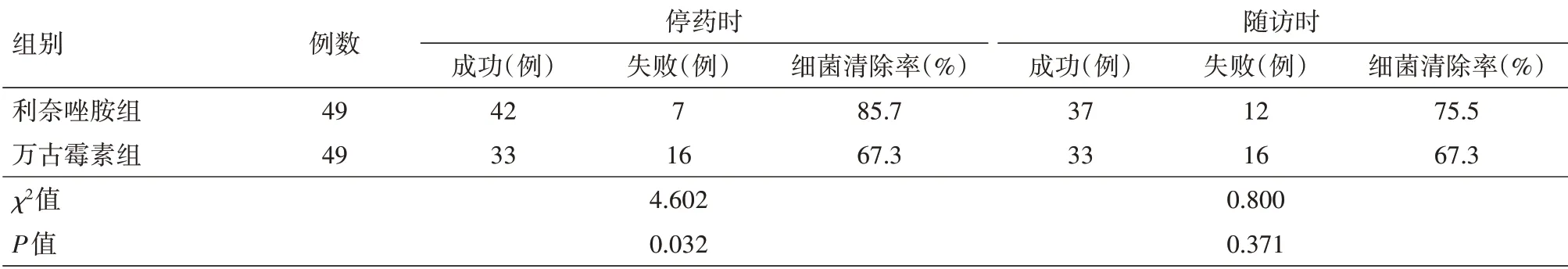
表1 两组复杂皮肤和软组织感染患者在停药时与随访时的细菌清除率比较

表2 两组复杂皮肤和软组织感染患者在停药时与随访时的临床治愈率比较
2.2 治疗前后血清IL-6、IL-1β和TNF-α的变化 与治疗前相比,治疗后两组患者血清促炎症因子IL-6、IL-1β和TNF-α水平均显著降低(均P<0.001),但治疗前后两组间比较差异均无统计学意义(均P>0.05),见表3。
表3 两组复杂皮肤和软组织感染患者治疗前后血清IL-6、IL-1β和TNF-α的变化比较

表3 两组复杂皮肤和软组织感染患者治疗前后血清IL-6、IL-1β和TNF-α的变化比较
注:IL-6为白细胞介素-6,IL-1β为白细胞介素-1β,TNF-α为肿瘤坏死因子-α;与本组治疗前相比,a P<0.001
组别利奈唑胺组万古霉素组t值P值例数49 49 IL-6(pg/ml)治疗前119.52±28.19 118.45±31.12 0.178 0.859治疗后5.48±0.54a 5.71±0.64a 1.923 0.057治疗后75.13±25.09a 75.24±23.09a 0.023 0.982 IL-1β(mg/L)治疗前46.38±5.04 45.21±7.04 0.946 0.347治疗后19.41±4.06a 18.21±5.06a 1.295 0.198 TNF-α(pg/ml)治疗前34.38±5.04 34.08±4.38 0.314 0.754
2.3 治疗前后患者外周血Th17占CD4+T细胞的比例变化 在治疗前、后时,利奈唑胺组患者外周血Th17占CD4+T细胞的比例分别为(3.30±0.40)%和(0.89±0.28)%,万古霉素组患者外周血Th17占CD4+T细胞的比例分别为(3.27±0.35)%和(0.90±0.25)%。两组患者治疗后Th17占CD4+T细胞的比例均显著降低(均P<0.001),组间比较差异均无统计学意义(均P>0.05)。
2.4 不良反应比较 利奈唑胺组患者不良反应总发生率显著低于万古霉素组患者,见表4。此外,值得注意的是万古霉素组更常发生治疗相关性肾毒性不良事件(少尿、肾功能衰竭、慢性肾功能衰竭、肾损害和血肌酐升高)。

表4 两组复杂皮肤和软组织感染患者不良反应情况比较[例(%)]
2.5 治疗成本比较 利奈唑胺组患者的住院时间为(7.6±0.5)d,万古霉素组患者为(8.9±0.6)d(t=11.651,P<0.001)。利奈唑胺组患者的静脉治疗时间为(5.6±0.3)d,万古霉素组患者为(10.4±0.7)d(t=44.119,P<0.001)。利奈唑胺组患者平均住院时间和静脉治疗时间均显著短于万古霉素组患者。
3 讨 论
中国MRSA感染的发病率很高,2005年从中国医院获得的临床分离株中MRSA的检出率为52%~93%[16]。耐多药的革兰阳性菌的出现,尤其是VISA的出现,突显了开发新的抗生素治疗的迫切。
利奈唑胺是治疗由革兰阳性菌感染的一个新选择。在由革兰阳性生物体引起的严重感染(包括肺炎和cSSTIs)的治疗中,利奈唑胺疗效良好,推荐剂量水平为每12 h 600 mg[17-18]。停药后,与药物有关的不良反应主要是短暂的和可逆的,且目前金黄色葡萄球菌分离株中对利奈唑胺的耐药性很低[19-20]。
本研究获得的主要数据支持使用利奈唑胺作为MRSA引起cSSTIs的有效治疗药物。通过对于利奈唑胺和万古霉素这两种药物的临床疗效、治疗成本和引起的不良反应的比较,我们认为利奈唑胺显示出与万古霉素相近的临床疗效、更低的治疗成本和更轻微的不良反应。
在停药时,每个方案人群中利奈唑胺的细菌清除率显著高于万古霉素。虽然在随防时,两组患者的细菌清除率差异无统计学意义,但利奈唑胺组的细菌清除患者数目仍高于万古霉素组。停药时观察到显著的微生物学结果,反映了利奈唑胺具有良好的组织渗透。此外,在停药时两组患者血清促炎症因子IL-6、IL-1β和TNF-α水平均显著降低(均P<0.001),外周血Th17占CD4+T细胞的比例也显著下降(P<0.001),且两组患者组间比较差异均无统计学意义(均P>0.05)。本研究结果表明,利奈唑胺在治疗由MRSA引起的cSSTIs是有效的,且具有有良好的耐受性。本研究中万古霉素和利奈唑胺的治疗效果相当,两组患者临床有效率差异无统计学意义(P>0.05)。
住院时间占严重感染治疗总费用的70%~90%,住院早期的费用往往最高[21]。在这项研究中,接受利奈唑胺治疗的患者住院时间和静脉注射时间显着短于接受万古霉素治疗的患者,这表明利奈唑胺治疗方案有利于降低医疗成本,节约医疗资源。
利奈唑胺组患者不良反应总发生率显著低于万古霉素组患者(P<0.001)。而且在利奈唑胺组中,不良事件的严重程度通常轻微至中度且可逆。且万古霉素组患者更常发生治疗相关性肾毒性不良事件(少尿、肾功能衰竭、慢性肾功能衰竭、肾损害和血肌酐升高)。
综上所述,利奈唑胺在治疗MRSA引起的cSSTIs疗效良好,安全可靠,且能够降低医疗成本,节约医疗资源,是万古霉素的有效替代药物。
利益冲突:作者已申明文章无相关利益冲突。

