ERAS对腹腔镜结直肠癌患者术后机体应激及炎性反应的影响
张焱辉,李靖锋,张 蛟,朱志贤,奚 惠
(1.靖江市中医院 普外科,江苏 靖江 214500;2.中国人民解放军东部战区总医院 外科,江苏 南京 210006)
结直肠癌是临床上常见的消化道恶性肿瘤,且呈逐年上升趋势[1]。目前,临床治疗结直肠癌最为常用的方法是手术根治,且向微创化发展,特别是随着腹腔镜技术的迅速发展,腹腔镜下结直肠癌根治术逐渐在该类患者的治疗中得到了推广应用,并取得了不错的临床效果[2]。然而毕竟手术为创伤性操作,围术期仍会引发一定的应激反应,加之该类患者身体机能以及心理承受能力往往较差,一定程度上影响手术治疗效果及预后恢复。因此,加强围术期护理意义重大。加速康复外科(ehanced recovery after surgery,ERAS)是指通过利用临床证实的各种有效方法避免或减少围术期可能出现的并发症及应激反应,使患者尽早康复[3]。本研究拟探究ERAS对腹腔镜结直肠癌患者术后机体应激反应及免疫功能的影响,现将结果报道如下。
1 资料与方法
1.1 一般资料 回顾性分析2016年6月~2019年12月靖江市中医院普外科收治的98例结直肠癌患者的临床资料。纳入标准[1]:①病理确诊为结直肠癌,肿瘤临床分期(TNM)≤Ⅲ期[根据美国癌症联合委员会(AJCC)第八版TNM肿瘤分期];②美国麻醉医师协会(ASA) 分级Ⅰ~>Ⅲ级;③患者临床资料完善,病情稳定,意识清醒,沟通及表达能力较好,依从性强,知情同意本次研究。排除标准[1,4]:①急诊手术、中转开腹、术中无法建立气腹者;②合并其他胃肠疾病或恶性肿瘤者;③合并心、肝、肾等严重异常者。根据临床资料显示的护理手段将患者分为ERAS组和常规对照组,各49例。两组年龄分布、性别比例、疾病类型、TNM分期、合并症等一般资料比较,差异均无统计学意义(P>0.05),具有可比性,见表1。

表1 两组患者一般资料比较
1.2 方法
1.2.1 手术方法 两组患者均采用腹腔镜结直肠癌根治手术。肠段游离和淋巴结清扫在腹腔镜下完成,肠段切除和(或)消化道重建经辅助小切口完成。
1.2.2 护理干预
1.2.2.1 常规对照组 给予围术期传统护理措施。①术前常规宣教;②术前1 d行机械性的肠道准备;③术前12 h禁食,6 h 禁水;④术前患者常规放置胃管及尿管,术后待肛门排气后拔除胃管,尿管术后留置5~7 d;⑤术后待肛门排气开始进流质食物,少量多次并根据患者适应情况逐渐过渡至普通食物;⑥术后下床活动根据患者意愿进行,一般术后次日开始活动;⑦术后常规静脉输液2 500~3 000 mL/d;⑧术后给予盐酸哌替啶等药物镇痛,必要时给予自控静脉镇痛泵干预。
1.2.2.2 ERAS组 在常规护理基础上实施ERAS护理。①成立ERAS小组,护士长担任ERAS小组组长,成员包括2名临床经验丰富的药师、2名麻醉师、2名外科医生及6名主管护师,确定ERAS护理方案及措施,并统一培训ERAS理论知识及标准化流程;②术前宣教:护师经统一培训后对手术方案确定的患者进行术前健康宣教,通过宣传册、微信公众平台信息推送(文字、图片和视频)向患者、患者家属介绍结直肠癌的诊疗路径、ERAS措施、手术镇痛方案、术后早期进食水的方法、术后早期下床活动指导及意义等,开展术前营养及呼吸系统筛查,帮助患者提前了解并正确认识术后疼痛,缓解患者的焦虑、恐惧、紧张,利于患者配合围手术期管理;③术前准备:术前给予合理营养支持,术前3 d给予无渣整蛋白型肠内营养制剂,术前1 d午夜饮12.5%麦芽糊精果糖饮品(素乾)800 mL,术前2 h饮400 mL,以改变患者空腹情况下的能量储备和保持碳水化合物的代谢,降低术后胰岛素抵抗,缓解术前口渴、饥饿和焦虑等,此外术前不行机械性肠道准备,不放置胃管及空肠营养管,仅置尿管,术前口服聚乙二醇电解质散剂清洁肠道,服后按摩腹部,适当行走,观察大便形状,密切检测患者生命体征和营养状态;④术中护理:术中注意保暖、温蒸馏水冲洗腹腔,术中严格控制液体入量,控制性补液1 L左右,减少引流管的使用;⑤镇痛护理:完善急性疼痛工作模式,要求小组相关成员评估患者疼痛后及时反馈医生给予镇痛干预,一般术前30min超前镇痛管理,术后使用自控镇痛泵(PCA) 镇痛,硬膜外注入0.2%盐酸罗哌卡因,且需向患者及家属详细介绍镇痛使用情况及不良反应,提高对不良反应发生的预见性,避免发生严重并发症;⑥术后护理:术后12 h内禁食不禁饮,术后第1天进清流质食物,排气后进半流质食物,术后24~48 h给予抗生素,48 h后拔除镇痛泵、尿管,术后第5天根据患者伤口愈合情况拔除引流管,术后12 h在小组医师或护师指导下适当进行屈膝、翻身、坐立等床上活动,并对患者按摩、叩背、协助排痰,术后次日即鼓励患者下床活动并自行排便。
1.3 观察指标 记录并比较两组患者胃肠功能恢复时间、首次排气时间、首次下床活动时间、术后住院时间,此外观察并比较两组术后并发症发生情况,包括吻合口瘘、切口感染及尿潴留等,并比较术前及术后3 d炎症反应及免疫功能情况,其中炎症反应指标包括C-反应蛋白(CRP)、白细胞介素6(IL-6)及肿瘤坏死因子(TNF-α),免疫功能指标主要为T细胞表面标志物CD3+、CD4+、CD8+,均于清晨空腹抽取肘静脉分离血清完成检测,其中IL-6、TNF-α通过ELISA测定,CRP采用免疫比浊法测定,T细胞表面标志物通过Epics.XLⅡ型流式细胞仪检测[4]。
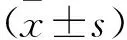
2 结果
2.1 两组术后恢复情况及并发症比较 ERAS组术后胃肠功能恢复时间、首次排气时间、首次下床活动时间、术后住院时间均少于常规对照组(P<0.05),两组术后主要并发症为切口感染及尿潴留,ERAS组术后并发症的发生率少于常规对照组(P<0.05)。见表2。
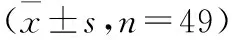
表2 两组患者术后恢复情况及并发症比较
2.2 两组手术前后炎症反应情况比较 两组患者术后3 d炎性指标水平均有不同程度增大,但与同期常规对照组比较,ERAS组CRP、IL-6、TNF-α水平更低,差异有统计学意义(P<0.05)。见表3。

表3 两组手术前后炎症反应情况比较
2.3 两组手术前后免疫功能比较 两组术后CD3+、CD4+和 CD4+/CD8+均较术前降低(P<0.05),但与同期常规对照组比较,ERAS组术后3 d CD3+、CD4+和 CD4+/CD8+水平更高(P<0.05)。见表4。
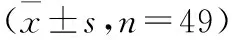
表4 两组手术前后免疫功能比较
3 讨论
目前临床上结直肠癌的治疗方案以根治性手术为主,且以腹腔镜手术为主[5-6]。本次所选受试者均采用腹腔镜手术完成结直肠癌的根治。然而手术本身就是一种应激源,手术创伤、术后疼痛等不可避免地影响患者的配合及预后,加之该类患者往往年龄较大、病程较长、缺乏对疾病及治疗方案的认识等更不耐受治疗[4,7]。因此,迫切需要行之有效的针对性干预措施以降低或减轻患者术后疼痛、并发症等不利影响,防止疾病术后迁延影响治疗。
ERAS概念最早是Kehlet在2001年提出的,主要的理念是在围术期通过各种有循证医学证据的优化措施来减少手术应激及并发症,缓解患者术后痛苦等以促进快速康复[8]。ERAS已在胃肠外科、骨科、肝胆外科、妇产科等多个外科领域得到应用并被证实[9-10]。本次试验选择将ERAS应用于围术期腹腔镜结直肠癌患者,结果显示围术期ERAS方案有效减少了患者术后胃肠功能恢复时间、首次排气时间、首次下床活动时间及术后住院时间,同时减少了切口感染等术后并发症的发生,提示围术期ERAS方案可提升腹腔镜结直肠癌患者的手术效果及安全性,与孙叶飞等[11]的研究结果一致。
手术的侵入性操作常造成机体出现明显炎症反应且会产生免疫抑制作用[8]。CRP是一种全身性炎症反应急性期的蛋白,可反映机体炎症状态,研究证实机体血清CRP水平与系统炎症反应呈显著正相关[9]。IL-6为活化的T细胞及成纤维细胞产生的淋巴因子,具有调节免疫应答和介导免疫功能的作用[10]。TNF-α为最早的一种炎症介质,具有促进其他免疫细胞因子的合成与释放的作用[11]。临床上常通过上述指标评价机体炎症反应[4]。本研究结果显示围术期ERAS方案对炎症反应影响更小,认为ERAS措施可帮助患者在手术期间及时调整身体状态使其适应手术,加强了机体修复创伤能力,导致的炎症反应相对较轻。此外手术创伤可引起强烈的应激反应,导致机体免疫功能发生变化[12]。T淋巴细胞亚群是参与机体免疫的重要因子,CD3+、CD4+和 CD4+/CD8+水平可反映评价机体细胞免疫功能状态[12]。本研究结果显示ERAS方案对患者细胞免疫功能影响小,提示ERAS方案中积极的术前宣教、合理的术前准备(减少置管及机械性肠道准备)、术后镇痛及护理等减轻了患者的心理和生理应激刺激,对机体细胞免疫功能影响小,加快恢复进程。
综上所述,围术期实施ERAS方案是一种安全、有效的干预模式。不过本次研究亦存在着一些不足之处,比如缺乏大样本量的研究使得所得结果说服力低,这有待后续研究继续深入。

