镂空α-氧化铁纳米带制备及其光催化性能研究
王晨鑫,陈美丽,田蒙奎,杨万亮
(贵州大学化学与化工学院,贵州贵阳550025)
纳米结构的α-Fe2O3是一种非常重要的金属氧化物材料,在多个领域都有广泛的应用[1],例如:电化学[2]、气敏[3]、光催化等领域[4]。同时,因为纳米结构的α-Fe2O3材料无毒、成本低、制备消耗少、稳定性较好、具有适宜的带隙(~2.1 eV)并且可以响应可见光,吸引了众多光催化领域研究人员的关注[5]。但是,因为α-Fe2O3颗粒容易团聚、无固定规则形貌、结晶度差等缺点限制了其应用,如何通过简单的方法制备出具有特殊形貌结构且具有良好结晶度的纳米α-Fe2O3成为研究的焦点之一。Wang等[6]采用酸性pH条件下水解FeCl3,成功制备了立方体、球形、片状、圆盘状、四面体聚集体、六角形结构和不规则形貌的α-Fe2O3。Ivanova等[7]通过溶胶-分子法将Fe2O3自组装在永久模板纳米纤维素(NCC)上,得到高度多孔结构的α-Fe2O3。Takashima等[8]成功合成了具有立方、六方双金字塔和平板形貌的赤铁矿(α-Fe2O3)纳米颗粒。Sun等[9]通过微波辅助热溶剂法制备了α-Fe2O3纳米片组装的分级中空介孔微球。 除此之外,纳米针[10]、纳米棒[11]、纳米线[12]、类哈密瓜状[13]、纳米片聚集的花状结构[14]等特殊结构的制备也已有报道。虽然已经有许多方法用来制备具有特殊形貌和结构的α-Fe2O3,却有着步骤较繁琐、不宜重复等缺点,限制了其实际应用。目前以较为廉价的三聚氰胺作为模板制备镂空α-Fe2O3纳米带的方法还鲜有报道。
笔者采用煅烧三聚氰胺硝酸铁超分子水凝胶前驱体的方法,制备出镂空纳米带α-Fe2O3。通过SEM、TEM、XRD、XPS、BET等对镂空α-Fe2O3纳米带的物理化学性质和微观结构进行了系统表征。详细测试了不同催化剂用量和H2O2用量对可见光催化降解RhB的影响,并考察了催化剂的光催化循环稳定性。
1 实验部分
1.1 试剂与仪器
试 剂:三 聚 氰 胺[C3N3(NH2)3]、九 水 硝 酸 铁[Fe(NO3)3·9H2O]、浓硝酸(纯度为68%)、罗丹明B(RhB)均为分析纯,实验用水为去离子水。
仪器:FA2104型电子分析天平;DZF6050型电热鼓风恒温干燥箱;TNX1200-50型箱式梯度炉;JHH-2A型恒温水浴锅;PLS-SXE300/300UV型氙灯(外照式);UV-6100S型紫外-可见分光光度计;JJ-1B型机械搅拌器;H1850型高速离心机。
1.2 实验方法
1.2.1 镂空α-Fe2O3纳米带(NB-α-Fe2O3)的制备
在三口烧瓶中加入一定量三聚氰胺和160 mL去离子水,在一定水浴温度下搅拌至溶解;取与三聚氰胺物质的量比为1∶1的九水硝酸铁,溶于20 mL去离子水中。将2 mL硝酸逐滴加入三口烧瓶中,搅拌10 min。将硝酸铁溶液加入三口烧瓶中,搅拌30 min。将三口烧瓶移出冷却。将得到的固体凝胶物质在恒温干燥箱中于60℃干燥72 h。将干燥样品放在不封闭的坩埚中,在550℃煅烧2 h,得到红色固体,命名为NB-α-Fe2O3(NB即nanobelts)。
1.2.2 样品表征与分析
采用SU8010型扫描电子显微镜、Tecnai G2 F20型场发射透射电镜对样品的微观形貌和粒径进行分析;采用K-Alpha型X射线光电子能谱仪和EMPYREAN型X射线粉末衍射分析仪对样品的化学性质进行分析;采用ASAP2460型比表面积测试仪对样品的比表面积、孔径和孔容进行分析;采用图像处理软件Image J进行粒径分布统计。
1.2.3 光催化性能测试
以300 W氙灯作为光源,使用420 nm滤波片滤去紫外光。将30 mg光催化剂与100 mL质量浓度为20 mg/L的RhB水溶液加入250 mL反应器中,在黑暗遮光条件下搅拌30 min,达到吸附-解吸平衡状态(所有测试都是在25℃恒温条件下进行,使用冷凝水循环保持温度)。滴加H2O2,开灯光照,每30 min从反应液中取出4 mL溶液,离心取上清液,用紫外-可见分光光度计测量反应前后溶液RhB的质量浓度,在波长为553 nm处检测相应的吸光度,根据吸光度与质量浓度的关系计算出对应的质量浓度。因为光催化降解满足伪一级动力学反应方程,故按照式(1)计算光催化降解RhB的反应速率常数(k)。

式中:ρ为每30 min取样的RhB质量浓度,mg/L;ρ0为光照前RhB的质量浓度,mg/L;t为取样时间,min。
2 结果与讨论
2.1 XRD分析
NB-α-Fe2O3的XRD谱图见图1。从图1看出,NB-α-Fe2O3的所有衍射峰都具有尖锐的峰型,说明NB-α-Fe2O3具有较好的结晶度[14]。同时位于24.1、33.1、35.6°处的3个衍射峰未发生明显偏移,分别与α-Fe2O3的(012)(104)(110)晶面对应,这与标准α-Fe2O3的特征峰位置吻合(标准卡片号JCPDS#87-1165),而且没有其他杂峰出现。综上所述,制备的NB-α-Fe2O3具有良好的纯度和结晶度。
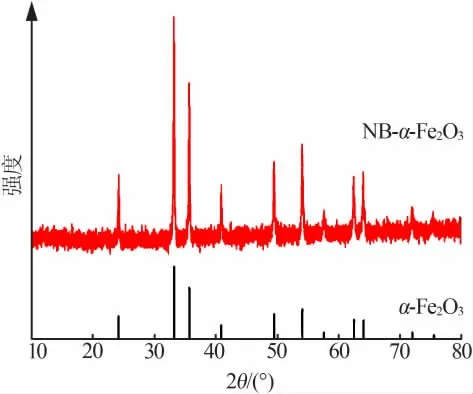
图1 NB-α-Fe2O3的XRD谱图Fig.1 XRD pattern of NB-α-Fe2O3
2.2 形貌与粒径分析
图2a、b分别为NB-α-Fe2O3煅烧前后的SEM照片。从图2a看出,三聚氰胺硝酸铁前驱体主要以棒状结构存在,棒状结构是形成镂空纳米带状α-Fe2O3的重要基础。从图2b看出,煅烧后的NB-α-Fe2O3可以明显地观察到大量规整的镂空带状结构。镂空结构的形成是因为三聚氰胺煅烧时产生大量的气体(三聚氰胺高温下分解产生)冲出,形成了镂空结构。带状结构形成的原因是Fe3+均匀分布在三聚氰胺表面,当三聚氰胺分解成气体逸出后,Fe3+在高温条件下形成α-Fe2O3,产生的颗粒沿着原三聚氰胺的棒状表面结构有序分布连接,形成了大量的带状镂空结构。图2c为NB-α-Fe2O3的SEM照片局部放大图,其中能明显地观察到由α-Fe2O3颗粒连接形成的镂空带状结构,样品的颗粒粒径为40~70 nm。为进一步研究样品的微观形貌,对NB-α-Fe2O3进行了HR-TEM表征。图2d、e分别为NB-α-Fe2O3的高分辨透射电镜照片与对应的局部放大图。从图2e看出,镂空带状结构是由α-Fe2O3颗粒相互连接形成的。在样品的HR-TEM中仍能观察到纳米α-Fe2O3颗粒直径主要分布在40~70 nm,这与图2f通过图像处理软件Image J统计的HR-TEM下α-Fe2O3颗粒粒径分布图的数据基本一致。上述表征结果表明,煅烧三聚氰胺硝酸铁超分子水凝胶法能够制备出纳米带状镂空α-Fe2O3,制备的NBα-Fe2O3属于纳米级材料(颗粒直径≤100 nm)。

图2 NB-α-Fe2O3煅烧前(a)和煅烧后(b)SEM照片;NB-α-Fe2O3的SEM照片局部放大图(c);NB-α-Fe2O3的HR-TEM照片(d)、局部放大图(e)和粒径分布图(f)Fig.2 SEMimage of NB-α-Fe2O3 before calcination(a)and after calcination(b),partial enlarged for SEM image(c),HR-TEM image(d),partial enlarged for HRTEM image(e)and size distribution of the NB-α-Fe2O3(f)
2.3 比表面积和孔径分布分析
采用BET测试确定NB-α-Fe2O3的比表面积、孔径和孔容等。图3a为NB-α-Fe2O3的N2吸附-脱附曲线,根据IUPAC分类可知吸附-脱附曲线属于H4型回滞环等温线,比表面积为3.19 m2/g。图3b为NB-α-Fe2O3的孔径分布曲线,可以看出样品的孔径分布主要集中在2~20 nm。但从样品的HR-TEM照片得知α-Fe2O3以实心颗粒形式存在,故NB-α-Fe2O3的孔道主要是以堆积孔的形式存在,所以存在很小的孔容(0.016 6 cm3/g)。

图3 NB-α-Fe2O3的N2吸附-脱附曲线(a)和孔径分布曲线(b)Fig.3 N2 adsorption-desorption isotherms(a)and pore size distribution of the NB-α-Fe2O3(b)
2.4 XPS分析
对NB-α-Fe2O3进行了XPS表征,结果见图4。图4a为NB-α-Fe2O3的XPS总图,可以清楚地观察到在529.27、710.20 eV处出现的峰分别是O 1s和Fe 2p主峰。在图4b中,NB-α-Fe2O3的O 1s峰可以分峰为两个峰,一个峰位于530.80 eV,对应于吸附在表面的水分子;另一个峰在529.30 eV,属于α-Fe2O3中的晶格氧原子。图4c中Fe 2p的XPS图由4个峰组成,710.30 eV的峰代表Fe 2p 3/2,724.10 eV的峰是Fe 2p 1/2,两个卫星峰分别在731.40、718.30 eV[15]。上述峰的出现进一步证明制备的材料是α-Fe2O3。
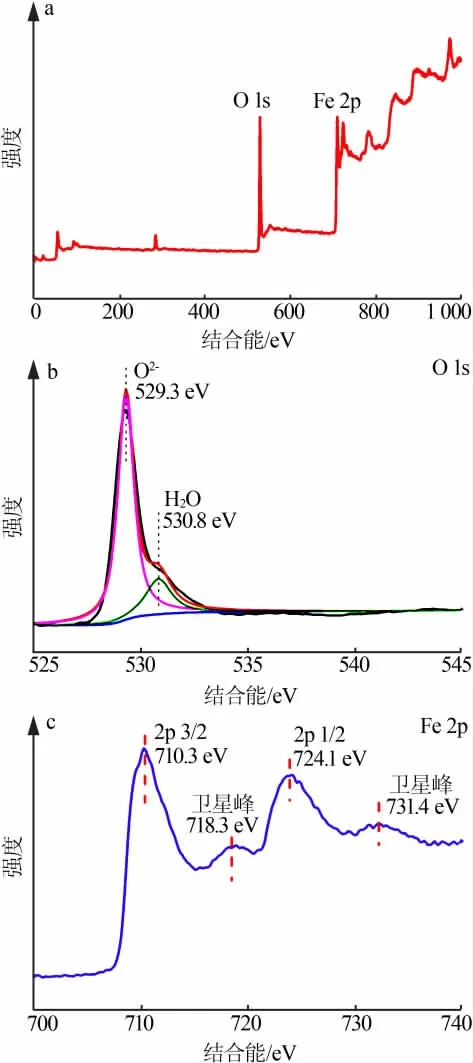
图4 NB-α-Fe2O3的XPS图:总图(a);O 1s(b);Fe 2p(c)Fig.4 XPS data for survey spectra(a),O 1s(b),Fe 2p regions of NB-α-Fe2O3(c)
2.5 NB-α-Fe2O3光催化性能分析
图5a、b分别为不同NB-α-Fe2O3用量光催化降解RhB的效果及相应的速率常数。其他条件:过氧化氢用量为0.3 mL,RhB质量浓度为20 mg/L,100 mL的RhB溶液。从图5a看出,催化剂用量为30 mg的降解速率远高于10 mg的降解速率。这是因为NB-α-Fe2O3在光照条件下催化氧化过氧化氢降解RhB,随着催化剂用量增加催化效果随之提升,降解效果明显增加。当催化剂用量进一步增加时,催化剂的浓度已经达到饱和,进一步增加催化剂用量不会明显提高降解速率。因此,选择NB-α-Fe2O3用量为30 mg。
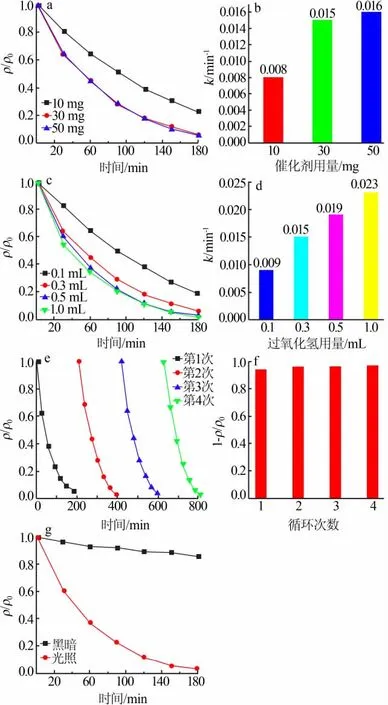
图5 不同NB-α-Fe2O3用量光催化降解RhB的效果(a)及相应的速率常数(b);不同H2O2用量光催化降解RhB的效果(c)及相应的速率常数(d);NB-α-Fe2O3光催化降解RhB的循环性能(e)及相应的降解效率(f);光照和黑暗遮光NB-α-Fe2O3降解RhB的效果(g)Fig.5 Photocatalytic degradation of RhB with different amount of NB-α-Fe2O3(a)and corresponding rate constant(b),effect of different amount of H2O2 on photocatalytic degradation of RhB(c)and corresponding rate constant(d),cyclic performance photocatalytic degradation of RhB(e)and corresponding degradation efficiency of NB-α-Fe2O3(f),effect of light and dark shading on RhB degradation by NB-α-Fe2O3(g)
图5c、d分别为不同H2O2用量光催化降低RhB的效果及相应的速率常数。其他条件:NB-α-Fe2O3用量为30 mg,RhB质量浓度为20 mg/L,100 mL的RhB溶液。从图5c、d看出,光催化降解RhB的速率随着H2O2用量的增加而增加。在RhB的催化降解过程中,H2O2的主要作用是生成氢氧自由基(·OH),因此过氧化氢用量增加时RhB的降解速率随之增加。但是当过氧化氢用量从0.5 mL增加到1.0 mL时,RhB的降解速率上升,增速却降低。这是因为H2O2产生的·OH具有氧化作用,但是因为NB-α-Fe2O3的用量是定值,所以游离的·OH重新结合生成H2O2,反而减少了·OH的数量[16],使光催化速率的增速减慢。从经济和降解速率两方面综合考虑,选择过氧化氢用量为0.5 mL。
通过对NB-α-Fe2O3在相同条件下连续进行4次光催化降解RhB循环反应,对其光催化循环稳定性进行了分析,结果见图5e、f。实验条件:NB-α-Fe2O3用量为30 mg,过氧化氢用量为0.5 mL,RhB质量浓度为20 mg/L,100 mL的RhB溶液。从图5e、f看出,4次循环之后光催化降解速率没有明显下降(第4次降解率为96.8%),说明制备的NB-α-Fe2O3催化剂具有较好的光催化稳定性。
图5g为光照和黑暗遮光NB-α-Fe2O3降解RhB的效果。从图5g看出,光照条件下NB-α-Fe2O3的降解效率远高于黑暗遮光条件下的降解效率,说明光照对反应起着重要作用,存在“光-Fenton反应”。
3 结论
使用煅烧凝胶前驱体法成功制备了镂空α-Fe2O3纳米带。SEM和TEM表征结果表明,制备的镂空纳米带由40~70 nm的α-Fe2O3纳米晶自组装形成;XRD和XPS表征结果表明,制备的样品属于α-Fe2O3,具有较好的结晶度和较高的纯度。光催化降解RhB时,适宜的催化剂用量为30 mg、H2O2用量为0.5 mL。得益于较好的结晶度和颗粒粒径,α-Fe2O3具有较好的光催化循环稳定性,光催化降解循环4次后,光催化降解率仍然达到96.8%。本研究为镂空纳米带状材料的制备提供了新的研究方法和思路。

