程序性死亡受体 1与肝癌相关性及程序性死亡受体 1单抗治疗肝癌疗效的Meta分析△
潘赐明,曹蓓苓,汪康,李长明,符晨阳,王育田,陈文慧
云南中医药大学基础医学院,昆明650500
研究显示,恶性肿瘤病死率第1位的是肺癌,其次为肝癌、结直肠癌、胃癌和胰腺癌,病死率前10位的恶性肿瘤占全部恶性肿瘤死亡的81.34%。目前肝癌的治疗方法主要为外科手术,但肝癌患者术后5年复发率高达70%,复发性肝癌患者二次手术后的5年生存率约为60%。针对免疫检查点的肿瘤免疫治疗成为了肝癌治疗的新途径,程序性死亡受体 1(programmed cell death 1,PDCD1,也称PD-1)在肿瘤免疫过程中发挥重要作用,可诱导肿瘤免疫抑制微环境,促进肿瘤细胞增殖和转移。PD-1是一种免疫共抑制受体,在T细胞上,PD-1通过与其配体程序性死亡受体配体1(programmed cell death 1 ligand 1,PDCD1LG1,也称PD-L1)和程序性死亡受体配体2(programmed cell death 1 ligand 2,PDCD1LG2,也称PD-L2)的相互作用抑制T细胞的活化。PD-1单抗在晚期肝癌治疗中取得了突破性进展,本研究采用Meta分析方法系统评价外周血PD-1与肝癌的相关性及PD-1单抗治疗肝癌的疗效及安全性,旨在为临床用药提供循证参考,现报道如下。
1 资料与方法
1.1 检索策略
本研究采用自由词的方法,通过计算机在CNKI、维普、万方、PubMed和CBM等数据库中检索相关文献。检索时间为建库至2020年10月30日。中文检索词为“肝癌”“原发性肝癌”“肝细胞肝癌”“肝细胞癌”“程序性死亡受体1”。英文检索词为“liver cancer”“primary liver cancer”“hepatocellular carcinoma”“programmed cell death 1”“PD-1”。
1.2 纳入和排除标准
纳入标准:①国内外公开发表的文献;②具有题目、作者、发表年份、发表期刊及发表时间等信息;③具有患者例数、年龄、性别等资料;④具有明确的干预措施;⑤具有结局指标,包括CD4PD-1、CD8PD-1、客观缓解率(objective response rate,ORR)、疾病控制率(disease control rate,DCR)等;⑥记录了相关不良事件。排除标准:①重复发表的文献;②非临床研究;③会议文献;④质量明显低劣的文献;⑤有明显错误、不规范的文献;⑥无法获取全文的文献。
1.3 纳入研究的偏倚风险评估
由3名研究者进行文献筛选和资料提取。由2名评价员按照非随机对照试验方法学评价指标(methodological index for non-randomized studies,MINORS)评价纳入研究的偏倚风险,每一条为0~2分,最高为16分。
1.4 统计学分析
采用StataMP 14.0软件对数据进行分析,CD4PD-1、CD8PD-1与肝癌相关性以及PD-1单抗治疗肝癌的ORR、DCR、不良反应发生率采用连续型变量Meta分析;效应量标准化均数差(standardized mean difference,SMD)和效应尺度(effect size,ES)均提供其95%置信区间(confidence interval,CI);采用CochraneQ
检验并结合I
定量判断异质性大小,I
>50%时,表明各研究间存在异质性,采用随机效应模型;反之,采用固定效应模型;绘制星状图进行敏感性分析,排除异质性较大的研究后,重新进行Meta分析,但本研究允许单臂Meta分析存在异质性。以P
<0.05为差异有统计学意义。2 结果
2.1 文献筛选结果
初步筛选相关文献179篇,其中中文文献34篇,英文文献145篇。通过Endnote排除重复文献后获取29篇,阅读摘要后剔除19篇,其中与研究内容不符9篇,综述和个案报道10篇。余10篇文献阅读全文后,剔除1篇无法获取原文的文献,最终纳入9篇文献。
2.2 纳入研究的基本信息及质量评价结果
最终纳入9篇文献,PD-1与肝癌相关性的研究5篇,其中英文文献1篇,中文文献4篇,肝癌组246例,健康组150例;PD-1单抗治疗肝癌的研究4篇,均为英文文献,接受PD-1单抗治疗的患者共852例。(表1、表2)

表1 PD- 1与肝癌相关性研究的基本信息及质量评价结果
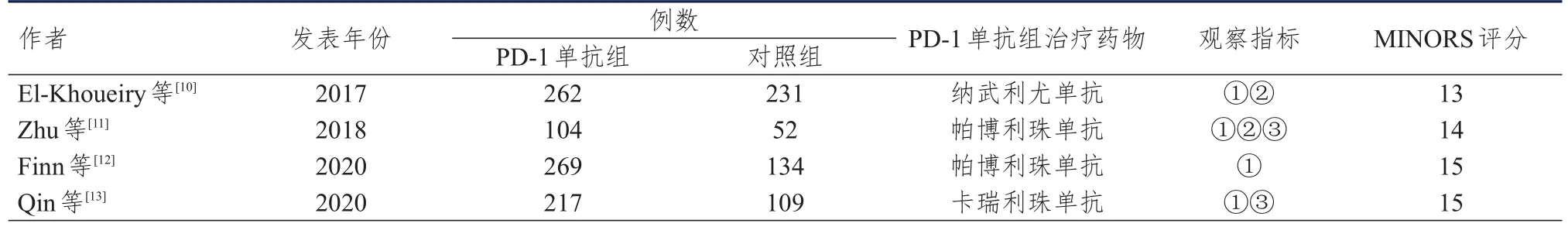
表2 PD- 1单抗治疗肝癌研究的基本信息及质量评价结果
2.3 Meta分析结果
2.3.1 CD 4PD- 1与肝癌相关性CD4PD-1与肝癌相关性的研究共3篇,异质性检验结果显示,各研究间存在显著异质性(I=98.40%,P<0.1),达到中度异质。因此继续进行敏感性分析考察造成异质的原因。结果显示,无任何一篇文献对本次Meta分析的结果造成很大干扰,意味着本研究具有较好的稳定性。采用随机效应模型进行Meta分析,结果显示,肝癌患者外周血中CD4PD-1的表达水平高于健康者,差异有统计学意义(SMD=3.06,95%CI:2.62~3.50,P<0.01)。(图1)
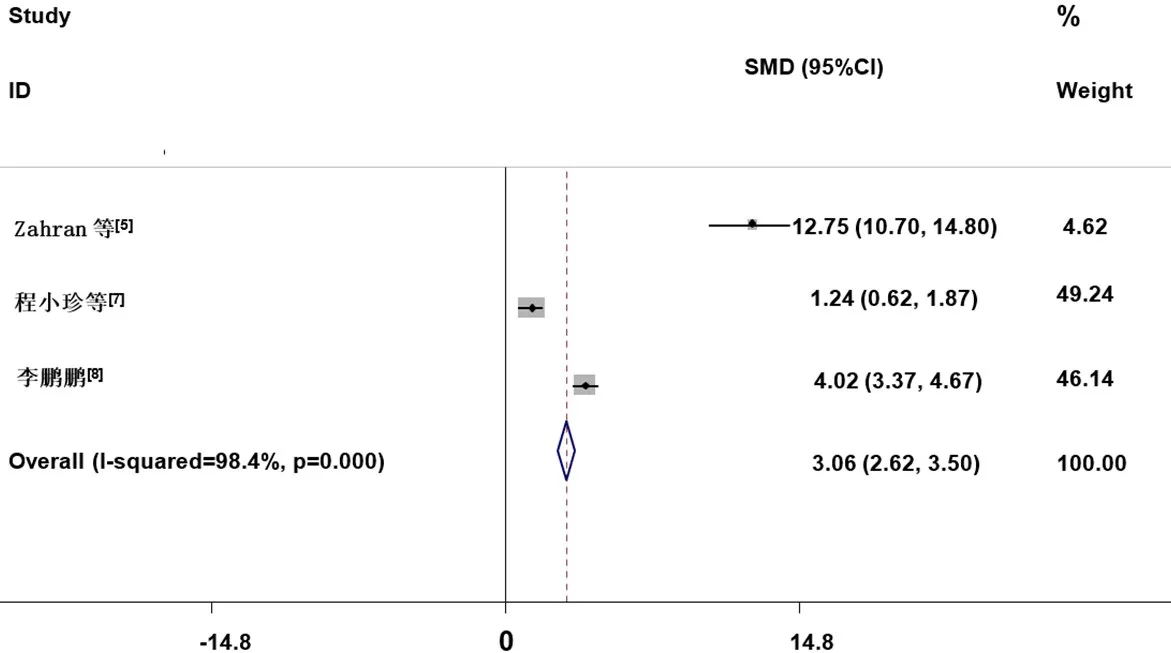
图1 CD 4+PD- 1与肝癌相关性的Meta分析森林图
2.3.2 CD 8PD- 1与肝癌相关性CD8PD-1与肝癌相关性的研究共5篇,异质性检验结果显示,各研究间存在显著异质性(I=98.40%,P<0.1),达到中度异质,因此继续进行敏感性分析考察造成异质的原因。结果显示,张敏娜的文献对本次Meta分析的结果造成很大干扰,排除之后重新分析。采用随机效应模型进行Meta分析,结果显示,肝癌患者外周血中CD8PD-1的表达水平高于健康者,差异有统计学意义(ES=7.05,95%CI:3.95~10.15,P<0.01)。(图2)
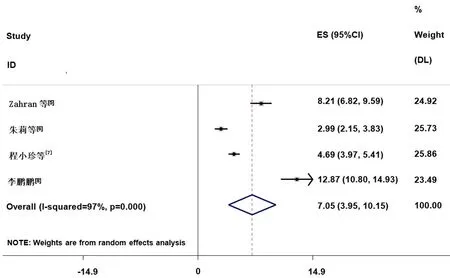
图2 CD 8+PD- 1与肝癌相关性的Meta分析森林图
2.3.3 ORR 4篇文献报道了PD-1单抗治疗肝癌的ORR,异质性检验结果显示,各研究间不存在显著异质性(I=0%,P>0.1),因此选择固定效应模型进行Meta分析。为了保证研究的准确性和稳定性,继续进行敏感性分析。结果显示,无任何一篇文献对本次Meta分析的结果造成很大干扰,意味着本研究具有较好的稳定性。Meta分析结果显示,PD-1单抗组肝癌患者的ORR高于对照组,但差异无统计学意义(ES=0.18,95%CI:0.15~0.20,P=0.053>0.05)。(图3)
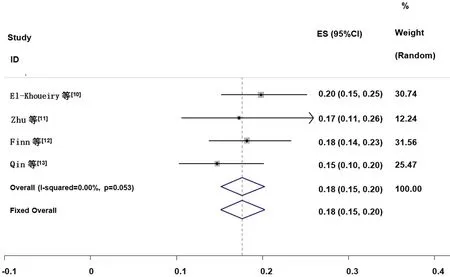
图3 PD- 1单抗组和对照组肝癌患者ORR的Meta分析森林图
2.3.4 DCR 2篇文献报道了PD-1单抗治疗肝癌的DCR,异质性检验结果显示,各研究间不存在显著异质性(I=0%,P>0.1),因此选择固定效应模型进行Meta分析。结果显示,PD-1单抗组肝癌患者的DCR高于对照组,差异有统计学意义(SMD=0.64,95%CI:0.59~0.69,P<0.05),提示PD-1单抗治疗肝癌显著有效。
2.3.5 相关不良事件2篇文献报道了PD-1单抗治疗肝癌的相关不良事件,异质性检验结果显示,各研究间不存在显著异质性(I=0%,P>0.1),因此选择固定效应模型进行Meta分析。结果显示,PD-1单抗组肝癌患者的不良反应发生率低于对照组,差异有统计学意义(SMD=0.24,95%CI:0.59~0.69,P<0.05),提示PD-1单抗治疗肝癌的不良反应较少。
3 讨论
随着生活方式和饮食习惯的改变,中国肝病的发病率逐年上升,居全部恶性肿瘤的第4位。目前肝癌的早期诊断缺少灵敏度和特异度较高的标志物,因此寻找肝癌标志物迫在眉睫。1992年PD-1在杂交瘤细胞中首先被发现,PD-1属于T细胞上的跨膜受体,在细胞凋亡过程中具有重要作用。2018年,有关PD-1抑制剂的多项基础与临床研究取得了显著成果,国家食品药品监督管理总局(China Food and Drug Administration,CFDA)批准PD-1/PD-L1抑制剂应用于多种类型的肿瘤。近年来,研究显示肝癌组织中PD-1阳性表达率高于癌旁组织,说明PD-1、PD-L1可能参与原发性肝癌的发生。
PD-1通路在肿瘤微环境的形成中发挥着关键作用。研究显示,PD-1在周围组织的效应T细胞中表达尤为强烈,在一些细胞因子的作用下,PD-1的配体PD-L1在肿瘤细胞的作用下上调,从而使PD-1与PD-L1结合,导致T细胞的攻击性减弱,进一步诱导T细胞凋亡,同时减少γ-干扰素、肿瘤坏死因子等分泌以及抑制颗粒酶和穿孔素产生,最终导致免疫耐受或逃逸。也有研究显示,不同治疗方式的患者中PD-1的表达水平不同。本研究显示,外周血中CD4PD-1、CD8PD-1的高表达均与肝癌有关(P<0.01)。提示肝癌患者外周血CD4PD-1、CD8PD-1表达明显,与健康者具有明显差异,值得进一步研究,为肝癌的早期诊断提供更多的证据。
帕博利珠单抗是目前适应证最广的PD-1抑制剂。纳武利尤单抗虽然是第二个美国食品药品管理局(Food and Drug Administration,FDA)批准用于肝细胞肝癌二线治疗的PD-1抑制剂,但帕博利珠单抗属于中国最先公布治疗肝癌的PD-1抑制剂。卡瑞利珠单抗是中国自主研发并在国内首个获批肝细胞肝癌适应证的PD-1抑制剂。本研究显示,PD-1单抗组肝癌患者的ORR高于对照组,但差异无统计学意义(ES=0.18,95%CI:0.15~0.20,P>0.05);PD-1单抗组肝癌患者的DCR高于对照组,差异有统计学意义(SMD=0.64,95%CI:0.59~0.69,P<0.05);PD-1单抗组肝癌患者的不良反应发生率低于对照组,差异有统计学意义(SMD=0.24,95%CI:0.59~0.69,P<0.05)。然而本研究也有不足之处,纳入文献较少,而且仅分析了ORR、DCR和不良反应发生率,未对总生存期和无进展生存期进行Meta分析,有待进一步研究。综上所述,外周血PD-1表达水平与肝癌有关,PD-1单抗对肝癌具有明显的治疗效果,亦具有较好的安全性。

