基于高内涵细胞影像分析系统的多种中药成分肝毒性筛选与评价
余 璇马 喆王 萌
(天津中医药大学中医药研究院 组分中药国家重点实验室,天津301617)
肝脏是人体药物代谢的重要器官,也是药源性损伤的主要靶器官之一[1]。中药在发挥药效的同时,一些有效成分或配伍中的其他成分会对肝脏产生一定的损害甚至造成药源性肝损伤——指药物及其活性代谢物通过脂质过氧化、细胞因子平衡失调而导致线粒体功能障碍,膜通透性改变,对细胞凋亡或坏死进行触发,从而引起肝细胞损伤[2⁃3]。
中药因其自身成分、作用机制复杂等因素,其药源性肝损伤评价成本较高、试验周期较长且结果争议较大[4⁃5]。近年来,应用于肝毒性研究评价的新方法和新技术不断发展,如肝细胞和亚细胞模型体外实验法,精密肝切片法,斑马鱼模型,以及基于基因组学、代谢组学和蛋白质组学的实验方法,但部分方法因仪器价格昂贵、技术要求较高等原因难以大范围的使用[6⁃7]。
高内涵影像分析(HCA)是一种在细胞水平上的多系统、多途径、多靶标的动态筛选技术,能够在保持细胞结构和功能完整性的前提下,利用不同的荧光染料同时检测化合物对细胞形态学、生化指标和细胞功能的影响,具有高通量、多指标、自动化、可定量等优点[8⁃9]。目前,HCA技术已用于肝毒性[10⁃11]、肾毒性[12⁃13]、心脏毒性[14]和神经毒性[15⁃16]的化合物筛选和研究。其中用于肝毒性检测的报道较多,常见的筛选细胞株主要有HepG2,HepaRG,人原代肝细胞等[10⁃11]。其中HepG2 易于培养,分化程度较高,所含的生物转化酶与人正常肝细胞具有同源性,是最为常用的药物评价筛选工具细胞[17]。课题组前期建立了HepG2 的HCA 肝毒性评价方法,测定丹红注射液、复方苦参注射液等四种临床常用中药注射液的肝毒性,并通过动物毒性试验对HCA 结果进行验证,得出该测定方法快速、简便、准确[18]。另外,正常人肝细胞L02 具有典型的肝细胞形态学特征,更适用于谷丙转氨酶(ALT)、谷草转氨酶(AST)和乳酸脱氢酶(LDH)渗漏率等多种肝损伤相关酶类的检测[19]。近年来,利用该细胞对中药成分进行HCA肝毒性筛选评价也可见报道[20]。有研究表明,同一成分在HepG2 和L02 上的敏感性不一致,如紫茎泽兰对L02 的肝毒性作用大于HepG2[21],而藤黄酸对HepG2 的毒性则大于L02[22]。另外,其抑制细胞增殖的作用机制也有一定区别。如补骨脂素对HepG2 和L02 均具有肝毒性但作用机制不一致,在L02 细胞上通过将细胞阻滞于S 期以抑制增殖,降低生存率,而在HepG2 上并无周期阻滞或诱导细胞凋亡的作用[23]。
本实验在之前工作的基础上,利用三种荧光探针建立并优化了基于L02 细胞的HCA 肝毒性评价方法。此外,选取2015 版《中国药典》 中记载有大毒的药物13 种,有毒的药物50 种,有小毒的药物35 种(表1),对除动物药材(蜈蚣、蕲蛇)和矿物药材(胆矾、红粉、砒石、雄黄、铅丹、密陀僧、朱砂)外的89 种植物药进行文献分析,根据报道确定了其中56 种可能具有潜在毒性的活性成分(表2)。通过建立的HCA 肝毒性检测方法分别在人源性肝癌细胞HepG2 和人正常肝细胞L02 上进行肝毒性快速评价实验,使用Hoechst 33342 荧光分子探针对细胞核进行染色,利用HCA 技术同时考察药物对细胞生存率和细胞核面积的影响,并将两种细胞株上的结果对比分析,以期对具有潜在肝毒性的药物进行更准确的早期筛选。

表1 《中国药典》 记录的肝毒性药物

表2 潜在肝毒性中药成分
1 材料
1.1 细胞株 人肝癌细胞HepG2、人正常肝细胞L02,均购自中国科学院典型培养物保藏委员会上海细胞库。
1.2 试剂 DMEM 培养基(批号1996842)、胰酶(批号1676922)购自美国Gibco 公司;胎牛血清(批号1658396)购自以色列Biological Industry 公司;青链霉素(批号1697550)购自美国HyClone 公司;Hoechst 33342(批号1801208)、Mito Tracker Deep Red FM(批 号1941460)、Rhodamine123(批号R⁃22420)荧光分子探针购自美国Invitrogen公司;DMSO 购自美国Sigma⁃Aldrich 公司。
1.3 仪器 IL⁃161HI CO2恒温培养箱(施都凯仪器设备有限公司);荧光倒置显微镜(日本Nikon 公司);Operetta高内涵筛选系统(美国PerkinElmer 公司)。
1.4 药物 阳性药碳酰氰⁃4⁃三氟甲氧基苯腙(FCCP)(批 号024M4003V)、对乙酰 氨基酚(APAP)(批 号061M0042V)购自美国Sigma⁃Aldrich 公司。56 种药品及其代码见表2,三七皂苷R1 购自天津一方科技有限公司,异常山碱、青藤碱、野百合碱购自上海源叶生物科技有限公司,其余药品均购自天津中新药业股份有限公司。
2 方法
2.1 细胞培养 人肝癌细胞HepG2 和人正常肝细胞L02均培养于含10%胎牛血清、1%青链霉素的DMEM 培养基中,在37 ℃、5% CO2培养箱中培养,取对数生长期的细胞用于实验。
2.2 药物配制 FCCP 用DMEM 完全培养基分别稀释至0.032、0.16、0.8、4、20、100 μmol/L,APAP 分别稀释至0.032、0.16、0.8、4、20、100 mmol/L。各中药活性成分经DMSO 溶解后,分别用DMEM 完全培养基稀释至浓度1.0×10-6mol/L。
2.3 L02 细胞HCA 多指标肝毒性筛选方法的建立 收集对数生长期细胞,L02 调整细胞浓度至4×105/mL,每孔加入100 μL 细胞悬液,于37 ℃,5% CO2培养24 h。吸弃培养基,加入以DMEM 完全培养基稀释的各浓度阳性药(100 μL/孔),每组3 个复孔,于37 ℃、5% CO2下培养24 h。之后向每孔加入分别含Hoechst 33342 1 μg/mL、Mito Tracker Deep Red FM 0.25 μg/mL、Rhodamine123 1 μg/mL的DMED 完全培养基100 μL,于37 ℃、5% CO2下避光培养30 min,用DMEM 漂洗2 次。采用HCA,选择Hoechst 33342、Mito Tracker Deep Red FM、Rhodamine123 三个通道对细胞进行影像学分析,计算细胞数量、细胞核面积、线粒体质量和线粒体膜电位4 项指标,考察阳性药对细胞核数量、形态以及线粒体功能的影响。
2.4 多种中药活性成分对HepG2 细胞和L02 细胞的肝毒性 在已建立的HCA 肝毒性检测方法上进行简化。收集对数生长期细胞,HepG2 和L02 的细胞培养方式同“2.3”项下。1×10-6mol/L 是在药物筛选中较常用的起效浓度[24⁃25],而阿霉素,顺铂等阳性药在该浓度下也已表现出较明显的毒性作用[12,26],故各中药活性成分以该浓度加入至各孔中,培养24 h,以Hoechst 33342 荧光探针进行染色,并对细胞进行影像学分析,计算细胞数量和细胞核面积,考察各中药成分对细胞核数量和形态的影响。
2.5 统计学分析 采用Harmony 3.0、Columbus 软件(美国Perkin Elmer公司)对HCA 图像进行分析。通过GraphPad Prism 8.0、SPSS 21.0 对数据进行统计分析,多组间比较采用方差分析,P<0.05 为差异无统计学意义。
3 结果
3.1 基于L02 细胞的HCA 肝毒性检测方法 基于L02 细胞的HCA 肝毒性检测结果见图1~2。FCCP 对细胞生存率的半数抑制剂量(IC50)为3.560 μmol/L。在0.032~100 μmol/L浓度范围内,可见细胞核面积随浓度升高有明显皱缩,线粒体质量明显升高,线粒体膜电位发生改变,这与FCCP 能够抑制线粒体呼吸链有关[27]。APAP 的IC50为5.389 mmol/L,与文献报道基本一致[28⁃30]。L02 细胞线粒体质量和线粒体膜电位均有显著下降。且细胞核面积在0.032~4 mmol/L 浓度范围内有肿大趋势,这是APAP 诱导细胞坏死和继发性坏死而引起细胞器肿胀的形态学特征[31]。FCCP 与APAP 在L02 细胞上的多种指标表明,该方法准确可靠,可以用于潜在肝毒性药物的快速筛选。
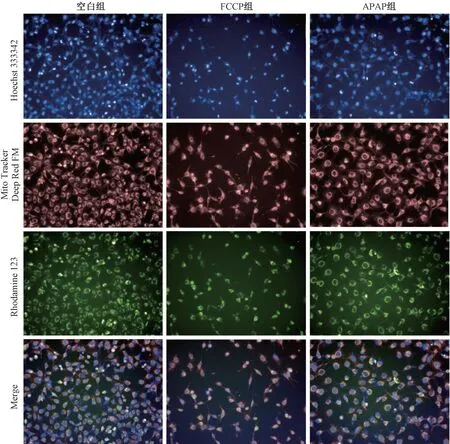
图1 阳性药对L02 细胞形态影响的HCA 代表图像

图2 FCCP 和APAP 对L02 细胞数目、线粒体质量、线粒体膜电位和细胞核面积的量效关系图(n=3)
3.2 中药成分肝细胞毒性快速筛选研究 本实验分别利用HepG2 和L02 的HCA 肝毒性检测方法,以最直观的细胞数目和细胞核面积为评价指标,分析56 种成分对两种细胞的生存率和细胞核面积的影响,HCA 形态学代表图见图3,采用origin 2019b 对实验结果绘制热图,见图4。在HepG2细胞上,各中药活性成分浓度1 μmol/L 时,A3、B3、A4、C3、D7、E4、E5、E6、E7、F1、F5、F6、G5、G6、H6 等15 种成分能够引起细胞数目的下降,与空白组相比有统计学差异(P<0.05,P<0.01),表明它们对HepG2 有一定的增殖抑制作用;A3、A4、C3、E4、G5 等5 个成分的细胞核面积与空白组相比均有不同程度的减小,差异具有统计学意义,表明它们能够引起HepG2 细胞核的皱缩。
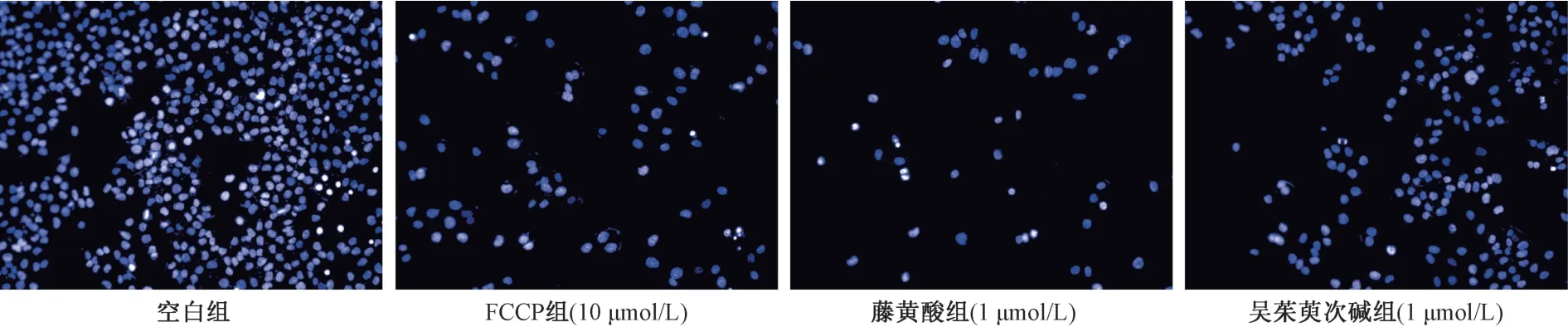
图3 两种中药活性成分对HepG2 细胞形态影响的HCA 代表图像

图4 各中药活性成分(1 μmol/L)对HepG2 细胞生存率(A)、L02 细胞生存率(B)、HepG2 细胞核面积(C)、L02 细胞核面积(D)的影响(n=3)
在L02 细胞上,A3、B3、C3、E7、E6、F1、F6、G5、G6、G7、H3、H6 等12 种成分会引起细胞数目的下降,与空白组相比差异有统计学意义(P<0.05,P<0.01),表明它们对L02 细胞有一定的毒性作用。另外,A3、B3、C3、E4、E5、E6、E7、F5、F6、G5、G6、G7、H6、H7 等14种成分能够引起L02 细胞核不同程度的皱缩。
综合分析各中药活性成分在HepG2 和L02 上的HCA 肝毒性筛选结果发现,在1 μmol/L 浓度下能导致两细胞株的细胞生存率均降低的药物有雷公藤红素(A3)、雷公藤甲素(B3)、雷公藤内酯酮(C3)、地高辛(E6)、杠柳次苷(E7)、鬼臼毒素(F1)、洋地黄毒苷(F6)、藤黄酸(G5)、西地兰(G6)和去乙酰毛花苷(H6)。在对细胞生存率分析的基础上,观察各成分细胞核形态的变化,发现L02 的细胞核经Hoechst 染色后核面积明显减小,皱缩程度剧烈,且均显著高于HepG2,表明在同一药物的影响下,L02 细胞可以更明显的体现出细胞核形态的变化,对肝毒性评价的结果具有更清晰的指示性。
此外,补骨脂素(G7)可同时导致L02 细胞生存率的降低和细胞核面积减小,吴茱萸碱(H3)和补骨脂酚(H7)则分别对L02 的细胞生存率和细胞核形态产生明显影响,且以上三种成分同一浓度下在HepG2 细胞上的生存率和细胞核形态均无显著变化。而吴茱萸次碱(A4)和杠柳毒苷(D7)能够导致HepG2 细胞生存率的降低。
4 讨论
本实验首先建立了HCA 肝毒性检测方法,FCCP 是一种氧化磷酸化的解偶联剂,通过破坏膜电位,抑制ATP 的生成,影响线粒体功能引起细胞损伤,产生肝毒性[32]。APAP 是临床常用的解热镇痛药,在代谢过程中,过量的高活性中间产物N⁃乙酰亚胺醌会与细胞蛋白尤其是线粒体蛋白中的巯基结合,引起氧化应激功能障碍导致肝细胞坏死[33]。实验分别选择了这两种不同肝毒性机理的药物作为阳性药,并通过HCA 分析其细胞数量、细胞核面积、线粒体质量和线粒体膜电位4 项指标的变化,表明两种阳性药对细胞核和线粒体功能均产生了一定的影响,与已报道的文献相符,检测方法快速可行。
利用已建立的HCA 肝毒性检测方法,对56 种中药活性成分进行肝毒性检测,有报道[25]表示细胞数目是药物肝毒性检测中最敏感的指标,在细胞凋亡早期即可检测到,适合作为药物毒性的筛选指标,而细胞核面积的变化是直观反应细胞调亡和坏死的形态学指标。因此,本实验选用细胞数目和细胞核面积,对具有潜在肝毒性的中药成分进行初步快速筛选。
从实验结果可以看出,对HepG2 和L02 细胞均有明显毒性的成分主要有雷公藤中所含的雷公藤甲素、雷公藤红素和雷公藤内酯酮,强心苷类成分洋地黄毒苷、西地兰、地高辛、去乙酰毛花苷和杠柳次苷,以及藤黄酸、鬼臼毒素等。有关雷公藤毒副作用的报道较为常见,主要有药物性肝炎、肝功能异常、肾衰竭等,其中肝毒性的发生率最高,雷公藤甲素、雷公藤红素和雷公藤内酯均是已被明确报道的主要毒性成分[34]。藤黄酸具有较强的抗肿瘤作用,有研究表明藤黄酸对人肝癌细胞株HepG2(IC50为5.29 μmol/L)的毒性较大,而对人正常肝细胞株L02 作用相对较弱(IC50为27.96 μmol/L)[22,35],与本文的研究结果一致。另外,强心苷类的治疗窗窄、毒性作用强[36],鬼臼毒素类[37]、吴茱萸碱[38]、吴茱萸次碱[39]、补骨脂素和补骨脂酚[40]等成分具有细胞毒性或抗肿瘤作用也均有报道。由于本实验使用了HepG2 和L02 两种肝细胞株且药物作用浓度较低(1×10-6mol/L),故马钱子碱、士的宁等有严重神经毒性的药物[41]以及中乌头碱、次乌头碱等对心肌细胞更为敏感[42⁃43]的有毒药物并未被筛选出来,也说明该方法具有一定的准确度和灵敏性。虽然HCA 检测方法能够从细胞水平上对药物进行筛选,并多层次、多靶点的深入探讨中药的作用机制,但其是否能够代表药物在体内的代谢过程以及其毒性实验结果与体内毒性相关性的综合分析仍有待探讨。
本实验筛选出的十种能同时导致HepG2 和L02 细胞生存率明显降低的药物中,其L02 上细胞核皱缩的程度均明显高于HepG2,说明L02 可以更明显的体现出细胞核形态的变化,对肝毒性评价的结果具有更清晰的指示性。因此,我们认为两种细胞株在肝毒性药物的筛选上有一定差异,其综合分析结果更具有代表性。本实验成功建立了HCA 肝毒性检测方法,并对56 种中药活性成分的肝毒性进行快速评价,初步构建了中药潜在肝毒性组分库。该方法操作简单,快速,稳定,特别适用于中药复杂化学体系的初步毒性筛选评价。

