有机-无机磷钨酸盐无溶剂催化氧化环己烯制己二酸
王璐璐,曾祥瑞,史庆伟,王海彦,王钰佳
(1. 中国石油大学(华东) 化学工程学院,山东 青岛 266580;2. 辽宁石油化工大学 石油化工学院,辽宁 抚顺 113001)
己二酸是合成尼龙-66和化工塑料的重要原料[1-2],工业上主要采用硝酸氧化法或环己烷两步氧化法合成[3]。上述方法的己二酸收率和选择性虽然较高,但是面临生产设备腐蚀较严重、硝酸氧化排放N2O严重破坏生态环境等问题[4-5]。近年来,催化剂联合H2O2直接氧化环己烯制己二酸工艺由于具有工艺路线短、清洁环保和投资成本低等优点而备受关注。Sato等[6]首次开发了以Na2WO4为催化剂、H2O2为氧化剂,直接催化氧化环己烯制己二酸的清洁生产工艺,为环己烯清洁催化制备己二酸的研究提供了以钨元素为活性中心的思路。随后,各种基于钨酸盐的均相催化剂相继得到了研究,如(H2en)3[P2W18O62]·6.48H2O[7]、WO(O2)2·2QOH[8]和H3PW12O40[9]等。这些研究结果表明,钨酸盐具有显著的环己烯氧化制己二酸的催化活性。但这些均相催化剂良好的水溶性导致了反应后产物难以提纯,催化剂回收困难等问题。为此,一些杂多酸盐,如Cs3PW12O40[10]、K3PW12O40[1]等非均相催化剂被开发出来以缓解上述问题,但在制备己二酸过程中添加的大量溶剂与产物之间的分离又成为新的问题。在多金属氧酸盐中添加醋酸[8]、盐酸[11]、酸性离子液体[12]等B酸助剂有助于提高己二酸收率,但该工艺存在离子液体或酸性溶剂浸出等问题。近年来,基于杂多酸的有机-无机杂化材料的合成及应用得到了广泛关注,该类材料与单一的杂多酸相比,具有催化活性高、助剂依赖性低等优点。
本工作以1-(3-磺丙基)吗啡啉为有机阳离子、磷钨酸(HPW)为无机阴离子,制备了有机-无机杂多酸盐,利用FTIR,TG,XRF,GC-MS,UVVis等方法考察了杂多酸盐的性能及催化环己烯氧化制己二酸的活性,并探讨了催化反应机理。
1 实验部分
1.1 主要试剂与仪器
N-甲基吗啡啉、HPW、环己烯、H2O2(30%(w))、N,N-二甲基甲酰胺(DMF)、无水乙醇、丙酮:分析纯,国药集团化学试剂有限公司;1,3-丙烷磺酸内酯:纯度99%(w),武汉中德远东精细化工有限公司;实验用水均为去离子水。
Spectrum One型傅里叶变换红外光谱仪:Perkin Elmer公司;Q600型热重-差热分析仪:TA公司;Agilent Cary 5000型紫外可见近红外分光光度计、Agilent 7890A/5975C型气质联用仪:安捷伦科技有限公司;S8 Tiger波长型X射线荧光光谱仪:Bruker AXS公司。
1.2 催化剂制备
将一定量1,3-丙烷磺酸内酯溶于丙酮中,在冰浴下用滴液漏斗向反应器中边搅拌边滴加N-甲基吗啡啉(1,3-丙烷磺酸内酯与N-甲基吗啡啉的摩尔比为1∶1),反应1 h后生成的白色固体用丙酮洗涤3次,80 ℃下干燥后得中间体1-(3-磺丙基)吗啡啉。
取一定量脱除结晶水后的HPW溶于去离子水中,然后加入1-(3-磺丙基)吗啡啉(1-(3-磺丙基)吗啡啉与HPW的摩尔比为3∶1),室温下反应24 h,将所得产物减压蒸馏脱水,将得到的固体置于真空干燥箱中80 ℃下干燥24 h,得灰绿色固体,即为1-(3-磺丙基)吗啡啉磷钨酸盐([C3SO3Hnhm]3PW12O40)。
N-甲基-N-丁基吗啡啉磷钨酸盐([Nbmm]3·PW12O40)参考本课题组前期工作[13]合成。
1.3 催化氧化反应
催化氧化环己烯制己二酸的反应在装有温度计和恒压滴液漏斗的三口烧瓶(100 mL)中进行。先将一定量催化剂与H2O2均匀混合,然后打开恒压滴液漏斗旋塞,缓慢滴加环己烯(50 mmol,5 mL),搅拌至反应设定时间后停止加热,冰水浴冷却、离心分离,将液体减压蒸馏,得到固体催化剂,剩余液体用GC-MS方法分析组成。将离心分离折出的白色固体用冷水洗涤后重结晶,再抽滤、烘干得到纯白色晶体即为己二酸,它的FTIR谱图和熔点(151~153 ℃)与标准试样一致。产物己二酸收率(Y)的计算见式(1)。

式中,m1为实际得到的己二酸晶体质量,g;m2为按照化学计量式计算的理论己二酸晶体质量,g。
1.4 催化剂结构表征
采用KBr压片法进行FTIR测试,扫描波数范围400~4 000 cm-1。
TG测试:氮气氛围,升温速率10 ℃/min,室温~700 ℃。
XRF测试:管功率4 kW,Rh靶,75 mm铍窗,采用硼酸包边固体制样法制样,best测试模式。
GC-MS测试:HP-5MS柱(30 m×250 μm×0.25 μm),进样口温度280 ℃,50 ℃保持2 min,然后以10 ℃/min升温至300 ℃保持5 min。
UV-Vis测试:测试试样在乙腈溶液中的吸光度,波长范围200~800 nm。
试样的酸强度测定方法[12]:以对硝基苯胺为指示剂,配制对硝基苯胺-乙腈溶液,待测试样配制成不同浓度的乙腈溶液。向待测试样中加入一定量对硝基苯胺-乙腈溶液,利用UV-Vis法测定上述溶液在最大吸收波长下的吸光度,由式(2)计算试样的Hammett酸函数(H0)。

式中,pKa为指示剂的解离常数,对硝基苯胺的pKa为0.99;xB为指示剂未被质子化部分的摩尔分数,%;xBH+为指示剂在溶剂中的质子化部分的摩尔分数,%。
2 结果与讨论
2.1 UV-Vis表征结果
钨系杂多化合物在紫外可见区有很强的吸收,通过UV-Vis表征,能够观察到过渡金属的d-d跃迁以及由电荷转移引起的其他跃迁。试样的UV-Vis谱图见图1。从图1可看出,试样均在200~400 nm范围内有吸收峰。其中在206 nm附近是O→P的吸收峰,而在265 nm附近出现的吸收峰是O2-W6+之间的金属电荷迁移[14]。在[C3SO3Hnhm]3PW12O40中206 nm处的吸收峰发生了蓝移,这表明离子液体和HPW阴离子杂化材料之间存在一定的相互作用。
试样在乙腈溶液中的H0见表1。
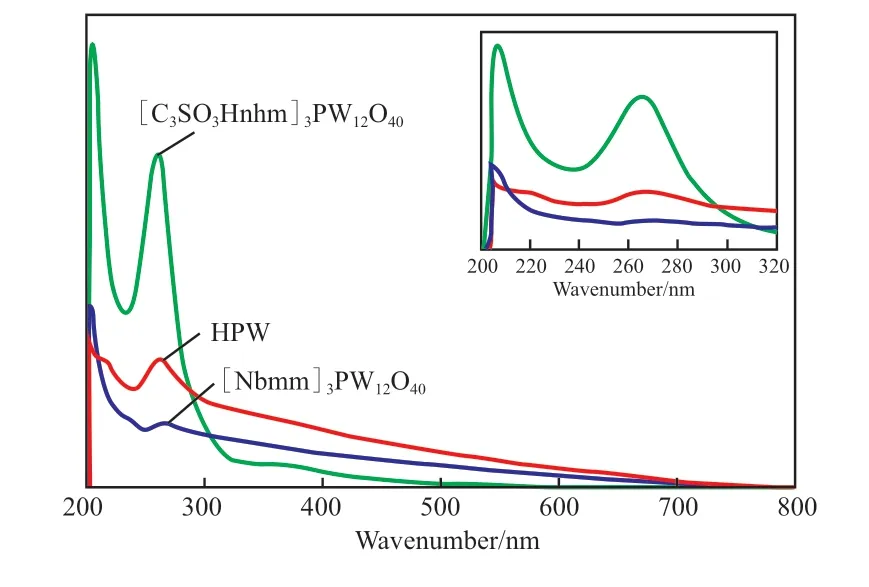
图1 试样的UV-Vis谱图Fig.1 UV-Vis spectra of the samples.

表1 试样的H0Table 1 Hammett-function(H0) of the samples
从表1可看出,随浓度的增大,试样的H0均减小;相同浓度下,不同试样的H0由大到小的顺序为:[Nbmm]3PW12O40>HPW>[C3SO3Hnhm]3PW12O40,说明在乙腈溶液中,相同浓度下[C3SO3Hnhm]3PW12O40的酸强度最大。
2.2 XRF表征结果
试样的XRF表征结果见表2。从表2可以看出,各元素含量的测试值与理论值基本相符,说明制备的试样与预期结构一致。[C3SO3Hnhm]3PW12O40重复催化使用6次后的元素含量与新鲜催化剂相比基本没有改变,说明[C3SO3Hnhm]3PW12O40具有较好的重复使用性。
2.3 催化剂的热稳定性
试样的TG曲线见图2。从图2可以看出,[C3SO3Hnhm]3PW12O40和[Nbmm]3PW12O40的热分解温度分别为250,380 ℃,这可能是由于磺酸基团的引入减弱了分子间作用力;升温至650 ℃后,二者的失重曲线基本稳定,且失重率分别达到18.36%和18.91%,说明它们的有机阳离子已基本分解完全。

表2 试样的XRF表征结果Table 2 XRF results of the samples

图2 试样的TG曲线Fig.2 TG curves of the samples.
2.4 催化剂的活性
不同催化剂氧化环己烯制己二酸的催化活性见图3。
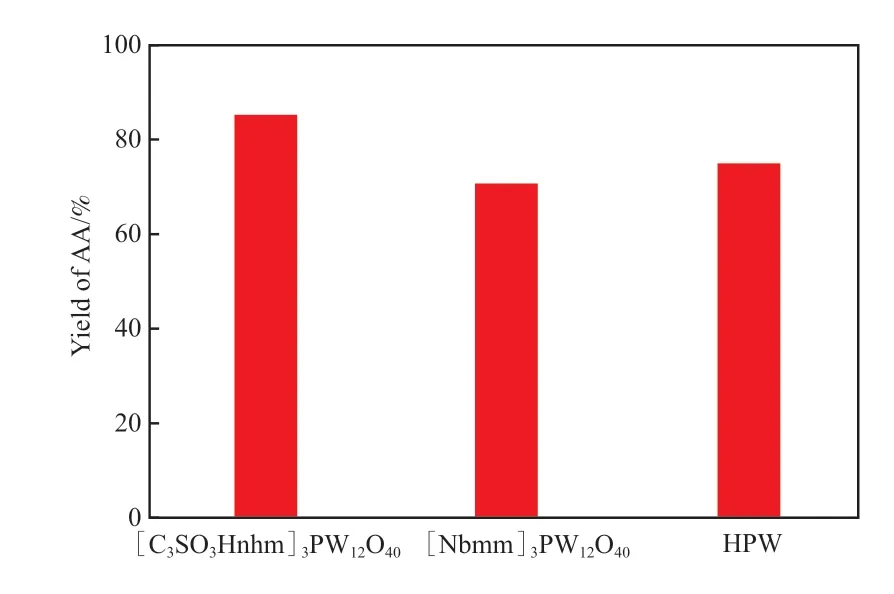
图3 催化剂的催化活性Fig.3 Catalytic activity of catalysts.
从图3可看出,三种催化剂的活性大小顺序为:[C3SO3Hnhm]3PW12O40>HPW>[Nbmm]3PW12O40,这与H0表示的酸强度结果一致,说明催化剂酸性对催化活性有一定影响。[C3SO3Hnhm]3PW12O40由于不含较强的自由基激发活性位点,保证了反应体系不会沿自由基路线反应,而是沿双键氧化路线进行[12,15],含有的磺酸基酸性位点能够活化水分子,并与中间产物环氧环己烷反应生成1,2-环己二醇,再进一步反应生成己二酸,这与王新国等[16]的研究结果基本一致。
2.5 反应条件的影响
反应条件对己二酸收率的影响见图4。从图4a可看出,随反应时间的延长,己二酸收率增大,当反应时间达10 h时,己二酸收率可达85.3%;此后继续延长反应时间,己二酸收率变化不大。因此,选择10 h为最佳反应时间。从图4b可看出,随温度的升高,反应速率加快,己二酸收率增大,但温度超过90 ℃后,己二酸收率增幅减小。这可能是因为,H2O2氧化环己烯需要更高的反应温度才能实现氧原子的转移[17],但温度过高,H2O2均裂生成羟基自由基,会引发烯丙基副反应[18]。为了保证反应体系沿双键氧化的路线反应,反应体系的温度不宜过高,因此,最佳的反应温度为90 ℃。从图4c可看出,催化剂用量的增大可大幅提高己二酸收率,当催化剂加入量达到1.0 g时,己二酸收率达到最高;继续增加催化剂加入量,己二酸收率反而下降,可能是因为过量的催化剂反而加快了副反应的发生。因此,最佳的催化剂加入量为1.0 g。由图4d可看出,随H2O2用量的增加,己二酸收率逐渐提高,当n(H2O2)∶n(环己烯)=4.4时,己二酸收率达到最大,此后继续增加H2O2用量,己二酸收率反而降低,可能是因为过量的H2O2导致了副反应加剧。因此,最佳的n(H2O2)∶n(环己烯)=4.4。
2.6 催化剂的重复使用性能
为了考察[C3SO3Hnhm]3PW12O40的重复使用效果,反应结束后将分离得到的固体催化剂用溶剂DMF洗涤3次,然后在烘箱中150 ℃下干燥至恒重,重复用于环己烯氧化反应,结果见图5。
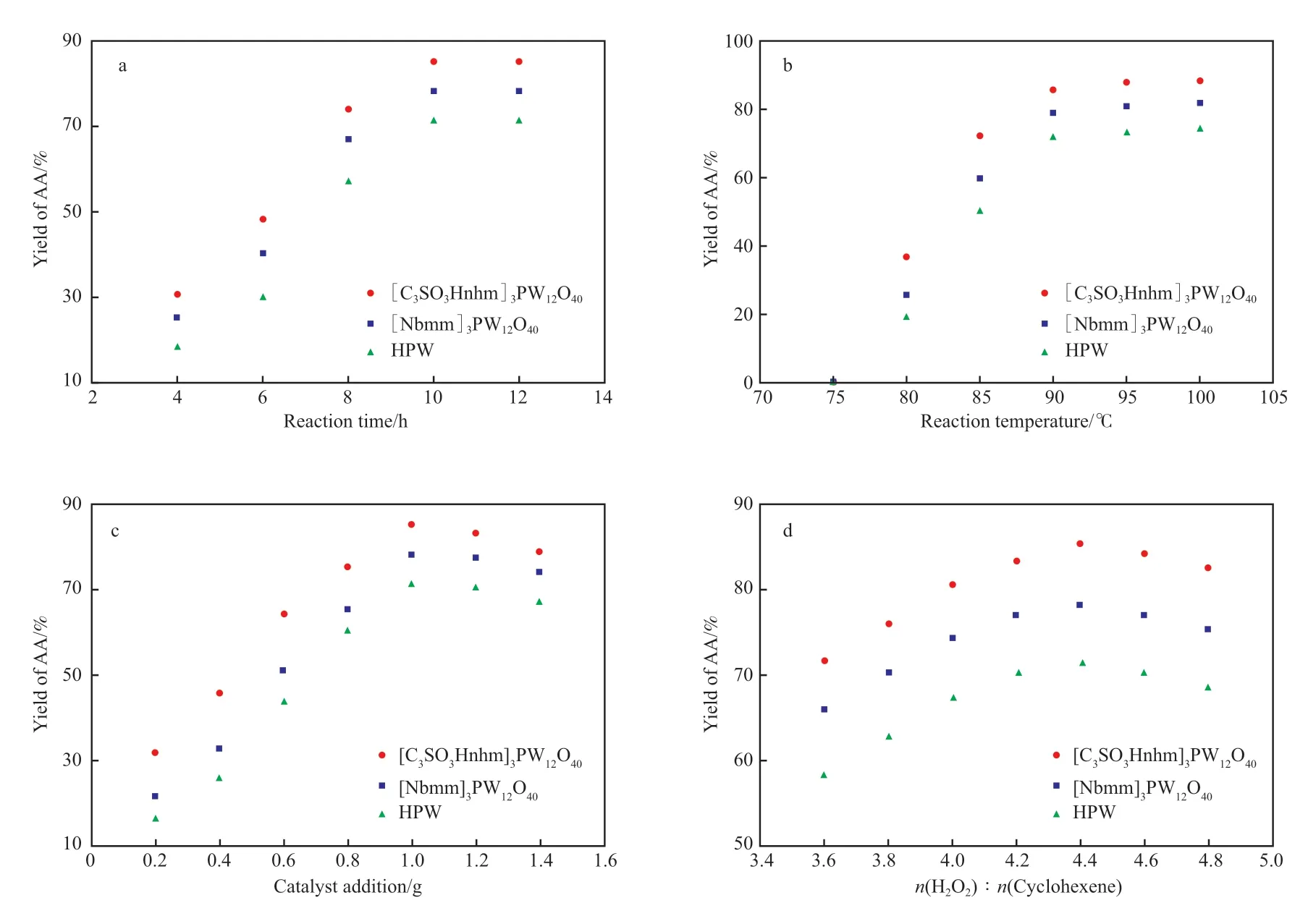
图4 工艺条件对己二酸收率的影响Fig.4 The effect of reaction conditions on the yield of AA.
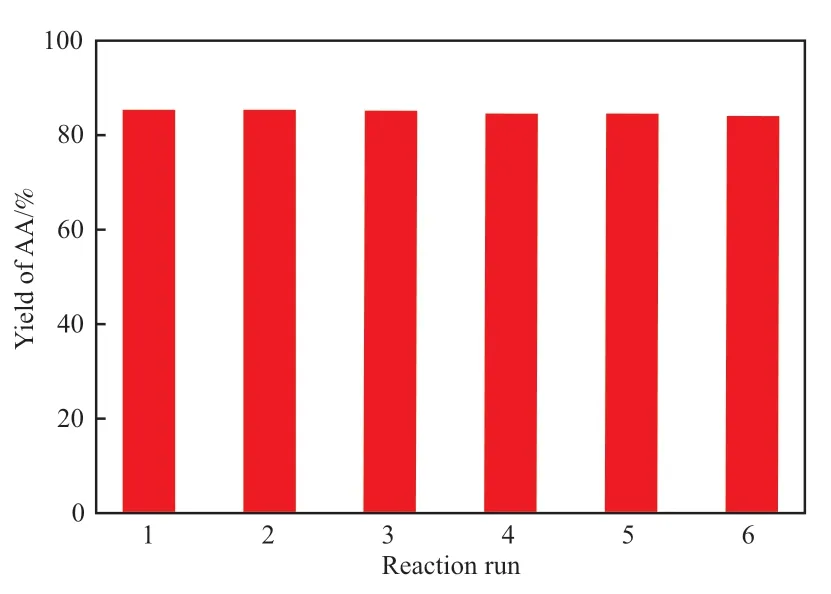
图5 [C3SO3Hnhm]3PW12O40重复使用性能Fig.5 The reusability of[C3SO3Hnhm]3PW12O40.Reaction conditions referred to Fig.3.
从图5可以看出,[C3SO3Hnhm]3PW12O40重复使用6次后,己二酸收率仍能达到84%。
[C3SO3Hnhm]3PW12O40使用前和重复使用6次后的FTIR谱图见图6。由图6可知,两个试样均存在属于Keggin结构的4个特征吸收峰[19],分别为1 078(P-Oa),982(W-Od),894(W-Ob-W),803(W-Oc-W) cm-1。3 442 cm-1(O—H键伸缩振动),2 967 cm-1和2 873 cm-1(甲基中C—H键的不对称和对称伸缩振动),1 470 cm-1(—CH3),1 633 cm-1(季铵基团),1 118 cm-1(C—N键伸缩振动),1 165 cm-1(—S=O)均属于有机阳离子的特征峰。FTIR表征结果显示,[C3SO3Hnhm]3PW12O40使用前后均保留了有机阳离子和杂多阴离子的结构。

图6 [C3SO3Hnhm]3PW12O40使用前(a)和重复使用6次后(b)的FTIR谱图Fig.6 FTIR spectra of [C3SO3Hnhm]3PW12O40 before(a) and after used for 6 times(b).
2.7 催化反应机理
有机-无机磷钨酸盐催化氧化环己烯制己二酸反应发生在催化剂表面。为了探究反应机理,在反应9 h后,对析出己二酸晶体后剩余的液体进行GC-MS分析,结果见图7。从图7可看出,除了主产物己二酸外,还生成了1,2-环己二醇等,这些都是环己烯双键氧化的中间产物,初步估计环己烯在[C3SO3Hnhm]3PW12O40的作用下是沿着双键氧化的路径进行反应。反应机理见图8。

图7 液体的GC-MS谱图Fig.7 GC-MS spectra of liquid.
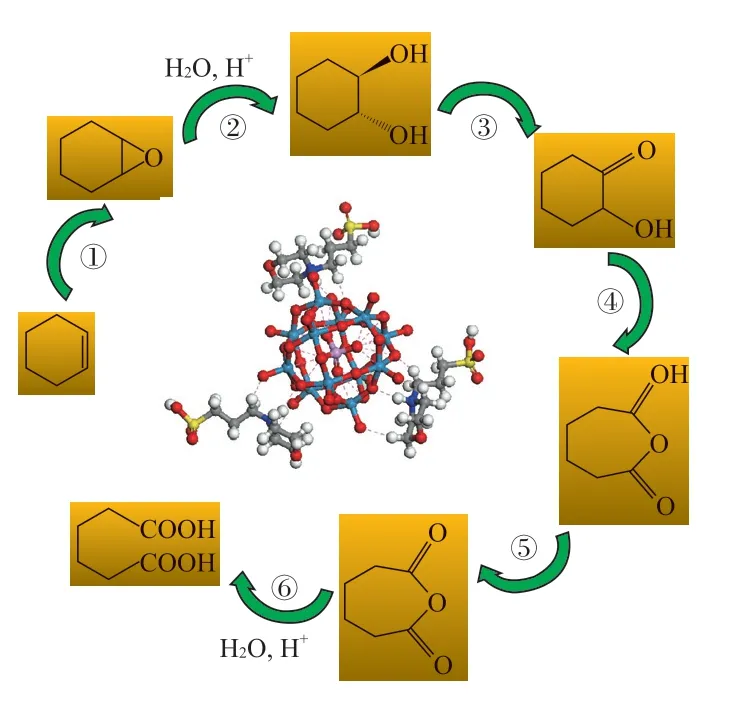
图8 反应机理Fig.8 The reaction mechanism.
从图8可看出,W首先被H2O2氧化为过氧钨酸盐[WO(O2)2(OH)2]2-,[WO(O2)2(OH)2]2-是环己烯氧化的催化活性物质,环己烯双键氧化生成环氧环己烷;有机配体上的磺酸提供了B酸,在B酸作用下环氧环己烷发生水解进一步被氧化为1,2-环己二醇,最终被氧化为己二酸。由于[C3SO3Hnhm]3PW12O40不含较强的自由基激发活性位点,因而在催化环己烯氧化制己二酸的反应中表现出较强的催化性能。而[WO(O2)2(OH)2]2-被还原为PW12O3-40,催化剂得以重复使用,H2O2被不断消耗。
2.8 催化氧化对比实验
[C3SO3Hnhm]3PW12O40与其他催化剂进行对比的结果见表3。由表3可知,本工作最优工艺条件下的己二酸收率为85.3%,远高于文献中[CH3(CH2)15N(CH3)3]3{PO4[WO(O2)2]4},K3PW12O40,Na2WO4·(H2O)2的己二酸收率。尽管H2WO4的己二酸收率有96.0%,但它需要在离子液体中反应,而离子液体制备成本高,且回收过程存在分离和流失问题。因此,和其他固体催化体系相比,[C3SO3Hnhm]3PW12O40展现了更高的催化活性和更好的经济适应性。

表3 [C3SO3]3PW12O40和其他固体催化剂的催化性能对比Table 3 Comparison of catalytic performance between[C3SO3Hnhm]3PW12O40 and reported solid catalysts
3 结论
1)制备了有机-无机磷钨酸盐[C3SO3Hnhm]3·PW12O40和[Nbmm]3PW12O40,酸强度由大至小顺序为[C3SO3Hnhm]3PW12O40>HPW>[Nbmm]3PW12O40,与催化氧化环己烯制备己二酸的催化活性一致。
2)在反应温度90 ℃、反应时间10 h、催化剂加入量1.0 g、H2O2用量22 mL、环己烯用量5 mL(n(H2O2)∶n(环己烯)=4.4)的条件下,[C3SO3Hnhm]3PW12O40表现出最佳的催化活性,己二酸收率达到85.3%。催化剂循环使用6次后结构仍没有变化,且己二酸收率没有明显下降。与其他催化剂对比,[C3SO3Hnhm]3PW12O40显示了更高的催化活性和更好的经济适应性。
——吗啡

