对活化能相关模型的反思
邹国华 童文昭 杨梓生


摘要:模型与建模在科学教育中具有重要地位,以活化能相关模型作为研究对象,发现活化能相关模型教学中存在未正确理解模型内涵,导致迷思概念以及固守已有模型形成思维定势等问题。分析问题出现的原因,对活化能相关的模型教学进行反思,为科学模型教学提出相应的建议。
关键词:科学模型;活化能;模型教学
文章编号:1005-6629(2021)05-0091-06 中图分类号:G633.8 文献标识码:B
模型与建模的研究由来已久,其外显的思想沟通和表达作用以及强大的解释和预测功能,使其受到科学研究者的广泛重视,而模型和建模对于科学研究的重要性在很大程度上决定了其在科学教育中的重要地位。科学家在科学研究中常通过科学建模来记录、描述研究成果,以便更好地理解和运用成果;在教育领域,教育家也提出要通过科学模型和建模来提升教师和学生对科学本质的理解,提高他们对复杂问题的解決能力。王磊认为,科学模型是对于一个复杂系统的简化和抽象表示,目的是用来解释或者预测某些科学现象;科学建模指产生科学模型的过程,是一个动态的历程,通常包括建构、应用、评估和修正四个方面。
《普通高中化学课程标准(2017年版)》首次将“模型认知”写入其中,并将其归为化学学科核心素养之一。此后,化学学科关于模型与建模的研究受到前所未有的重视,相关研究成果如雨后春笋般涌现。模型在科学认识中具有描述、解释和预测等功能,是理论发展的一种重要方式,教学中模型的使用能促进学生对学科核心概念、科学本质的理解。从教学实践来看,科学模型的教学方面还存在一些值得思考和改进的问题,下面以与活化能相关的几个模型为例进行分析探讨。
1活化能相关模型教学中存在的问题及讨论
1.1未理解模型内涵,导致迷思概念
教学建模的目的之一是将科学知识、规律等内容深入浅出地进行表征,促进学生对科学本质的理解。正确理解教学中的模型,应先厘清各概念的内涵与外延,梳理概念与概念之间的联系,否则,可能因未正确理解模型,导致迷思概念,对后续学习造成一定的困扰。
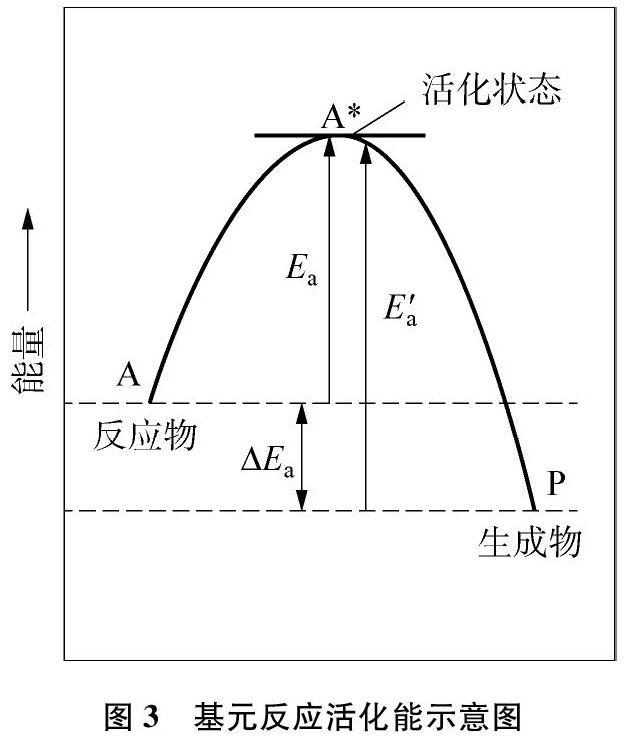
鲁科版化学必修第二册第2章第2节“化学反应与能量转化”中,教材为了阐述反应过程中键能与能量变化的关系,呈现了如图1所示的模型,并注释“E1为破坏旧化学键吸收的能量,E2为形成新化学键释放的能量”。人教版化学反应原理第二章第一节“化学反应速率”中,以图2所示模型解释反应物、生成物的能量与活化能的关系,文中解释“E1表示反应的活化能,E2表示活化分子变成生成物分子放出的能量”,图1和2是高中阶段常见模型,在作业、试题中频繁出现。表面上看,图1和2基本相同,而E1在图1代表破坏旧化学键吸收的能量,在图2代表活化能。交谈中发现,不少教师、学生由图1和图2总结出“破坏旧化学键吸收的能量等于活化能”“反应物的总键能等于活化能”等结论。那么,反应物的总键能是否等于活化能?键能与活化能之间有怎样的联系?为此,笔者开展了相应的科学模型教学的研究。
1.1.1正确理解活化能的科学模型
《普通高中化学课程标准(2017年版)》关于活化能内容要求为:知道化学反应是有历程的,认识基元反应活化能对化学反应速率的影响。活化能具体内涵不属于高中化学课程的要求,各版高中化学教材也未做深入介绍,而高中常出现与活化能相关的科学模型,学生容易因未正确理解而产生困惑。作为教师,应先理解活化能的科学模型,在学生存在困惑时深入浅出地进行解惑。
1.1.2厘清键能、活化能两个模型间的关联
高中阶段将“101.3 kPa、298 K条件下,断开1molAB(g)分子中的化学键,使其分别生成气态A原子和气态B原子所吸收的能量称为A—B键的键能”,从定义可知,键能与活化能之间有区别,通过查阅资料发现,可通过键能粗略估算活化能。

