无创指标对慢性冠脉综合征患者猝死预警分析
李爱英,魏芳晶,任润梅,阴淑莹,胡淑敏,景国强
(内蒙古医科大学附属医院心血管内科,内蒙古 呼和浩特 010050)
2019年,在《2019ESC慢性冠状动脉综合征诊断与处理指南》提出了一个全新的冠状动脉疾病的概念——慢性冠状动脉综合征(chronic coronary syndrome,CCS),吸引了全球心血管学者和医生的注意[1]。CCS包括有稳定型心绞痛(stable angina pectoris,SAP)、缺血性心肌病(ischemic cardiomyopathy,ICM)和隐匿型冠心病,本文主要对前两种临床类型做研究,观察多项无创猝死预警指标对CCS患者主要不良心血管事件(major adverse cardiovascular events,MACE)的预警分析。
1 资料与方法
1.1 病例入选和排除标准
(1)入选标准:①符合CCS诊断标准;②窦性心律;(2)剔除标准:①异位心律:心房纤颤、心房扑动;②二度或三度房室传导阻滞、病态窦房结综合征、起搏心律;③内分泌疾病:糖尿病、甲亢;④恶性肿瘤、血液病;⑤严重肝肾功不全
1.2 临床资料
本研究入选了2019-06~2020-05在我院住院的CCS患者共98例为观察组,其中52例SAP患者;46例ICM患者。男71例,女27例,年龄48~87岁,平均(65.23±8.64)岁。选择50例同期健康人作为对照组,男36例,女14例,年龄44~83岁,平均(62.84±8.38)岁。年龄性别的比较对照组与观察组差异无统计学意义(P>0.05)。
1.3 CCS的诊断标准
《2019年ESC慢性冠脉综合征诊断和管理指南》。
1.4 研究方法
1.4.1 动态心电图 给受检者佩戴动态心电图仪(北京今科公司生产MIC系列),行24h监测。回放24h记录,通过人机对话去掉干扰、伪差,对室上性期前收缩、室性期前收缩做出标记,由系统自动分析获得连续心率减速力(heart rate deceleration runs,DRs)值。
(1)DRs的计算方法:①将不同DR周期值制成顺序图,横坐标为心动周期序号,纵坐标为测量出的每一跳RR值;②心率减速力的相对值是用心率减速力各绝对值(DR1~DR10),除以窦性心律RR间期的总数值得到;③连续3个心动周期中最后2个心动周期相继发生心率减速现象为DR2,正常值>5.4%;连续5个心动周期中最后4个心动周期相继发生心率减速现象为DR4,正常值>0.05%;连续9个心动周期中最后8个心动周期相继发生心率减速现象为DR8,正常值>0.005%;(2)DRs猝死危险分层方法:DR2异常为≤5.4%;DR4异常为≤0.05%;DR8异常为≤0.005%。先看DR4,异常为猝死高危险;三者均正常为低危险。若DR4正常,再分析DR8和DR2,二者其一异常为中危险。
1.4.2 QT离散度(QT dispersion,QTd)QT是指同步12导联心电图上不同导联最大QT间期(QTmax)与最小QT间期(QTmin)的差值。测量方法:当判断不清某一导联T波边界时,可省略该导联。总测量数≥10个即可。把TP做为等电位线,以Q波的起点(无Q波时以R波的起点)为QT间期的起点,终点是T波的降支与等电位线的交点。当T波后有U波时,取T、U之间的最低点为终点。
1.4.3 超声心动图GE公司VividE9彩色多普勒超声诊断仪,探头型号为M5s,频率为2.5MHz。患者取左侧卧位,采用Simpson,s法测量出左室收缩末容积(ES)和舒张末容积(EDV),计算左室射血分数(left ventricular ejection fraction,LVEF)EF=(EDVES)*100%/EDV,正常范围:50%~70%。左室舒张末径(left ventricular end-diastolic diameter,LVEDd)正常范围:36~55mm。
1.5 观察在院期间MACE
包括再发心梗、严重心力衰竭、恶性室性心律失常(室速、室颤)、心源性死亡。
1.6 统计学分析
采用SPSS 20.0软件进行统计学分析,计量资料用均数±标准差表示,组间比较采用t检验,计数资料采用χ2检验。检验水准α=0.05,P<0.05为差异有统计学意义。对MACE发生的预测指标进行单因素分析及二元logistic回归分析,出和入的检验水准是入是0.05,出是0.1。
2 结果
2.1 实验组各亚组与对照组间无创预警指标比较
DR2值、DR4值和DR8值SAP组、ICM组和对照组比较,差异有统计学意义(P<0.05)。EF值三组两两比较,差异有统计学意义(P均<0.05)。LVEDD值ICM组和对照组及SAP组比较,差异有统计学意义(P<0.05)。QTd值SAP组和对照组比较、ICM组和SAP组及对照组比较,差异有统计学意义(P<0.05)。余两两比较无统计学差异(P>0.05)(见表1)。
表1 实验组各亚组与对照组间无创预警指标比较(±s)

表1 实验组各亚组与对照组间无创预警指标比较(±s)
注:aDR2:SAP、ICM和对照组比较P<0.05;bDR4:SAP、ICM和对照组比较P<0.05;cDR8:SAP、ICM和对照组比较P<0.05;dEF:两组间比较P均<0.05;eLVEDD:ICM和对照组及SAP比较P均<0.05;fQTd:SAP和对照组比较P<0.05,ICM和SAP及对照组比较P均<0.05。余两两比较P>0.05。
组别nDR2(%)DR4(%)DR8(%)EF(%)LVEDD(mm)QTd(ms)对照组508.668±1.8870.651±0.2870.038±0.02568.16±5.8045.52±3.6457.36±18.14 SAP组527.779±1.875a0.519±0.218b0.028±0.012c62.58±8.89d46.75±4.2366.58±19.89f ICM组467.392±1.854a0.435±0.279b0.022±0.010c41.41±10.42d60.00±7.52e91.26±27.80f
2.2 根据DRs对患者进行危险分层,实验组各亚组与对照组间危险分层的比较
发现在低危患者和中高危患者中ICM组和SAP组、对照组比较,差异有统计学意义(P<0.05)。在中危患者中ICM组和对照组比较,差异有统计学意义(P<0.05)。余两两比较,无统计学差异(P>0.05)(见表2)。
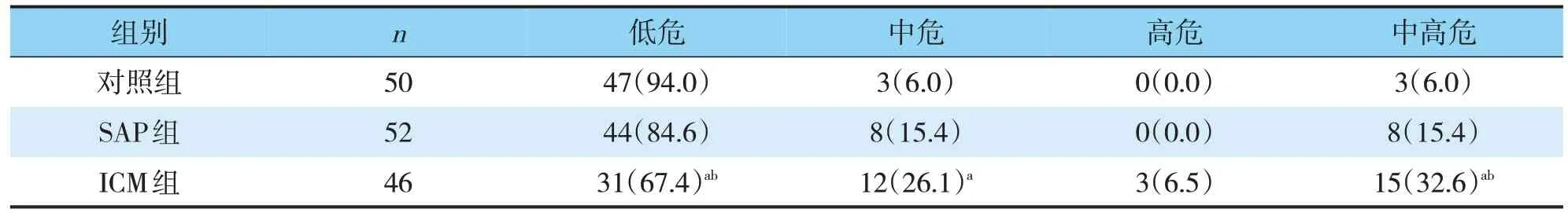
表2 实验亚组与对照组间DRs危险分层的比较(n,%)
2.3 观察组患者中MACE发生的预测指标分析
住院期间观察组患者发生MACE事件共13例,均发生于ICM组,其中心源性死亡2例;室速11例。通过单因素分析发现LVEF、LVEDD、QTd是导致MACE发生的主要预测指标,这三指标P<0.05,符合进入的检验水准0.05,进行二元logistic回归分析,回归分析发现LVEF对MACE发生的预警价值更高(见表3、4)。
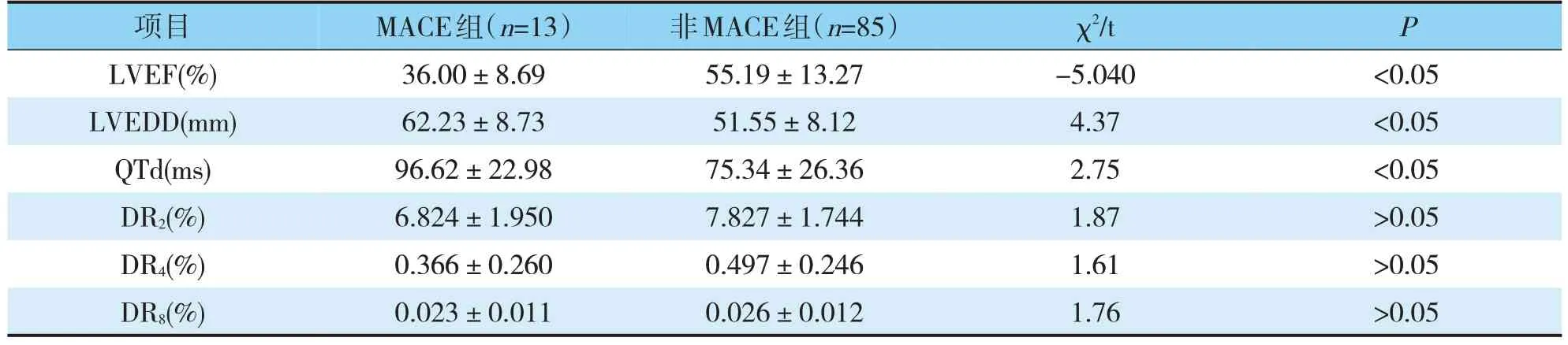
表3 观察组患者中MACE发生的单因素分析

表4 观察组患者中MACE发生的logistic回归分析
3 讨论
CCS是基于急性冠状动脉综合征(acute coronary syndrome,ACS)的基础上提出的[2],我们既往研究的热点多集中在ACS患者,因为这样的患者急而重,猝死率高。而对于CCS患者研究相对较少,SAP患者也可有左主干病变或三支血管病变,有发生急性心肌梗死甚至猝死的危险。而ICM患者冠状动脉管腔发生狭窄甚至是闭塞,心肌长期缺血,出现弥漫性纤维化改变,心腔扩大,心脏收缩舒张功能受累,易发生顽固心衰、恶性心律失常和猝死。本研究在于观察多项无创猝死预警指标对CCS患者MACE的预警分析。
DRs是2011年Georg Schmidt教授提出的一种新的预警心脏性猝死高危患者的无创心电技术。其价值在于可以定量分析迷走神经的作用,而不受外界因素的干扰,对猝死危险分层清晰,便于推广应用。本研究同时联合分析了反映心脏结构改变的指标:EF和LVEDD,以及反映心室复极不均一性的QTd。从多个角度对CCS患者发生MACE事件的预警价值进行分析。
本研究发现DRs中的DR2值、DR4值和DR8值ICM组、SAP组和对照组比较差异均有统计学意义(P<0.05)(见表1)。ICM组的DRs明显减低,与国内朱王亮等[3]研究一致。CCS组的DRs值较正常对照组明显降低,说明CCS患者迷走神经功能减弱甚至明显下降,交感神经兴奋性增高,恶性心律失常增加。
DRs的另一个重要价值就是可以进行危险分层,重在识别高危患者,及早做猝死的预防。本研究发现ICM组中高危患者较多,与对照组及SAP组比较有统计学差异(P<0.05)(见表2)。DRs危险分层与自主神经损害程度相关,越是高危患者,自主神经损害越严重,迷走神经张力降低明显,MACE风险增加[4]。住院期间观察组患者发生MACE事件共13例,均发生于ICM组,其中心源性死亡2例;室速11例。
QTd值SAP组和对照组比较,差异有统计学意义(P<0.05)(见表1)。因为SAP组心肌缺血后心肌细胞功能会有不同程度的影响,心肌细胞复极化不一致,心肌电活动不稳定,QTd会增大[5]。QTd值ICM组和SAP组及对照组比较,差异有统计学意义(P<0.05)(见表1)。ICM组往往是反复心梗的患者或多支血管病变,存在心脏瘢痕或顿抑心肌,易造成复极不均一,致QTd明显增大,恶性心律失常增加,猝死风险加大[6]。国外Rodríguez-Jiménez AE等研究校正QTd是预测心肌梗死复发的心电图工具[7]。
通过单因素分析发现LVEF、LVEDD、QTd是导致MACE发生的主要预测指标,通过二元logistic回归分析发现LVEF对MACE发生的预警价值更高(见表3、4)。EF值三组两两比较,差异有统计学意义(P均<0.05)(见表1)。国内何新为[8]的研究结果:LVEF与缺血性心肌病患者死亡呈负相关。ICM患者很多是反复心梗、心脏瘢痕化、纤维化所致,ICM组往往随着心脏结构改变,心脏明显扩大,射血分数明显降低,逐渐出现心功能的失代偿,出现心衰,恶性心律失常,最终走向心脏病的终末期,死亡率明显增高。ICM很多患者都有陈旧性心梗的病史,所以心肌梗死后左心室射血分数的再评估是当前临床实践和不良重塑的决定因素[9],尤其是心梗后40天。急性心梗若未及时开通血管,就会留有心肌瘢痕,Gupta A等[10]研究表明LVEF≤35%的患者中,适当的ICD电击和心源性猝死患者与心肌瘢痕而非缺血有关。所以目前使用植入式心律转复除颤器(ICDs)预防猝死的指南主要基于对左心室射血分数(LVEF)的测量[11]。而在LVEF≥35%的心肌梗死患者中,DRs异常与突发性心律失常风险增高独立相关[12,13]。所以对于EF减低不明显或没有减低的患者DRs的危险分层对猝死的评估显得尤为重要。
综上研究表明DRs能够对迷走神经定量测定,对CCS患者进行危险分级,DRs高危患者猝死率高,与国内王春光等[14]研究一致。发生MACE的患者普遍心率增快,那是迷走神经功能下降的表现,其结果减弱了对心脏的保护作用,降低了室颤阈值,增加了MACE的发生。HR持续升高即可能发生缺血、斑块不稳定、触发心律失常,所以心率可作为ACS和CCS的治疗靶点[15]。筛选室性心律失常和猝死易感性的新试验检查了心室复极异常、自主神经系统功能和电异质性。由于猝死是由多种机制引起的,因此风险因素的组合可能会证明对风险分层更为精确。从而说明反映不同机制的猝死预警指标的联合评估,对风险评估及猝死的预测更为准确。而CCS患者虽然是慢性冠状动脉综合征,但仍存在着较大的猝死风险,需要引起临床的注意。SAP的高危患者随时可能转化成ACS患者,而ICM患者中尤其是EF值减低、QTd增加的患者猝死率明显增加。

