竹笋膳食纤维的结构特性及其功能性质
万仁口,李功景,贺杨正,李红艳,袁传明,邓泽元*
(1 南昌大学食品科学与技术国家重点实验室 南昌330047 2 江西广雅食品有限公司 江西乐安344300)
膳食纤维是一类不易被人体本身所具有的内源酶消化且不易被人体吸收的物质[1-3]。它是一种公认的功能性食材,被列为“第七大营养素”[4],同时还被称作“肠道清道夫”。依据在水中溶解性的不同,膳食纤维分为可溶性膳食纤维(SDF)和不溶性膳食纤维(IDF)2 种[5-6]。膳食纤维具表现出极强的水合性质,吸水膨大后在人体小肠内形成胶状物,可增加饱腹感、促进肠道的收缩和蠕动,进而有效地控制肥胖[7-8]。膳食纤维不仅可吸附NO2-、胆酸盐等小分子物质,减少外源有害物质的危害,还能够吸附葡萄糖分子,进而延缓和抑制对糖的吸收,降低餐后血糖值,预防糖尿病[9]。膳食纤维能阻滞或者降低人体对脂质吸收,进而起到调节血脂的作用。膳食纤维可减少心血管和胃肠道疾病,预防结肠癌[10-11]。大量研究表明,SDF 比IDF 在各上表现更为优异,然而也有报导称IDF 对有害物质的吸附性优于SDF[12]。不同来源的膳食纤维的化学组成(单糖和多糖组成)和结构特性(形状、键合结构、粒度、结晶状态)不同,使得其理化性质各不相同,导致其保健功能可能存在较大差异。从膳食纤维结构特性和功能性质两方面研究,对认识不同来源的膳食纤维具有重要的意义。
竹笋是一种极具开发前景的新型膳食纤维资源,含有多种生物活性物质[13]。本研究以竹笋为原料,采用纤维素酶解法制备竹笋膳食纤维,并在此基础上测定3 种膳食纤维的基本物理性质和单糖的组成情况,通过扫描电镜、傅里叶红外光谱、X光衍射和热稳定性等方法研究它们的结构特性和理化性质,为竹笋膳食纤维的加工利用提供试验数据。
1 材料与方法
1.1 材料与试剂
竹笋,江西广雅食品有限公司;食品级纤维素酶,南宁庞博生物工程有限公司;食品级糖化酶、α-淀粉酶,化学纯胰酶、盐酸萘乙二胺、对氨基苯磺酸、糠醛,Aladdin;化学纯亚硝酸钠、胆酸钠、盐酸、苯胺、酒石酸钾钠、苯酚,上海西陇科学股份有限公司。
1.2 仪器与设备
JSM 6701F 环境扫描电镜(SEM),日本Hitachi 公司;D8 ADVANCEX 射线衍射仪,德国Bruker 公司;TGA 4000 热重分析仪,美国PE 公司;Nicolet5700 傅里叶红外光谱仪,美国Thermo Fisher Nicolet 公司;气相色谱仪,美国Agilent 公司;酶标仪,美国BioTek 公司。
1.3 方法
1.3.1 纤维素酶制取竹笋膳食纤维的工艺 准确称取5 g 竹笋样品于500 mL 高脚烧杯中,加入200 mL 0.05 mol/L MES-TRIS 缓冲液,依次加入250 μL α-淀粉酶、500 μL 糖化酶及0.225 g 胰酶,于60℃恒温振荡水浴环境中分别反应30 min,以去除淀粉、脂质以及蛋白质,过滤即得总膳食纤维(TDF)。添加0.7%纤维素酶(酶解pH 值为5.0,温度45℃)后水浴振荡3.5 h,用G2 砂芯坩埚过滤得IDF 和滤液,而后向滤液中加入95%乙醇溶液,醇沉4 h,离心得SDF 沉淀。IDF 和SDF 冷冻干燥后即得干燥粉末。
1.3.2 基础物理性质的测定 按照耿乙文等[14]的方法对竹笋SDF、IDF 以及TDF 的颜色、堆积密度及其休止角等基础物理性质进行测定。
1.3.3 单糖组成测定
1)样品的处理及衍生化[15]称取10 mg 样品加入含有2 mL TFA(2 mol/L)的安瓿瓶中,酒精喷灯封管后于110℃恒温干燥箱中水解3 h,冷却至室温,氮气吹干,彻底蒸除三氟乙酸。分别称取各种单糖标品10 mg 与处理后的样品同步进行糖腈乙酰化衍生反应,操作如下:加入盐酸羟胺10 mg,吡啶0.5 mL,90℃水浴振荡30 min 后冷却,加入0.5 mL 醋酸酐后于90℃水浴振荡30 min,冷却后进行GC 分析。
2)GC 分析条件色谱柱:Agilent HP-5 毛细管柱;检测器:FID 检测器;载气:高纯氮气,流速1 mL/min,分流比为20∶1;气化室温度:250℃;检测器温度:250℃;程序升温:160℃保持2 min,然后以2℃/min 升至240℃保持5 min;进样量:1 μL。
1.3.4 结构特性 少量竹笋粉末样品喷金后,用电镜观察粉末表观形态。膳食纤维用KBr 压片法制样后,采用红外光谱仪测定纤维中基团的种类,波数测定范围400~4 000 cm-1。取10 mg 膳食纤维试样放入热重分析仪样品池中进行热性能测定,试验条件为:氮气流速50 mL/min,升温速度10℃/min,温度范围30~900℃。将纤维样品压入样品架中,在X 射线衍射仪上进行XRD 分析,试验条件为:Cu 靶Ka 辐射(X 射线波长0.154 nm),管电流30 mA,衍射方向0~20 联动扫描方式,扫描角度5 °~50 °,扫描速度5 °/min。根据Segal 等[16]的研究,结晶度的计算公式如下:

式中,CI——结晶度,%;I002——膳食纤维的最大衍射强度;Iam——2θ角为18°下的衍射强度。
1.3.5 膳食纤维的基本特性 膨胀性(Swelling capacity,SC)、持水性(Water holding capacity,WHC)和持油性(Oil holding capacity,OHC)参照刘红开等[5]的方法测定。
1.3.6 阳离子交换性(Canon exchange capacity,CEC)[16]称取适量样品浸没于装有0.10 mol/L HC1 溶液的锥形瓶中,于37℃振荡24 h 后过滤,收集滤渣。用蒸馏水不断冲洗滤渣直至用10%AgNO3检测不到氯离子为止,最后减压干燥至恒重。0.1 g 恒重样品置于装有100 mL 5% NaCl 溶液的锥形瓶中,充分振荡混合均匀,用NaOH 溶液(0.01 mol/L)缓慢滴定(酚酞作指示剂),5 min 后不变色即为滴定终点。同时用纯水替代盐酸做空白试验,CEC 按式(2)计算:

式中,m——样品质量,g;V1——试样消耗NaOH 的体积,mL;V2——空白消耗NaOH 的体积,mL;c——NaOH 浓度,mol/L。
1.3.7 膳食纤维的吸附性能
1.3.7.1 膳食纤维对亚硝酸根离子的吸附性NO2-标准曲线的制作参照GB 5009.33-2016《食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定》。称取1.0 g 样品于装有100 mL 的亚硝酸溶液(100 μmol/L)的锥形瓶内,调节pH 值,37℃水浴振摇2 h 后过滤,弃去初滤液20 mL 后吸取1 mL 上清液。标准曲线为:y=0.7475x+0.0576,R2=0.9960,亚硝酸根离子的吸附量按式(3)计算:

1.3.7.2 膳食纤维对胆酸钠的吸附性 称取1.0 g 样品加入装有100 mL 0.15 mol/L NaCl 溶液(含0.2 g 胆酸钠)的锥形瓶内,调节pH 值至7.0,37℃水浴振荡3 h 后离心(4 200 r/min,25 min),取0.5 mL 上清液用纯水补充体积至1 mL。采用糠醛比色法测定,标准曲线为:y=0.8982x+0.0854,R2=0.9933,按式(4)计算胆酸钠吸附量。

1.4 数据处理与统计分析
2 结果与分析
2.1 基础物理性质
在食品原料中添加膳食纤维可能会影响产品的感官特征[3,8],因此对膳食纤维的色度、密度和流动性的测定十分必要。3 种膳食纤维的几个基本物理性质见表1。TDF 和IDF 的L、a、b 和ΔE 值相近,两者均呈浅绿色,TDF 颜色较IDF 略浅,而SDF 呈乳白色,可能与成分组成有关。堆积密度反映膳食纤维的疏松程度,堆积密度小的膳食纤维,其结构较为疏松,纤维之间空间较大,比表面积大,具有良好的表面活性。由表1可知,IDF 的堆积密度最小,结构最为蓬松。休止角是体现粉末流动性能的指标,角度越小则流动性越好,普遍认为θ≤40 °时流动性好且符合生产要求。SDF 的休止角为34.07 °,具有较好的流动性;其次是TDF,休止角为39.49 °,可以满足企业生产;而IDF 的休止角较大,流动性差,在产品生产中不太适合单一添加使用。

表1 膳食纤维的基本物理性质Table 1 Basic physical properties of dietary fiber
2.2 膳食纤维的单糖组成
3 种膳食纤维经三氟乙酸水解、硼氢化钠还原以及乙酸酐酯化为糖醇乙酸酯后通过GC 分析其主要的单糖组分。由表2可知,TDF 水解后的单糖以木糖、甘露糖和L-阿拉伯糖为主,含量之和可达87%以上,鼠李糖含量最低,仅为0.08%,可能与半纤维素的水解有关;SDF 中的阿拉伯糖、半乳糖和木糖的含量最高,分别为24.64%,38.05%和12.63%。IDF 中的木糖和L-阿拉伯糖含量最高,分别为41.77%和10.44%。
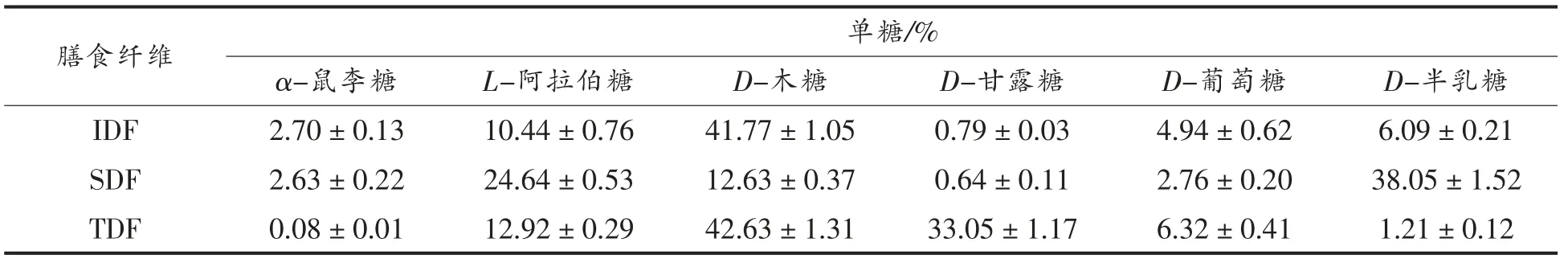
表2 膳食纤维单糖组成Table 2 The monosaccharide composition of dietary fiber
2.3 结构特性
2.3.1 膳食纤维微观结构 通过环境扫描电镜观测的竹笋3 种膳食纤维的微观结构见图1。3 种纤维的结构具有明显差异,TDF 的形状不规则,块状较大,表面有很多褶皱,可以吸附水和葡萄糖等小分子颗粒。SDF 的颗粒松散,形状较小且比较均一,颗粒表面蓬松且多有孔洞,比表面积大。IDF呈现附着颗粒状物质的紧致片层结构,表面有球形物质,可能是蛋白质或淀粉颗粒。

图1 膳食纤维的微观结构Fig.1 The micro-structure of dietary fiber
2.3.2 膳食纤维的红外谱图如图2所示,IDF、SDF 和TDF 三者的峰型比较类似,说明3 种竹笋膳食纤维的化学组成成分基本相同。3 414.46 cm-1处是由分子间或分子内-OH 基伸缩振动引起[17];2 929.19 cm-1处的小尖峰是由糖类甲基和亚甲基上的C-H 伸缩振动引起的;1 619.87 cm-1 处的吸收峰由CHO 的C=O 非对称收缩振动形成[18]。在此波数下,膳食纤维的吸收峰强弱顺序为IDF>TDF>SDF,表明相较TDF 而言,-COO-在IDF 中含量较高,在SDF 中含量较少。在酶解提取SDF的过程中,部分结构被一定程度降解,致使特征吸收峰有所减弱。1 384.20 cm-1和1 250.22cm-1 处的小尖峰是由-CH 变形振动引起的,为糖类特征吸收峰,SDF 在这2 个波数下的峰更加尖锐,可能与半纤维素降解、糖单元间链接键断裂、β糖苷键外露有关[19]。1 047.27 cm-1处的吸收峰是半纤维素糖单元中的环状C-O-C 中的C=O 伸缩振动或者CO-H 中的O-H 变形振动峰引起的[20]。在波数1 047 cm-1处,IDF 和TDF 的吸收谱带相对SDF 较宽,说明羟基所形成的氢键作用增强;620.20 cm-1处是糖分子中β型C-H 直立键的变形振动吸收峰。

图2 竹笋膳食纤维红外图谱Fig.2 The infrared spectrum of dietary fiber from bamboo shoot
2.3.3 膳食纤维的衍射图 研究表明,纤维素类物质由有序结晶区和无序非结晶区两部分组成[20-21]。衍射强度受纤维的结晶度以及照射角2θ的影响,根据它们的变化可以绘制XRD 曲线。图3是3 种竹笋膳食纤维的衍射图。由图3可知,TDF 的衍射峰的2θ角有3 个,分别在21.92 °,31.15 °和45.50 °左右,表明该竹笋的纤维结晶属于纤维素Ⅰ型;IDF 有1 个衍射峰,2θ角在21.72 °左右,衍射峰强度较TDF 大;SDF 有1 个衍射峰,其2θ角为20.22 °,衍射峰强度较TDF 小。衍射角2θ在15 °~25 °范围内主要是纤维素和半纤维素衍射峰,SDF 的分子质量小,聚合度低,导致其纤维素和半纤维素结晶区强度弱,衍射峰强小。通过X 射线衍射图谱不仅可以推断竹笋纤维的结晶类型,还可以估算其结晶度大小。经计算,TDF、IDF 和SDF 三者的结晶度分别为27.32%,25.48%和17.86%,SDF 的结晶度最低,不溶性膳食纤维与总膳食纤维的结晶度相近。

图3 膳食纤维衍射图Fig.3 XRD of dietary fiber
2.3.4 膳食纤维的热稳定性 膳食纤维的热稳定性分析结果见图4。在热重曲线(Thermal Gravity Analysis,TG)曲线中,3 种膳食纤维表现出相似的失重规律:第1 阶段,从50℃开始,随着温度的升高,膳食纤维质量缓慢地降低,可能是与膳食纤维中的水分损失有关;第2 阶段,温度在250℃左右,膳食纤维的质量开始显著减少,在450~500℃范围内失重放缓,与纤维的高温分解有关。最终TDF 的保留率为21.21%,其次是IDF 为19.77%,SDF 的保留率最低,为15.67%。SEM 表明TDF 与IDF 结构较SDF 更为紧致,需要更高的温度才能被降解。一般认为降解温度越高,纤维的热稳定性越好,其结晶度也越高[22]。综合XRD 分析结果,TDF 的结晶度最高,因此其稳定性最好。

图4 膳食纤维的热稳定性Fig.4 The TG of dietary fiber
2.4 膳食纤维基本特性
由表3可知,SDF、TDF 和IDF 3 种膳食纤维的WHC 分别为7.40,4.68 g/g 和6.48 g/g,OHC 分别为6.54,2.21 g/g 和5.73 g/g,SC 分别为6.62,4.07 mL/g 和1.75 mL/g,表明可溶性膳食纤维表现出更好的水合性能。持水性、持油性表示膳食纤维吸附小分子的能力,膨胀性表示因膳食纤维吸水而膨胀的能力[23],它们均与纤维的结构、化学组成、表面性质以及疏水亲油性能等有关[24]。SEM 结果表明SDF 的粒径较小且疏松多孔,比表面积大,因此暴露的亲水基团多,能够很好地吸附油和水等小分子物质而表现出好的水合性能[25-26]。
3 种膳食纤维的CEC 如表3所示。CEC 排序为:SDF(0.56 mmol/g)>TDF(0.459 mmol/g)>IDF(0.30 mmol/g),说明SDF 具有较强的阳离子吸附能力。膳食纤维CEC 的大小取决于不同数量的官能团,其主要受纤维结构中亲水基团的影响[27]。SDF 的粒径小,暴露的羟基和羧基等基团多,这些基团使其CEC 相对更强,能在短时间内降低某一阳离子浓度,从而影响肠道环境,给消化吸收提供缓冲环境[1]。
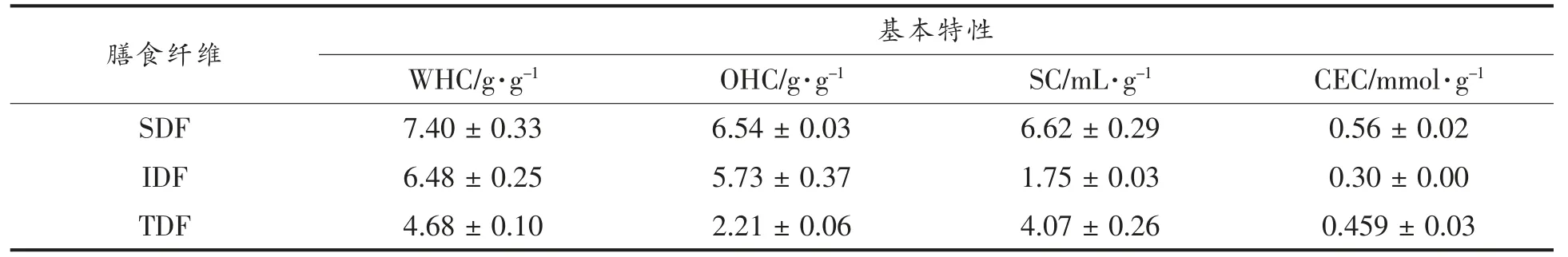
表3 膳食纤维的持水性、持油性、膨胀性及阳离子交换能力Table 3 WHC,OHC,SC and CEC of dietary fibres
2.5 膳食纤维的吸附性能
2.5.1 膳食纤维对亚硝酸根离子的吸附性NO2-是一种能够在体内与仲胺等物质结合并生成致癌物的活性离子,正常情况下,食物中膳食纤维对NO2-的吸附主要发生在胃部(pH=2),这可以保护胃部,进而避免或者减轻NO2-对人体的毒害作用[28]。膳食纤维对NO2-吸附性能是评价其品质的重要指标[29],本试验测定了SDF、TDF 和IDF 3 种膳食纤维吸附亚硝酸根离子的能力,结果如图6所示。当pH 值为2 时,SDF、TDF、IDF 3 种膳食纤维亚亚硝酸根离子的吸附量分别为4.65,6.30,6.20 μg/g,TDF 和IDF 对NO2-离子的吸附能力基本一致,均显著强于SDF 的吸附能力。当pH 为7时,3 种膳食纤维的亚硝酸根离子吸附量均显著降低,分别为2.41,3.31,2.87 μg/g,这主要是由于随着pH 值的增加,膳食纤维表面的负电荷密度增加,对亚硝酸根离子的排斥增加,降低了膳食纤维的吸附能力。
2.5.2 膳食纤维对胆酸钠的吸附性 通过SDF、TDF 和IDF 体外吸附胆酸钠试验,检测0 h 和12 h 时膳食纤维对胆酸钠的吸附量,结果如图7所示。当吸附时间为0 h 时,3 种膳食纤维的吸附性能差异显著,SDF 的吸附能力最好,为27.98 mg/g;其次是不溶性膳食纤维,吸附能力为18.18 mg/g;最后是TDF,为14.67 mg/g。当吸附时间为12 h时,SDF、IDF 以及TDF 3 种膳食纤维的胆酸钠的吸附量分别为29.73,18.46,15.44 mg/g,相较0 h有略微的增加,但吸附能力顺序保持不变。膳食纤维对胆酸钠吸附呈动态波动变化,这与体系内胆酸钠的浓度和吸附时间有一定关系。随着时间的推移或体系内胆酸钠浓度的增加,膳食纤维对胆酸钠的吸附量会逐渐增加至某一固定值附近波动,从而维持食物中脂肪的正常代谢,保证机体的正常生理活动[30-31]。SDF 在溶液中吸水膨胀形成呈网状结构的胶类物质,可吸附胆酸盐等小分子物质,因此,摄食高SDF 的食品能够更有效地降低人体中的胆酸盐,对人体更为有益。
3 结论
3 种膳食纤维因其单糖组成和形态的差异而表现出不同的结构特性和功能特性。SDF 粒径小、比表面积大,主要由阿拉伯糖(24.64%)与半乳糖(38.05%)2 种单糖组成,其糖类的红外特征吸收峰更为尖锐,结晶度相对较低,热稳定性较差,但水合特性、阳离子交换性能以及胆酸钠的吸附性能最好;IDF 和TDF 呈不规则片状结构,因TDF中IDF 含量高达80%以上,故2 种膳食纤维表现出相似的结构和功能性质。由此可见,单一的膳食纤维不足以体现膳食纤维所有优良的结构和功能特性,在今后的竹笋膳食纤维产品的开发中可按照适当的比例综合利用SDF 和IDF。

图5 膳食纤维对亚硝酸根离子的吸附性Fig.5 Adsorption capacity of dietary fiber to nitrite ion
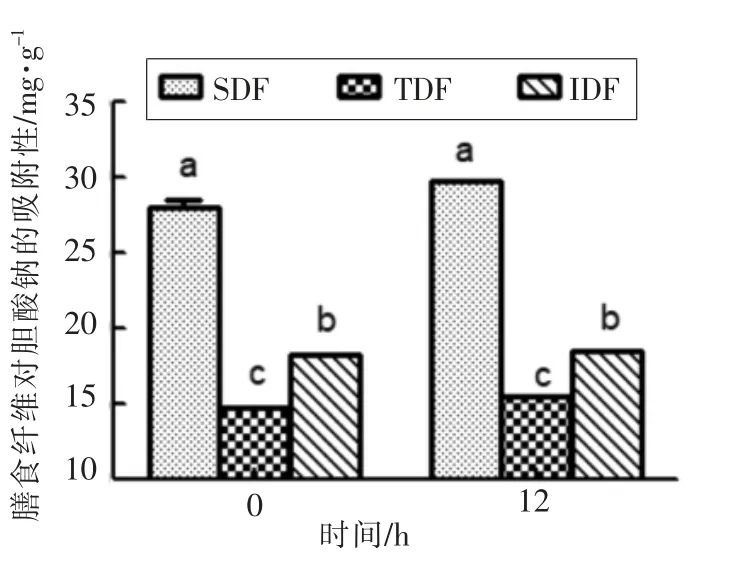
图6 膳食纤维对胆酸钠的吸附性Fig.6 Adsorption capacity of dietary fiber to sodium cholate

