PPV联合抗VEGF治疗增殖性糖尿病性视网膜病变远期疗效的Meta分析
胡文强,纪晓萍,周雪滨,邹 慧,高 阳,刘早霞
0引言
增殖性糖尿病性视网膜病变(PDR)主要表现为玻璃体出血、新生血管形成、纤维血管增殖和牵拉性视网膜脱离。如若不及时治疗,可导致视力进一步下降甚至失明。平坦部玻璃体切除手术(PPV)是PDR患者的主要治疗方法,包括清除玻璃体积血、去除纤维血管膜和解除玻璃体视网膜牵引。然而,PDR患者在PPV术中及术后可能会出现多种并发症,如术中出血、医源性视网膜裂孔、术后出血、视网膜脱离、新生血管性青光眼等,导致预后不理想。近年来,大量临床研究证明PDR患者PPV术前给予抗血管内皮生长因子(VEGF)药物治疗,可有效减少PDR患者手术时间,降低术中出血、医源性视网膜裂孔等并发症发生率,减少术中电凝使用频率,降低术中对视网膜的损害;术后玻璃体出血的发生率也显著降低[1-4]。然而,关于PPV术前行抗VEGF治疗对PDR患者术后视网膜脱离发生率、黄斑中心凹厚度的研究并不多,很多只是小样本随机对照研究和回顾性研究,存在一定的局限性。Arevalo等[5]研究发现,PPV联合抗VEGF治疗PDR患者术后视网膜脱离的发生率比未行抗VEGF治疗患者低,但无统计学差异(P=0.097)。然而,目前关于术前行抗VEGF药物治疗是否有助于降低PDR患者PPV术后视网膜脱离发生率尚无明确结论。本研究针对术前行抗VEGF治疗对PDR患者PPV术后视网膜脱离发生率、黄斑中心凹厚度、最佳矫正视力(BCVA)等远期疗效展开分析。
1资料和方法
1.1资料
1.1.1检索策略检索PUBMED、EMBASE、Cochrane Central Register of Controlled Trials(CENTRAL)、Web of Science等数据库建库至2020-07-02已正式发表的关于比较PPV术前是否行抗VEGF药物治疗PDR预后效果的临床随机对照试验(RCT),采用主题词与自由词相结合的检索方式,搜集检索词为“Proliferative diabetic retinopathy” OR “PDR”;“Vascular endothelial growth factors” OR “vascular endothelial growth factor” OR “anti-VEGF” OR “angiogenesis inhibitors” OR “VEGF” OR “VEGFs” OR “ranibizumab” OR “lucentis” OR “RhuFab V2” OR “bevacizumab” OR “avastin” OR “aflibercept “ OR “VEGF-Trap” OR “Conbercept”。
1.1.2纳入标准(1)研究对象:确诊的需要行PPV术治疗的1型或2型糖尿病合并PDR患者;(2)治疗方案:玻切组仅行PPV术,联合组PPV术前7d内给予玻璃体腔内注射抗VEGF药物治疗;(3)主要评判指标:术后发生视网膜脱离情况、黄斑中心凹厚度、BCVA;(4)设计原则:遵循随机对照原则。
1.1.3排除标准(1)纳入患者合并新生血管性青光眼、黄斑裂孔等其他影响视力的疾病,既往有PPV术或玻璃体腔抗VEGF药物治疗史;(2)PPV术前玻璃体腔内注射抗VEGF药物时间超过7d;(3)PPV术中需要联合白内障手术等;(4)PPV术毕及术后行玻璃体腔注射抗VEGF药物治疗。
1.2方法由2名研究者按照文献纳入和排除标准独立完成文献的筛查,详细阅读符合要求的文献摘要、全文并再次筛选和核对,如果遇到分歧,讨论解决或者由第三方独立裁定,并最终确定纳入研究的文献。提取研究所需的相关数据,包括作者姓名、发表年限、样本量、年龄、干预措施、结局指标、随访时间等。另外两名研究成员使用Cochrane偏倚风险工具进行文献质量评价[6]。任何差异均由审查小组中的其他调查员小组协商一致和仲裁解决。
统计学分析:采用Review Manager 5.3软件进行Meta分析。二分类变量采用相对危险度(risk ratio,RR)值作为效应指标,连续型变量采用均数差(mean difference,MD)值作为效应指标,各个效应量计算估计值和95%可信区间(confidence interval,CI)。采用Q值、I2统计量对数据进行异质性检验,若I2<50%、P>0.1,表明纳入的研究异质性无统计学意义,使用固定效应模型进行数据分析;若I2>50%、P<0.1,表明纳入的研究异质性具有统计学意义,则使用随机效应模型进行数据分析,比较结果以森林图表示并解释说明。采用StataSE15.1软件进行Egger检验评估文献的发表偏倚。以P<0.05为差异具有统计学意义。
2结果
2.1文献检索结果及质量评价初步检索文献4 487篇,多次筛选后,获得可能符合条件的文献全文118篇。本研究指定纳入文献至少要包括1项主要评判指标,严格按照纳入和排除标准,最终纳入11篇文献[1-3,5,7-13],涉及患眼880眼。文献筛选流程见图1,纳入文献的基本特征见表1。纳入的11篇RCT研究对3种不同抗VEGF药物进行分析,除Modarres等[1]玻璃体腔注射贝伐单抗(Bevacizumab)剂量采用2.5mg/0.1mL外,其余研究者均给予PDR患者玻璃体腔注射标准剂量抗VEGF药物:贝伐单抗1.25mg/0.05mL,雷珠单抗(Ranibizumab)0.5mg/0.05mL,康柏西普(Conbercept)0.5mg/0.05mL。对纳入的11篇RCT研究进行质量评价,偏倚属于中低风险,证据质量高,见图2。
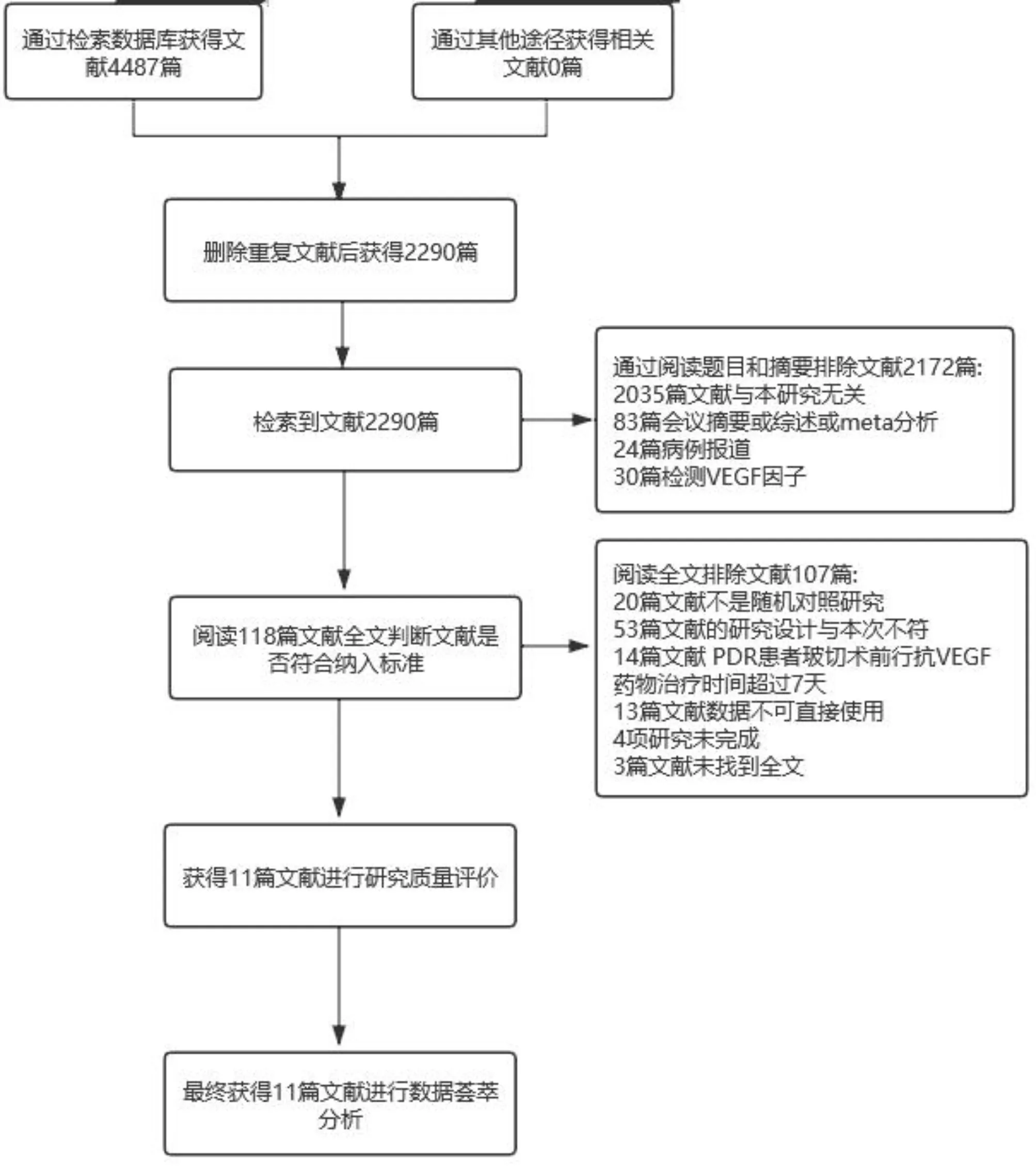
图1 文献筛选流程图。
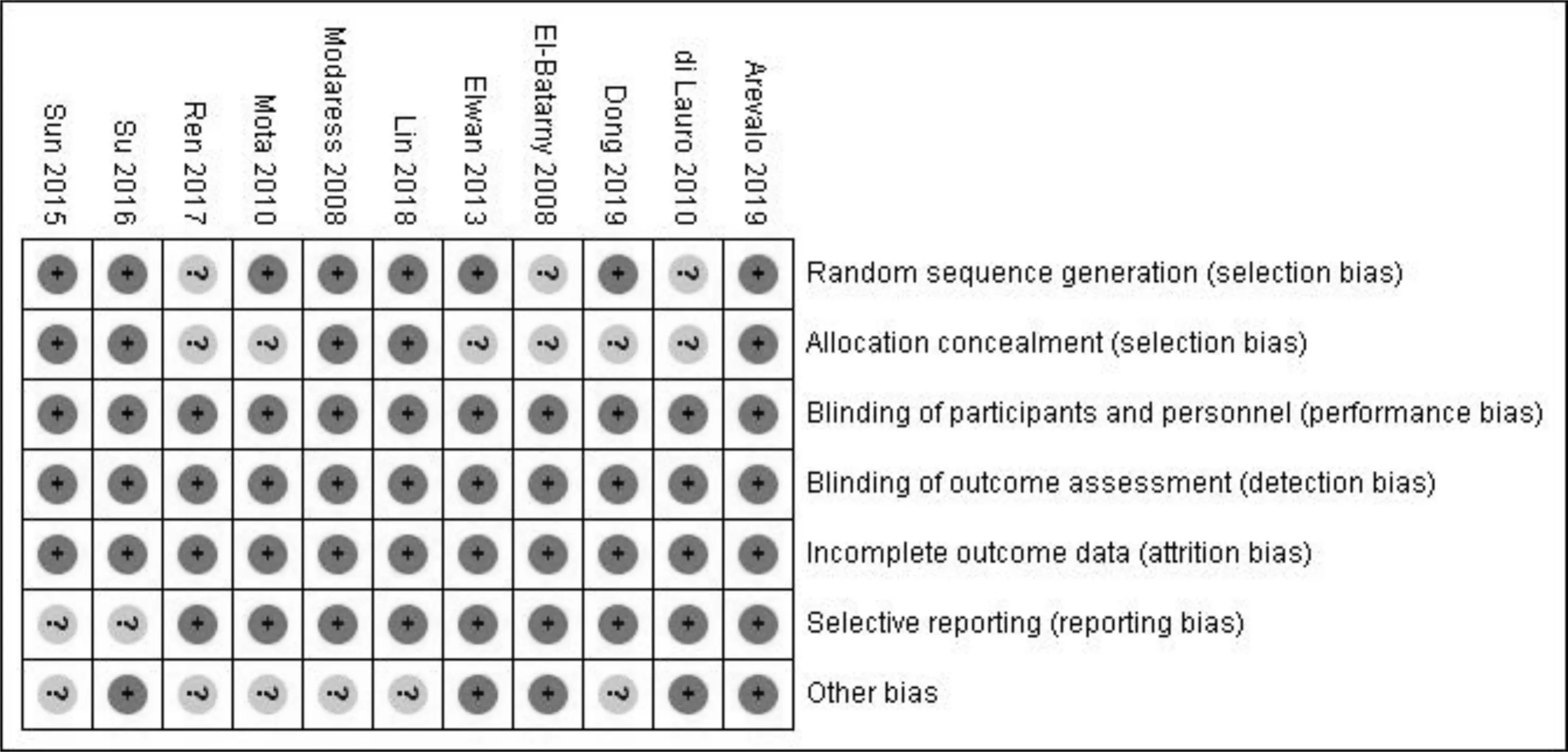
图2 纳入文献偏倚风险评估。

表1 纳入文献基本特征
2.2术后视网膜脱离情况纳入文献中8篇文献[1,3,5,7-9,11,13](676眼)比较了PPV术前行抗VEGF治疗与未行抗VEGF治疗的PDR患者术后视网膜脱离发生率,见表2。Meta分析显示各研究间具有同质性(I2=0,P=0.94),采用敏感性分析逐篇剔除文献,提示合并效应值稳健可信,见表3,故采用固定效应模型合并数据。森林图显示PPV术前行抗VEGF治疗与未行抗VEGF治疗的PDR患者术后视网膜脱离发生率差异具有统计学意义(RR=0.39,95%CI0.22~0.71,P=0.002),表明PPV术前行抗VEGF治疗可降低术后视网膜脱离发生率,见图3。
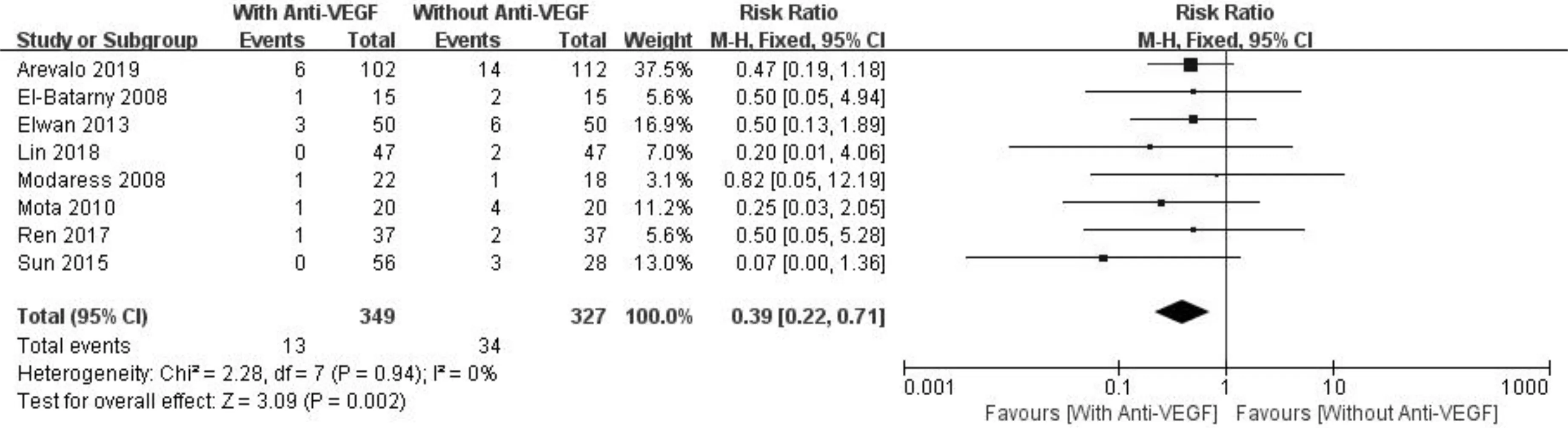
图3 术后视网膜脱离发生情况Meta分析森林图。

表2 术后视网膜脱离情况
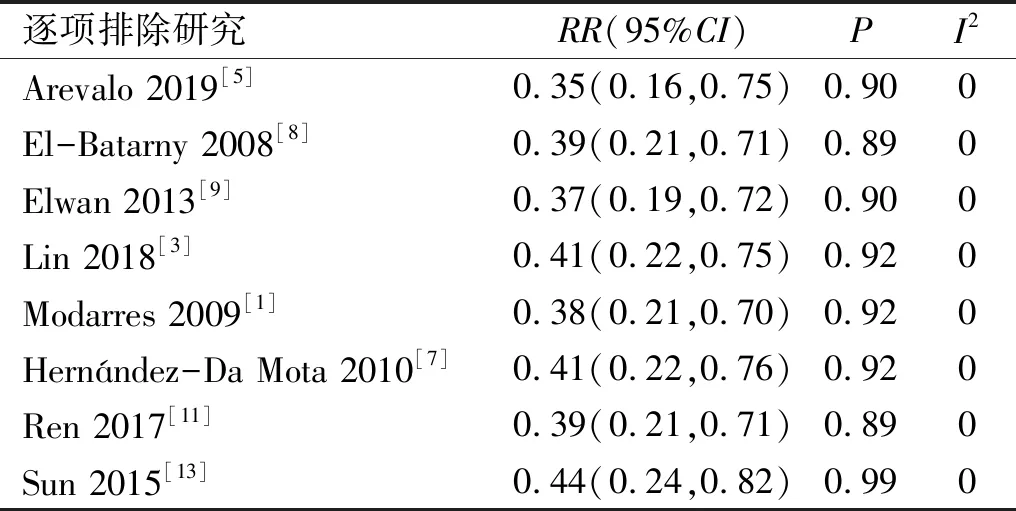
表3 术后视网膜脱离敏感性分析
对亚裔[3,11,13]和非亚裔[1,5,7-9]患者术后视网膜脱离发生率进行亚组分析,结果显示亚裔和非亚裔患者间无统计学异质性(I2=0,P=0.94)。3篇文献[3,11,13]报道了亚裔患者PPV联合抗VEGF治疗与单纯PPV术后视网膜脱离发生率,Meta分析显示各研究间具有同质性(I2=0,P=0.60),采用敏感性分析逐篇剔除文献,提示合并效应值稳健可信,见表4,因此采用固定效应模型分析。森林图显示PPV术前行抗VEGF治疗的亚裔PDR患者术后视网膜脱离发生率较未行抗VEGF治疗的患者低,差异具有统计学意义(RR=0.20,95%CI0.05~0.87,P=0.03),见图4。5篇文献[1,5,7-9]报道了非亚裔患者PPV联合抗VEGF治疗与单纯PPV术后视网膜脱离发生率,Meta分析显示各研究间具有同质性(I2=0,P=0.97),采用敏感性分析逐篇剔除文献,提示合并效应值稳健可信,见表4,因此采用固定效应模型分析。森林图显示PPV术前行抗VEGF治疗的非亚裔PDR患者术后视网膜脱离发生率较未行抗VEGF治疗的患者低,差异具有统计学意义(RR=0.46,95%CI0.24~0.89,P=0.02),见图4。
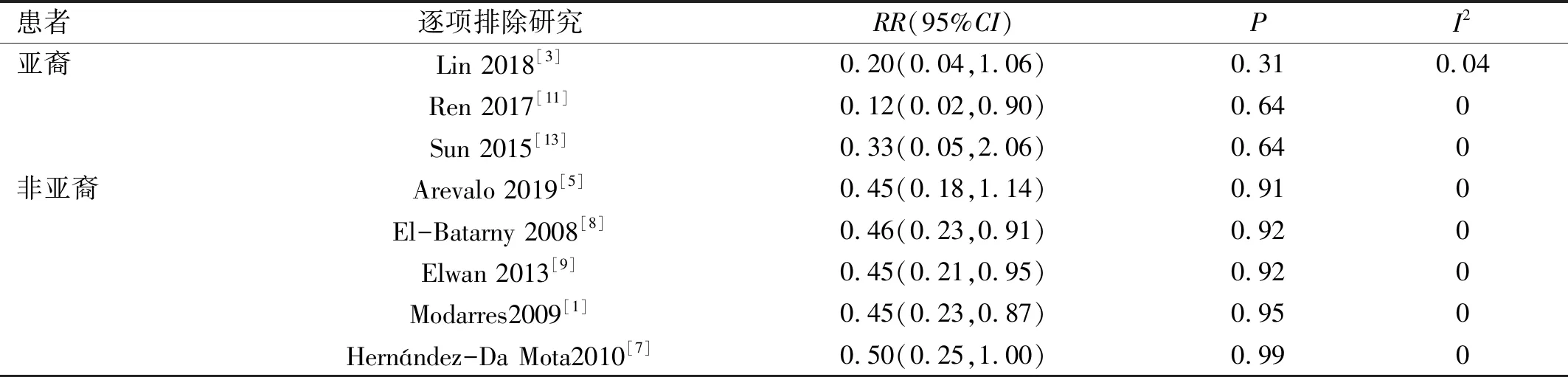
表4 亚裔与非亚裔患者术后视网膜脱离情况敏感性分析

图4 亚裔与非亚裔患者术后视网膜脱离情况Meta分析森林图。
2.3术后黄斑中心凹厚度纳入文献中2篇文献[3,11](168眼)比较了PPV术前行抗VEGF治疗与未行抗VEGF治疗的PDR患者术后3mo黄斑中心凹厚度,见表5。Meta分析显示各研究间有同质性(I2=27%,P=0.24),采用固定效应模型合并数据。森林图显示PPV术前抗VEGF治疗与未行抗VEGF治疗的PDR患者术后3mo黄斑中心凹厚度差异具有统计学意义(MD=-78.49,95%CI-94.81~-62.17,P<0.00001),表明PPV术前行抗VEGF治疗可有效降低术后3mo黄斑中心凹厚度,见图5。2篇文献[2,3](214眼)比较了PPV术前行抗VEGF治疗与未行抗VEGF治疗的PDR患者术后6mo黄斑中心凹厚度。Meta分析显示各研究间具有同质性(I2=22%,P=0.26),采用固定效应模型进行分析。森林图显示PPV术前行抗VEGF治疗与未行抗VEGF治疗的PDR患者术后6mo黄斑中心凹厚度差异仍具有统计学意义(MD=-39.62, 95%CI-48.44~-30.80,P<0.00001),表明PPV术前行抗VEGF治疗仍可有效降低术后6mo黄斑中心凹厚度,见图5。

图5 术后黄斑中心凹厚度Meta分析森林图。

表5 术后黄斑中心凹厚度
2.4术后最佳矫正视力6篇文献[1-3, 5, 8, 10](546眼)比较了PPV术前行抗VEGF治疗与未行抗VEGF治疗的PDR患者术后6mo BCVA,见表6。Meta分析显示各研究间具有异质性(I2=57%,P=0.04),因此采用随机效应模型进行分析。森林图显示PPV术前抗VEGF治疗与未行抗VEGF治疗的PDR患者术后6mo BCVA差异具有统计学意义(MD=-0.22,95%CI-0.34~-0.11,P<0.0001),表明PPV术前行抗VEGF治疗的PDR患者术后BCVA优于未行抗VEGF治疗的患者,见图6。 采用敏感性分析逐篇剔除文献,发现Dong 2019[2]研究是异质性的来源,见表7。剔除Dong 2019[2]研究后,Meta分析显示剩余5篇文献合并效应值稳健可信,采用固定效应模型合并统计量。森林图显示PPV术前行抗VEGF治疗的PDR患者术后6mo BCVA优于未行抗VEGF治疗的患者(MD=-0.16,95%CI-0.21~-0.10,P<0.00001),见图7,与之前结果一致,因此Dong 2019[2]研究的异质性对结果分析影响较小。
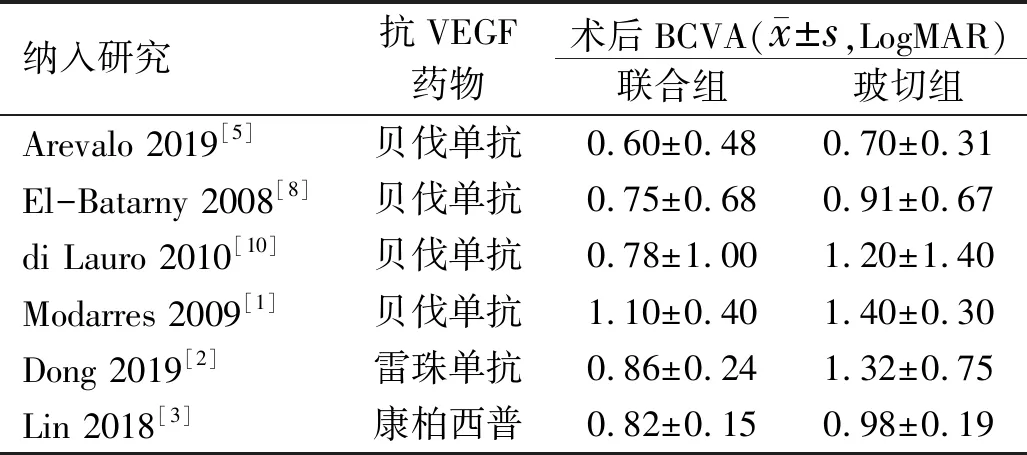
表6 术后最佳矫正视力
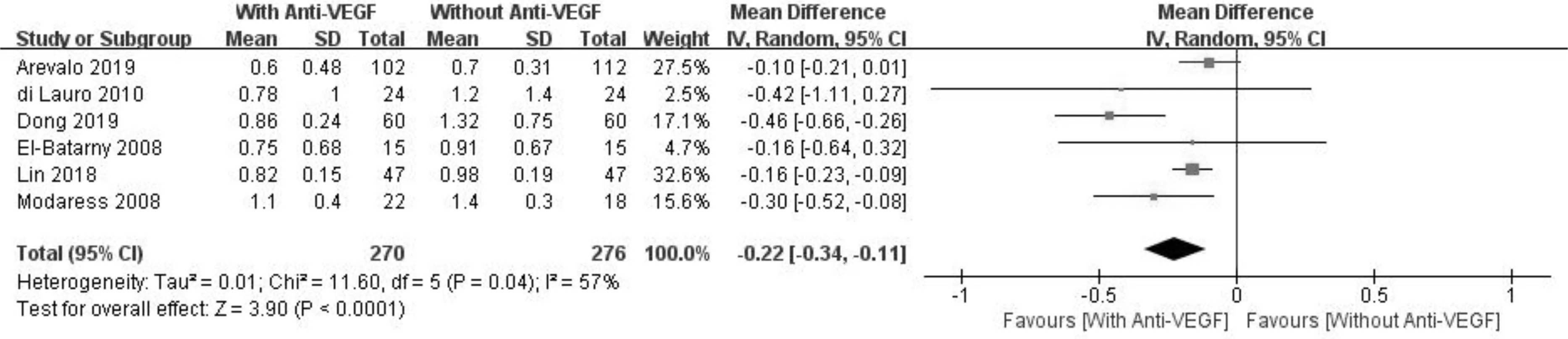
图6 术后BCVA Meta分析森林图(敏感性分析前)。

图7 术后BCVA Meta分析森林图(敏感性分析后)。
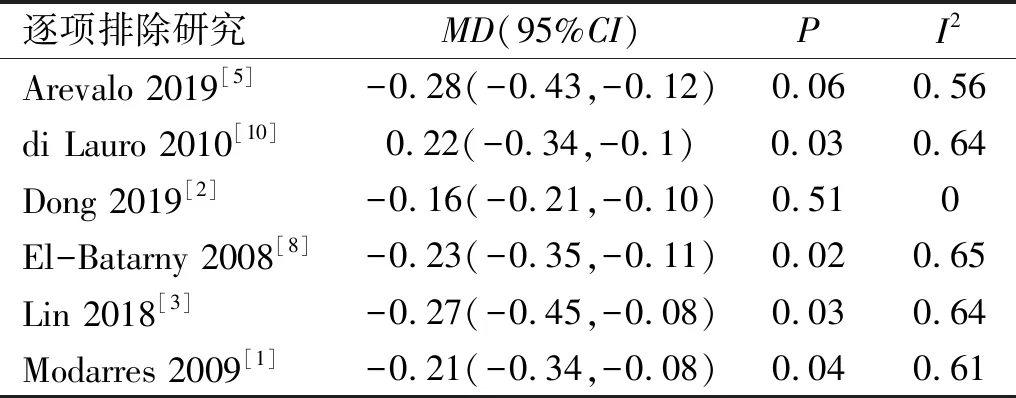
表7 术后最佳矫正视力敏感性分析
2.5发表偏倚采用StataSE15.1软件Egger 检验进行发表偏倚分析,结果显示术后发生视网膜脱离情况、黄斑中心凹厚度、BCVA发表偏倚P值分别为0.255、0.202、0.530,提示分析结果不存在发表偏倚。
3讨论
PDR由于微血管异常导致视网膜缺血、缺氧,诱导VEGF高表达,高浓度的VEGF刺激视网膜新生血管生成,毛细血管渗漏增加,引起糖尿病性黄斑水肿、玻璃体积血、纤维血管膜增生、牵拉性视网膜脱离等,出现严重视力障碍。术前玻璃体腔内注射抗VEGF药物可有效降低玻璃体腔VEGF水平,抑制炎症因子活动,从而减少视网膜血管渗漏,促使新生血管消退,继而降低术中出血的风险,有助于术中增殖膜的剥离[14-15]。El-Sabagh等[16]对不同时间段玻璃体腔注射抗VEGF药物后的增殖膜进行组织学分析发现,增殖膜上新生血管成分不断减少,收缩成分(肌动蛋白、胶原蛋白)显著增加,并逐渐转为促纤维化,尤其在药物注射后10d的转变尤为明显。Ishikawa等[17]研究指出,玻璃体腔注射抗VEGF药物7d后可能会加重视网膜新生血管纤维化,导致牵拉性视网膜脱离。 但目前对于围手术期注射抗VEGF药物的最佳时机仍有争议[18],本研究仅纳入注药7d内行PPV术的研究,尽量避免因注药时机不同对临床预后的影响。
本研究对PDR患者PPV术后视网膜脱离的发生情况进行荟萃分析,合并数据后显示没有异质性,结果表明术前行抗VEGF治疗可减少PDR患者PPV术后视网膜脱离的发生。然而这一结果与既往部分研究[3,5,19]结果明显不同,上述研究认为术前抗VEGF治疗与不抗VEGF治疗PPV术后视网膜脱离发生率没有显著性差异。出现这种结果可能是因为上述研究纳入的病例较少,视网膜脱离发生率低,统计学差异并不是很明显。本研究纳入多项RCT研究数据进行荟萃分析得出的结论更具说服力。分析其作用机制可能是抗VEGF治疗抑制VEGF表达,减少新生血管生成,降低了PDR患者术后早期和晚期出血的风险,抑制纤维血管膜再增殖,减少增殖膜因进一步牵拉而引起的视网膜脱离发生。
本研究对术后3、6mo黄斑中心凹厚度进行Meta分析发现,PPV术前行抗VEGF治疗的PDR患者术后黄斑中心凹厚度持续低于未行抗VEGF治疗的患者,表明PPV术前行抗VEGF治疗可有效缓解PDR患者术后黄斑水肿情况,并且发挥作用时间至少持续6mo以上。段松岚等[20]研究也得到相同结论。抗VEGF药物通过降低眼内VEGF浓度,抑制新生血管生成,同时降低血管的通透性,血管渗出减少,促进水肿吸收,表现为黄斑中心凹厚度降低,黄斑区视网膜形态显著改善,有效减轻了术后视力低下等不适症状的发生。
Murakami等[21]和Uji等[22]研究发现,PDR患者PPV术后6mo视力低下与黄斑中心凹光感受器损伤明显相关。De等[23]进一步研究揭示抗VEGF药物治疗可有效促进糖尿病性黄斑水肿患者中心凹光感受器损伤的修复(尤其是外界膜和椭圆体带区),视力明显改善。这也解释了为什么在本研究中抗VEGF治疗患者术后6mo BCVA 改善尤为明显。一方面,抗VEGF药物的使用有助于PDR新生血管消退,降低术中出血风险,改善手术视野,易于增殖膜剥离,减少术中医源性裂孔的发生和电凝使用频率,使术中对视网膜损伤大大降低。另一方面,抗VEGF药物也缓解了PDR患者术后黄斑水肿,并促进中心凹光感受器的恢复。
本研究也存在一定的局限性,我们对筛查到的文献进行了严格筛选,尽可能保证纳入文献的同质性,由于PPV术后发生视网膜脱离的情况较为罕见,需要较长随访期,相关研究较少,故纳入的RCT研究数量有限,但是为Meta分析提供了比单独报告更有力的证据。许多临床研究也发现,贝伐单抗、雷珠单抗和康柏西普三种抗VEGF药物在PDR患者PPV术中及术后的疗效基本一样[13,24-26],所以本研究未对三种抗VEGF药物进行亚组分析。受到纳入研究数量的限制,仅对视网膜脱离发生率进行了人种分析。同时,本研究也存在发表偏倚的可能性。因此,仍需要长期随访的随机对照研究进一步验证本研究结论。
综上所述,PPV术前行抗VEGF治疗可有效减少PDR患者术后视网膜脱离的发生,降低黄斑中心凹厚度,缓解术后黄斑水肿,提高视力,但玻璃体腔注射抗VEGF药物的时间和剂量仍需要进一步探究。
- 国际眼科杂志的其它文章
- An overview on dry eye disease diagnosis: options for new non-invasive testing technologies
- Change of subretinal fluid thickness and choroidal thickness after scleral buckling surgery
- 人翼状胬肉中miR-486-3p的表达及其潜在靶基因的生物信息学分析
- 重组人生长激素对兔角膜损伤早期修复的研究
- 基于SD-OCT建立新的前膜分级法评估IMEM对年龄相关性白内障患者术后视功能的影响
- 氯喹性视网膜病变的监测方法

