硫酸镁联合拉贝洛尔对妊娠高血压综合征患者炎性应激反应及血管内皮功能的影响
董高霞,王晓丽,齐 慧
(山东第一医科大学附属聊城二医院产二科,山东 临清 252600)
妊娠高血压综合征(PIHS)是妊娠期特有性疾病,发病率为5%~12%,高血压、水肿、蛋白尿等为临床主要表现,如不及时治疗会威胁母婴健康[1]。硫酸镁可通过拮抗乙酰胆碱生成、释放镁离子、舒张血管等多种途径,控制血压水平。拉贝洛尔是一种兼具阻断肾上腺素α、β受体阻滞剂,可通过抑制肾上腺素分泌、降低外周血管阻力等途径实现降压目的[2]。硫酸镁联合拉贝洛尔可从不同作用路径发挥协同降压效果。PIHS发病机制尚未完全清楚,可能与炎症浸润、氧化应激、血管内皮功能受损等因素有关[3,4]。硫酸镁联合拉贝洛尔治疗是否通过抑制炎症浸润及氧化应激、调节血管内皮功能等途径发挥治疗作用,目前尚缺乏足够的文献报道,也一定程度影响到研究的深度及广度。本文主要分析硫酸镁联合拉贝洛尔PIHS临床疗效及可能作用机制。
1 资料与方法
1.1 一般资料2018年10月至2019年12月我院收治的PIHS患者96例,均符合中华医学会PIHS[5]诊断标准,PIHS分型参照1983年我国第二届妊高征防治科研协作会议[6]分为轻度(血压>130/100 mmHg,或基础血压升高30/15 mmHg,伴有轻度蛋白尿或水肿)、中度(160/100 mmHg>血压>104/100 mmHg,尿蛋白+,伴水肿及轻度头晕症状)、重度(血压>160/100 mmHg,伴水肿及头痛症状);单胎;患者均知情同意。排除心肝肾等严重脏器功能障碍者、对本次研究药物过敏者。96例患者年龄24~38岁,孕周32~38周,初产妇73例,经产妇23例。采用分层随机分组的方法(即将不同年龄、孕周、产次、PIHS分型进行分层,再随机分配到两组)分为试验组和对照组各48例,两组患者基线资料比较,差异无统计学意义(P>0.05)。见表1。
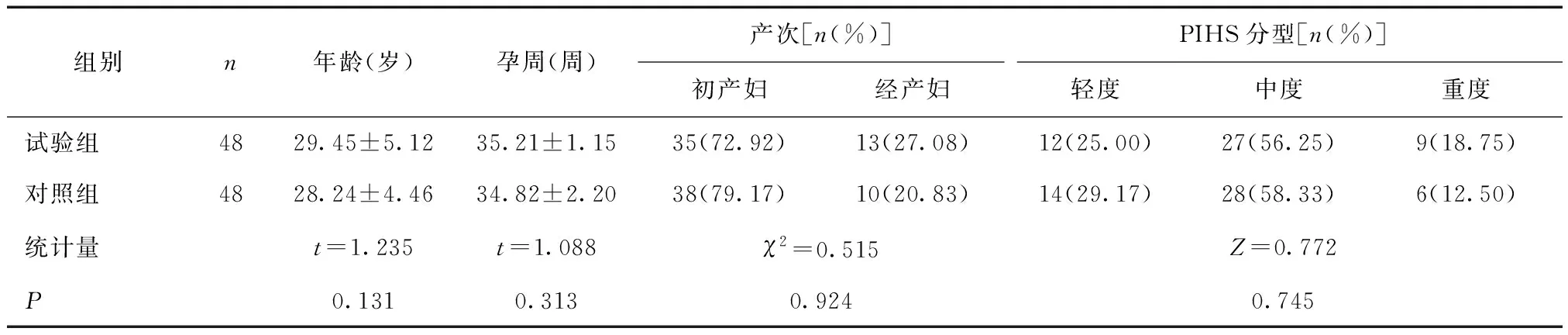
表1 两组PIHS患者基线资料比较
1.2 方法①两组均给予妊娠期高血压疾病患者给予分层、分类管理。妊娠期高血压者给予休息、镇静,监测母儿情况,酌情降压治疗;重度妊娠期高血压按重度子痫前期处理;子痫前期者采用有指征地降压、利尿和纠正低蛋白血症,预防抽搐,镇静,密切监测母儿情况,预防和治疗严重并发症的发生,适时终止妊娠。②对照组同时给予硫酸镁(哈药集团,国药准字H23022445)静脉滴注,首剂20 ml硫酸镁加入20 ml 5%生理盐水中,如无不适症状(30 min),则60 ml硫酸镁加入1000 ml 5%生理盐水中,维持滴注(8~12 h)。1次/天。③试验组给予硫酸镁联合拉贝洛尔(江苏赛诺制药,国药准字H32026122)治疗。硫酸镁同对照组。拉贝洛尔口服,2片/次,3次/天。两组均连续治疗至分娩前。
1.3 观察指标①炎性应激反应:治疗前后,采集患者空腹静脉血4 ml取血清,采用日立7600全自动生化分析仪检测血清白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)、丙二醛(MDA)、超氧化物歧化酶(SOD)含量。②血管内皮功能:治疗前后,同上取血清,检测血浆内皮素(ET)、一氧化氮(NO)。③血压控制:治疗前后采用便携式血压计测量收缩压(SBP)、舒张压(DBP)。④分娩方式及母婴结局。
1.4 统计学方法应用SPSS 20.0软件对数据进行分析处理。计量资料以均数±标准差表示,组间比较采用t检验;计数资料以[n(%)]表示,比较采用χ2或Z检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者炎性应激反应比较与同组治疗前比较,两组PIHS患者IL-6、TNF-α、MDA降低,SOD升高(P<0.05),且试验组IL-6、TNF-α、MDA低于对照组,SOD高于对照组(P<0.05)。见表2。
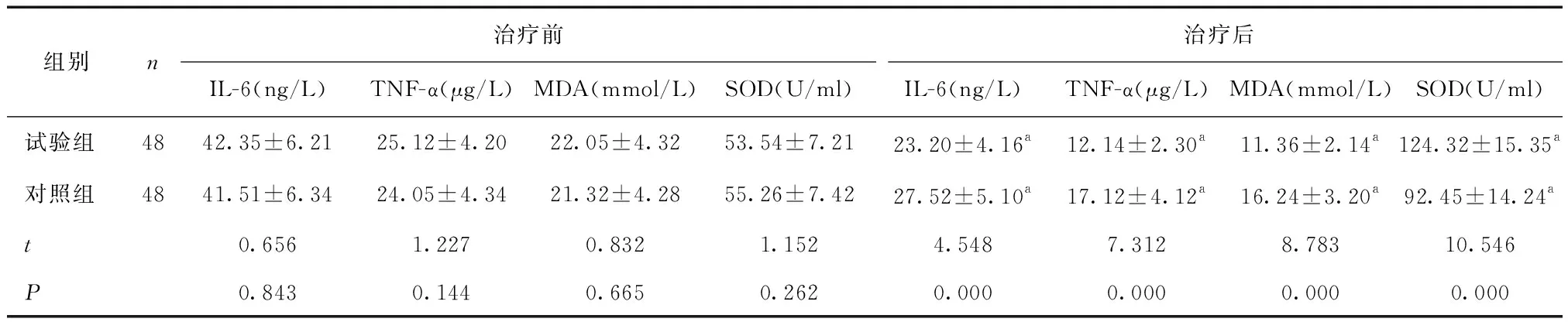
表2 两组PIHS治疗前后炎性应激反应比较
2.2 两组患者血管内皮功能与血压控制水平比较
治疗后,两组PIHS患者ET、SBP、DBP均低于治疗前,NO高于治疗前(P<0.05),且试验组患者ET、SBP、DBP低于对照组,NO高于对照组(P<0.05)。见表3。
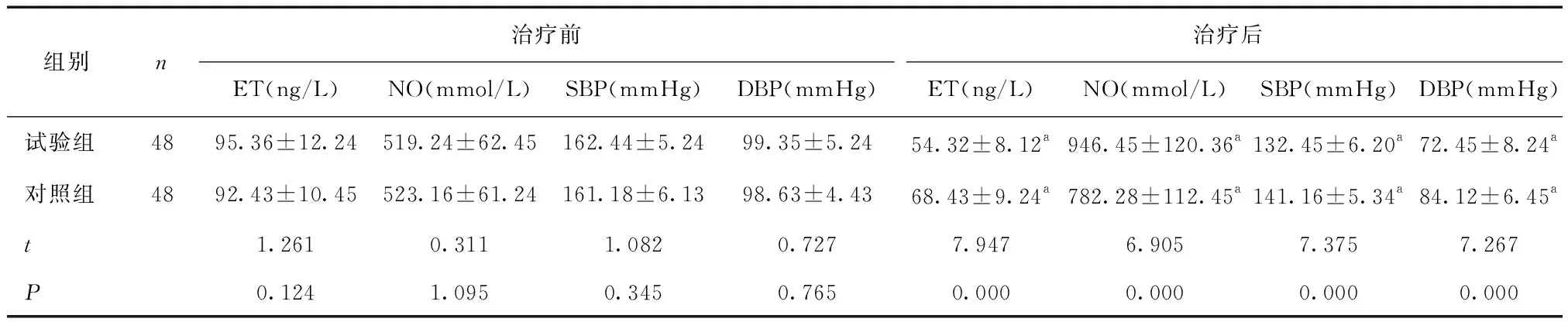
表3 两组PIHS患者治疗前后血管内皮功能及血压控制水平比较
2.3 两组患者分娩方式及母婴结比较试验组PIHS患者顺产率高于对照组,早产、新生儿窒息、胎儿窘迫发生率低于对照组(P<0.05)。见表4。
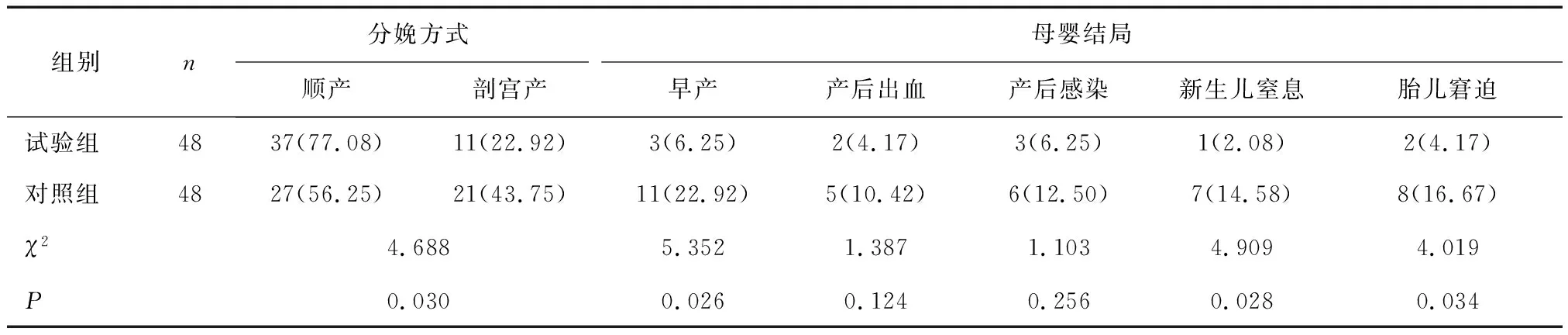
表4 两组分娩方式及母婴结局比较 [n(%)]
3 讨论
我国PIHS发病率为9.4%,随着生活水平提高及二胎政策放开,肥胖及高龄产妇逐渐增加,PIHS发病率近年也呈上升趋势[7]。PIHS治疗基本原则为镇静、解痉、降压、利尿等,硫酸镁可通过Mg2+刺激乙酰胆碱释放,阻断神经与肌肉间的信息传导。也能促进前列腺素合成,缓解血管痉挛状态[8]。但单独应用在促进血管扩张、控制血压水平、减少尿蛋白等方面效果不佳,长期大剂量应用也有诱发镁中毒的风险[9]。
拉贝洛尔作为常用肾上腺素受体阻断剂,能选择性地拮抗交感神经系统α1肾上腺素受体,抑制肾素分泌,舒张血管,减少外周血管阻力[10]。也能非选择性地拮抗β2肾上腺素受体,抑制心肌和血管平滑肌收缩,增加冠状动脉血流灌注,缓解冠状动脉痉挛,实现降低血压的目的[11]。硫酸镁联合拉贝洛尔可通过抑制乙酰胆碱和钙离子释放、拮抗肾上腺素受体等不同途径,发挥协同作用。相关研究证实,拉贝洛尔α受体阻滞能大幅降低心肌耗氧量,β受体阻滞能抑制房室传导控制心率,可实施快速稳定降压的效果,能够弥补硫酸镁单独应用降压缓慢且易反弹的缺陷[12,13]。拉贝洛尔是中国《妊娠期高血压疾病诊治指南(2020)》[14]、美国妇产科医师学会《妊娠期高血压和子痫前期指南2019版》[15]均推荐的证据等级为Ⅰ-A级的降压药物,因其主要通过降低外周血管阻力途径降低血压,不会明显改变母体心率及胎盘血流灌注,被许多委员会专家认为拉贝洛尔可作为治疗轻中度妊娠期高血压的一线治疗药物。颜亚美[16]研究报道,拉贝洛尔联合硫酸镁治疗能更好控制PIHS患者(37例)血压水平,改善母婴结果。本文通过比较两组PIHS患者SBP、DBP、分娩方式及母婴结局等指标,所得结论也支持上述文献观点。
高血压属于一种慢性炎症浸润性疾病,小动脉痉挛也会诱导血管内皮细胞损伤,加重炎症浸润程度。胎盘氧化应激也是诱发PIHS的重要因素[17]。IL-6可通过激活血小板、诱导血小板聚集等途径,损伤血管内皮细胞,引起动脉痉挛,诱导血压升高。TNF-α可通过激活氧自由基、选择性结合血管内皮受体等途径,诱导血管内皮细胞损伤[18]。MDA属于反映组织中自由基水平与脂质过氧化损伤程度敏感指标。SOD是一种抗氧化酶,可防御机体氧自由基破坏与损伤。硫酸镁可通过抑制神经末梢乙酰胆碱释放、下调平滑肌细胞Ca2+水平等途径,达到缓解氧化应激、舒张血管的作用[19]。也可通过释放Mg2+增强抗炎消肿效果。拉贝洛尔是作用于动脉平滑肌上的药,可呈剂量依赖性的抗炎、抗氧化、促进血管扩张[20]。两者抗炎、抗氧化路径存在差异,联合应用能发挥多靶点治疗效果。吴海荣等[21]研究报道,硫酸镁联合拉贝洛尔能有效降低PIHS患者血清hs-CRP水平。谢桂英等[22]研究发现,拉贝洛尔联合硫酸镁能下调血清(TNF-α、CRP)水平,改善中重度PIHS患者(60例)妊娠结局。本文研究中,试验组PIHS患者血清IL-6、TNF-α、MDA低于对照组,SOD高于对照组,说明硫酸镁联合拉贝洛尔可能通过拮抗炎症浸润、缓解氧化应激,发挥治疗PIHS的作用,这也可能是拉贝洛尔联合硫酸钡治疗妊娠期高血压疾病的主要作用机制之一。
血管内皮功能受损是PIHS主要发病机制之一,主要表现为血管内皮修复与损伤平衡受到破坏。ET、NO分别为反映血管收缩、血管舒张的血管活性因子,一旦血管内皮功能受损,ET合成增加,NO合成减少,会诱导血管痉挛、血压升高[23]。硫酸镁能够通过抑制内皮素合成、降解血管紧张素Ⅱ反应、拮抗平滑肌Ca2+浓度升高等多种缓解血管内皮功能损伤作用路径[24]。拉贝洛尔通过拮抗α、β肾上腺素受体,解除血管痉挛,增加冠状动脉血流灌注[25]。从结果上分析,试验组PIHS患者ET低于对照组、NO高于对照组,与田宁[26]文献报道基本相似。
综上,硫酸镁联合拉贝洛尔疗治疗PIHS患者,可能通过拮抗炎症浸润、缓解氧化应激反应、调节血管内皮功能等途径,达成控制血压、改善妊娠结局的目的。硫酸镁联合拉贝洛尔通过何种协同机制、作用路径影响炎性应激反应、血管内皮功能,后续将作进一步研究。

