精准外科时代3 D可视化技术在肝癌切除术中的应用价值
张光亚,金鑫,王治伟,高王军
安康市中心医院普外科,陕西安康725000
肝癌是目前世界上病死率最高的恶性肿瘤之一,肝切除术是原发性肝癌的主要治疗方法。由于肝内血管、胆管分支复杂且多变异以及肝肿瘤与大血管关系密切,使得肝癌手术难度大、风险高。随着科技的不断进步,包括影像学、数字外科等新技术的兴起,外科实践的确定性得到了显著提升,有可能实现病灶清除、脏器保护和损伤控制这3个要素的平衡,从而最终实现外科治疗的优化。精准外科这一新型外科范式的核心理念和科学内涵是立足于手术安全性、治疗有效性、干预微创化和合理效费比4个维度的交集上,给予恰当的干预,获取病灶清除、脏器保护和损伤控制3个外科要素的最大公约数,从而实现外科实践最优化和患者获益最大化的终极目标。随着数字化技术的发展,3D可视化与医学影像技术的相互融合使肝癌的早期诊断和治疗有了明显进步。本研究探讨了精准外科时代3D可视化技术在肝癌切除术中的应用价值,现报道如下。
1 对象与方法
1.1 研究对象
选取2017年6月至2019年6月于安康市中心医院接受治疗的100例原发性肝癌患者。纳入标准:①经病理检查确诊为原发性肝癌;②符合原发性肝癌切除术适应证;③首次确诊,未接受过手术或放化疗治疗;④Child-Pugh分级为A或B级;⑤临床资料完整。排除标准:①以往接受过腹部手术;②具有肝脏切除史;③合并其他恶性肿瘤或其他重大疾病;④肝癌细胞已发生远处转移;⑤近3个月内发生过呼吸道大出血和严重感染等疾病。采用随机数字表法将患者分为3D组和常规组,每组50例,3D组患者实施3D可视化技术辅助肝癌切除术,常规组患者实施常规肝癌切除术。两组患者的性别、年龄、肝炎病史、合并疾病情况等基线特征比较,差异均无统计学意义(P
﹥0.05)(表1),具有可比性。本研究经医院伦理委员会审核通过,所有患者及家属均对本研究知情并签署知情同意书。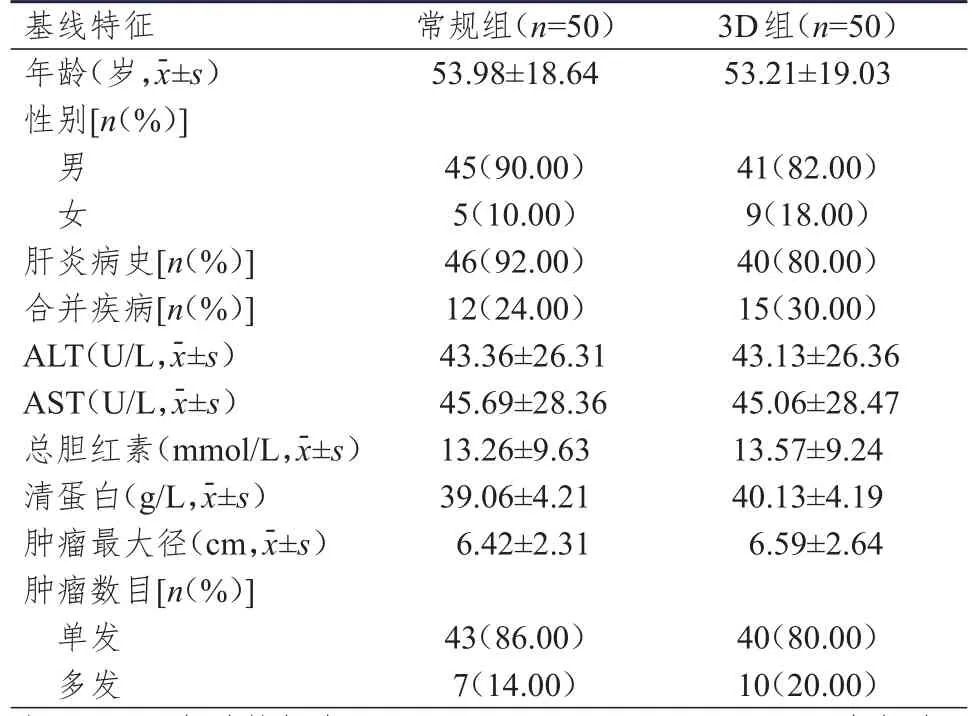
表1 两组患者的基线特征
1.2 治疗方法
1.2.1 术前评估及手术规划常规组:手术前对患者的身体机能进行检查,检查项目主要包括肝功能指标、凝血功能指标、心肺功能指标、上腹部增强CT等。测定肝功能指标的主要目的是对肝脏的储备功能进行评估,肝脏切除术后对剩余肝脏体积的计算与评估需借助术前CT检查,通过CT检查以及术中主刀医师对患者肝脏实际癌变情况和病变体积进行大致目测,选择切除体积。术前规划的制订主要是通过观察患者的术前CT图像,凭借术者的临床经验及空间想象力进行大致估测,再结合术中情况临时调整。
3D组:手术前对患者的身体机能进行检查,在常规检查的基础上另增加以下检查步骤。第一步,对患者进行个体化三维可视化建模,即先对患者进行上腹部增强CT扫描,扫描设备及参数如下:管电流250 mAs,管电压120 kV,层厚和层间隔均为0.625 mm,双筒高压注射器匀速注射浓度较高(300~500 mg/ml)的非离子型碘对比剂,扫描时相包括平扫、动脉期、门脉期、静脉期及延迟期。扫描完成后,重建和探测器准直宽度、层厚度相同的薄层图像,16层CT层厚为1.000~1.500 mm,层间隔为0.800~1.000 mm,64层CT层厚为0.500~0.625 mm,层间隔为0.400~0.500 mm。将CT扫描图像以DICOM格式保存后导入三维人体可视化成像系统进行重建,将薄层CT数据导入腹部医学图像三维可视化系统(medical imaging three dimensional visual system,MI-3DVS)进行肝脏实体、管道系统及肿瘤的三维可视化,通过旋转、放大及透明化操作,在三维可视化模型上对肝动脉、肝静脉、胆管系统的走行、是否存在变异、管道与肿瘤的空间关系进行观察分析。第二步,对患者的肝脏进行个体化分段,根据患者体内肝静脉及门静脉的脉络及行走方向,利用MI-3DVS对患者的肝脏进行个体化分段,对患者肝脏中肿瘤的位置进行精确定位。第三步,定位完成后对患者进行手术规划,根据患者肝组织中肝癌细胞的位置以及动脉和静脉管的关系,在3D可视化模型中进行预切线的划定,并进行反复模拟,确保切除病变组织的同时,尽可能多地保留正常肝组织,在此操作原则下,确定采取3D可视化技术切取的最合理的肝面积。第四步,在模拟演练达到要求后进行仿真手术的演练,即将STL格式的三维重建文件导入虚拟手术器械仿真系统中,开始进行手术前的仿真练习手术,并明确、清晰地认识和了解手术中必须隔离和切断及可以保留的管道、需要放弃或者保护的肝段及切缘等信息,便于手术中指导医师进行操作,避免因术中操作不当导致的损伤。
1.2.2 术中操作常规组:实施常规肝癌切除术,切除范围主要依据对人体解剖的生理认知及主刀医师的临床经验确定,切除肝癌组织的边界需要距离正常肝组织≥1.5 mm,且根据切除组织的范围及大小,需要采用超声刀离断肝实质,配合电灼、结扎、缝扎等临床缝合方法,仔细处理肝组织的血管管道结构。
3D组:实施3D可视化技术辅助肝癌切除术,即肝癌切除术前需要详细分析患者肝脏的3D可视化模型,确定即将要切除的肝组织,并将设计的肝组织模型带到手术室,作为手术过程中的参考模型,进一步对患者的肝切除面及肝内脉管位置和走形进行定位,充分确定术中情况与3D可视化模型相互匹配后,离断较大的管道系统,开始手术操作。
常规组与3D组在手术实施过程中均采用相同型号的超声刀离断肝实质,且由同组医师进行操作。
1.3 观察指标
1.3.1 手术情况比较两组患者的手术情况,包括术中出血量、肝门阻断时间、手术时间、实际切除肝体积。
1.3.2 肝功能指标分别于术后第1天、第3天、第5天抽取两组患者的空腹静脉血5 ml,置于抗凝管中,4000 r/min离心8 min,取上清液,检测丙氨酸转氨酶(alanine aminotransferase,ALT)、天冬氨酸转氨酶(aspartate aminotransferase,AST)水平。
1.3.3 肝功能损伤程度分别于术后第3天、第7天、第10天、第14天抽取两组患者的空腹静脉血3 ml,置于抗凝管中,血液采集2 h内检测凝血酶原时间和总胆红素水平,同时监测肝性脑病、腹腔积液等术后并发症的发生情况,以此评定术后肝功能损伤程度。依据总胆红素水平评分:0分,总胆红素水平为3.4~17.1 μmol/L;1 分,17.1 μmol/L﹤总胆红素水平≤34.2 μmol/L;2分,34.2 μmol/L﹤总胆红素水平≤51.3 μmol/L;3分,总胆红素水平﹥51.3 μmol/L。依据凝血酶原时间(prothrombin time,PT)延长时间评分:0分,PT延长时间﹤3 s;1分,3 s≤PT延长时间﹤4 s;2分,4 s≤PT延长时间≤6 s;3分,PT延长时间﹥6 s。依据腹腔积液评分:0分,无腹腔积液;1分,仅有少量腹腔积液;2分,腹腔积液处于中等程度;3分,大量腹腔积液。依据肝性脑病评分:0分,无肝性脑病;1分,肝性脑病处于Ⅰ~Ⅱ期;2分,肝性脑病处于Ⅲ~Ⅳ期。各个指标的评分相加,0分为无损伤,1~2分为轻度损伤,3~4分为中度损伤,﹥4分则为重度损伤。
1.3.4 术后并发症发生情况比较两组患者的术后并发症发生情况,主要包括切口感染、肺不张、肺部感染、肠梗阻、腹腔积液、胸腔积液、胆漏、单器官衰竭。
1.3.5 术后 1年生存及复发情况采用电话或门诊方式对患者进行随访,患者出院后半年内每个月随访1次,半年后每3个月随访1次。随访内容主要包括甲胎蛋白检测、上腹部CT或MRI检查等。记录两组患者的1年生存及复发情况。
1.4 统计学方法
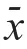
2 结果
2.1 手术情况的比较
3D组患者的术中出血量明显少于常规组,肝门阻断时间和手术时间均明显短于常规组,差异均有统计学意义(P
﹤0.01)。两组患者的实际切除肝体积比较,差异无统计学意义(P
﹥0.05)。(表2)
表2 两组患者手术情况的比较
2.2 肝功能指标的比较
术后第1天、第3天、第5天,3D组患者的ALT和AST水平均低于常规组,差异均有统计学意义(P
﹤0.05)。(表3)
表3 术后不同时间点两组患者肝功能指标的比较(U/L,± s)
2.3 肝功能损伤程度的比较
3D组患者的肝功能损伤程度明显小于常规组,差异有统计学意义(Z
=29.899,P
﹤0.01)。(表4)
表4 两组患者的肝功能损伤程度[ n(%)]
2.4 术后并发症发生情况的比较
3D组患者的术后并发症总发生率为18.0%(9/50),明显低于常规组的56.0%(28/50),差异有统计学意义(χ
=15.487,P
﹤0.01)。(表5)
表5 两组患者的术后并发症发生情况[ n(%)]
2.5 生存及复发情况的比较
3D组患者的1年生存率高于常规组,1年复发率低于常规组,差异均有统计学意义(P
﹤0.05)。(表6)
表6 两组患者生存及复发情况的比较[ n(%)]
3 讨论
精准外科是以对患者病情的精确评估和预后的准确判断为基础,依据循证医学法则,结合患者需求与医者经验进行最优化的临床决策,继而通过高精度、高效度和可控性手术作业及围手术期处理实现预期的治疗目标。肝癌切除术的3D可视化技术是将CT或MRI二维影像数据进行重建,然后转化为数字化三维可视化肝模型。这种技术便于直观、全方位地进行肝实质、脉管系统及目标病灶的信息采集,清晰、透明地呈现各管道、病灶及组织的空间位置、毗邻关系等,解决了CT、MRI图像模糊、不稳定、抽象的问题。更为重要的是3D可视化技术可根据病灶切除的需要,对各个部位进行旋转、缩放、切割、拖拽、隐藏等操作,将计算机技术、医学成像技术及图像处理技术结合,划定手术切除线,建立切除平面,自动计算切除病灶体积、残余肝体积及标准全肝体积,评估切除的可行性和风险。
本研究采用3D可视化技术对患者的三维影像数据进行处理,使目标病灶、肝内胆管、肝静脉、肝动脉、门静脉等结构重建成像,依靠三维成像图分析其分支走形、空间位置,确定各脉管的支配区域;应用虚拟手术功能,划定手术切除线,沿最小损伤、最大获益的路径切除病灶,且自动评估切除的可行性与风险。本研究对患者的术前基线特征进行比较,结果发现,两组患者的性别、年龄、肝炎病史、合并疾病情况、肝功能指标等比较,差异均无统计学意义(P
﹥0.05),表明本研究具有可操作性。本研究结果显示,3D组患者的术中出血量明显少于常规组,肝门阻断时间和手术时间均明显短于常规组,差异均有统计学意义(P
﹤0.01)。两组患者的实际切除肝体积比较,差异无统计学意义(P
﹥0.05);术后第1天、第3天、第5天,3D组患者的ALT和AST水平均低于常规组,差异均有统计学意义(P
﹤0.05);3D组患者的肝功能损伤程度明显小于常规组,差异有统计学意义(P
﹤0.01)。说明将3D可视化技术应用于肝癌切除术中能够有效减轻对机体造成的损伤,减少术中出血量,缩短肝门阻断时间和手术时间,增加了手术的安全性。分析原因主要是3D可视化技术能够全方面地对病变部位和大小、全肝体积、残肝体积等相关参数进行评定,同时又结合术前其他资料,进一步提高了术前评估的准确性,同时也由于3D模型能够清晰直观地显示肝组织的解剖结构,使肝脏的脉络管及病变部位清晰地呈现,有利于精准切除方案的制订与实施。本研究结果与Fang等的研究结果一致,均表明3D可视化技术能够有效地提高肝癌切除术的准确度。本研究结果还显示,3D组患者的术后并发症总发生率明显低于常规组,差异有统计学意义(P
﹤0.01),3D组的并发症种类和发病人数均少于常规组;3D组患者的1年生存率高于常规组,1年复发率低于常规组,差异均有统计学意义(P
﹤0.05)。表明将3D可视化技术应用于肝癌切除术中可以有效降低术后并发症发生率,提高生存率,降低复发率,与Kawaguchi等研究结果相符,通过3D可视化技术构建模型对患者病变部位进行精确定位,进一步提高了手术的可操作性与精准度。本研究通过3D可视化技术对患者的肝脏进行建模,通过术前精确评估、完善手术规划以及反复进行虚拟手术练习,并将构建的3D可视化模型带入手术室指导手术,使手术操作的精准度得到有效提升,从而有效降低了术后并发症发生率,延长了患者的生存时间。综上所述,将3D可视化技术应用于肝癌切除术中能够有效减轻患者肝组织的损伤程度,减少术后并发症,延长患者的生存时间,具有良好的应用价值。

