早期血运重建及体外膜肺氧合支持治疗急性心肌梗死合并心原性休克的疗效观察及影响因素分析
韩宗茂,高洁,高传玉,张优,张静,朱中玉,齐大屯,黑飞龙,Rafiq Ahmed BHAT
急性心肌梗死(AMI)合并心原性休克是一种由心脏泵血功能障碍导致的外周器官和组织灌注不足,出现以缺血缺氧及重要脏器受损为特点的急危重症,发生率约3%~13%[1]。血运重建治疗已得到认可及广泛实施,但患者的死亡率仍居高不下。机械循环支持(MCS)如体外膜肺氧合(ECMO)和主动脉内球囊反搏(IABP)可在患者急性循环障碍时部分替代心脏功能,提高血流灌注的同时降低后负荷,维持患者循环稳定,为心肌复苏创造条件[2]。本研究旨在探讨早期血运重建及ECMO 支持治疗AMI 合并心原性休克患者的疗效并分析影响患者院内结局的因素。
1 资料与方法
1.1 研究对象
回顾性分析郑州大学人民医院2018 年1 月至2019 年12 月经早期血运重建及ECMO 支持救治的66 例AMI 合并心原性休克患者的临床资料。患者入选标准:(1)以AMI 为首诊,首发或病情进展过程中出现心原性休克,充分药物治疗后血压仍难以维持[收缩压<90 mmHg(1 mmHg=0.133 kPa)]并出现组织低灌注的表现;(2)整个疗程中同时包括早期血运重建治疗及ECMO 辅助支持;(3)签署介入手术及特殊治疗知情同意书。研究已通过本院医学伦理会批准。
1.2 资料收集
收集患者一般资料、院前状态、病情特点、合并症、冠状动脉病变特点、血运重建方式及时间、ECMO 应用时长及并发症、是否联合IABP 及院内结局等。记录所有患者治疗前后左心室射血分数及血流动力学、乳酸、pH 等数据变化。
1.3 早期血运重建
根据患者病变特点、复杂程度及是否合并急性机械并发症选择手术方式。结合患者病情及医师经验行入院即刻极早期血运重建或院内延迟早期血运重建。所有患者术前及术后均进行充分的双联抗血小板治疗。
1.4 ECMO 的建立及管理
使用德国索林(Sorin)公司生产的ECMO 主机,美国Edward 公司生产的动静脉穿刺导管,成人氧合器(D905)、离心泵头、管路均为胆碱涂层材料,所有患者均采用V-A ECMO 模式,同时提供呼吸、循环辅助。给予100 µg/kg 肝素钠抗凝后,于无菌条件下进行ECMO 股动、静脉置管。
ECMO 辅助初期根据患者心功能、循环状态等尽量提高有效循环灌注。灌注改善后下调正性肌力及血管活性药物用量,根据心率、血压、中心静脉压等调整最适流量,根据血气结果调整酸碱电解质平衡,并维持动脉氧分压80~120 mmHg、二氧化碳分压35~45 mmHg。治疗过程中持续泵入肝素,使活化凝血时间维持在150~200 s。每日监测管路状态及患者基本生命体征调整ECMO 参数。
1.5 ECMO 评估撤机
当ECMO 循环流量仅为患者血流量的20%、超声心动图检查示心功能恢复、血流动力学稳定如成人平均动脉压>60 mmHg、中心静脉血氧饱和度>60%、左心室射血分数>40%可逐渐下调ECMO 流量,当流量<10 ml/kg 时可考虑停机[3]。停机后观察1~3 h 后患者病情稳定可拔除循环管路。
1.6 统计学方法
采用SPSS 23.0 软件进行统计分析,符合正态分布的定量资料以均数±标准差()表示,不符合的以中位数(P25,P75)表示,定性资料以构成比表示。两组定量资料比较采用t检验或Wilcoxon 秩和检验,二分类资料采用卡方检验或Fisher 确切概率法。应用Logistic 回归模型分析影响患者院内结局的因素,P<0.05 为差异有统计学意义。
2 结果
2.1 66 例患者临床资料及结局(表1)
66 例患者,年龄(56.6±11.7)岁,男性46 例(69.7%)。25 例(37.9%)在入院前出现呼吸心脏骤停及意识丧失而行心肺复苏,4 例并发室间隔穿孔,3例腱索乳头肌断裂,1 例出现冠状动脉夹层并延伸至主动脉根及弓部,4 例因高度房室传导阻滞应用临时起搏器;5 例(7.6%)行冠状动脉旁路移植术(中位时间为9 d),61 例(92.4%)行PCI,其中44 例(66.7%)行入院即刻早期血运重建,17 例(25.8%)行延迟早期血运重建(中位时间为5 d);共42 例(63.6%)患者为多支冠状动脉病变(定义为心外膜下3 条主支血管或其主要分支血管直径狭窄率超过50%),其中5 例行直接完全血运重建(3 例最终死于心脏骤停及多器官功能衰竭),2 例行院内分期完全血运重建(1 例最终死于心脏骤停),余均为仅罪犯血管的血运重建。39 例(59.1%)在治疗中使用IABP。66 例患者中38 例成功撤离ECMO,30 例存活出院,36 例死亡。并发症情况见表1。
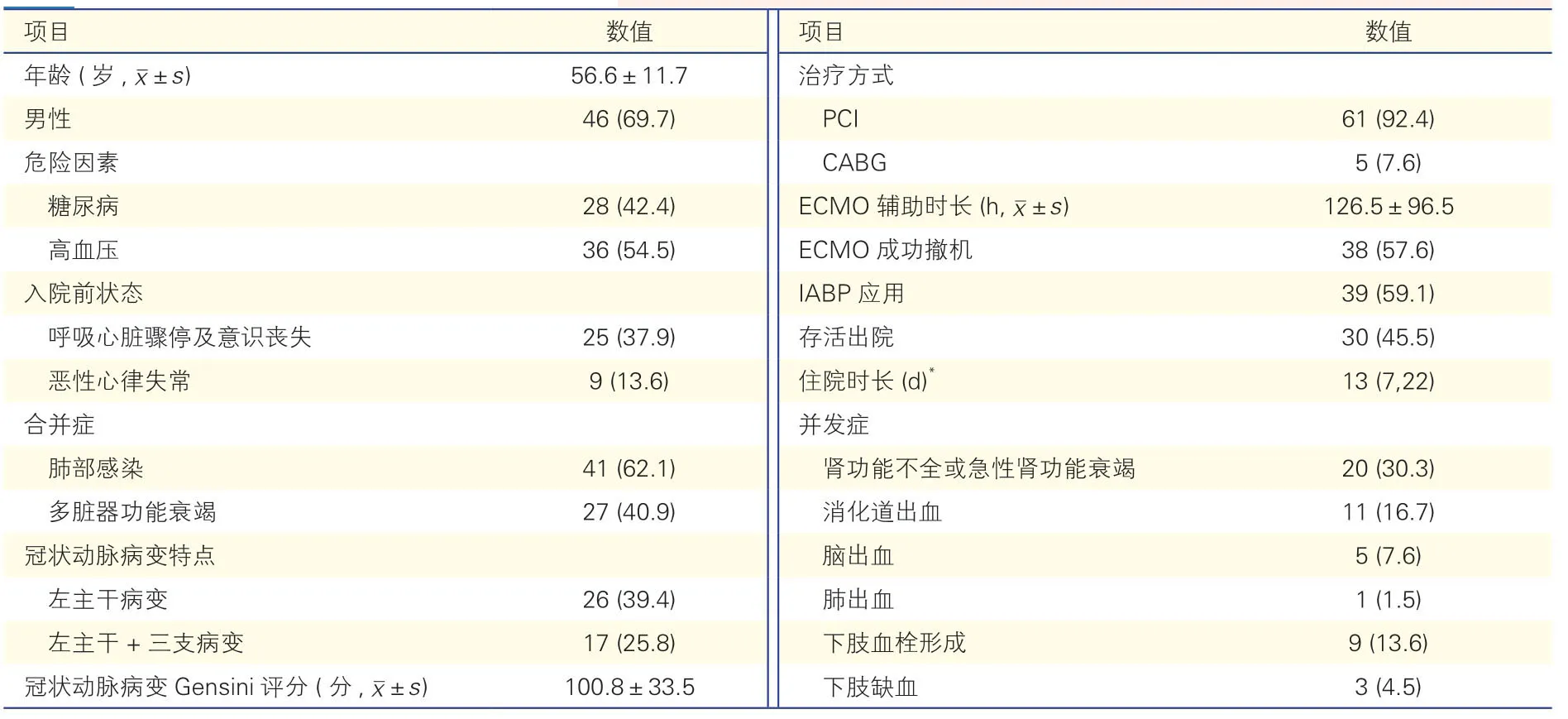
表1 66 例患者临床资料及结局[例(%)]
2.2 66 例血运重建及ECMO 辅助治疗前后患者主要临床指标变化(表2)
表2 66 例血运重建及ECMO 辅助治疗前后患者主要临床指标的变化()
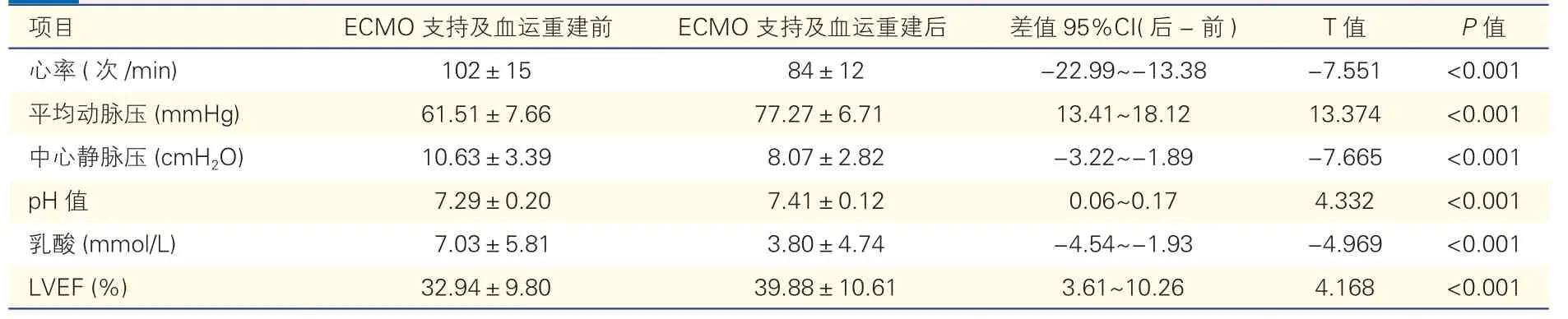
表2 66 例血运重建及ECMO 辅助治疗前后患者主要临床指标的变化()
注:LVEF:左心室射血分数;ECMO:体外膜肺氧合。1 mmHg=0.133 kPa ;1 cmH2O=0.098 kPa
经血运重建及ECMO 辅助治疗后患者左心室射血分数及平均动脉压上升,心率、中心静脉压及乳酸水平降低,pH 值较前改善,差异均有统计学意义(P均<0.001)。
2.3 存活患者和死亡患者临床资料比较(表3)
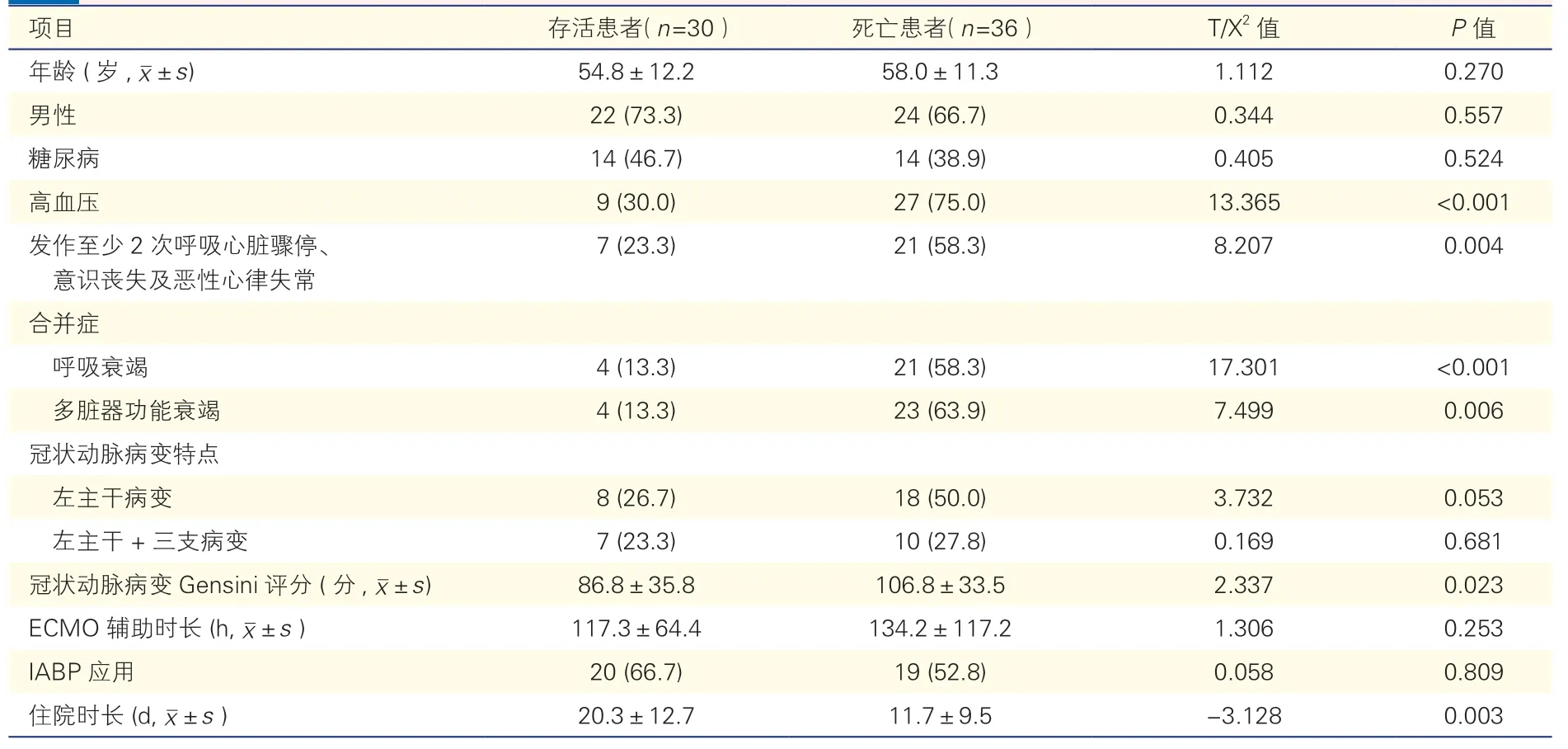
表3 院内存活患者与死亡患者临床资料比较[例(%)]
存活患者和死亡患者在高血压发病率,发作至少2 次呼吸心脏骤停、意识丧失及恶性心律失常,呼吸衰竭,多脏器功能衰竭,冠状动脉病变Gensini评分及住院时长上差异均有统计学意义(P<0.05),而年龄、性别、糖尿病发病率、冠状动脉病变特点、是否应用IABP 及ECMO 辅助时长差异无统计学意义。
2.4 院内死亡结局的多因素Logistic 回归分析(表4)
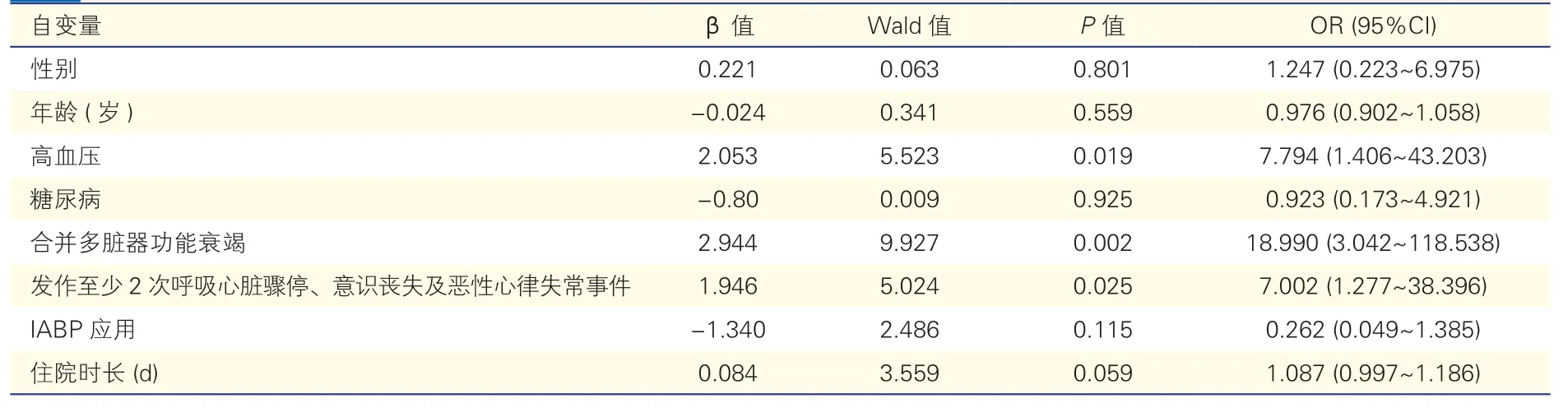
表4 院内死亡的多因素Logistic 回归分析
以院内结局为因变量,性别、年龄、高血压、糖尿病、合并多脏器功能衰竭,发生至少2 次呼吸心脏骤停、意识丧失及恶性心律失常事件,应用IABP 和住院时长等为自变量进行多因素Logistic 回归分析,结果显示高血压(OR=7.794),合并多脏器功能衰竭(OR=18.990)及发作至少2 次呼吸心脏骤停、意识丧失及恶性心律失常事件(OR=7.002)为患者院内死亡的高危因素(P<0.05),应用IABP 对院内结局无显著影响。
3 讨论
AMI 合并心原性休克作为心血管疾病的急危重症死亡率极高,若合并室间隔穿孔短期死亡率可超过80%[4]。SHOCK 试验证实了血运重建的优势[5],且被证实是最强的长期生存预测因子[6]。在时间节点上目前欧洲指南指出对于合并心原性休克的AMI患者无论发病时间长短均应尽可能行早期血运重建治疗,且越早越好。本研究共44 例(66.7%)行极早期PCI(入院即刻),17 例(25.8%)行延迟早期PCI(中位时间为5 d),仅1 例入院行紧急冠状动脉旁路移植术,该结果符合指南的推荐。
AMI 合并心原性休克的患者大部分为多支病变,是否完全血运重建在早期意见不一。最近的COMPLETE 研究显示,无论是即刻或择期的多支血管完全血运重建其获益均明显高于仅罪犯血管的血运重建[7],但研究纳入的心原性休克患者较少。CULPRIT-SHOCK 研究全部纳入心原性休克人群,结果证实仅罪犯血管血运重建的30 d 死亡率和肾功能衰竭风险显著低于完全血运重建[8],1 年死亡率差异无统计学意义[9];同时也有研究表明AMI 合并心原性休克患者完全血运重建后3 年全因死亡及再发AMI 风险低于仅罪犯血管血运重建[10]。因此指南目前对于AMI 合并心原性休克的患者推荐行早期仅罪犯血管的血运重建治疗,待患者情况好转后行分期的完全血运重建改善患者长期预后[11]。本研究共42 例(63.6%)为多支冠状动脉病变,其中5 例为直接完全血运重建,2 例为院内分期完全血运重建,余均为仅罪犯血管的血运重建。因行直接完全血运重建的患者例数太少致使其无法进入多因素Logistic回归模型,但依照目前指南仅罪犯血管的血运重建治疗是正确的。
AMI 患者多因急性心功能不全发展至心原性休克,而心原性休克又导致机体循环系统紊乱,后负荷代偿性增加的同时心肌血供进一步下降,心脏及下游组织器官持续受损,从而形成恶性循环。早期血运重建虽可开通冠状动脉提高心肌灌注,但心功能及休克状态难以即刻纠正。而机械循环支持可暂时替代心脏为机体循环提供动力,成为强有效的辅助治疗手段。
IABP 最早为心原性休克救治首选,但最近研究显示IABP 在30 天、1 年、6 年均未能改善AMI合并心原性休克患者死亡率或其他临床结局[12]。因此指南将IABP 推荐等级由Ⅰ类降至ⅢB 类[11]。ECMO 同样应用于心原性休克患者,且V-A ECMO能提供8 L/min 的血流支持,能迅速降低心脏负荷、提高外周灌注并改善通气及氧合[13]。体外生命支持组织(ELSO)数据显示当其用于心原性疾病时,患者存活率可达41%。本研究显示有57.6%的患者成功撤机,45.5%的患者存活出院。ECMO 弊端在于其并发症,可增加额外死亡风险。本研究共20 例(30.3%)出现肾功能不全或急性肾功能衰竭,11 例(16.7%)消化道出血、5 例(7.6%)脑出血、1 例(1.5%)肺出血、9 例(13.6%)下肢血栓形成、3 例(4.5%)下肢缺血。研究人群较高的肾脏并发症比例既包含ECMO 辅助过程溶血带来的肾功能损害又包括由心原性休克导致的肾前性肾功能衰竭,其作为多脏器功能衰竭的一部分可增加患者死亡风险。因此及时应用连续肾脏替代治疗(CRRT)尤为重要,但其治疗方式及管路建立模式仍需进一步研究。
除以上并发症外,ECMO 外周插管还可增加左心室后负荷,约10 %~ 60%的患者会出现左心室扩张[14],因此有学者提出ECMO 联合IABP 降低左心室负荷的策略[15],但目前证据不一且争议较大。有研究显示联合治疗策略与生存结局无显著关系[16],但也有证据显示其可降低院内死亡率[17-18]。而本研究显示应用IABP 对院内结局无显著影响。
本研究还发现高血压及发作至少2 次呼吸心脏骤停、意识丧失及恶性心律失常事件可增加患者死亡风险。原因可能是高血压患者基础血压较常人高,休克对循环灌注的打击较大,尤其是脑循环;而心脏骤停及恶性心律失常可直接致循环停滞,同样对脑灌注造成致命打击。但脑循环灌注受损是否显著影响临床结局目前尚无明确证据。另外也研究显示外周VA-ECMO 联合 IABP 也可影响脑循环[19],但这同时受到心肌状态和装置插管部位的双重影响[20]。
总的来说AMI 合并心原性休克的救治非常复杂,尽管近年来早期血运重建联合机械循环支持辅助治疗发展较快,但其死亡率仍维持在40%~60%[1]。多学科联合救治是必要的,而护理工作同样重要,加强循环支持、保护重要器官功能及减少并发症是未来努力的重点。本研究作为回顾性分析,纳入样本较少,尚需扩大样本量进行前瞻性随机对照研究,虽然实施困难,但对以后的救治工作有重要指导意义。
利益冲突:所有作者均声明不存在利益冲突

