马尾松树皮在离子液体中的溶解及组分分离研究
黄健 朱宇 陈瑞英 林春香

摘要:针对目前树皮组分难以有效利用的问题,以离子液体1-烯丙基-3-甲基咪唑氯盐([Amim ] Cl )为溶剂,对球磨后的马尾松(Pinus massoniana L.)树皮进行溶解,随后以 NaOH 溶液及乙醇为沉淀剂,对树皮中的纤维素、木质素和半纤维素组分进行分级分离。结果表明,球磨24h 后的马尾松树皮在100℃、溶解5h 的条件下,能够在离子液体中完全溶解;再生后树皮中纤维素的晶型由 I 型转变为 II 型,结晶度降低,但再生后树皮主要化学成分与原料相同。采用1% NaOH 溶液及乙醇溶液处理溶解后的树皮可有效分离得到纤维素、木质素和半纤维素,分离后各组分的化学结构未发生明显改变。离子液体经5次循环再利用后,其回收率依旧可以保持90%以上。
关键词:离子液体;马尾松树皮;组分分离;木质纤维素
中图分类号:TS721文献标识码:A DOI:10.11981/j. issn.1000?6842.2021.04.01
树皮是木材采伐和加工过程中的剩余物,全球每年树皮剩余物的产量可达4~5亿m3,储量较大。树皮生物质具有廉价、可再生及可生物降解等优良特性,可用于生物质燃料颗粒、人造板、胶黏剂、重金属离子吸附等领域[1-2]。但目前我国对树皮的利用研究进展较缓慢,大量树皮被丢弃,没有得到有效利用,造成资源的较大浪费[3]。因此,随着资源短缺及环境污染问题日益严峻,对树皮进行高值化利用显得尤为迫切。树皮主要由木质纤维素组成,不论是作为能源还是材料使用,高值化利用的关键是对其进行组分分离;只有将其主要组分(纤维素、半纤维素及木质素)进行有效分离、提取,并各自加以利用,才能达到树皮的高值化利用目的。然而,树皮内各组分的复杂化学结构及其较强的分子间与分子内作用力,导致纤维素、半纤维素和木质素三大组分难以被分离,阻碍了对树皮的综合利用。传统分离方法中多采用酸、碱或有机溶剂等,但这些方法很难实现对生物质的全组分利用,且溶剂难以回收[4-5]。因此,开发高效、清洁、绿色的树皮全组分分离体系及途径,促进树皮资源的高值化利用具有重要意义。
离子液体是指完全由阳离子和阴离子构成、且在室温或近室温下呈液体状态的熔融盐[6]。自2002年Swatloski等[7]首次发现离子液体可溶解纤维素以来,离子液体凭借其优异的性能在纤维素的资源化转化与利用方面表现出极大的潜力。随后的研究报道发现,离子液体不仅可有效溶解生物质中的单一组分如木质素[8]、半纤维素[9]、淀粉[10]、甲壳素[11]等,还可对木质纤维素全组分进行溶解[12-14],是分离木质纤维素中各组分的理想溶剂。
马尾松是福建省人工针叶林的主要树种,经济价值高,因而树皮产量大。因此,本研究以马尾松树皮为原料,以对木质纤维素溶解性最好的离子液体1-烯丙基-3-甲基咪唑氯盐([Amim ]Cl)为溶剂,研究马尾松树皮在[ Amim ]Cl 中的溶解及其三大组分的分离情况,探讨溶解条件及预处理对马尾松树皮溶解效率的影响;采用傅里叶变换红外光谱( FT-IR )、 X 射线衍射( XRD )等分析手段对溶解前后的马尾松树皮进行表征,并对各组分的化学结构进行分析和鉴定,为其在后续工业中的利用提供一定的理论基础。
1 实验
1.1 试剂及原料
实验所用原料为马尾松树皮,产地为福建省。将马尾松树皮晒干后使用植物粉碎机进行磨碎,取40~60目的部分备用,使用之前在60℃烘箱中干燥24h。离子液体[ Amim ]Cl (熔点28℃、纯度99%)由上海成捷离子液体公司提供;二甲基亚砜、丙酮、无水乙醇等药品均为市售,纯度>99%。
1.2 马尾松树皮组分分析方法
马尾松树皮中各组分的测定参照 GB/T 2677.3—1993 (灰分)、 GB/10337—1989 (酸不溶木质素)、 GB/T 10337—2008 (酸溶木质素)、 GB/T 2677.10—1995(综纤维素)、 GB/T 2677.4—1993(冷、热水抽出物)、 GB/T 2677.6—1993 (苯醇抽出物)、 GB/T 2677.5—1993(1% NaOH 抽出物);采用硝酸乙醇法测定综纤维素中纤维素的含量[15],综纤维素含量减去纤维素的含量即为半纤维素含量;将木质素测定中的滤液进行稀释,采用 LC-20AT 高效液相色谱-示差折光率检测法测定其中糖含量。
1.3 马尾松树皮在离子液体中的溶解与再生
马尾松树皮在离子液体中的溶解与再生可参考纤维素在离子液体中的溶解和再生过程[7],溶解条件根据马尾松树皮的特性进行适当调整:取40~60目的马尾松树皮样品,按照0.02∶1~0.04∶1的比例(质量比)加入已熔融的离子液体[ Amim ]Cl ,并分别在110℃~170℃的油浴中溶解一定时间。反应完毕后加入50%(相对离子液体的质量)的二甲基亚砜稀释并过滤,使用蒸馏水彻底洗涤得到的未溶解物质,干燥并称重,根据式(1)计算马尾松树皮的溶解率。将溶解后的马尾松树皮倒入去离子水中,溶解的马尾松树皮析出,过滤洗涤后干燥,得到再生马尾松树皮。
1.4 马尾松树皮在离子液體中的组分分离
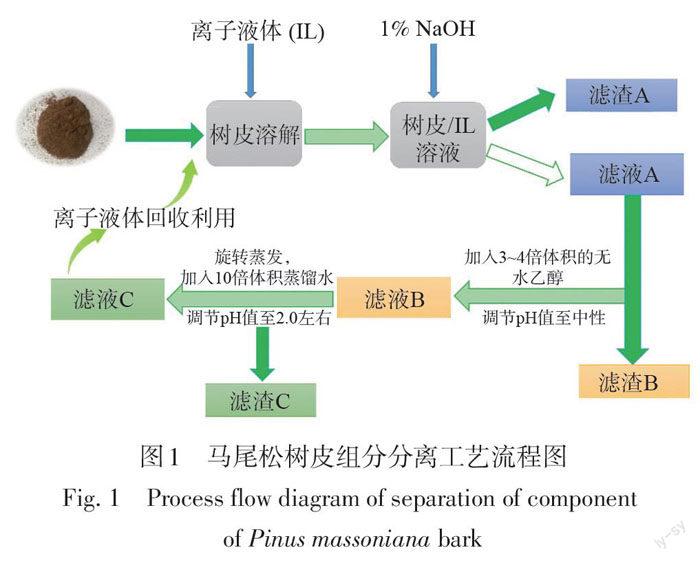
马尾松树皮组分分离工艺流程如图1所示。分离过程如下:将25 g马尾松树皮/离子液体溶液加入100 mL 1%的 NaOH 溶液中,搅拌1 h 后离心分离得滤渣 A 和滤液 A 。将滤液 A 的 pH 值调至中性,加入3~4倍体积的无水乙醇,离心分离后得滤渣 B 和滤液 B 。将滤液B 低压旋转蒸发以除去乙醇,并将浓缩液加入到10倍体积的蒸馏水中,pH 值调至2.0左右,静置后过滤,得滤渣 C 和滤液 C 。各滤渣得率( Y,%)的计算公式如式(2)所示。
Y (%)=滤渣的质量/树皮的质量×100% (2)
1.5 离子液体的回收
离子液体回收工艺如下:滤液 C 经0.1 mol/L 盐酸溶液中和后通过层析柱(直径5cm ,高度50 cm),层析柱从上到下分别是活性炭(5 cm)、薄层层析硅胶(D≥38?m ,1 cm)、柱层层析硅胶(100~200目,3 cm)和棉花(1 cm)。将通过层析柱后的滤液置于旋转蒸发仪中除去水分,设置工作参数为转速40 r/min 、真空度?0.1 MPa ,在70℃下反应2~5 h ,待液体中不再产生蒸发的气泡,结束反应。将旋转蒸发后剩余的产物置于真空干燥箱中,设置温度为60℃,时间24 h,除去旋转蒸发无法除掉的水分。随后将干燥所得的固体溶于乙腈溶剂,过滤去除不溶物,然后在真空下脱除乙腈,并将回收的离子液体在70℃下真空干燥,将所得固体称重,得M2(g),按式(3)计算离子液体的回收率(R ,%)。
R(%)= M2/M1 ×100%(3)
式中,M1为最初溶解树皮加入的离子液体的质量,g;M2为回收的离子液体的质量,g。
1.6 各组分理化性质分析及表征
通过 KBr 压片法,利用傅里叶变换红外光谱仪(Nicolet iS5,美国 Nicolet 公司)对样品的官能团进行分析;使用 X 射线衍射仪(X'Pert Pro MPD ,荷兰 Philips-FEI 公司)分别对样品进行扫描分析,根据 Se? gal's 法计算样品的结晶度( CrI)[16];将溶解过程中的马尾松树皮/离子液体溶液置于偏光显微镜( ZYP-1000E ,福州中诺电子有限公司)下观察;利用凝胶渗透色谱仪( GPC , Waters2414,美国 Waters 公司)对木质素的分子质量进行测定;采用铜乙二胺溶液法测定纤维素的聚合度( GB 5888—1986)。
2 结果与讨论
2.1 马尾松树皮组分分析
马尾松树皮中各组分含量如表1所示。由表1可知,马尾松树皮化学成分较复杂,木质素、纤维素和半纤维素是马尾松树皮的主要成分,含量分别为30.28%、32.47%和24.52%;灰分和单宁含量分别为7.36%和6.14%;冷、热水抽出物主要为树皮中水溶性成分,如无机盐类、糖、植物碱等,其含量分别为4.82%和17.02%,说明树皮中水溶性物质含量不高;而1% NaOH 抽提除能溶出被冷、热水溶出的物质外,还能溶出一部分木质素、聚戊糖、聚己糖、树脂酸等物质,实验测得的此抽出物含量为36.62%,说明马尾松树皮中抽出物含量较高;苯醇抽出物为树皮中可以溶于苯醇的疏水性物质,主要包括黄酮类化合物、萜烯类化合物及其他芳香族化合物等,其含量相对较少,为2.08%,说明马尾松树皮中蜡质、树脂酸和脂肪酸等物质含量较少。
2.2 马尾松树皮在离子液体中的溶解
自Swatloski等[7]报道了纤维素可在离子液体中溶解之后,离子液体在生物质溶解及应用方面的研究陆续被报道。在溶解过程中,离子液体首先渗透进入木质纤维内部使其润胀,随后溶解非结晶区碳水化合物(如纤维素和半纤维素),同时伴随着少量木质素的溶解,最后溶解结晶区的纤维素;若在高温条件下继续加热反应,木质纤维中各组分可能会降解成小分子物质,可导致木质纤维素液化[17]。Kilpel?inen等[18] 曾指出,离子液体[ Amim ]Cl 对木质纤维素具有优异的溶解性能,通过简单地将干木屑样品与离子液体[ Amim ]Cl 混合,并在80~120℃条件下机械搅拌混合,即可实现木屑的完全溶解。因此,本研究采用[ Amim ]Cl 为溶剂,研究马尾松树皮在离子液体中的溶解性能。
不同条件下,马尾松树皮在离子液体中的溶解情况如表2所示。其中,对于球磨的马尾松树皮样品,其颗粒尺寸以球磨时间表示,下同。从表2可以看出,马尾松树皮的颗粒尺寸、溶解时间和温度对树皮在离子液体中的溶解率均有较大影响。升高温度、延长反应时间、减小树皮的颗粒尺寸,均能提高其溶解率。在高温条件下,离子液体更容易渗透进入树皮内部,促进树皮中大分子链的润胀和溶解;但若在此条件下继续延长溶解时间,可能会导致木质纤维的各组分降解成小分子物质,木质纤维素被液化。此外,树皮的颗粒尺寸也对离子液体的溶解性能有较大影响。将马尾松树皮分别球磨12 h 和24 h 后进行离子液体溶解实验发现,树皮的溶解率大大提高,甚至可以完全溶解;且随着球磨时间延长,树皮在离子液体中达到完全溶解所需时间缩短。因此,对马尾松树皮进行适当的预处理,可提高离子液体对马尾松树皮的溶解率。
图2为 [ Amim ]Cl 对马尾松树皮溶解过程的偏光显微镜照片。从图2可以看出,未球磨的马尾松树皮在100℃分别溶解5h 和7h 后,其颗粒尺寸降低,但未溶解完全,视野中分布较多树皮颗粒;而球磨12 h 和24 h 后,离子液体可在较低温度下(100℃),分别于7 h 和5 h 之内将树皮完全溶解,此结果与表2中数据一致。
2.3 马尾松树皮的再生
马尾松树皮在离子液体中完全溶解后,将其倒入过量去离子水中,在快速机械搅拌下进行再生,得到再生的马尾松树皮。为了研究马尾松树皮在离子液体中溶解前后结构和性能的变化,对其溶解前后的结构进行相应的分析。
图3(a)为马尾松树皮溶解前后的 XRD 谱图。从图3(a)可以看出,溶解前,馬尾松树皮在2θ为15°和22°附近均出现一个明显的尖峰;而溶解再生后,马尾松树皮在结晶区的 X 射线衍射信号消失,只在2θ=22.1°附近出现一个较宽的非晶衍射峰;且结晶度也由原来树皮的27.3%降至再生马尾松树皮的17.6%。在早期研究中, Fu 等[19] 曾利用 FT-IR 、XRD 和热重( TG )分析手段研究了利用离子液体BMIMCl再生的纤维素与溶解前纤维素之间的结构差异;研究结果显示,纤维素经离子液体BMIMCl再生后,其晶型由纤维素 I 型转变为纤维素 II 型。据此可知,本研究实验结果与文献相符,马尾松树皮在再生过程中发生了纤维素晶型从 I 型到 II 型的转变,结晶度降低。
马尾松树皮溶解再生前后的 FT-IR 谱图如图3(b)所示。由图3(b)可知,树皮溶解再生前后的 FT-IR 谱图大体相同,如1024 cm-1处的吸收峰是由综纤维素中 C—O 、木质素伯醇 C―O 和愈创木基木质素中 C—H 的伸缩振动引起,1510 cm-1附近的吸收峰主要是由木质素中苯环骨架的伸缩振动引起,1615和1735 cm-1 附近的吸收峰是由纤维素和半纤维素中 C=O 的伸缩振动引起[20],说明马尾松树皮的化学结构经溶解再生后未发生明显变化,其在离子液体溶解过程中未发生衍生化反应。但部分特征吸收峰在强度上存在明显差异,马尾松树皮溶解再生后,2850 cm-1 (—CH2的对称伸缩振动峰)和1735 cm-1 (半纤维素中非共轭 C=O 伸缩振动峰) 处的吸收峰强度减弱,而1024 cm-1处的 C—O 特征吸收峰加强;且溶解前,马尾松树皮的 O—H 伸缩振动吸收峰位于3290 cm-1处,而经离子液体溶解再生后,该吸收峰发生了蓝移(移至3350 cm-1处),说明马尾松树皮在溶解过程中各组分的氢键体系被破坏,树皮组分中的氢键作用减弱,纤维素、半纤维素及木质素被暴露,使得 C—O 的振动加强[21]。
2.4 马尾松树皮在离子液体中的组分分离
木质纤维经离子液体处理后,再加入一定浓度的沉淀剂,可实现树皮中各组分的分离。常用沉淀剂有丙酮或其水溶液[22]、NaOH 溶液[23]等,这些溶剂通过选择性溶解木质纤维中的部分组分,以达到组分分离的目的。按照图1的工艺流程,马尾松树皮经离子液体溶解后,加入1% NaOH 溶液,部分半纤维素和木质素溶于 NaOH 和离子液体的溶液中,而纤维素则以沉淀形式存在(滤渣 A);溶解的半纤维素和木质素则可通过调节溶液 pH 值及加入乙醇溶液进行分步沉淀(滤渣 B 和滤渣 C),从而达到马尾松树皮中三大组分的分离。各组分得率结果如表3所示。
由表3可知,利用离子液体对球磨12 h 的马尾松树皮进行溶解,以 NaOH 溶液作为沉淀剂得到滤渣 A、滤渣 B 和滤渣 C ,其得率分别为52.39%,25.88%和6.78%。当球磨时间增加至24 h 时,滤渣 A 得率降至47.82%,而滤渣 B 和滤渣 C 的得率分别增至31.37%和8.32%。在球磨过程中,木质纤维素分子间的化学键容易受到破坏,使得树皮中纤维素、木质素和半纤维素更容易分离出来。随着球磨时间的延长,滤渣 A 脱除了更多的木质素和半纤维素,因此,得率下降;更多的木质素和半纤维素被分离出来,使得滤渣 B 和滤渣 C 得率提高。为了验证球磨对组分分离的作用,对滤渣 A 、滤渣 B 和滤渣 C 的木质素含量(%,相对于绝干马尾松树皮)进行分析,并进一步对滤渣 A 的木质素含量和糖含量进行测定,结果如图4所示。由图4(a)可知,增加球磨时间,滤渣 A 和滤渣 B 的木质素含量降低,而滤渣 C 的木质素含量提高,进而提高分离所得纤维素、半纤维素和木质素的纯度。图4(b)结果表明,滤渣 A 的主要成分是纤维素,含有少量木质素和半纤维素;当球磨时间增至24 h 时,滤渣 A 中木质素含量和木糖含量下降,而葡萄糖含量提高,此结果进一步证明,增加球磨时间可提高滤渣 A (纤维素)的纯度。
2.5 马尾松树皮分离组分的结构表征
對滤渣 A 、滤渣 B 和滤渣 C 进行 FT-IR 分析,结果如图5所示。从图5可以看出,滤渣 A 在3400、2900、1640、1360和1027 cm-1等处出现了纤维素的特征吸收峰[20]。滤渣 B 中,1040 cm-1处的吸收峰是半纤维素的典型吸收峰,该吸收峰主要来自糖苷键的 C—O—C 伸缩振动;位于2920 cm-1附近的吸收峰为 C—H 键的伸缩振动峰;3400 cm-1处的吸收峰为—OH 的伸缩振动吸收峰,1600 cm-1处为半纤维素中残余水分引起的吸收峰,1158 cm-1是典型的聚阿拉伯糖木糖的吸收峰,896 cm-1处为糖单元之间β-糖苷键的吸收峰,表明滤渣 B 的主要成分为半纤维素[24]。此外,1510 cm-1处为木质素苯环的特征吸收峰,说明滤渣 B 中残留有少量的木质素。而滤渣C 在1605和1510 cm-1 处出现木质素芳香基骨架振动的特征吸收峰;在1160和1029 cm?1处分别出现紫丁香基和愈创木基的特征吸收峰,说明滤渣 C 的主要成分为木质素[25]。
为了进一步对分离的木质素和纤维素结构及半纤维素中糖含量进行分析,采用 GPC 分析马尾松树皮磨木木质素( MWL )的分子质量,并对分离出的纤维素的聚合度( DP )、半纤维素中的主要糖成分及其含量进行测定,结果如表4所示。从表4可以看出,滤渣 C 的质均分子质量(Mw)和数均分子质量(Mn)分别为8132和3533,分子质量分布 (Mw/Mn)为2.302;而马尾松树皮 MWL 具有较高的分子质量及分子质量分布。这主要是由于树皮在溶解过程中,较高的温度易使木质素单元间的部分β-O-4连接断裂,导致分子质量降低;而在滤渣 C 分离时,碱性作用下醚键和酯键断裂,使其分子质量进一步减小。此外,木质素中半纤维素的存在会影响木质素分子质量分布。马尾松树皮 MWL 由于未经碱处理,因此其结构中存在部分半纤维,使得分子质量分布变宽[26];而滤渣 C 经 NaOH 溶液处理后,所得木质素组分较纯( FT-IR 表征中也未见明显半纤维素的特征峰),因此,其分子质量分布较窄。从表4还可知,纤维素(滤渣 A)的聚合度较低,说明在分离马尾松树皮各组分的过程中,纤维素发生了一定程度的降解,导致其聚合度降低;半纤维素(滤渣 B)中葡萄糖、木糖和半乳糖是3种主要的单糖组分,其含量分别为17.25%、65.76%和4.32%。
2.6 离子液体的回收与性能
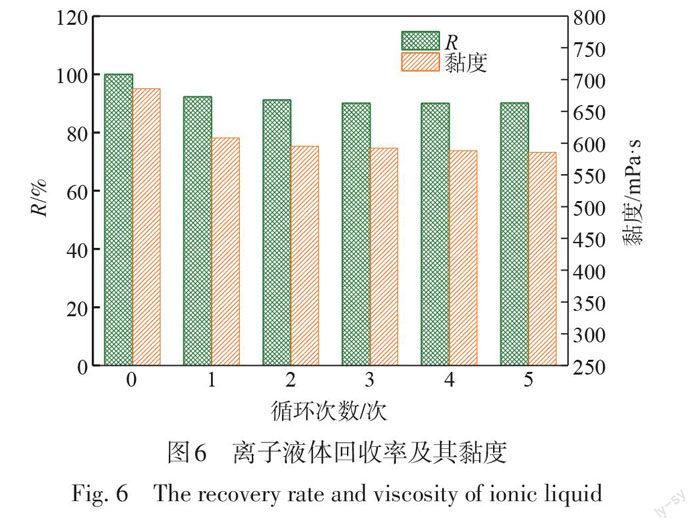
离子液体溶解树皮的过程中,其回收及重复利用是该方法能否产业化应用的关键。本研究通过中和、蒸发、溶解、过滤等步骤对离子液体进行回收,并对回收后的离子液体进行再利用。图6为离子液体的回收率及其黏度测试结果。从图6可以看出,5次循环利用后,离子液体的回收率仍可保持在90%以上;但与新鲜离子液体相比,循环回收得到的离子液体黏度略有下降,可能是由于回收过程中依旧残留有水分的原因所致。
图7为新鲜离子液体及回收离子液体(第1次回用、第2次回用和第3次回用)的 FT-IR 谱图及外观图(内插图片)。从图7可以看出,回收得到的离子液体外观颜色逐渐加深,这可能是因为离子液体溶解树皮过程中,温度较高,少量离子液体发生了氧化反应,导致其颜色加深。由图7还可知,与新鲜离子液体相比,回收的离子液体在3400 cm-1附近的特征吸收峰明显加强,表明回收的离子液体中含有未去除的水分;此外,4种离子液体的 FT-IR 谱图主要特征吸收峰出峰位置并未发生明显变化,表明回收的离子液体依旧保持原本的化学结构。
3 结论
本研究以离子液体1-烯丙基-3-甲基咪唑氯盐([Amim ]Cl)为溶剂,对球磨后的马尾松( Pinus mas- soniana L.)树皮进行溶解,隨后以1% NaOH 溶液及乙醇为沉淀剂,对树皮中的纤维素、木质素和半纤维素组分进行分级分离,主要结论如下。
3.1 马尾松树皮可在离子液体[ Amim ]Cl 中溶解,升高温度、延长反应时间及球磨预处理均能提高树皮在离子液体中的溶解性能。马尾松树皮球磨24 h 后,在100℃、5 h 条件下可在离子液体中完全溶解。
3.2 马尾松树皮在离子液体中溶解后,可在去离子水中进行再生。再生后的马尾松树皮由于树皮的溶解及氢键体系的破坏,其纤维素晶型由 I 型变为Ⅱ型,结晶度下降;再生后树皮的红外光谱分析显示各组分的主要化学结构未发生变化,但树皮各组分间的氢键体系被破坏。
3.3 以 NaOH 溶液和乙醇为沉淀剂,可实现马尾松树皮中纤维素、半纤维素和木质素组分的分离,球磨过程可提高各组分的分离效率;红外光谱分析进一步证明了各滤渣主要成分分别为纤维素、半纤维素和木质素;分离后,木质素的分子质量降低、分子质量分布变窄,且纤维素有一定程度的降解。
3.4 对离子液体进行回收再利用,结果表明,回收的离子液体含有部分水,但其化学结构未发生明显变化;回用5次后,离子液体的回收率仍能保持90%以上,但其黏度略有降低。
参考文献
[1] MANDAL A , MUKHOPADHYAY P , DAS S K. AdsorptiveRemoval of Phenol From Wastewater Using Guava Tree Bark [J]. Environmental Science and Pollution Research ,2020,27(19):23937-23949.
[2] MARIANA,MULANA F,MUCHTAR S,et al. The Utilization ofActivated Carbon from Jamblang Tree Bark to Adsorb Lead Heavy Metal Ion [J]. IOP Conference Series Materials Science and Engineering,2021,DOI:10.1088/1757-899X/1087/1/012062.
[3] 翟旭航,李霞,元英进.木质纤维素预处理及高值化技术研究进展[J].生物技术通报,2021,37(3):162-174.
ZHAI X H,LI X,YUAN Y J. Research Progress of Lignocellulose Pretreatment and Valorization Method[J]. Biotechnology Bulletin,2021,37(3):162-174.
[4] 陈浩.桉树皮资源改性酚醛树脂木材胶粘剂的研究[D ].南宁:广西大学,2019.
CHEN H. Study on the Modification of Phenolic Resin Wood Adhesive with Eucalyptus Bark Resource [ D ]. Nanning :Guangxi University,2019.
[5] PENG F , BIAN J , REN J L , et al. Fractionation andcharacterization of alkali-extracted hemicelluloses from peashrub [J]. Biomass & Bioenergy,2012,39:20-30.
[6] 童欣怡,李琦,陈文倩,等.杨木屑木聚糖碱法提取及其制备低聚木糖的工艺研究[J].林业工程学报,2020,5(1):61-68.
TONG X Y,LI Q,CHEN W Q,et al. Alkali Extraction of Xylanfrom Poplar Sawdust and Preparation of Xylooligosaccharide by Enzymatic Hydrolysis[J]. Journal of Forestry Engineering,2020,5(1):61-68.
[7] SWATLOSKI R P,SPEAR S K,HOBREY J D,et al. Dissolution ofCellulose with Ionic Liquids[J]. Journal of the American Chemical Society,2002,124(18):4974-4975.
[8] PU Y Q,JIANG N ,RAGAUSKAS A J. Ionic liquid as a GreenSolvent for Lignin[J]. Journal of Wood Chemistry and Technology,2007,27(1):23-33.
[9] 郑勇,彭聪虎,郑永军,等.半纤维素在离子液体中的溶解和再生过程研究[J].轻工学报,2016,31(2):15-20.
ZHENG Y ,PENG C H ,ZHENG Y J ,et al. Research on the Dissolution and Regeneration of Hemicellulose in Ionic Liquids[J]. Journal of Light Industry,2016,31(2):15-20.
[10] LI D D,ZHANG X W,TIAN Y Q. Ionic Liquids as Novel Solventsfor Biosynthesis of Octenyl Succinic Anhydride-modified Waxy Maize Starch [J]. International Journal of Biological Macromolecules,2016,86:119-125.
[11] 岳盼盼,付亙悫,胡亚洁,等.木质纤维生物质半纤维素分离研究进展[J].中国造纸,2019,38(6):73-78.
YUE P P,FU G Q,HU Y J,et al. Research Advance in Isolation of Lignocellulosic Biomass Hemicelluloses [J]. China Pulp & Paper,2019,38(6):73-78.
[12] LI W Y , SUN N , STONER B , et al. Rapid Dissolution ofLignocellulosic Biomass in Ionic Liquids using Temperatures Above the Glass Transition of Ligin[J]. Green Chemistry,2011,13:2038-2047.
[13] SUN N,JIANG X Y,MAXIM M L,et al. Use of PolyoxometalateCatalysts in Ionic Liquids to Enhance the Dissolution and Delignification of Woody Biomass [J]. ChemSusChem,2011,4(1):65-73.
[14] 王林风,程远超.硝酸乙醇法测定纤维素含量[J].化学研究,2011,22(4):52-55,71.
WANG L F,CHENG Y C. Determination the Content of Cellulose by Nitric Acid-ethanol Method[J]. Chemical Research,2011,22(4):52-55,71.
[15] SEGAL L ,CREELY J J,MARTIN A E ,et al. An EmpiricalMethod for Estimating the Degree of Crystallinity of Native Cellulose Using the X-ray Diffractometer[J]. Text Res J,1959,29:786-794.
[16] SUN N ,RAHMAN M ,QIN Y ,et al. Complete Dissolution andPartial Delignification of Wood in the Ionic Liquid 1-Ethyl-3- Methylimidazolium Acetate [J]. Green Chemistry,2009,11(5):646-655.
[17] MIYAFUJI H,MIYATA K,SAKA S,et al. Reaction Behavior ofWood in An Ionic Liquid ,1-Ethyl-3-Methylimidazolium Chloride [J]. Journal of Wood Science,2009,55(3):215-219.
[18] KILPEL?INEN I,XIE H B,KING A,et al. Dissolution of Wood inIonic Liqids[J]. Journal of Agricultural and Food Chemistry,2007,55(22):9142-9148.
[19] FU S,XIE C. Etherification of Alkali-pretreated Sugarcane BagasseCellulose in Tetrahydrofuran[J]. Paper and Biomaterials,2020,5(3):44-50,61.
[20] ZHAI W , CHEN H Z , MA R Y. Structural Characteristics ofCellulose after Dissolution and Regeneration from the Ionic Liquid [ Bmim ] Cl [J]. Journal of Beijing University of Chemical Technology,2007,34(2):138-141.
[21] ZHANG H,WU J,ZHANG J,et al. 1-Allyl-3-methylimidazoliumChloride Room Temperature Ionic Liquid:A New and Powerful Nonderivatizing Solvent for Cellulose [J]. Macromolecules ,2005,38(20):8272-8277.
[22] TAN S S Y,MACFARLANE D R,UPFAL J,et al. Extraction ofLignin from Lignocellulose at Atmospheric Pressure Using Alkylbenzenesulfonate Ionic Liquid [J]. Green Chemistry ,2009,11:339-345.
[23] FU L H,LIU S,LI S M,et al. Characterization of HemicellulosesExtracted from Populus tomentosa Carr. by the Hydrothermal Method with Ethanol[J]. Paper and Biomaterials,2017,2(3):1-11.
[24] 朱夢妮,田维珍,王兴,等.不同来源木质素抗氧化活性研究[J].中国造纸学报,2019,34(4):14-20.
ZHU M N,TIAN W Z,WANG X,et al. Chemical Structure and Antioxidant Activity of Different Sources of Lignin[J]. Transactions of China Pulp and Paper,2019,34(4):14-20.
[25] SHEN D K,GU S,BRIDGWATER A V. The Thermal Performanceof the Polysaccharides Extracted from Hardwood:Cellulose and Hemicellulose[J]. Carbohydrate Polymers,2010,82(1):39-45.
[26] EVTUGUIN D V,NETO C P,SILVA A M S,et al. ComprehensiveStudy on the Chemical Structure of Dioxane Lignin from Plantation Eucalyptus Globulus Wood [J]. Journal of Agricultural and Food Chemistry,2001,49(9):4252-4261.
Study on the Dissolution and Fractionation of Pinus Massoniana Bark in Ionic Liquid
HUANG Jian1,2,3 ZHU Yu1 CHEN Ruiying4 LIN Chunxiang1,2,3,*
(1. School ofAdvanced Manufacturing,Fuzhou University,Jinjiang,Fujian Province,362200;2. Key Laboratory ofPulp andPaper Science & Technology ofMinistry ofEducation/Shandong Province,Qilu University of Technology,Ji'nan,ShandongProvince,250353;3. College of Environment and Resources,Fuzhou University,Fuzhou,Fujian Province,350108;4. College of Material Engineering,Fujian Agriculture and Forestry University,Fuzhou,Fujian Province,350116)
(*E-mail :lcx2010@fzu. edu. cn)
Abstract: The ball-milled Pinus massoniana (Pinus massoniana L.) bark was dissolved in ionic liquid—1-allyl-3-methylimidazolium chlo? ride ([Amim]Cl) and subsequently fractionated from the bark to cellulose,lignin,and hemicellulose using dilute alkali and ethanol solution as the precipitant. The results showed that Pinus massoniana bark could be completely dissolved in [Amim]Cl at 100℃ for 5 h after 24 h of ball milling. After regeneration,the cellulose crystal form of the bark was changed from type I to type II with decreased crystallinity while the chemical structure of each component in the bark did not change . Cellulose,hemicellulose,and lignin could be fractionated by treating the abovementioned dissolved bark with 1% NaOH and ethanol solution with negligible change in the chemical structure of each component . Af? ter recycled and reused for 5 times,the ionic liquids maintained a recovery rate above 90%.
Keywords :ionic liquid;Pinus massoniana bark;fractionation;lignocellulose
(责任编辑:杨艳)

