A1-42、tau和MDA在阿尔茨海默病患者中的表达及其临床意义
喻长法,叶丽君,黎敏,傅攀
阿尔茨海默病(AD)是一种以认知能力下降为特征的神经退行性疾病,是痴呆的主要原因。AD的病理特征主要包括 淀粉样蛋白(A)沉积和异常磷酸化的tau蛋白聚集、血管淀粉样变性、皮层和海马神经元丢失导致的细胞外神经原纤维缠结形成的老年斑(SP)[1]。AD导致不可逆的心理和认知缺陷,包括人格障碍、记忆力减退和智力异常,疾病晚期包括视觉系统在内的中央感觉系统也会受到影响。总的来说,AD并发症会缩短寿命,影响患者生活质量并导致身体受损。为了降低社会和经济成本以及疾病对患者及其家人的负担,人们进行了一些尝试来确定疾病诊断标记物[2]。本研究旨在探讨-淀粉样蛋白1-42(A1-42)、tau蛋白和丙二醛(MDA)在AD患者中的表达及其意义,报道如下。
1 资料与方法
1.1 一般资料选取2017年1月至2019年12月在浙江省台州市第一人民医院住院的82例AD患者为AD组,纳入标准:(1)符合AD诊断标准[3];(2)临床资料完整;(3)年龄61~88岁;(4)能配合各项检查。排除标准:(1)有明确的精神类疾病病史者;(2)癫痫病或脑外伤史者;(3)合并慢性肝、肾疾病者;(4)合并肿瘤、感染性疾病者;(5)依从性差者。另选同期来院健康体检者40例为对照组。本研究经本院医学伦理委员会批准,且患者及家属均知情,并签同意书。
1.2 方法采集受试者清晨空腹外周血3 ml,离心取血清置于-80℃冰箱保存备检。采用双抗体夹心酶联免疫吸附试验(ELISA)检测外周血清中的A1-42和tau水平,试剂盒由武汉默沙克生物科技有限公司提供;采用硫代巴比妥酸(TAB)法检测MDA水平,试剂盒由自南京建成生物工程研究所提供。
1.3 统计方法采用SPSS 22.0统计软件进行分析,计量资料用均数±标准差表示,采用t检验;计数资料比较采用2检验;诊断效能评价采用受试者工作特征曲线(ROC)。P<0.05为差异有统计学意义。
2 结果
2.1 两组临床资料比较两组年龄、性别、糖尿病、高血压和受教育年限等差异均无统计学意义(均P>0.05),两组MMSE评分差异均有统计学意义(P<0.05),见表1。
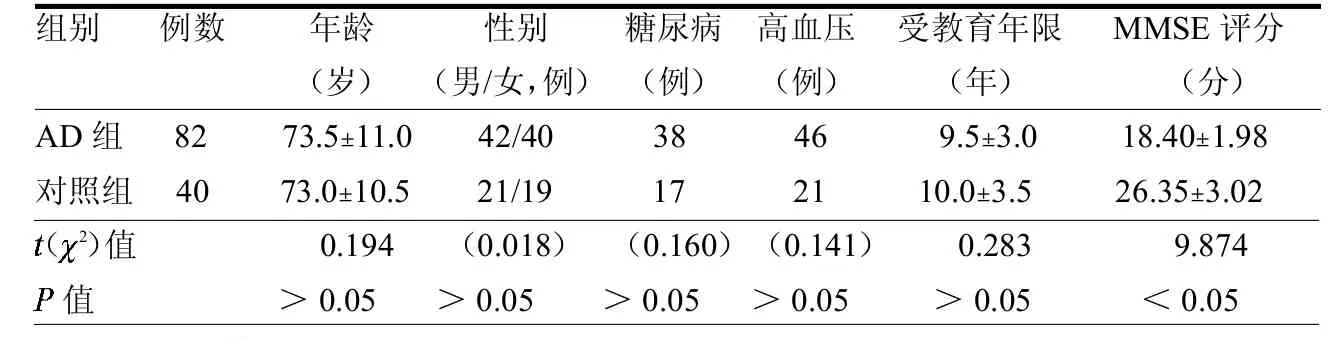
表1 两组基础资料比较
2.2 两组A1-42、tau和MDA水平比较AD组A1-42水平低于对照组,而tau和MDA水平均高于对照组(均P<0.05),见表2。
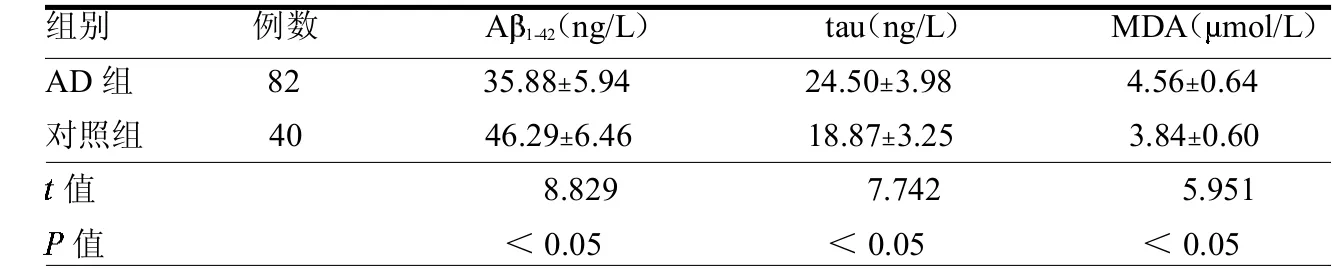
表2 两组A 1-42、tau和MDA水平比较
2.3 不同程度AD患者A1-42、tau和MDA水平比较轻度AD组A1-42水平高于中、重度组,而tau和MDA水平低于中、重度组(均P<0.05),见表3。

表3 不同程度AD患者A 1-42、tau和MDA水平比较
2.4 A1-42、tau和MDA对AD的诊断效能评价A1-42、tau和MDA对AD的诊断曲线下面积(AUC)分别为0.877、0.856和0.803,见封二彩图3。
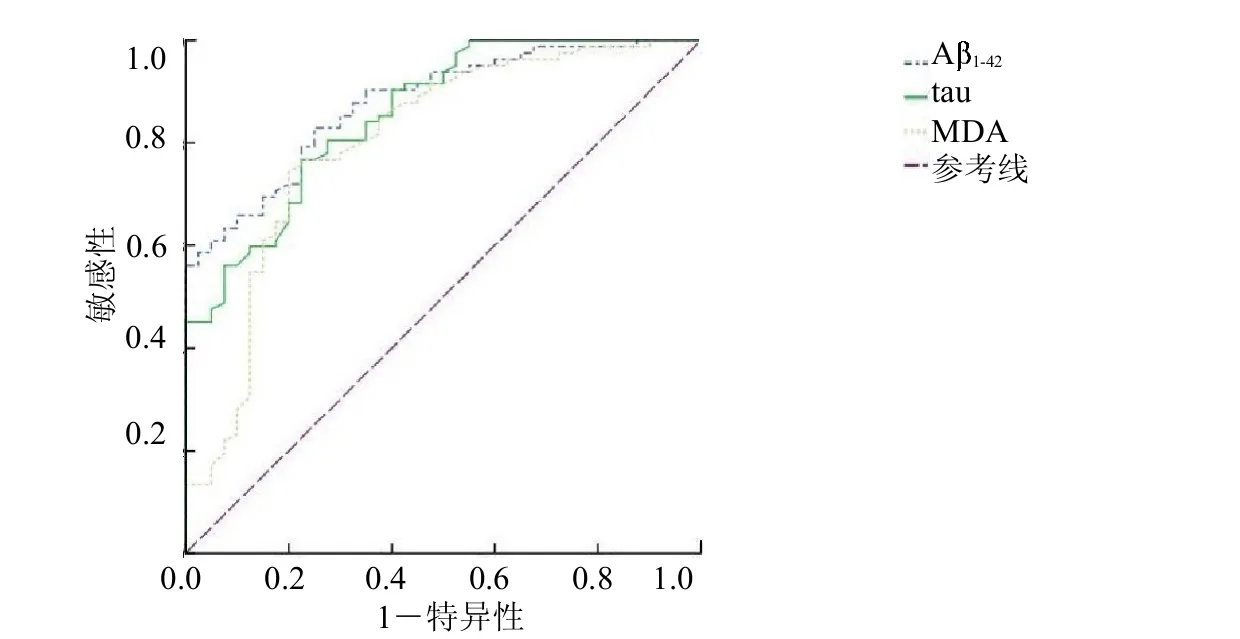
图3 A 1-42、tau和MDA对AD的诊断效能
3 讨论
AD是最常见的神经退行性疾病,在行为上以进行性痴呆为特征,人口老龄化正在增加痴呆症的患病率和社会成本。据估计,到2050年,痴呆症患者的人数将达到1.3亿[4]。
A是淀粉样前体蛋白经酶裂解后的氨基酸片段,主要有A1-40、A1-42两种结构形式,其中A1-42容易形成低聚物而沉积构成老年斑的核心,具有较强的神经毒性及聚集性,是AD患者脑内A主要的类型[5]。正常情况下,人体中A的生成与代谢处于动态平衡,若这种平衡打破或A过度生成,则会引起A沉积,以及沉积部位脑组织炎症反应,激活炎症反应通路,引起多种炎症因子释放、神经元凋亡、轴突损伤,最终导致AD的发生[6]。本研究显示,AD患者A1-42水平低于对照组,这可能是AD发生时,脑脊液中大量的A1-42蛋白在脑内缠绕形成神经元炎性斑,进而导致分泌外周血中的A1-42蛋白减少。
Tau蛋白基因位于人类染色体tau蛋白17q21.31上,是一种微管相关蛋白,其主要生理功能是与微管蛋白质结合,促进其聚合形成微管、维持微管稳定性、降低微管蛋白分子的解离并诱导微管成束[7]。本研究显示,AD组tau表达水平高于对照组(P<0.05),随着疾病的进展,其表达水平呈上升趋势。Tau蛋白过度磷酸化易形成神经原纤维缠结,而神经原纤维缠结的数量与临床痴呆程度呈正相关,高磷酸化、错误折叠的tau蛋白积聚到神经原纤维缠结中,再加上A1-42沉积到细胞外斑块中,是AD的两个标志性病理特征[8]。
MDA是由氧自由基引起的一种氧化反应的代谢产物,其含量可以反映体内生物膜中不饱和脂肪酸的过氧化程度,从而可以间接反映生物膜不饱和脂肪酸发生过氧化反应的氧自由基的水平[9]。AD患者体内自由基的水平较高,可加速细胞膜脂质的过氧化速度,并最终导致细胞膜受损和神经元的死亡。本研究显示,AD组MDA表达水平高于对照组(P<0.05),随着病情的加重,MDA表达水平也升高。这证实氧化应激在AD的发生和发展中起着重要作用,并且与AD的发病机制密切相关。
综上所述,A1-42、tau和MDA可作为AD诊断中重要生物学标记物,为AD的诊断及病情判断提供临床依据。

