小麦抗条锈基因 Yr10的抗病通路研究
高花雨,何 琪,贾劲松,丁 焱,王亚茹,王晓静,康振生
(1.西北农林科技大学植物保护学院/旱区作物逆境生物学国家重点实验室,陕西杨凌 712100;2.西北农林科技大学生命科学学院/旱区作物逆境生物学国家重点实验室,陕西杨凌 712100;3.西北农林科技大学创新实验学院/旱区作物逆境生物学国家重点实验室,陕西杨凌 712100)
小麦条锈病是由条形柄锈菌(Pucciniastriiformisf.sp.triticii)引起的一种世界性气传真菌病害。该病害发生历史久远,危害范围广,病原菌可随气流远距离传播,且极易发生变异,也是我国小麦危害最为严重的一类病害。该病害多次在全国大流行,造成严重的产量和经济损失,直接影响我国粮食安全[1]。利用抗病品种是防治小麦条锈病最根本和有效的措施,但条锈菌毒性变异频繁,已导致我国90%以上的小麦生产品种“丧失”抗锈性,对小麦生产和粮食安全构成极大威胁[1]。因此,加强小麦抗锈机制研究,合理利用小麦抗锈性,对延缓病菌变异和持续控制条锈病具有重要的意义。
经典的基因对基因学说阐明了植物中的抗病基因(R)在病原菌中都有互作的无毒基因(Avr)[2]。在植物中,目前已经克隆的植物抗病基因中,核苷酸结合位点-亮氨酸富集重复蛋白(nucleotide-binding site,leucine-rich repeat receptors,NBS-LRR)抗病基因占大多数,是一类非常重要的抗病基因,这类抗病基因编码的蛋白作为受体与病原菌Avr基因编码的蛋白直接或间接互作会引发一系列反应,包括活性氧的迸发、离子流、蛋白质的磷酸化和水杨酸(SA)含量的变化等[3-4],最终激活防御反应信号途径,产生过敏性坏死反应(hypersensitive response,HR)[5]。在NBS-LRR介导的信号通路中,植物激素SA作为信号分子诱导病程相关蛋白(PR)基因的表达上调,产生HR和整个植株广谱持久的系统获得抗性(systemic acquired resistance,SAR)[5-7]。抗病通路中很多抗病相关基因也直接参与R基因介导的抗病通路,如RAR1、SGT1和HSP90基因编码的蛋白已经被证明在NBS-LRR类R基因介导的SA抗病信号通路中起作用[8-9]。研究这些基因在小麦防御条锈菌过程中的表达和功能对阐明R基因介导的防御信号通路有重要意义[10]。
抗病基因的结构复杂多样,其抗病通路也不同。目前已经克隆的抗条锈病基因中,Yr5和Yr7是NBS-LRR类型的抗病基因,在N-端有一个保守的含锌指结构(zinc-finger)的BED结构域,该结构域通过结合转录因子WKRY来激活防御反应[11]。已有研究表明,WRKY70基因在SA信号通路中调节基因的表达[12]。Yr15是一个广谱且具有全生育期抗性的基因,其编码一个含有串联激酶结构域的蛋白WTK1(wheat tandem kinase 1),该结构域与植物抗病防御相关。Yr18(Lr34/Sr57/Pm38)编码的蛋白是一个ABC转运子(ATP-binding cassette,ABC),目前证明其作用底物是脱落酸(ABA),通过ABA影响病原菌的生长,达到抗病的目的[13]。Yr36基因编码的蛋白是一个含START结构域的激酶(Kinase-START)[14],该激酶可以通过跨膜运输进入到叶绿体,与类囊体抗坏血酸过氧化物酶结合使其磷酸化,干扰其分解过氧化氢,造成活性氧的积累,从而加速细胞死亡,有效地限制了条锈菌在小麦叶片组织内增殖[15]。Tada等[3]的研究结果表明,在寄主植物防御病原真菌引起的过敏反应中,伴随有大量的活性氧产生,并且这些活性氧的产生可能和过敏反应的起始以及发展有密切的关系。但目前对抗病基因的通路研究还非常局限,对抗病防御反应的激活和抗病信号的传导仍需深入的研究。
小麦抗条锈病基因Yr10定位于小麦1B染色体上,具有全生育期抗性的特点[16]。根据早期获得的Yr10的分子标记,Liu等[17]通过转基因和病毒介导的基因沉默(virus-induced gene silencing,VIGS)等技术,证明该基因抗条锈病,其编码的蛋白属于NBS-LRR类受体蛋白。
长期以来的研究和生产实践证明,合理利用抗病基因,培育和推广高效、稳定、广谱、持久抗病品种是防治小麦条锈病最经济、安全和有效的方法,但单一抗病品种多年使用,容易导致品种抗性丧失。因此,研究抗病基因的抗病通路,可以为传统育种提供新的思路和策略。本研究通过研究抗病基因Yr10介导的抗病通路中植株活性氧积累和侵染部位细胞坏死情况,分析内源激素SA的积累量变化和抗病相关基因的表达,以期为解析Yr10的抗病通路奠定基础,从而为将来合理利用抗病资源、培育持久高效抗病小麦材料提供理论 依据。
1 材料与方法
1.1 供试材料
供试小麦材料为AvocetS (以下简写为AvS)及其近等基因系AvSYr10NIL (near-isogenic lines,以下简写为AvS+Yr10),条锈菌生理小种为CYR31,均由西北农林科技大学旱区作物逆境生物学国家重点实验室植物免疫研究室提供。
1.2 供试材料中活性氧含量的测定
待AvS和AvS+Yr10小麦材料长至一叶一心时期,接种条锈菌CYR31,分别在接菌后0、12、24、48、72、96和120 h后剪取幼苗叶片,每个样品3个生物学重复。利用PBS缓冲液对样品进行研磨。按照植物活性氧酶联免疫分析试剂盒方法(上海沪鼎生物科技有限公司进口分装)进行H2O2含量的测定。
1.3 供试材料的细胞组织学观察
分别在接种条锈菌48和72 h后剪取叶片,将叶片剪成1~2 cm 小段,置于乙醇∶冰醋酸=1∶1的固定液中脱色固定,定期更换固定液,待叶片绿色脱净,用饱和水合氯醛溶液处理6 h后,保存于30%甘油中,Olympus BX-51 微分干涉显微镜观察细胞的坏死状况。
1.4 供试材料中内源SA含量的测定
样品的取样方法同1.2,样品称取鲜重后用液氮速冻,用破碎仪破碎样品。加浸提液(甲醇∶水∶冰醋酸=89∶10∶1)涡旋样品后,12 000 r·min-1室温离心,转移上清液到新的离心管中。重复操作2~3次。获得的样品加水稀释至甲醇浓度为50%,超低温冰箱冷冻后放置冷冻干燥仪中过夜。干燥后的样品用色谱级甲醇溶解后,用 0.22 μm有机系过滤膜过滤至上样瓶中。利用西北农林科技大学生命学院实验平台的质谱仪器LC-30A+TripleTOF5600+(AB SCIEX,Singapore)测定SA的含量。
1.5 QRT-PCR 分析
AvS和AvS+Yr10小麦样品的取样方法同1.2,采用Biozol法提取各时间点采集的小麦样品RNA,用反转录试剂盒(Thermo,美国)将RNA反转录为cDNA,利用Primer Premier 5.0软件设计基因定量分析引物(表1)。其中,以肌动蛋白actin基因作为内参基因。以反转录的各时间点cDNA为模板,利用Bio-Rad Real-time PCR仪分别检测TaRAR1、TaHSP90、TaSGT1和PR1基因的表达量。PCR扩增体系为20 μL,包括cDNA 2 μL,SYBR Green mix 1μL,上下游引物各1 μL,ddH2O补齐到20 μL。PCR反应程序为:95 ℃预变性10 min;然后95 ℃变性15 s,60 ℃延伸1 min,40个循环。收集溶解曲线程序:60 ℃升至95 ℃时,PCR仪每隔1 ℃检测一次信号。用2-ΔΔCt法[18]计算基因的相对表达量,每个处理 3次生物学重复。
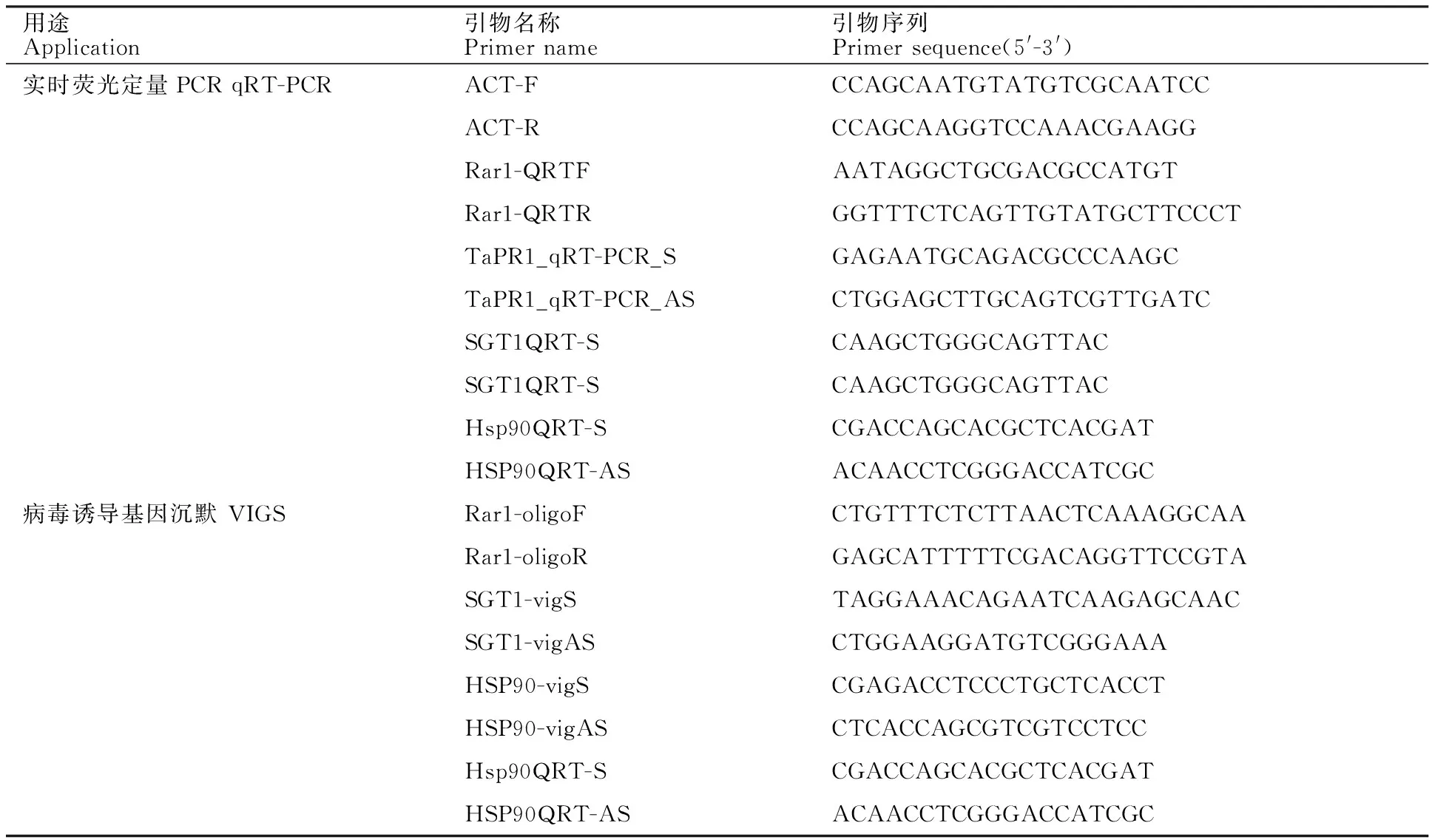
表1 试验所用引物Table 1 Primers used in the study
2 结果与分析
2.1 供试小麦材料接种条锈菌后活性氧和SA积累量的变化
从表2可以看出,SA和活性氧的积累量都存在两个高峰,但高峰出现的时间点不同。接种条锈菌后,AvS和AvS+Yr10小麦材料叶片中的H2O2含量均在接菌后24和96 h有迸发现象,在接菌72 h后H2O2含量最低,在96 h后又有所降低。AvS小麦材料的内源SA含量在接菌后12和96 h出现峰值,在接菌48 h含量最低,72 h有所回升,到120 h又恢复至接菌前水平;AvS+Yr10小麦材料的内源SA含量在接菌后12和 72 h出现峰值,在接菌后24 h内源SA含量最低, 48 h又有所升高,到120 h又恢复到接菌前的水平。总体来看,AvS小麦材料的H2O2和内源SA含量低于AvS+Yr10小麦材料。
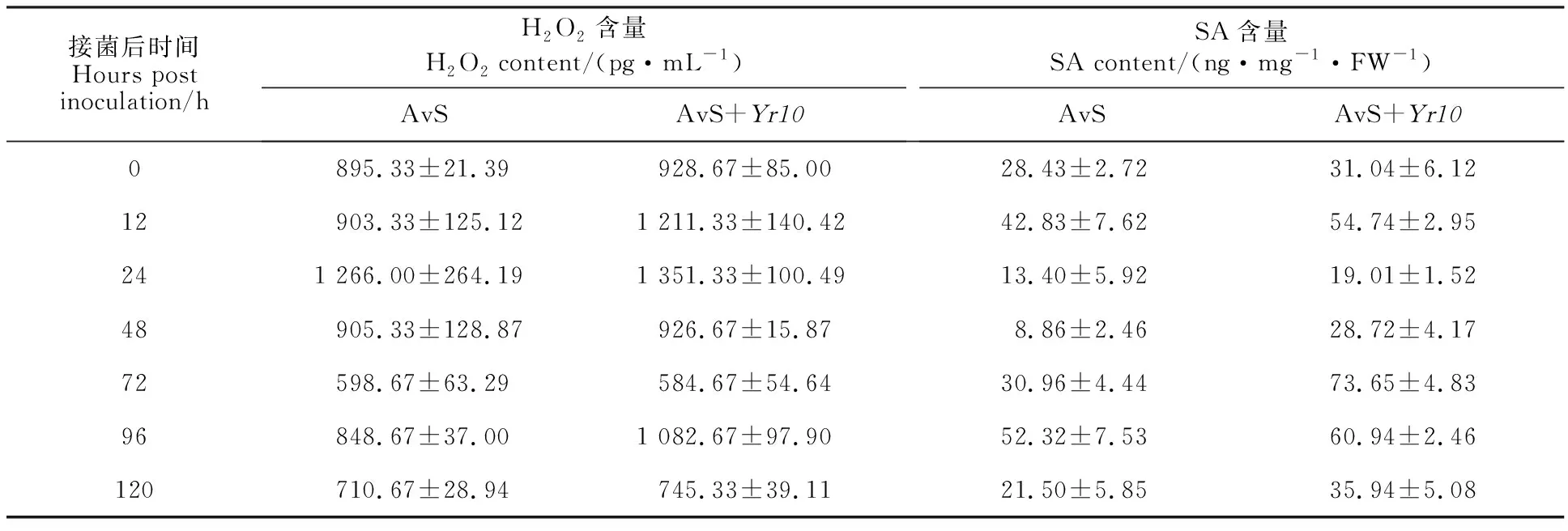
表2 接种条锈菌后AvS和AvS+ Yr10叶片中H2O2和内源SA含量的变化Table 2 H2O2 accumulation and endogenous SA concentration in AvS and AvS+ Yr10 leaves after inoculation with stripe rust
2.2 供试小麦材料接种条锈菌后细胞坏死状况
接菌后48和72 h,通过组织学观察AvS和AvS+Yr10小麦材料中条锈菌在侵染位点叶肉细胞的坏死产生情况,结果(图1)发现,在接菌后48和72 h,在微分干涉显微镜明场下均可观察到形成气孔下囊(SV)的侵染点(图1a、图1c、图1e和图1g)。活性氧的产生通常会引起侵染位点附近的叶肉细胞坏死,在接菌后48和72 h,在荧光显微镜下均可观察到AvS+Yr10小麦材料叶肉细胞产生黄色的自发荧光(图1d和1h),说明该细胞发生了HR反应,并且72 h的自发荧光面积比48 h的自发荧光面积大,表明坏死面积随侵染时间的推移而增大(图1d和1h)。而接菌后48和72 h,AvS小麦材料中没有自发荧光产生(图1b和1f)。
2.3 供试小麦材料接种条锈菌后 PR1基因的表达分析
从图2可以看出,PR1基因的表达量在AvS和AvS+Yr10小麦材料中趋势一致,均呈先升高后降低的趋势。但在接菌后不同时间点,PR1基因的表达量在含有Yr10抗病基因的小麦体内积累较多,在病原菌侵染48和72 h时,PR1基因的表达量在AvS和AvS+Yr10小麦材料间的差异达到了极显著水平,说明PR1基因在Yr10的抗病信号通路中发挥着重要作用。
2.4 抗病相关基因的表达和功能分析
利用实时定量分析抗病相关基因RAR1、SGT1和HSP90在AvS和AvS+Yr10小麦材料中接种条锈菌后的表达水平,结果(表3)发现,接菌后不同时间三个基因的表达趋势基本一致。在0~24 h均表现为上调表达,并且SGT1和HSP90基因均在AvS+Yr10材料中显著上调表达。在接菌后48 h,AvS+Yr10材料中三个基因的表达量均显著高于AvS材料。说明在Yr10介导的抗病通路中三个基因都参与了小麦对条锈菌的防御反应。
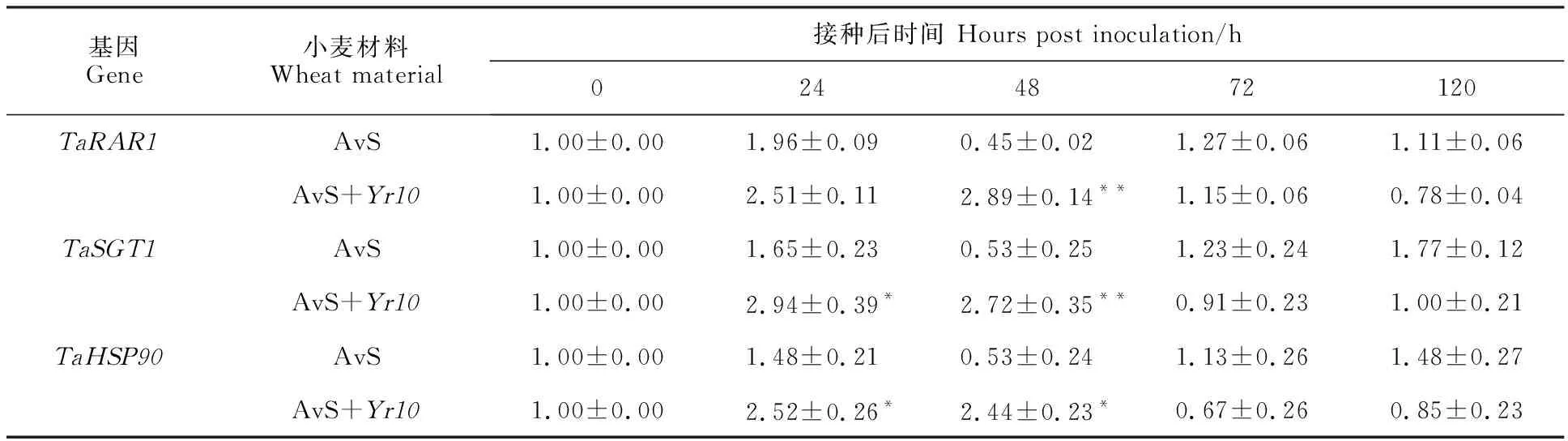
表3 TaRAR1、 TaSGT1和 TaHSP90在小麦材料AvS和AvS+ Yr10接菌后的相对表达量Table 3 Relative expression of TaRAR1, TaSGT1 and TaHSP90 in wheat material AvS and AvS+ Yr10after inoclulation of stripe rust
为了进一步验证三个基因在Yr10介导的抗病通路中的功能,对三个基因分别进行病毒诱导的基因沉默实验。摩擦接毒后12 d,接种BSMV:PDS病毒植株的第4叶出现明显光漂白现象,表明病毒RNA介导的基因沉默已经发生(图3A);沉默后的植株接种条锈菌CYR31,在接种后15 d进行表型观察,发现在不含Yr10抗病基因的AvS材料中,不做接毒处理的对照组Mock和只接病毒的对照组BSMV:00与实验组BSMV:HSP90和BSMV:RAR1的叶片均产孢,并且产孢数量无明显差异(图3B)。而在含有Yr10抗病基因的小麦材料AvS+Yr10中,BSMV:HSP90和BSMV:RAR1实验组与对照组BSMV:00相比,过敏性坏死反应程度降低(图3A)。结果表明,TaRAR1和TaHSP90在Yr10抗病基因引起的过敏性坏死反应中起作用。TaSGT1由于沉默后严重影响植物的发育,未展示结果。
为确定TaRAR1和TaHSP90基因的沉默效率,通过实时定量检测沉默后叶片中这2个基因的表达量。在接种BSMV:PDS病毒植株出现光漂白现象时,分别对接种BSMV:HSP90和BSMV:RAR1的沉默植株进行取样,并测定TaHSP90和TaRAR1基因的表达量。与接种空病毒BSMV:00对照组相比,亲和组合AvS/CYR31中TaHSP90和TaRAR1基因的沉默效率分别为67%和83%,非亲和组合AvS+Yr10/CYR31中TaHSP90和TaRAR1基因的沉默效率分别为66%和91%,表明两个基因都被显著抑制(表4)。

表4 TaHSP90和 TaRAR1基因沉默的小麦材料中的相对表达量Table 4 Relative expression of TaHSP90 and TaRAR1 in gene silenced wheat
3 讨 论
活性氧在植物的防御反应中扮演一个重要的角色[19-20]。寄主抗病基因R识别病原菌Avr基因编码的蛋白后会快速迸发活性氧,然后诱导侵染部位发生HR反应及抗病相关基因的表达[5]。本研究对小麦材料AvS和含有Yr10抗病基因的近等基因系AvS+Yr10接种条锈菌小种CYR31分别组成亲和与非亲和体系。通过酶联免疫法和组织学检测法研究非亲和体系中活性氧积累和细胞的坏死情况。在非亲和体系中,活性氧在接菌后24和96 h出现迸发现象。伴随活性氧的产生,侵染位点的组织细胞坏死。说明在Yr10介导的植物防御反应中活性氧的产生作为早期事件,细胞内活性氧的升高抑制了条锈菌的菌丝发育和菌落形成,并在侵染点的寄主细胞发生典型的过敏性细胞坏死,完成植物防御反应。这些变化与条锈菌和其他抗病品种的非亲和组合所表现出的特征基本一致[19,21]。
R基因介导的抗性触发了信号转导而导致局部细胞程序性死亡(PCD)和SAR,PCD即HR反应[22-23]。HR发生在感染部位可以限制活体寄生菌在内的病原菌在寄主体内的扩展。通过SA介导的信号传导途径,SAR经常与PR基因一起被诱导产生整株或广谱植物抗性[24-25]。在NBS-LRR介导的信号通路中,SA在植物防御反应过程中具有重要作用[4]。本研究结果表明,含抗条锈病基因Yr10的小麦材料AvS+Yr10中内源SA含量在接菌后12和72 h出现高峰,两个高峰出现的时间较活性氧迸发的时间较早。而在SA含量产生高峰前,H2O2含量虽未到达顶峰,但出现了快速的积累,其诱导了SA的快速积累并达至高峰。反之,SA的积累又加速了H2O2的积累,使得活性氧含量的第一个高峰出现。说明在非亲和体系中,SA信号作为一个更早的信号,与活性氧迸发之间存在一定的相关性,这种相关性形成一种微循环,互相促进植物防御反应的发生,最终使植物产生获得性免疫反应。PR基因的表达量也随SA的积累和活性氧的产生逐渐升高,在接菌后48和72 h亲和与非亲和组合出现显著差异。Wang等[9]研究表明,在水源11组成的非亲和体系中,内源SA和H2O2含量增加,小麦的抗性增强,这与本研究中Yr10抗病通路中的SA和活性氧含量的变化一致。在小麦抗病基因Yr10与Avr基因识别后,活性氧含量的升高引起SA信号的级联转导,诱发活性氧的迸发,进而引起下游PR蛋白的表达,导致HR反应和HR的发生。
在抗病通路中,HR反应是植物抗病基因和病原菌Avr基因编码的蛋白相互作用的结果,在这个过程中抗病蛋白复合体的激活往往由其他抗病相关基因调控,在抗病中具有重要作用[8,23]。如RARl编码的蛋白首次是从大麦抗白粉病基因Mla12介导的抗病信号途径中分离的一个重要信号元件。RAR1通常与SGT1和HSP90相互作用形成蛋白复合体,促进抗病基因复合物的形成和激活,对完成下游PR1基因的表达起到重要作用。本研究发现,与AvS材料相比,AvS+Yr10材料中RAR1、HSP90和SGT1基因的表达量均在接菌后24 h显著升高,并且基因沉默后能引起HR反应的降低。因此,在抗病通路中,SA激素、活性氧和抗病相关蛋白形成的复合体共同调节由抗病基因引起的寄主细胞坏死。基于本研究的初步研究结果,笔者提出Yr10介导的抗病通路模式为:在早期抗病基因R和病原菌的无毒基因Avr识别,抗病相关蛋白RAR1、HSP90和SGT1形成蛋白复合体通过某种方式维持抗病蛋白复合体的结构处于激活状态,随后SA信号分子的积累促进活性氧的迸发和HR反应,但其具体调节的分子机制还需要进一步研究。

