电感耦合等离子体质谱法测定土壤中有效钼
冯奇
(贵州省煤田地质局实验室,贵阳 550081)
钼(Mo)是植物必需的微量元素之一,在植物体内参与氮素循环,增强植物的光合作用,在植物体内的氧化还原反应中起着传递电子的作用,是硝酸还原酶和固氮酶的成分[1]。土壤中钼可分为水溶性钼、交换性钼、难溶性钼和有机结合态钼,能被植物吸收的钼统称为有效钼。有效钼广泛存在于土壤中,不同地区的土壤中钼含量存在较大差异,大部分地区含量为0.1~1 mg/kg,部分地区可达到5 mg/kg以上。当植物中钼含量低于0.1 mg/kg 时,叶片脉间失绿,甚至变黄、变厚、畸形,易出现斑点甚至焦枯。然而当植物体内钼含量高于200 mg/kg 时,会抑制植物的生长[2–5],使植物出现钼中毒症状。因此建立准确、便捷地测定土壤中有效钼含量的分析方法具有重要意义。
目前浸提土壤中有效钼的浸提剂主要有AB–DTPA(碳酸氢铵–二乙三胺五乙酸)溶液和Tamm(草酸–草酸铵)溶液。Tamm 溶液缓冲容量较大,适用于各种类型的土壤,应用较为广泛[6–10]。测定土壤中有效钼的方法主要有分光光度法[11]、极谱法[12]、石墨炉原子吸收光谱法[13]、电感耦合离子体发射光谱法[14]和化学发光法[15]等。上述方法前处理复杂,步骤繁琐,结果不稳定,灵敏度低。电感耦合等离子体质谱(ICP–MS)法具有线性范围宽、灵敏度高、干扰少、重现性好等优点。目前采用ICP–MS 法测定土壤中有效钼含量已有文献报道,林光西[16]以光谱纯MoO3配制标准溶液,采用ICP–MS法测定土壤中的钼。刘蜜等[17]对ICP–MS 测定方式进行了改进,采用氦气碰撞模式,提高了测定结果的准确性和重现性,但加标回收率不太理想。冯信平等[18]对ICP–MS 法测定土壤中有效钼含量的不确定度进行评定,从样品称量、标准溶液配制、提取过程、稀释过程和标准曲线拟合等方面,综合计算出扩展不确定度为0.028 mg/kg(k=2)。上述方法均是土壤浸提液不经分离和富集,采用定性滤纸干过滤,滤液直接上机测定。滤液中含有大量Ca、Na、K、Mg、Al、Ti、Fe、Mn 等离子,采用ICP–MS 法测定有效钼时会造成基体干扰,影响测定结果。笔者在前人研究的基础上,通过对滤液进行稀释,降低待测样品溶液中各组分的浓度,以降低基体干扰,建立了电感耦合等离子体质谱法测定土壤中有效钼的分析方法。该方法灵敏、准确、捷性,适用于土壤中有效钼的测定。
1 实验部分
1.1 主要仪器与试剂
电感耦合等离子体质谱仪:2000B 型,美国珀金埃尔默股份有限公司。
震荡器:HY–8A 型,常州朗越仪器制造有限公司。
pH 计:PHS–3cb 型,上海越平仪器有限公司。
电子天平:Scout 系列,感量为0.1 mg,奥豪斯仪器(常州)有限公司。
移液枪:1~10 mL,艾本德(中国)有限公司。
草酸、草酸铵、氨水、氯化铵、硝酸:均为优级纯,成都科隆化学有限公司。
Be、Ce、Fe、In、Li、Mg、Pb、U 多 元 素 仪 器调谐液:1 μg/L,基质为1%硝酸溶液,编号为N8145051,美国珀金埃尔默股份有限公司。
铑(103Rh)、钼(95Mo)单元素标准溶液:1 000 mg/L,编 号 分 别 为GSB 04–1746–2004 和GSB 04–1737–2004,国家有色金属及电子材料分析测试中心。
24 种元素(铝、砷,硼、钡、铍、铋、镉、钴、铬、铜、铁、镓、锂、镁、锰、镍、铅、锑、锡、锶、钛、铊、钒、锌)混合标准溶液:100 μg/mL,编号为GSB 04–1767–2004,国家有色金属及电子材料分析测试中心。
土壤有效态成分分析标准物质–黑龙江黑土:编号为NSA–1,有效钼含量为(0.11±0.03) mg/kg,地球物理地球化学勘查研究所。
土壤有效态成分参比物质–陕西延安黄绵土:编号为NSA–3,有效钼含量为(0.09±0.03)mg/kg,地球物理地球化学勘查研究所。
土壤样品:采集于贵州剑河地区,编号分别为T1(耕田),T2、T3(旱地),T4(果园),土壤样品基本性质见表1。
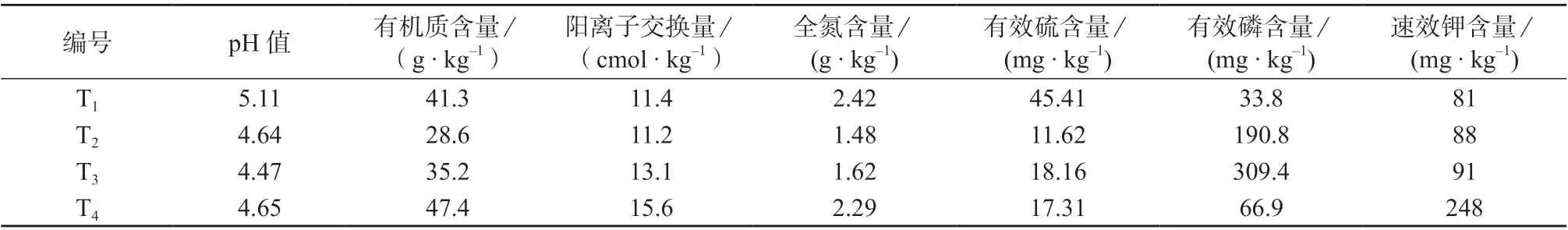
表1 土壤样品基本性质
氩气、氦气:体积分数均为99.999%。
实验用水为超纯水,电阻率大于18 MΩ·cm。
1.2 溶液配制
草酸–草酸铵缓冲溶液:称取24.9 g 草酸铵与12.6 g 草酸于烧杯中,加入超纯水加热,使其完全溶解,冷却,用质量浓度为20 g/L 的氯化铵溶液调节溶液pH 值为3.3,用超纯水定容至1 L。
硝酸溶液:5%,移取50 mL 浓硝酸于1 L 量杯中,加入超纯水至1 L,用玻璃棒搅拌均匀,现配现用。
铑内标溶液:10 μg/L,移取1 mL 铑单元素标准溶液于1 L 容量瓶中,用5%硝酸溶液定容至标线,摇匀,配制成质量浓度为1 000 μg/L 的铑内标中间溶液。移取10 mL 铑内标中间溶液于1 L 容量瓶中,用5%硝酸溶液定容至标线,摇匀。
钼单元素标准贮备溶液:1 000 μg/L,移取1 mL 钼单元素标准溶液于1 L 的容量中,用5%硝酸溶液定容至标线,摇匀。
系列钼标准工作溶液:依次移取钼单元素标准贮备溶液0、1.5、2.5、5、7、10 mL,分别置于6 只100 mL 容量瓶中,用5%硝酸溶液定容至标线,摇匀,配制成钼的质量浓度分别为0、15、25、50、70、100 μg/L 的系列钼标准工作溶液,然后分别将系列钼标准工作溶液转移至聚乙烯瓶中保存。
1.3 仪器工作条件
射频功率:1 250 W;辅助气:氩气,流量为0.7 L/min;雾化气:氩气,流量为0.8 L/min;等离子体气:氩气,流量为15 L/min;碰撞气:氦气,流量为5 mL/min;洗脱时间:20 s,读取时间:10 s;测量方式:跳峰。
1.4 样品处理
将采集的土壤样品在通风、阴凉处放置半月,待干燥后磨成粉末,过孔径为2 mm 的尼龙筛,按四分法装袋[19]。称取5.0 g 研磨好的土壤样品于250 mL 干净的聚乙烯瓶中,准确加入50 mL 草酸–草酸铵缓冲液,盖盖密封,置于25 ℃震荡室中,以150 r/min 转速震荡1 h,然后静置10~14 h。取1 mL上清液于25 mL 的离心管中,加入5%硝酸溶液10 mL 稀释,摇匀,待测。同法制备空白溶液。
2 结果与讨论
2.1 稀释液选择
按1.4 方法分别对土壤样品T1、T2、T3、T4和土壤有效态成分分析标准物质NSA–1、NSA–3 进行处理,将静置后的浸提液分别按不稀释、5%硝酸溶液稀释、超纯水稀释3 种方式处理,然后在1.3 仪器工作条件下进行测定,结果见表2。由表2 可知,不稀释时,标准样品NSA–1、NSA–3 钼含量测定值分别为0.16、0.11 μg/g,均大于标示值0.11、0.09 μg/g。采用5%硝酸溶液和超纯水稀释时,测定值与标示值基本一致。由表2 还可以看出,不稀释时,内标溶液103Rh 的回收率为75.11%~89.87%,说明土壤浸提液中干扰因素较多,测定结果有漂移。用5%硝酸稀释时,103Rh 的回收率为95.68%~105.02%;用超纯水稀释时,103Rh 的回收率为93.01%~97.57%,表明用5%硝酸溶液稀释土壤浸提液测定结果稳定性更好,因此选择5%硝酸溶液为稀释液。
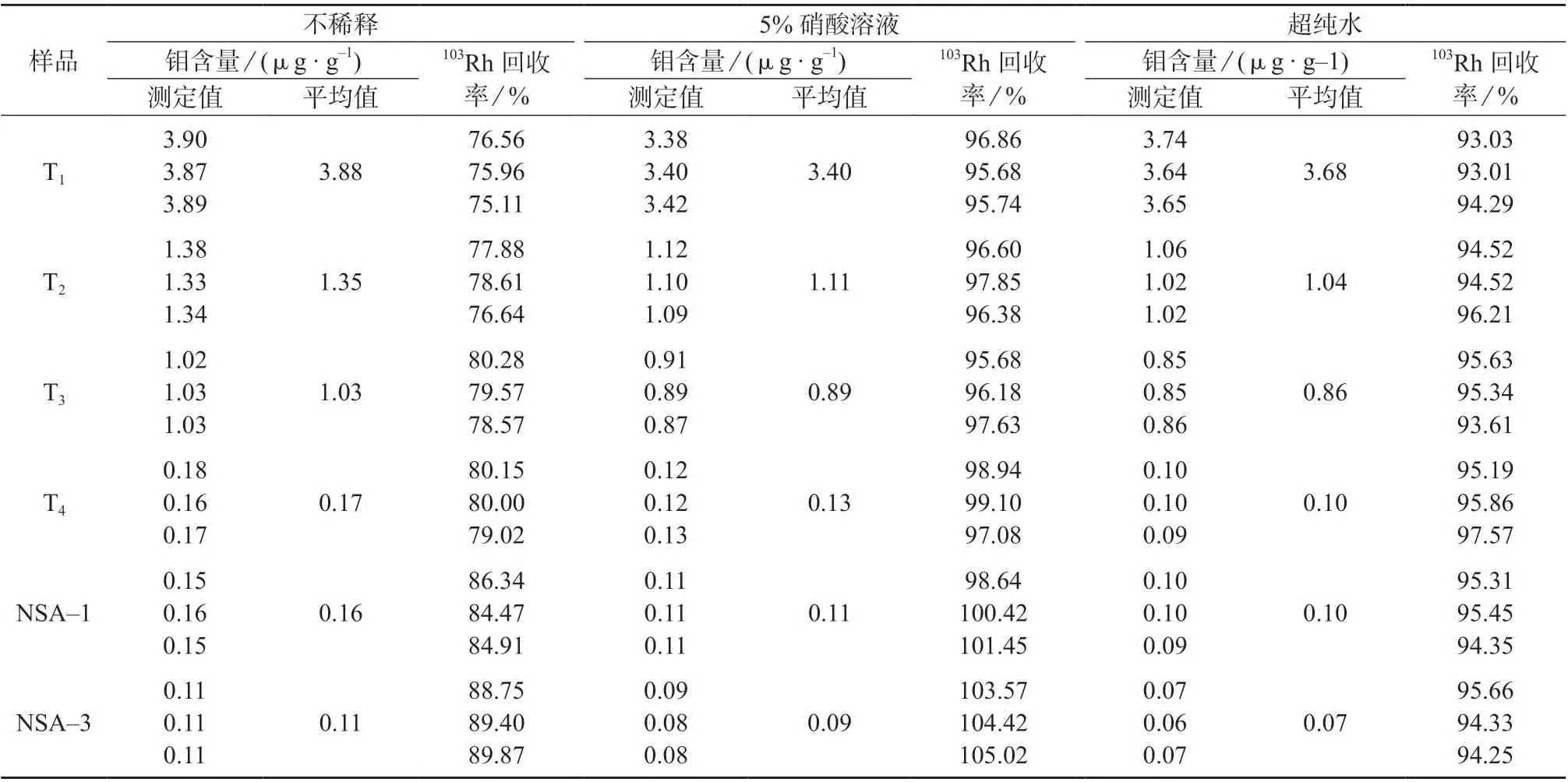
表2 不同稀释方式时的钼含量及103Rh 回收率
2.2 浸提液静置时间选择
选择土壤样品T1、T2、T3、T4和土壤有效态成分分析标准物质NSA–1、NSA–3,按1.4 样品处理方法,分别加入50 mL 草酸–草酸铵缓冲液,以150 r/min 的转速震荡1 h,然后分别在静置2、4、6、8、10、12、14、16、18、20 h 时移取上清液,用5%硝酸溶液稀释,在1.3 仪器工作条件下进行测定,考察不同静置时间对钼含量测定结果的影响,结果见表3 和图1。由表3 可知,当土壤中有效钼含量较低(T4、NSA–1、NSA–3)时,静置时间对测定结果影响不显著;当有效钼含量较高时(T1,T2),静置时间对测定结果影响较大。由图1 可以看出,当静置时间小于10 h 时,浸提液中有效钼的质量浓度测定结果普遍偏低,且随着静置时间的延长,测定值逐渐增大,这是因为浸提时间短,浸提剂与土壤中的钼离子螯合不完全,导致测定结果偏低;当静置时间为10~14 h 时,曲线趋于平缓,测定结果较为稳定;当静置时间大于14 h 时,随着土壤中Ca、Na、K、Mg、Al、Ti、Fe、Mn 等多种离子的溶解,土壤样品溶液中的基体发生改变,基体效应造成的干扰因素增强,导致测定结果偏高,综合考虑选择静置时间为10~14 h。
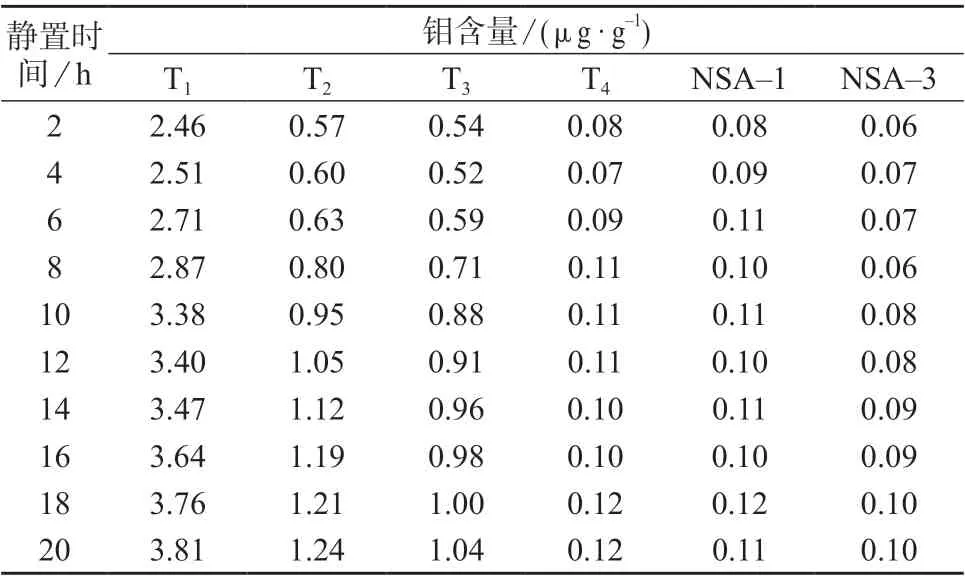
表3 滤液不同静置时间时的测定结果

图1 静置时间对浸提液中有效钼质量浓度的影响
2.3 基体效应
ICP–MS 痕量分析中的干扰主要分为质谱干扰和非质谱干扰。质谱干扰通过优化仪器工作条件进行消除;非质谱干扰即基体效应,主要是由于土壤中含有大量的Ca、Na、K、Mg、Al、Ti、Fe、Mn 等多种元素,基体组成复杂,测定时易导致等离子体中的电离平衡发生移动,进而引起待测物质分析信号变化[20–21]。为了探究基体效应的影响,以24 种元素混合标准溶液配制不同浓度的基体溶液,分别加入到NSA–1、NSA–3 土壤标准溶液中,在1.3 仪器工作条件下进行测定。结果表明,当基体质量浓度低于20 μg/mL 时,钼元素测定值基本不受干扰;当基体质量浓度大于30 μg/mL 时,钼元素测定值增加15%;当基体质量浓度大于50 μg/mL时,钼元素测定值增加50%,表明钼元素测定值随着基体质量浓度的增大逐渐增大。为降低基体干扰,本试验通过对浸提液进行稀释,减小了待测样品溶液中干扰元素的质量浓度,消除了基体干扰。同时在测定过程中加入103Rh 内标溶液作为监控和基体补偿。
2.4 仪器工作条件优化
为了提高仪器分析灵敏度、降低氧化物和双电荷产率的干扰,在质谱仪点火成功30 min 后,用Be、Ce、Fe、In、Li、Mg、Pb、U 多元素仪器调谐液优化仪器工作条件。当不同质量数元素的信号强度(IS)分别为IS(9Be)>4 500、IS(24Mg)>100 000、IS(115In)>40 000、IS(Pb)>3 000、IS(238U)>60 000 时,仪器灵敏度达到最高值,信号稳定。当Ce++/Ce 信号强度小于0.03,CeO/Ce 信号强度小于0.025 时,可消除氧化物和双电荷造成的质谱干扰。在谱线选择时,综合同量异位素干扰,背景干扰和元素丰度等因素,确定95Mo 为测量谱线。采用碰撞反应池模式,消除对95Mo 有干扰的多原子离子79Br16O+和40Ar39K16O+。为消除元素的记忆效应,延长进样的洗脱时间,优化结果见1.3。
2.5 线性方程与检出限
在1.3 仪器工作条件下,对1.2 中的系列钼标准工作溶液进行测定,以钼的质量浓度(X)为横坐标,以质谱信号强度(Y)为纵坐标,绘制标准工作曲线,计算得线性方程为Y=1 298X+146.32,相关系数为0.999 9,线性范围为0~100 μg/L。
在1.3 仪器工作条件下,对空白样品溶液连续测定13 次,计算标准偏差,以3 倍标准偏差作为检出限,计算得方法检出限为1.12 μg/L。
2.6 精密度试验
选择土壤样品T1、T2、T3、T4各7 份,按照1.4方法分别对样品进行处理,在1.3 仪器工作条件下测定,结果见表4。由表4 可知,测定结果的相对标准偏差为0.69%~1.38%,表明该方法具有较高的精密度,满足LY/T 1259—1999 《森林土壤有效钼的测定》要求[22]。
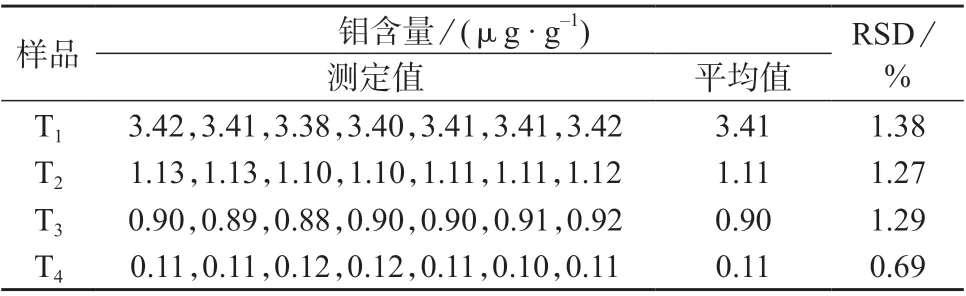
表4 精密度试验结果
2.7 准确度试验
按照1.4 方法对标准样品NSA–1,NSA–3 进行处理,在1.3 仪器工作条件下测定,结果见表5。由表5 可知,测定值与标示值基本一致,相对偏差均不大于11.76%,满足测定要求。
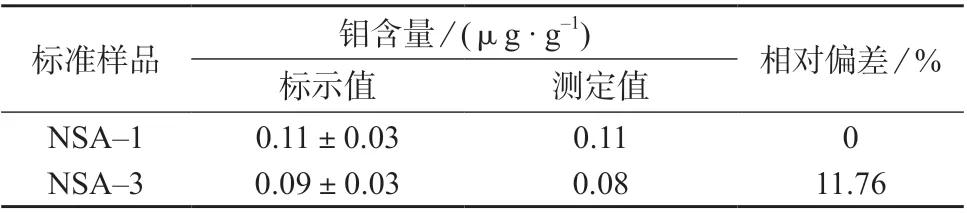
表5 准确度试验结果
2.8 加标回收试验
选择土壤样品T1、T2、T3、T4和土壤有效态成分分析标准物质NSA–1、NSA–3,分别加入一定量的钼标准溶液,按照1.4 方法对样品进行处理,在1.3仪器工作条件下测定,进行加标回收试验,结果见表6。由表6 可知,样品加标回收率为94%~104%,表明该方法有良好的准确度。
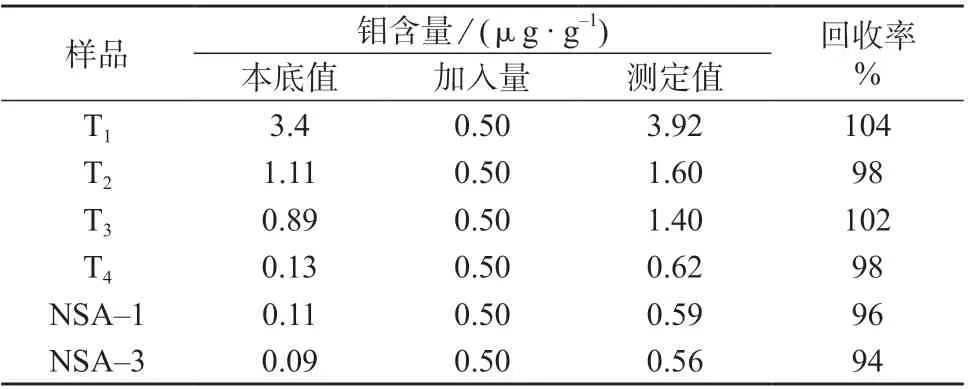
表6 加标回收试验结果
3 结语
建立了电感耦合等离子体质谱法测定土壤中有效钼含量的方法。采用草酸–草酸铵缓冲液浸提土壤样品,用5%硝酸溶液对浸提液进行稀释,以103Rh 为内标补偿基体效应和仪器信号的漂移,在氦气碰撞模式下进行测定。该方法灵敏,快速和准确,可用于土壤中有效钼的测定。

