石油污染土壤微生物群落分布特征
孙 娟, 王 宁, 陈宏坤, 宋权威, 杨晓晴, 赵朝成, 张秀霞, 郑秀志
(1.中国石油大学(华东) 化学工程学院,山东 青岛 266580;2.石油石化污染物控制与处理国家重点实验室,北京 102206;3.中国石油集团安全环保技术研究院有限公司,北京 102206)
石油是一种重要的能源,在促进经济发展的同时也带来了大量的环境问题。在石油开采、储运和生产加工等过程中,不可避免地会对土壤、地表水及地下水造成不同程度的污染。其中,在油田和油井钻凿过程中对周围土壤的污染、石油开采过程中形成的落地油、输油管路的渗漏等,是土壤石油污染的主要途径[1]。石油污染物可以影响土壤的微生物群落结构[2-10]。微生物与环境的相互作用是微生物在各种不同环境中生存和繁殖的关键。其中,土壤细菌群落是土壤微生物中数目最多、分布最广且成分最丰富的微生物之一,土壤真菌是土壤微生物的主要成员,古菌是土壤中存在的一种特殊的生命形式。它们共同作为土壤生态系统的重要组成部分,在碳循环、氮循环等生物地球化学进程中起着不可替代的作用。同时,土壤的理化性质和生物学特征也被土壤微生物通过不同途径改变,包括有机质的合成分解、污染物降解、养分固定与释放等[11-17]。
目前,对土壤微生物群落结构的研究可采用变性梯度凝胶电泳、实时荧光定量PCR、荧光原位杂交、序列标签标记的高通量测序以及宏基因组等技术。其中,高通量测序技术具有高准确度、低成本等优势[18-19]。因此,笔者采用高通量测序技术对不同污染程度的石油污染土壤样品中细菌、真菌以及古菌群落结构进行研究,探究微生物群落分布及其与石油污染土壤性质之间的关系,为深入认识油污土壤微生物群落分布特征以及油污土壤的高效生物修复技术的建立提供理论基础。
1 实验部分
1.1 原料和试剂
实验试剂:牛肉浸膏、胰蛋白胨、琼脂粉,BR,国药集团化学试剂有限公司产品;氯化钠、无水硫酸钠、四氯化碳、碳酸氢钠、正己烷,AR,上海泰坦科技股份有限公司产品;硅酸镁、氯化钾、重铬酸钾、浓硫酸、邻菲罗啉、硫酸亚铁、钼锑抗、硼酸、甲基红、溴甲酚绿、浓盐酸、高锰酸钾、硅胶,AR,国药集团化学试剂有限公司产品;二氯甲烷、氢氧化钠,AR,西陇科学股份有限公司产品。
油污土壤样品:油污土壤采集地点位于东营某炼油厂(东经118°5′,北纬38°15′)的油罐区(YGQ)、污油场(WYC)、垃圾场(LJC)3个地点,各采集 0~20 cm 上层土壤样品和20~50 cm下层土壤样品,分别记为YGQ0-20、YGQ20-50、WYC0-20、WYC20-50、LJC0-20、LJC20-50。将各土壤样品去除植物根系和石块后经2 mm尼龙筛过筛,备用。
1.2 土壤性质测定方法
采集的新鲜土壤样品立即采用烘干法进行含水率的测定,并采用平板计数法测量细菌总数。土壤样品风干后进行其他性质的测定。其中,采用筛分法测定土壤粒径,采用酸度计法测定土壤pH值,采用电导率仪测定土壤电导率,采用重铬酸钾容量法测定土壤有机质含量,采用凯氏定氮法测定土壤全氮含量,采用碳酸氢钠浸提-钼锑抗分光光度法(TU-1901双光束紫外可见分光光度计)测定土壤有效磷含量,采用四氯化碳萃取-红外分光光度法(红外光度测油仪2000-Ⅰ,吉林欧伊尔环保科技发展有限公司产品)测定土壤油含量,采用比重瓶法测定土壤密度。对于测定的土壤性质均进行3次测定取平均值。
1.3 油污土壤烃类组分分析方法
油污土壤样品用二氯甲烷萃取后脱水、浓缩后过层析柱,饱和烃和芳香烃洗出液均浓缩到0.9 mL,分别加入100 μL正构烷烃内标(C24D50,100 μg/mL)和100 μL多环芳烃内标(d14-三联苯,20 μg/mL),定容后采用安捷伦科技有限公司生产的7890A-5975C GC-ms联用仪(配备MS5975型质谱检测器和30 m×0.25 mm×0.25 μm的HP-5ms毛细管色谱柱)测定萃取液中烃类组分,并计算油污土壤中烃类组分的质量分数。
色谱条件:高纯N2为载气,流速为1.0 mL/min;进样口温度为280 ℃;进样方式为不分流;升温程序为初始温度50 ℃保持5 min,以升温速率 6 ℃/min 升温至300 ℃并保持20 min。
质谱条件:电子轰击电离源,离子源温度280 ℃,采用全扫描(SCAN) 模式。土壤样品中烃类组分含量(质量分数)计算方法如式(1)~(3)所示[20]。
(1)
(2)
(3)
式中:FRR(Relative response factor)为相对响应因子;AC0和AC1为标准样品和所测样品中组分峰面积;AI0和AI1为标准样品和所测样品中内标峰面积;mC0和mC1为标准样品和所测样品中组分质量,g;mI0和mI1为标准样品和所测样品中内标质量,g;n为稀释倍数;V1为所测样品体积,mL;V2为油污土壤萃取液总体积,mL;mT为土壤的质量,g;wT为土壤中组分质量分数,g/g。
1.4 高通量测序及统计分析
将采集的新鲜土壤样品进行脱氧核糖核酸(DNA)提取和高通量测序。采用分光光度计(Nanodrop)进行紫外定量检测总DNA,采用Q5高保真DNA聚合酶进行聚合酶链式反应(PCR)扩增。PCR扩增产物通过2%琼脂糖凝胶电泳进行检测,并采用AXYGEN公司生产的凝胶回收试剂盒对目标片段进行切胶回收。参照电泳初步定量结果,将PCR扩增回收产物进行荧光定量。根据荧光定量结果,按照每个样品的测序量需求,对各样品按相应比例进行混合。最后,采用Illumina MiSeq平台对土壤样品真菌、细菌、古菌群落DNA片段进行双端测序。使用QIIME软件,调用UCLUST这一序列比对工具,对前述获得的序列按照97%的序列相似度进行归并和可操作分类单元(Operational taxonomic unit,OTU)划分,并选取每个OTU中丰度最高的序列作为该OTU的代表序列。使用QIIME软件,获取各样品在门、纲、目、科、属5个分类水平上的组成和丰度分布表。通过主成分分析研究样品Beta多样性,对群落数据结构进行自然分解并通过对样品排序,观测样品之间的差异。
采用Chao1丰富度指数、ACE丰富度指数、Shannon多样性指数和Simpson多样性指数来反映其Alpha多样性,使用QIIME软件分别对每个样品计算上述4种多样性指数。使用R软件,对丰度前50位的属进行聚类分析并绘制热图。分析油污土壤微生物群落与土壤烃类组分的相关性,将各样品群落按照门及属水平分别进行整理,分析群落组成受石油污染的影响。
2 结果与讨论
2.1 油污土壤基本性质
图1为油污土壤样品的粒径分布。根据土壤的分类和定名标准[21],YGQ0-20、YGQ20-50、WYC0-20、WYC20-50、LJC0-20为粗砂,LJC20-50为中砂。表1为油污土壤的基本性质。由表1可以看出,YGQ0-20土壤样品含水率最低,仅为1.35%(质量分数),其次为WYC0-20,含水率为14.25%,其余土壤样品含水率均在20%以上。从土壤pH值可以看出,LJC0-20和LJC20-50为弱碱性土壤,其余样品为中性土壤,油污程度对pH值没有明显的影响。WYC0-20土壤样品中油质量分数最高为8.632 g/kg,其次为LJC0-20;YGQ取样点油含量明显低于WYC、LJC两点,YGQ20-50油含量最低;油污土壤样品的油含量与有机质含量呈正比关系。土壤有效磷质量分数为0.6~14.0 mg/kg,全氮质量分数为9~79 mg/kg,且油含量与有效磷含量和全氮含量无明显的相关性。

≥2 mm; 2-0.9 mm; 0.9-0.6 mm; 0.6-0.5 mm; 0.5-0.45 mm; 0.45-0.1 mm; 0.1-0.08 mm; ≤0.075 mm图1 油污土壤样品粒径分布Fig.1 Particle size distributions of oil-contaminated soil samples
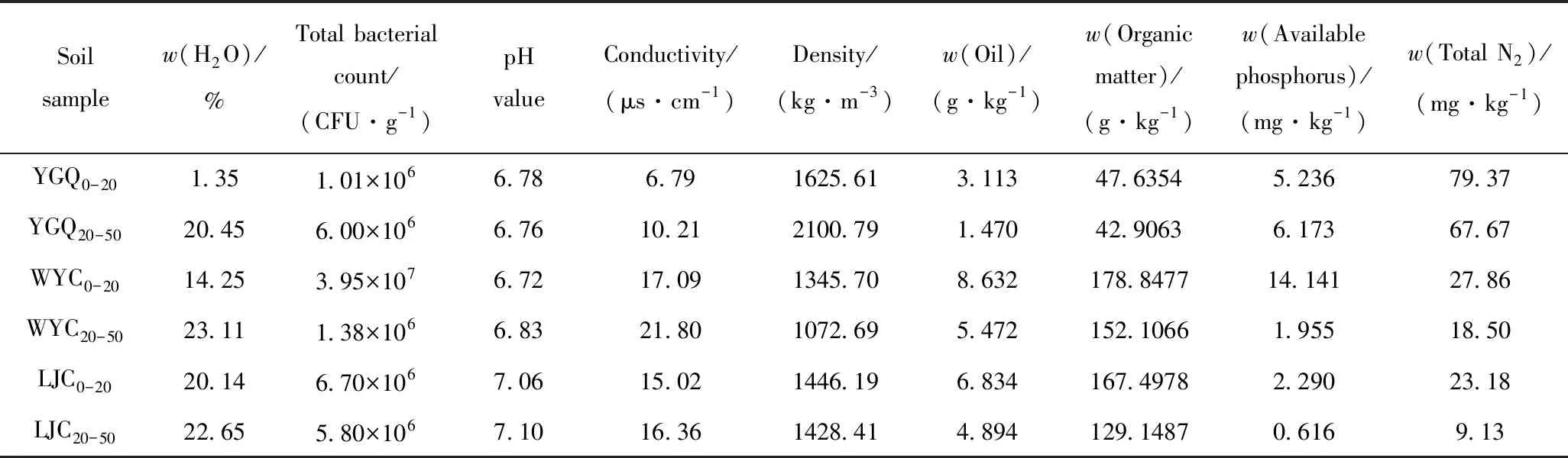
表1 油污土壤基本性质Table 1 Properties of oil-contaminated soil samples


F1—Normal paraffin; F2—Aromatic hydrocarbonsA—Anthracene; B—Benzene; C—Chrysene; D—Dibenzothiophene; F—Fluorene; N—Naphthalene; P—Phenanthrene; I—Pyrene图2 油污土壤中烃类组分含量分布Fig.2 Hydrocarbons mass fraction in oil-contaminated soil samples(a) YGQ-F1; (b) YGQ-F2; (c) WYC-F1; (d) WYC-F2; (e) LJC-F1; (f) LJC-F2
综上所述,可以认为油污土壤中正构烷烃碳数范围主要分布在C13~C32,同一取样点上层土壤中碳数范围在C16~C21的正构烷烃含量较高,而下层土壤中C22~C30的正构烷烃含量较高。上层土壤中芳香烃的种类和含量明显高于下层土壤。
2.2 油污土壤中微生物群落多样性指数分析
2.2.1 油污土壤的微生物群落丰富度及多样性
6个土壤样品通过质量筛查,且Index完全匹配时共获得272199条有效ITS序列、227067条有效细菌序列、210468条有效古菌序列。将以97%的序列相似度作为OTU划分和分类地位鉴定,此次测序结果可划分为845个真菌OTU、5444个细菌OTU及451个古菌OTU(分类至属水平)。图3为不同油含量的油污土壤中微生物群落的OTU数量。从图3可以看出,微生物群落OTU数量随着油污土壤油含量增加呈先增加后减少的趋势,这说明石油为微生物的生长提供了丰富的碳源,但当土壤中油质量分数(即污染程度)高于8.632 g/kg时,则会抑制微生物生长。

图3 不同油含量的油污土壤中微生物群落的可操作分类单元(OTU)数量Fig.3 Operational taxonomic unit (OTU) number of the microbial communities in the oil-contaminatedsoil samples with different oil contents
对于微生物群落而言,有多种指数来反映其Alpha多样性。常用的度量指数主要包括侧重于体现群落丰富度的Chao1指数和ACE指数,以及兼顾群落均匀度的Shannon指数和Simpson指数。一般而言,Chao1或ACE指数越大,表明微生物群落的丰富度越高;Simpson指数降低,表明微生物群落的多样性降低,Shannon指数越高,表明微生物群落的均一性越高。表2为不同油污土壤样品的真菌、细菌、古菌群落的多样性指数。根据Chao1或ACE指数可知,油污土壤样品真菌群落的丰富度由大到小顺序为LJC0-20、YGQ20-50、 LJC20-50、WYC20-50、 WYC0-20、YGQ0-20;其细菌群落的丰富度由大到小顺序为YGQ20-50、 LJC20-50、 WYC20-50、WYC0-20、LJC0-20、YGQ0-20;其古菌群落的丰富度由大到小顺序为LJC0-20、LJC20-50、WYC20-50、YGQ20-50、WYC0-20、YGQ0-20。根据Shannon和Simpson指数可得,油污土壤样品真菌群落的多样性由大到小顺序为LJC20-50、YGQ20-50、LJC0-20、WYC20-50、WYC0-20、YGQ0-20;其细菌群落的多样性由大到小顺序为YGQ20-50、LJC0-20、LJC20-50、WYC20-50、WYC0-20、YGQ0-20;其古菌群落的多样性由大到小顺序为LJC0-20、WYC20-50、LJC20-50、YGQ20-50、YGQ0-20、WYC0-20。可以看出:YGQ0-20和WYC0-20样品群落的丰富度和多样性均较差;这可能是因为YGQ0-20含水率过低(质量分数1.35%),影响了微生物群落的丰富度和多样性;WYC0-20土壤样品中油质量分数过高(8.632 g/kg),抑制了微生物生长,从而影响了其丰富度和多样性。
2.2.2 油污土壤的Beta多样性分析
使用R软件对加权(Weighted)的UniFrac距离矩阵进行非度量多维尺度分析(NMDS),通过二维排序图描述群落样品的结构分布(结果如图4所示),每个点代表1个样本,不同颜色的点属于不同样本(组),2点之间的距离越近,表明2个样本之间的微生物群落结构相似度越高,差异越小。从图4(a)可以看出,对于真菌群落,WYC和LJC取样点分布较为分散,而YGQ0-20和YGQ20-50距离较近,表明两者的群落构成差异较小。从图4(b)可以看出:对于细菌群落,油含量最低的YGQ20-50距离其他取样点较远,群落构成的差异也较大;而WYC0-20、WYC20-50、LJC0-20和LJC20-50油含量相近,群落相似性也较高。由图4(c) 可以看出,对于古菌群落,油含量最低的YGQ20-50和最高的WYC0-20距离较远,群落结构差异性也较大。由此可以认为,油污土壤中微生物群落的Beta多样性与其受石油污染程度有一定的关系,油含量相近的油污土壤样品,其微生物群落结构的相似度较高。Natsuko等[22]釆集美国不同油污地区的土壤进行微生物群落结构调查,发现油含量相近的土壤微生物种群差异不大。贾建丽等[23]分别采集中国不同地区的5个油田的油污土壤,研究微生物群落结构,也得出了相似的结果。
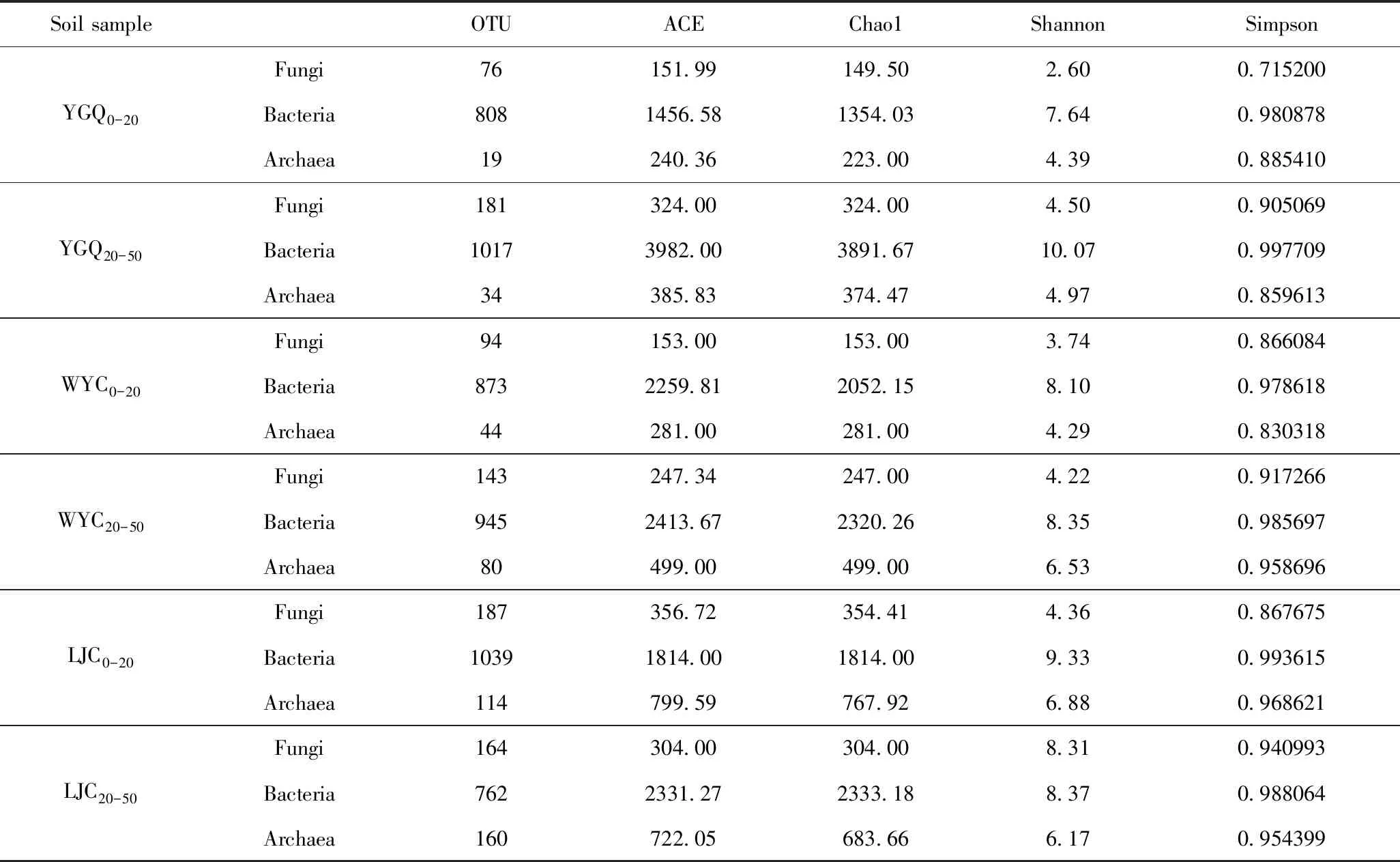
表2 不同油污土壤样品真菌、细菌、古菌群落的多样性指数Table 2 Diversity index of fungi, bacteria, archaea community in different oil-contaminated soil samples
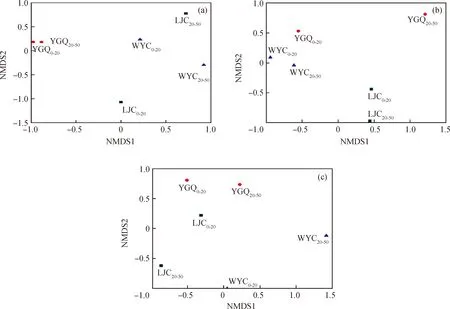
NMDS—Nonmetric multidimensional scaling图4 油污土壤中微生物群落的NMDS分析Fig.4 NMDS analysis of microbial community in oil contaminated soil(a) Fungi; (b) Bacteria; (c) Archaea
2.3 油污土壤微生物群落结构分析
图5为油污土壤微生物群落在门水平上的相对丰度(土壤微生物群落相对丰度=单个物种的绝对丰度/整个种群丰度总量)。从图5(a)可以看出:土壤真菌群落主要隶属于子囊菌门(Ascomycota)、担子菌门(Basidiomycota)、壶菌门(Chytridiomycota)等9个门;其中,子囊菌门的相对丰度最大,为54.4%~83.2%;其次为担子菌门,相对丰度为6.8%~35.5%。已有研究认为能够降解PAHs的真菌一般多见于子囊菌门、担子菌门等[24]。陈锐等[15]在研究安塞石油污染区土壤真菌群落结构分析时同样发现,在门水平上子囊菌门和担子菌门为土壤样品的绝对优势菌群。
由图5(b)可见,土壤样品细菌群落主要隶属于变形菌门(Proteobacteria)、放线菌门(Actinobacteria)、酸杆菌门(Acidobacteria)、绿弯菌门(Chloroflexi)、拟杆菌门(Bacteroidetes)、螺旋体菌门(Saccharibacteria)、蓝细菌门(Cyanobacteria)、硝化螺旋菌门(Nitrospirae)、疣微菌门(Verrucomicrobia)、浮霉菌门(Planctomycetes)、芽单胞菌门(Gemmatimonadetes)、厚壁菌门(Firmicutes)等20个门。其中,相对丰度最高的为变形菌门,为44.8%~79.5%。梁建芳等[13]通过研究表明,克拉玛依油田石油污染土壤细菌主要属于变形菌门、放线菌门、厚壁菌门、拟杆菌门和浮霉状菌门。刘臻证明厚壁菌门和变形菌门可以石油烃为碳源进行代谢,蓝细菌门在石油污染的水体中能够很好地利用石油烃作为碳源并维持生长[25]。在对大港油田土壤模拟生物修复过程中同样发现变形菌门、厚壁菌门、拟杆菌门、绿弯菌门、放线菌门和酸杆菌门是优势菌门,相对丰度为84.47%~94.66%[26]。
由图5(c)可见,土壤样品古菌群落主要隶属于奇古菌门(Thaumarchaeota)、广域古菌门(Euryarchaeota)、深古菌门(Bathyarchaeota)、厚壁菌门、拟杆菌门等13个门。相对丰度最大的为奇古菌门,为28.3%~93.1%;广域古菌门的相对丰度为0.2%~47.3%。宋震等[27]研究表明,原油和含油废水污染土壤样品中的优势菌门是广域古菌门,含油废水和原油都促进了土壤中广域古菌门的生长和发育,而石油污染程度较轻的土壤样品中,优势菌门是奇古菌门。本研究中同样发现,石油污染程度较重的WYC0-20、LJC0-20及LJC20-50土壤样品中,广域古菌门相对丰度明显高于其他样品,而污染程度较轻的YGQ0-20和YGQ20-50样品奇古菌门的相对丰度更大。

图5 油污土壤微生物群落门水平相对丰度Fig.5 Relative abundance of the microbial community phyla in oil contaminated soil samples(a) Fungi; (b) Bacteria; (c) Archaea
2.4 油污土壤微生物属水平上的物种聚类分析
图6为不同油污土壤中微生物属水平上的物种聚类图(红色代表在对应样品中丰富度较高的属,绿色代表丰富度较低的属)。石油污染程度和土壤深度变化会使土壤中优势菌群发生变化,这是由于土壤深度变化和土壤石油污染导致土壤中氧含量、压力以及营养元素发生了变化[25]。从图6(a)可以看出:污染程度最重的WYC0-20土壤样品中真菌踝节菌属(Talaromyces)、Phaeoacremonium、柱霉属(Scytalidium)、丝孢菌属(Scedosporium)、赭霉属(Ochroconis)、Sagenomella、念珠菌属(Candida)相对丰度较大;这些菌属在污染程度较轻的YGQ0-20和YGQ20-50土壤样品中相对丰度较低。而YGQ0-20中丰度较大的刺杯毛孢属(Dinemasporium)、青霉属(Penicillium)、外瓶霉属(Exophiala)以及YGQ20-50中丰度较大的尾梗霉属(Cercophora)、柄孢壳属(Zopfiella)、镰状瓶霉属(Harpophora)在WYC、LJC土壤样品中丰度较低。WYC0-20土壤样品中踝节菌属的相对丰度由0提高到31.6%,而青霉属的相对丰度显著降低,由44.9%降至0.1%。这说明青霉属可在石油污染环境中生存,但污染程度过高(土壤中油质量分数8.632 g/kg)时不利于其生存。研究人员从油污土壤或海洋环境中分离出的具有原油降解能力的真菌中就包括踝节菌属[28]。另外,有报道称曲霉属(Aspergillus)对原油中C11~C20的烃链有较好的降解作用,外瓶霉属可降解甲苯、多环芳烃类污染物,青霉属和茎点霉属(Phoma)可降解PAHs,念珠菌属对正构烷烃降解效果较好[24,29]。
从图6(b)可以看出,对于细菌,污染程度较轻的YGQ0-20中丰度较大的鞘脂单胞菌属(Sphingomonas)、假黄单胞菌属(Pseudoxanthomonas)、玫瑰单胞菌属(Roseomonas)、甲基杆菌属(Methylobacterium)、贪铜菌属(Cupriavidus)和YGQ20-50中丰度较大的变异杆菌属(Variibacter)、固氮弓菌属(Azoarcus)在WYC、LJC土壤样品中丰度较低。污染程度最重的WYC0-20中丰度较大的属有寡养单胞菌(Stenotrophomonas)、硫杆菌属(Thiobacillus)、慢生根瘤菌属(Bradyrhizobium)、纤维单胞菌属(Cellulomonas)。其中,寡养单胞菌的相对丰度由0.1%提升到1.9%,而甲基杆菌属由10.7%降到0.3%。肖建军等[30]通过在石油污染的土壤中筛选出寡养单胞菌并进行实验发现,其对甲苯有较好的去除效果。土壤样品中细菌属水平丰度较高的分枝杆菌(Mycobacterium)、假单胞菌属(Pseudomonas)都是能够降解石油烃的细菌菌属[25]。
从图6(c)可以看出,对于古菌,各取样点高丰度交叉菌属较少。污染程度最轻的YGQ0-20中丰度较大的属有甲烷杆菌属(Methanobacterium)、拟杆菌属(Bacteroides)。而污染程度最重的WYC0-20中丰度最高的属有甲烷杆菌属、甲烷八叠球菌属(Methanosarcina)和甲烷囊菌属(Methanoculleus)。其中,甲烷八叠球菌属的相对丰度由5.8%增至37.8%。有文献表明,产甲烷古菌对石油烃具有厌氧生物降解作用[31],甲烷八叠球菌属具有降解C12~C30的长链正构烷烃的能力[32]。
2.5 油污土壤微生物群落与土壤烃类组分的相关性

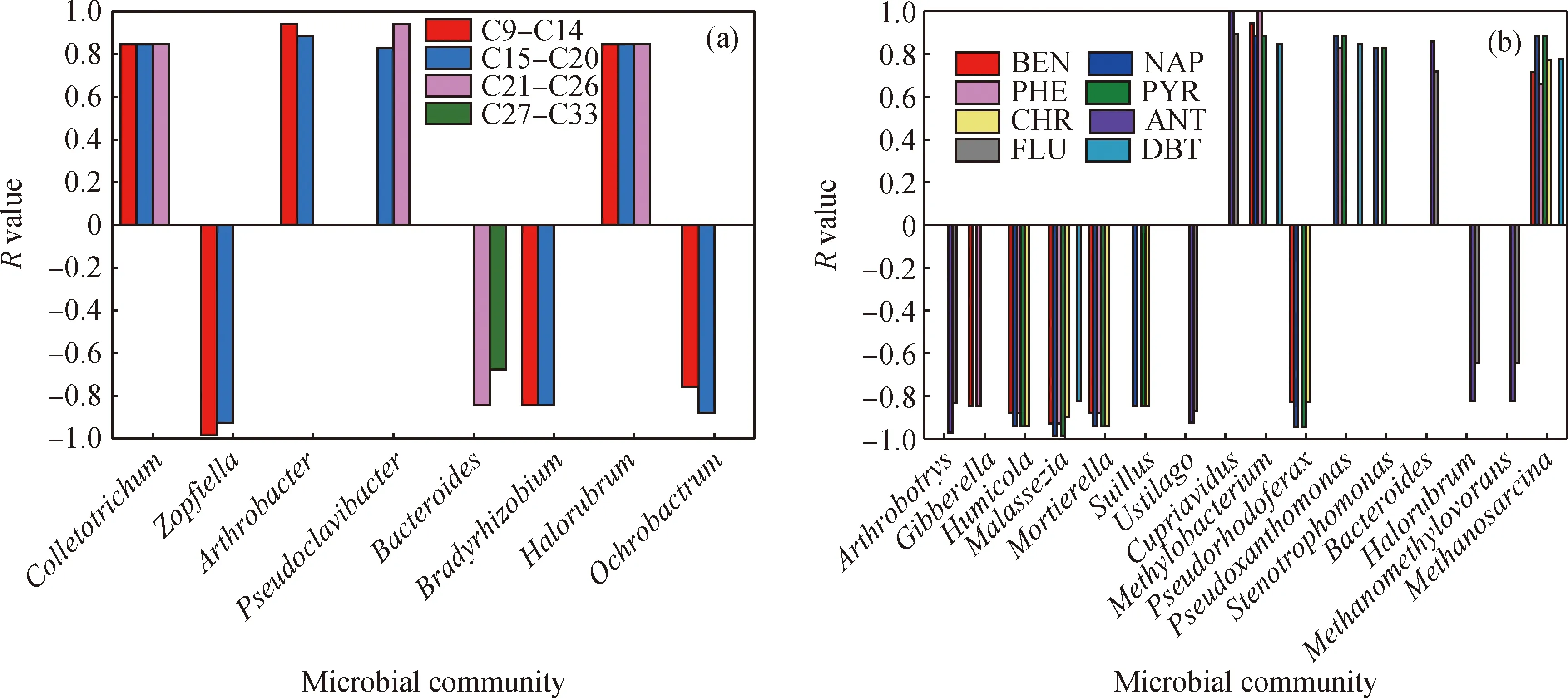
BEN—Benzene; NAP—Naphthalene; PHE—Phenanthrene; PYR—Pyrene; CHR—Chrysene;ANT—Anthracene; FLU—Fluorene; DBT—Dibenzothiophene图7 油污土壤微生物群落与烃类组分含量的相关性分析Fig.7 Correlation analysis of microbial community and hydrocarbon components in oil contaminated soil samples(a) Alkanes; (b) Aromatic hydrocarbons
3 结 论
(1)东营某炼油厂石油污染土壤中细菌、真菌和古菌的群落OTU数量随着土壤油含量的增加先增多后减少,群落结构的Beta多样性指数与土壤油含量有一定相关性,受污染程度相近的土壤样品,其微生物群落结构的相似度较高。
(2)油污土壤样品真菌群落中子囊菌门(Ascomycota)和担子菌门(Basidiomycota)的相对丰度最大;细菌群落中相对丰度最高的为变形菌门(Proteobacteria);古菌群落中相对丰度最大的为奇古菌门(Thaumarchaeota)和广域古菌门(Euryarchaeota)。随着土壤油含量增加,真菌踝节菌属(Talaromyces)的相对丰度由0提高到31.6%;细菌寡养单胞菌(Stenotrophomonas)由0.1%提升到1.9%;古菌群落中甲烷八叠球菌属(Methanosarcina)的相对丰度由5.8%增至37.8%。
(3)微生物群落结构与土壤中烃类组分含量相关性分析表明,真菌炭疽菌属(Colletotrichum)、细菌节杆菌属(Arthrobacter)、假枝杆菌(Pseudoclavibacter)、古菌盐红菌属(Halorubrum)与烷烃含量呈显著正相关性,而真菌柄孢壳属(Zopfiella)、古菌拟杆菌属(Bacteroides)与烷烃含量呈显著负相关性;细菌甲基杆菌属(Methylobacterium)和古菌甲烷八叠球菌属(Methanosarcina)、拟杆菌属(Bacteroides)与芳烃含量呈正相关性,真菌腐殖霉属(Humicola)和被孢霉属(Mortierella)与芳烃含量呈显著负相关。

