基于美国疫苗不良事件报告系统的新型冠状病毒肺炎疫苗相关不良事件报告分析
张 博,郭代红,郭海丽,李伯妍,王嘉熙,,刘思源,于承暄,朱 雨,孔祥豪,(1.解放军医学院,北京10085;.解放军总医院医疗保障中心药剂科,北京 10085;.重庆医科大学药学院,重庆 400016)
新型冠状病毒肺炎(coronavirus disease 2019,COVID-19)是近百年来人类遭遇的影响范围最广的全球性大流行病,严重威胁人类生命安全和健康[1]。据世界卫生组织(WHO)报告,截至2021年2月28日,全球COVID-19累计确诊病例数超1.13亿,其中死亡病例数超252万[2]。疫苗接种作为防控传染病最经济、最有效的手段[3-4],被认为是解决或者控制COVID-19进一步传播及暴发的有力措施[5-8]。据统计,迄今全球已接种了超1.28亿剂次COVID-19疫苗[9]。随着接种剂次的不断攀升,疫苗相关不良事件也越来越多。美国疫苗不良事件报告系统(Vaccine Adverse Event Reporting System,VAERS)[10]由美国疾病控制预防中心(Centers for Disease Control and Prevention,CDC)与食品药品管理局(Food and Drug Administration,FDA)共同构建,其数据库中有大量疫苗相关不良事件的原始数据,可随时从官方网站无条件获取(下载时输入网站随机生成的验证码即可),目前未见国内有基于VAERS数据库的COVID-19疫苗相关研究。本研究调取VAERS数据库中COVID-19疫苗相关不良事件的数据,进行统计分析,以期了解其发生情况和特点,为后续预防接种及科学研究提供参考[11-14]。
1 资料与方法
1.1 资料来源
截至2021年2月28日,美国FDA发布紧急使用授权的COVID-19疫苗共有两种,生产厂家分别为辉瑞[15]和莫德纳[16],均于2020年12月取得紧急使用授权。本研究涉及的两种疫苗相关原始数据提取自VAERS数据库,时间为2020年1月1日 - 2021年2月26日;所有数据包括3个子集,分别是报告数据(VAERS DATA)、症状数据(VAERS SYMPTOMS)和疫苗数据(VAERS VAX),三者均由唯一编码(VAERS_ID)链接;相关症状均采用国际医学用语词典(Medical Dictionary for Regulatory Activities,MedDRA)中的首选术语(preferred terms,PT)描述;将致受种者死亡、危及生命、住院、住院时间延长、残疾定义为严重不良事件。
1.2 纳入排除标准
纳入接种类别为COVID-19疫苗且受种者性别、年龄、疫苗生产厂家、不良事件临床症状等信息齐全的报告。由于辉瑞和莫德纳的COVID-19疫苗均须2剂次接种[17-18],且接种年龄起点分别为16岁[17]和18岁[18],故排除接种剂次在3次及以上和年龄不符合要求的报告。最终纳入18 184例COVID-19疫苗相关不良事件报告。
1.3 数据分析
采用Excel 2019和R软件等对资料数据进行整理及统计学分析。其中,计数资料用构成比和相对比描述,组间对比采用χ2检验,以P< 0.05为差异具有统计学意义。本研究依据是否有严重不良事件将报告分为一般报告和严重报告,并以此分组统计。由于同一例报告可能涉及多种严重不良事件或多个临床症状,故统计结果中严重不良事件或临床症状的例次数大于报告例数。
2 结果
2.1 受种者概况
18 184例报告中,严重报告3521例(19.36%)。其中男性4267例(23.47%),女性13 917例(76.53%),详见表1。男女受种者在一般和严重报告中的构成比差异有统计学意义(χ2= 805.23,P< 0.001)。年龄方面,一般报告中18 ~ 64岁的受种者最多,为13 564例(92.51%);严重报告中65岁及以上的受种者最多,为1809例(51.38%),详见表2。上述两个年龄段受种者在一般和严重报告中的构成比差异有统计学意义(χ2=4 081.59,P< 0.001)。
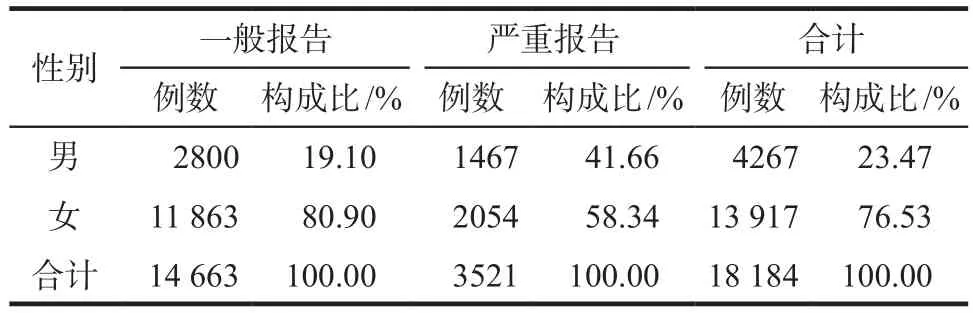
表1 18 184例不良事件报告性别分布Tab 1 Gender distribution of 18 184 adverse event reports

表2 18 184例不良事件报告年龄分布Tab 2 Age distribution of 18 184 adverse event reports
2.2 不良事件概况
接种剂次方面,14 194例(78.06%)不良事件发生于第1剂次接种后,第2剂次接种后有1383例(7.60%)不良事件发生,详见表3。第1剂次和第2剂次接种在一般和严重报告中的构成比差异有统计学意义(χ2= 1 155.22,P< 0.001)。

表3 18 184例不良事件报告接种剂次分布Tab 3 Dose series distribution of 18 184 adverse event reports
发生时间方面,13 675例(75.20%)不良事件发生在接种后2 d内,其中接种当天9396例(51.67%),接种后第1天4279例(23.53%);2 d及以上4068例(22.37%),详见表4。发生于上述三个时间段的不良事件之一般和严重报告构成比差异有统计学意义(χ2= 1 179.53,P< 0.001)。

表4 18 184例不良事件报告发生时间分布Tab 4 Occurrence time distribution of 18 184 adverse event reports
18 184例不良事件报告共涉及3092种(89 694例次)临床症状,排名前10位的症状主要为头痛、疲劳、发热、寒战、疼痛等,详见表5。

表5 89 694例次症状排名前10位分布Tab 5 Top 10 symptoms distribution of 89 694 cases
2.3 严重及死亡报告概况
3521例严重报告共涉及4284例次严重不良事件,其中,住院2230例次(52.06%),死亡916例次(21.38%),危及生命737例次(17.20%),残疾401例次(9.36%),无住院时间延长者。
916例死亡报告中,767例(83.73%)受种者年龄在65岁及以上;631例(68.89%)发生于第1剂次接种后;650例(70.96%)发生于接种后2周之内,详见表6。
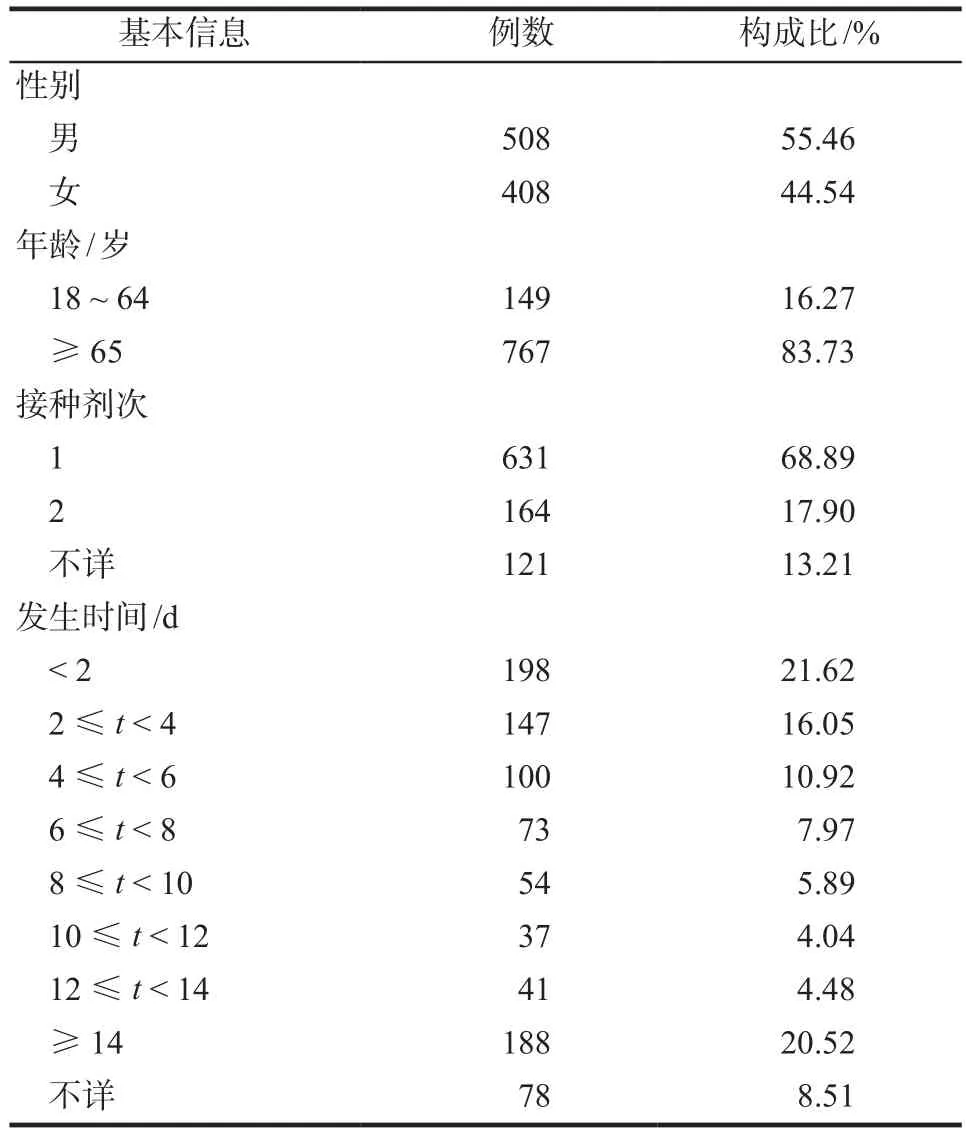
表6 916例死亡报告相关信息Tab 6 Relevant information of 916 death reports
3 讨论
3.1 受种者个体因素分析
本研究中,女性受种者与男性受种者的相对比为3.26∶1。这可能与女性受种者基数多于男性有关,也可能与女性较男性上报不良事件的意识更强有关,具体原因有待进一步研究。既往有研究[12,19]报道其他疫苗相关不良事件中男性构成比低于女性,但邢凯等[20]在COVID-19疫苗有效性和安全性的系统评价中未发现性别差异对安全性的影响。
纳入的18 184例报告中,65岁及以上的受种者在一般报告和所有报告中的构成比为7.46%和15.97%,但在严重报告和死亡报告中的构成比为51.38%和83.73%。这可能与老年人机体功能衰退有关,且该人群多伴有基础疾病,日常可能服用多种药物,无法排除自身疾病及合并用药对疫苗安全性的影响,故应重点关注老年受种者。此外,挪威药品管理局通报的23例接种COVID-19疫苗后死亡的报告均为老年人,但死亡事件与疫苗接种的关联性有待进一步评估[21]。
3.2 接种剂次及临床症状分析
Jackson等[22]有关莫德纳COVID-19疫苗的研究发现,第2剂次接种后不良事件的发生往往更加频繁和严重,而本研究结果显示,78.06%的不良事件发生在第1剂次接种之后。出现此种差异可能是由于受种者初次接种时更关注机体的不良感受,稍有不适即上报;而第2剂次接种后如若出现与初次相似的状况便可能选择不上报或观察数日后再上报。这也提示被动监测存在漏报、迟报等局限性[23-24]。
本研究统计的排名前10位临床症状与辉瑞和莫德纳两个厂家COVID-19疫苗的上市前研究结果基本一致[17-18],多属常见的接种不良反应[4,25]。但临床试验样本量相对较小,人群代表性有限,很难监测到罕见的、长期的不良反应[23,26],而被动监测可发现低发生率的不良反应,因此,其产生的真实世界证据[27]对于疫苗安全性评价及其上市后监管都十分重要。
3.3 预防接种异常反应监测
2019年12月1日起施行的《中华人民共和国疫苗管理法》明确国家加强预防接种异常反应监测。美国CDC在此次COVID-19疫苗紧急授权使用后采取的安全性监测措施值得学习借鉴。例如,美国CDC发布了一款基于智能手机的应用程序V-safe[28],让受种者更加方便快捷地上报不良事件,而工作人员亦可利用V-safe对受种者进行回访,从而获得更多疫苗安全性相关的信息。
虽然被动监测结果仅提示不良事件发生于疫苗接种之后,无法计算发病率、无法获得精准的因果关系[23-24];但预防接种异常反应监测可使公众对于疫苗接种的潜在风险有更全面的认知,有助于减少疫苗犹豫[29],从而提高接种率,最终有效控制COVID-19疫情。

