CYP11A1在牦牛不同级别卵泡及卵母细胞成熟过程中的表达
孙 莹,王 萌,王靖雷,孙晓军,马 睿,余四九,潘阳阳*
(1.甘肃农业大学 动物医学院,甘肃 兰州 730070;2.兰州市动物疫病预防控制中心,甘肃 兰州 730050)
细胞色素P450(CytochromeP450,CYP450)是可以自身氧化的亚铁血红蛋白家族,该家族成员覆盖了所有生物体,主要分布于细胞线粒体内膜及内质网中,是内、外源性物质及致癌性物质代谢过程中的关键酶,参与生物体内甾醇类激素合成的过程[1,2]。有研究表明,在女性生长发育过程中,缺乏细胞色素P450氧化还原酶会引起成年女性月经紊乱,甚至出现不孕现象[3]。哺乳动物卵巢的每个生理周期均会排出处于成熟阶段的卵泡用于受精,卵巢对雌性动物的生殖能力起决定性作用。由此可见,提高卵巢生理功能是目前研究的重点目标。
CYP11A1作为细胞色素P450家族的成员,参与催化生物转化、生物合成的过程[4]。在分子水平上,细胞色素P450CYP11A1通过裂解胆固醇侧链,催化合成类固醇激素的前体——孕烯醇酮(Pregnenolone),促进卵泡发育及卵母细胞的成熟[5,6]。有研究表明:CYP11A1的酶活性会受到雌激素、孕酮的调控,如雌二醇会影响孕烯醇酮的形成,具有促进卵巢发育、排卵的功能,与动物生长繁殖也密切相关[3][7,8]。
牦牛(Bos grunniens)是中国以青藏高原为中心的珍稀牛种之一[9,10]。它在低温高海拔、紫外线强的生态环境中生存,为牧民提供皮毛、牛奶、肉制品等多种生物制品,创造了极大的经济价值。但牦牛生产性能较低,90%以上的雌性牦牛产后同年无法发情,三年两胎,甚至两年一胎,生产过程极具局限性[11,12]。前有研究证明CYP11A1对家禽、藏猪、小尾寒羊等多种动物的生殖生理均有所影响,但在牦牛中未见报道[13,14]。因此,本研究以牦牛不同发育阶段的卵泡、COCs为模型,应用qRT-PCR、免疫荧光技术检测CYP11A1的表达水平及位置分布,为进一步了解哺乳动物、反刍动物生殖生理的特异性奠定了基础。
1 研究方法
1.1 主要试剂
磷酸缓冲盐溶液(phosphate buffered saline,PBS)、杜氏磷酸盐缓冲液(Dulbecco’s phosphate buffered saline,D-PBS)购自Sigma公司(美国);胎牛血清(fetal bovine serum,FBS)购于PAN公司(澳大利亚);TransZol RNA提取试剂盒(TransGen,北京);Evo M-MLV反转录试剂盒Ⅱ(艾科瑞生物,湖南);SYBR GreenⅡ荧光定量PCR试剂盒(宝生物,大连);CYP11A1 Antibody(亲科生物,常州)、免疫荧光检测试剂购于南京碧云天生物技术有限公司。
1.2 样品采集
2020年8—12月从青海省西宁市马佳肴屠宰场采集牦牛卵巢,置于装有35℃生理盐水(含青链霉素)的保温壶中,4 h内带回实验室。37℃生理盐水(含青链霉素)清洗3遍,用带有18G针头的注射器抽取卵巢表面2~8 mm卵泡中的卵泡液,然后与提前37℃恒温箱内平衡的采卵液(D-PBS+5%FBS)混匀;混合后的采卵液倒入50 mm培养皿中,静置后在体视显微镜下捡卵,并将卵移入装有37℃采卵液的培养皿中清洗3次,再转入卵母细胞成熟的培养液中,在37℃、5%CO2和饱和湿度培养箱中培养。分别收集未成熟卵母细胞(0 h)、成熟12 h、成熟18 h的卵母细胞以及成熟卵母细胞(24 h)各40枚,将每个阶段收集的40枚卵母细胞分为2份,一份用于提取RNA,-80℃保存,另一份置于固定液用于后续免疫荧光染色。
1.3 牦牛COCs及卵泡液RNA的提取与反转录
根据TransZol RNA提取试剂盒说明书提示,分别提取不同成熟阶段(0 h、12 h、18 h和24 h)COCs的RNA,且分别在卵泡大小为0~3 mm、3~5 mm、5~8 mm和>8 mm时提取卵泡液的RNA,再利用Evo M-MLV反转录试剂盒Ⅱ将其进行反转录,合成相应的cDNA,分别存于-20℃,用于后续qRT-PCR检测。
1.4 引物设计
参考GenBank上所公布的牛的CYP11A1基因序列(NM_176644.2),使用软件Primer 5 设计引物,并将肌动蛋白β-Actin基因(DQ838049.1)设为内参基因,由生工生物工程(上海)股份有限公司合成引物,详细信息及反应条件见表1。
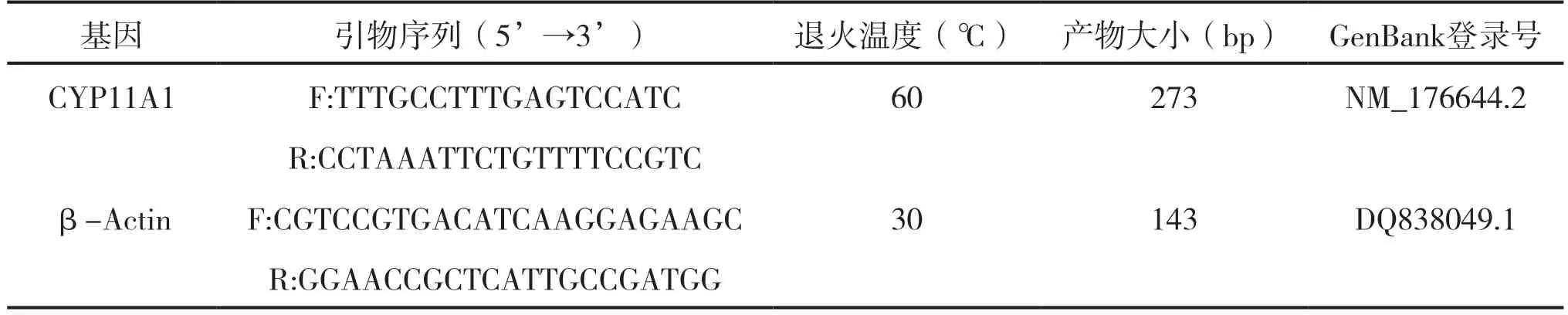
表1 CYP11A1引物信息
1.5 qRT-PCR技术检测CYP11A1基因的相对表达量
使用LightCycler®96 SW 1.1(Roch,Switzerland)实时荧光定量PCR仪。反应体系为模板cDNA 1 μl(500 ng/μl),上、下游引物各0.5μl(0.2 μmol/ml),2*SYBR Green PCRmix 10 μl,补加ddH2O 8 μl使体系至20 μl;反应条件:95℃预变性10 s;95℃变性10 s、退火10 s(具体温度见表1)、72℃延伸10 s,重复共40个循环,建立4个重复,β-Actin为内参,根据熔解曲线确定反应特异性,利用所得每个样品的循环阈值(Ct值),通过2-ΔΔCt法分析qRT-PCR所得数据,检测CYP11A1基因的相对表达量。
1.6 免疫荧光染色技术检测CYP11A1的表达定位
采用免疫荧光染色对COCs的CYP11A1蛋白进行定位检测,首先对在4℃用4%多聚甲醛固定后的细胞进行通透处理,使用免疫封闭液孵育1 h,再用CYP11A1抗体4℃孵育过夜,清洗3遍后与二抗孵育结合,再清洗3遍使用4',6-二脒基-2-苯基吲哚(4',6-diamidino-2-phenylindole,DAPI)染色,最后清洗3遍后封片镜验,用奥林巴斯荧光倒置显微镜观察并拍照。
1.7 数据分析
对每组数据进行单因素方差分析(oneway,ANOVA),每组至少重复3遍以上,所有结果用平均值±标准误表示,用Graphpad prism 7绘制柱状图,P<0.05表示差异显著。
2 结果与分析
2.1 验证CYP11A1引物特异性
2.1.1 核酸电泳检测引物特异性 已知CYP11A1、β-Actin PCR产物大小分别为273bp、143bp,以卵泡液、COCs反转录所得cDNA为模板进行普通PCR扩增,验证引物特异性。结果如图1所示,片段大小与预期一致,条带成像清晰,无非特异性结合片段,证明该引物特异性良好,可用于后续qRT-PCR检测。
2.1.2 CYP11A1扩增所得熔解曲线的结果 如图2所示,通过qRT-PCR扩增,CYP11A1所得产物的熔解曲线是单峰,且出峰位置即为退火温度。由此可见,该引物特异性及模板质量均良好。
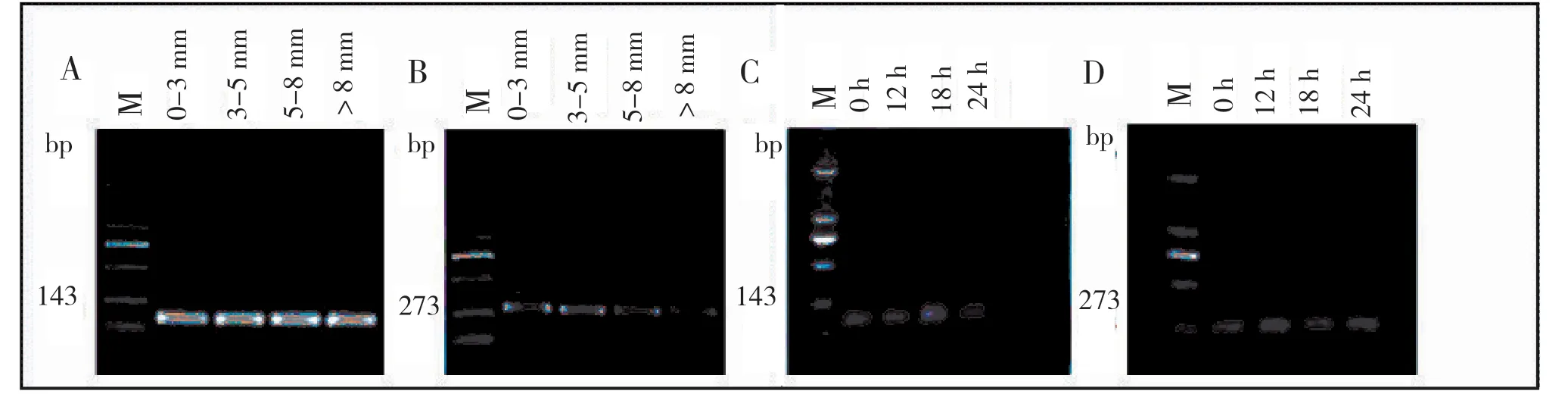
图1 CYP11A1在卵泡液和卵母细胞中表达的核酸电泳结果
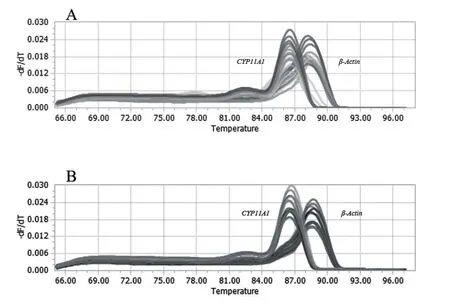
图2 qRT-PCR检测CYP11A1扩增所得熔解曲线的结果
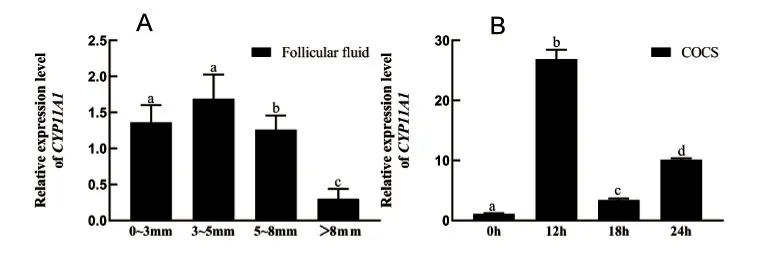
图3 CYP11A1在不同发育阶段的卵泡液及COCs中的表达
2.2 qRT-PCR检测结果
qRT-PCR检测结果如图3所示,CYP11A1在卵泡及COCs发育的各时期均有表达。在卵泡液中,相对表达量呈先升高后降低的趋势,在卵泡大小为3~5 mm时,表达量最高;而在COCs中,0 h时CYP11A1的相对表达量最低,12 h时相对表达量达到最高值,之后又呈现先下降后升高的趋势。
2.3 免疫荧光染色检测结果
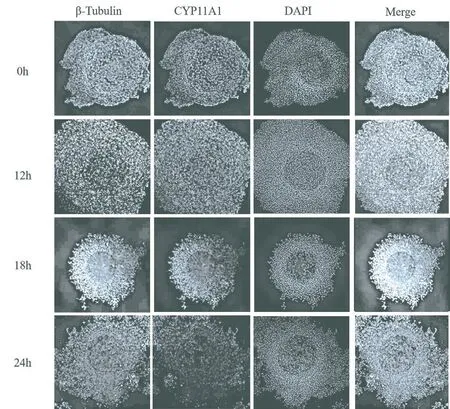
图4 蛋白CYP11A1在不同发育时期的卵丘-卵母细胞复合体中的分布
对不同发育时期的COCs(0 h、12 h、18 h、24 h)进行免疫荧光染色处理后,结果如图4所示,不同时期COCs的卵丘细胞和卵母细胞均表达CYP11A1,其中在成熟18 h的COCs放射冠中荧光信号尤为明显,其表达位置与骨架蛋白β-Tubulin的位置一致,且通过DAPI细胞核标记显示,CYP11A1主要在卵丘细胞的细胞质中表达。
3 讨论
促性腺激素在哺乳动物的早期卵泡生长发育中发挥着不可或缺的作用。由垂体分泌的促卵泡素(Follicle-stimulating hormone,FSH),与卵泡膜上相应受体结合,卵细胞周围颗粒细胞增殖,调控营养物质的交换,抑制卵泡闭锁,促进有腔卵泡和排卵前卵泡的生长发育[15,16]。同时,FSH还具有促进雌激素分泌的功能,所分泌雌激素中雌二醇的活性最高,对第二性征发育和卵巢排卵有积极的调控作用[17-19]。卵泡生长发育后期会分泌大量的促黄体生成素(Luteinizing hormone,LH),有助于孕酮的分泌。孕酮又称为黄体酮,起到调节黄体功能、保持受精卵在子宫中着床的位置、防止流产的作用[8]。另外,卵巢颗粒细胞分泌的孕酮会受到合成路径关键酶的影响[20,21]。LH的刺激促进类固醇合成急性调节蛋白的表达,有助于促进孕酮的合成分泌[22]。该蛋白将胆固醇转运到CYP11A1所在的线粒体内膜,由P450CYP11A1基因编码的细胞色素P450侧链裂解酶对其侧链进行裂解,产生孕烯醇酮,孕烯醇酮在CYP11A1脱氢酶活性的作用下发生双键位置异构,生成孕酮[21][23]。由此可见,卵巢中的CYP11A1基因是影响类固醇激素合成的关键调控基因,与哺乳动物繁殖力有关[7][24]。恶劣的高原环境可能引起牦牛卵巢损伤和功能障碍,造成了其繁殖性能的特殊性[25],而本研究表明CYP11A1会对牦牛的生长繁育产生积极影响,对提高牦牛生产性能具有重要的实践意义。
本研究通过利用qRT-PCR技术对不同发育时期的卵泡及卵母细胞中CYP11A1基因的相对表达量进行检测,结果显示CYP11A1基因在卵泡发育早期(3~5 mm)表达量最高,有研究表明雌激素在卵泡发育早期具有积极的刺激作用,而CYP11A1基因调控颗粒细胞分泌雌激素,该机制与本研究结果相互对应。CYP11A1参与卵泡发育的整个时期,但主要集中在早期,为卵母细胞成熟提供充足的营养物质,是整个发育过程的能量来源;在COCs放射冠形成前期,即M-MⅠ期CYP11A1表达量较高,而后显著下降,推测CYP11A1可能参与放射冠的形成。根据免疫荧光染色结果来看,CYP11A1在放射冠中的荧光更为明显,推测CYP11A1诱导激素分泌,增强卵丘细胞与卵母细胞间的物质代谢,促进卵母细胞的成熟,但由于CYP11A1蛋白在卵丘细胞和卵母细胞上均有所分布,不排除卵母细胞分泌蛋白作用于卵丘细胞的可能性,具体机制有待继续进行验证。
4 结论
本试验在牦牛不同级别卵泡发育及卵母细胞成熟的过程中对CYP11A1的表达进行定位分析,研究发现,牦牛卵泡及卵母细胞不同时期发育时期均可检测到CYP11A1的表达,在早中期表达量最高,而CYP11A1在COCs中的表达主要集中在放射冠,推测CYP11A1参与卵泡的发生和卵母细胞的形成,揭示了CYP11A1参与牦牛雌性生殖过程,对卵泡发育和卵母细胞的成熟均起到积极的调控作用。

