测量骶骨岬至直肠残端的距离在腹腔镜直肠癌根治术精准吻合中的应用价值
郑波波 屈亚琦 张松 岳育民 厍豪 汪光柱 董胜璞 邱健 王小强
在腹腔镜直肠癌手术中,游离左半结肠、直肠后,确定近切缘的传统方法是经辅助切口提出肿瘤及近端结肠,超过耻骨联合前下缘,以此处衡量结肠近端切断线。但这种衡量不够精准,有的患者吻合结束后吻合口上方结肠出现“悬空架桥”的情况,而这种吻合张力会增加吻合口漏的风险[1]。此时需再次游离结肠甚至涉险裁剪系膜等补救措施来降低吻合口张力,吻合完成后这样的操作可能增加吻合口近端结肠或血管弓损伤的风险。有的手术医生通过过多预留肿瘤近端结肠来避免吻合口张力,然而研究报道直肠癌肿瘤近段超过10 cm的肠旁淋巴结转移的发生率是4.5%[2],过多地预留肿瘤近段结肠可能增加肿瘤复发的风险;另外,肠系膜下动脉(inferior mesenteric artery,IMA)根部淋巴结清扫离断了肠系膜下神经丛分布至左半结肠的神经分支,预留近端结肠过长可增加肠道输出功能障碍的风险,这可能是术后便秘的一个危险因素[3]。当今,直肠癌经自然腔道取标本手术(natural orifice specimen extraction surgery,NOSES)蓬勃发展[4-6],如何在全腔镜情况下,精确确定预留近端结肠的长度,达到不但钉合牢靠而且张力恰当的精准吻合,而且尽可能多地切除直肠癌近段结肠是当下直肠癌手术的一个技术难点。为了解决这一难点,我们提出以骶骨岬这一显著且恒定的解剖标志为测量原点,精确测量直肠残端至骶骨岬的距离(记为Drp),来协助实测确定结肠近端切除线,然后进行精准吻合。本研究观察分析术中精确测量Drp在腹腔镜直肠癌手术中的应用价值,为腹腔镜直肠癌手术精准吻合提供借鉴。
资料与方法
一、研究对象
纳入陕西省人民医院普外一科2019年1月1日到2020年10月1日连续入院的中低位直肠癌(肿瘤下缘距离肛缘10 cm以内)的腹腔镜手术病例,收集临床病例资料并回顾手术视频。共收集39例直肠癌患者,其中男性28例,女性11例,年龄(62.2±11.4)岁,体重指数(21.3±4.1)kg/m2,肿瘤下缘距肛缘距离(6.5±2.3)cm。
二、手术方法
全麻后取改良截石头低右低体位,于脐右侧取1 cm弧形切口置入戳卡作为腹腔镜观察孔,分别于脐下1 cm水平两侧腹直肌外缘取0.5 cm切口,麦氏切口取1.2 cm切口,反麦氏切口取0.5 cm切口,分别置入戳卡作为操作孔;按照规范的腹腔镜直肠癌根治术进行不保留左结肠动脉的全系膜切除术,术中测量示意图见图1,具体步骤如下:(1)离断或者确定直肠下切端后,使用线段置于骶前,获得直肠残端或远切缘至骶骨岬的长度线段(Drp,图2A~2B);(2)拉直左半结肠及其系膜,于骶骨岬水平使用钛夹标记相应结肠处肠脂垂记录为A点(图2C);(3)全腔镜游离时,以A点为起点,以原Drp线段测量左半结肠Drp+3 cm处为直肠癌近端切除线(图2C~2D);(4)腔镜辅助时,取脐下正中切口约4 cm~6 cm作为辅助切口,托出左半结肠与直肠后,以原Drp线段测量左半结肠A点以远Drp+3 cm处使用荷包钳钳夹缝置荷包线后切断左半结肠移去标本,放置底钉座收紧荷包打结后还纳腹腔;(5)使用管型吻合器进行直-结肠端端吻合,经肛留置肛管行直肠腔内减压。新辅助放化疗患者均行末端回肠造口。
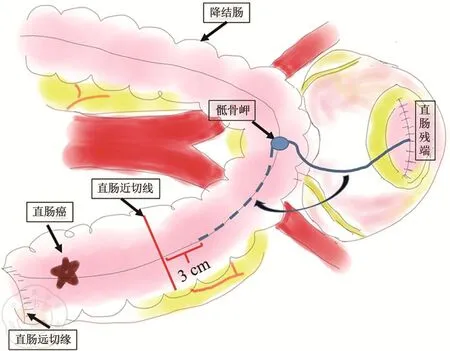
图1 术中测量示意图
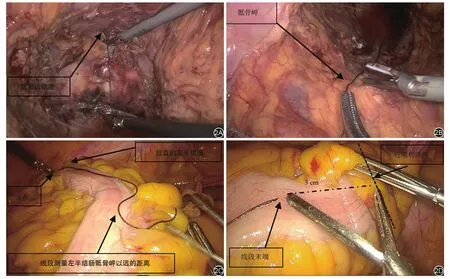
图2 术中测量详细步骤。2A:将线段一端与直肠远切断对齐;2B:将线段松弛地展开于骶前,于骶骨岬水平切断线段备用测量;2C:将左半结肠拉展后平骶骨岬水平标记为A点,再测量A点以远备用线段长度;2D:左半结肠测量线段长度后额外增加3 cm作为近切缘
三、测量指标
1.术中指标:吻合前游离脾区结肠的例数、吻合后盆腔结肠“悬空架桥”的例数、吻合后再度游离近端结肠的例数、吻合后裁剪左半结肠系膜的例数、手术时间及术中出血量。
2.术后标本:直肠远切端至骶骨岬的距离Drp(图3)、近切缘距肿瘤上缘的距离、远切缘距肿瘤下缘的距离及直肠全系膜切除的标本质量[7]。

图3 术后标本及测量骶骨岬到直肠远切缘的线段
3.术后指标:术后30天吻合口漏、吻合口出血、排气时间、排便时间、术后住院时间。吻合口漏定义:直肠手术吻合口漏由国际直肠癌研究组(International Study Group of Rectal Cancer,ISREC)定义为A,B,C级[8]。由于A级亚临床吻合口漏难以确诊,因此本研究只计算B或者C级临床吻合口漏。
四、统计学方法
本研究采用描述性统计方法,连续性变量计算均数±标准差,二分类变量以率的形式呈现结局指标。
结 果
39例直肠癌中行术前新辅助放化疗的9例,病理分期II期10例,III期29例;手术时间(247±57)min,估计术中出血量(35±15)mL。吻合前游离脾区结肠7例,该7例患者乙状结肠或者系膜相对较短;吻合后无盆腔结肠“悬空架桥”的病例,吻合后盆腔结肠均松弛的经过骶前;无吻合后再度游离近端结肠及吻合后裁剪左半结肠系膜的病例;直肠远切端至骶骨岬的距离平均(17.7±4.6)cm,近切端距肿瘤上缘的距离(16.4±3.2)cm,远切缘距肿瘤下缘的距离(2.3±1.1)cm,直肠全系膜切除的标本质量均为A级,直肠癌远近切缘无阳性病例;术后无B、C级吻合口漏发生,有1例患者术后第一天出现吻合口出血,通过保守治疗后出血停止;平均排气时间(3.1±1.2)天,平均排便时间(3.4±1.6)天,术后平均住院时间(9.1±2.3)天。
讨 论
直肠吻合口漏的发生与吻合口的张力存在直接关系,但是因为难以标化吻合口张力评价,既往吻合口漏的多因素分析常常遗漏吻合口张力这一重要因素。国际直肠癌研究组2010年提出直肠吻合口漏是指吻合口部位肠壁完整性发生中断或者缺损,使得肠腔内外相连通,且吻合部位旁出现脓肿[8]。我国直肠癌吻合口漏专家共识也采用了这个定义[9],共识提出直肠癌术后吻合口漏的危险因素包括性别、年龄、体质指数、肿瘤及其治疗情况和术前合并症等术前因素,手术方式及入路、吻合口位置、预防性造瘘以及直线闭合器数目等术中情况,术后吻合口出血、腹泻、非甾体抗炎药的使用等术后因素[9]。Shiwakoti等[10]回顾了北京友谊医院2012年到2017年185例腹腔镜直肠癌患者的病例资料,进行吻合口漏预测模型的构建,多因素Logistic回归分析显示BMI>25 kg/m2,肿瘤直径>5 cm,术前新辅助放化疗,手术时间大于180分钟是吻合口漏的高危因素。这些研究难以引入吻合口张力相关的术中评价指标作为自变量,这也在不同程度影响了这些预测模型的外推性与实践指导价值。
在直肠癌手术质量控制方面,多数专家注重手术解剖层面,注重全系膜切除、淋巴结清扫的范围和数量[11-13],因为标准的直肠全系膜切除联合规范的淋巴结清扫是影响直肠癌患者生存的关键因素[14-15]。但是,消化道重建对于手术的成败至为关键。发生吻合口并发症,如吻合口漏,将会不得不推后术后化疗时间,增加吻合口复发转移的风险,影响到直肠癌患者术后远期生存[16-17],直肠癌根治术的吻合质量是手术中质量控制的重要组成部分,主要包括吻合口血供、钉合质量和吻合口张力。吻合口血供可以用残端出血情况直观判断,也可以用吲哚菁绿观察末端血运情况[18];钉合质量可以用直肠充气实验来测试,也可以通过内镜直观检查[19]。而吻合口的张力往往靠术者的经验评价,缺乏保证吻合口恰当张力的标准操作流程,这对于手术经验不足的医师往往难以准确把握。既往通过牵出近端左半结肠,确定其与耻骨联合前下缘的距离而估计肿瘤近端切断线的操作方式,难以达到精准吻合的目的,同时无法适应NOSES时代全腔镜下切除精准吻合的要求。
骶骨岬是第一骶椎前方的骨性隆起,位于骨盆入口后部,双侧髂总动脉夹角内,是明显且恒定的骨性标志,在直肠及其系膜游离后容易识别定位。以骶骨岬作为测量原点,以线段无张力地放置于骶前表面,精确测量骶骨岬至直肠远切端的距离(Drp),再以骶骨岬为标志,测量左半结肠骶骨岬以远Drp,从而可以较为准确地估计吻合口近端预留的结肠长度。笔者团队起初以测量左半结肠骶骨岬以远Drp处作为近切缘,发现吻合完后仍然可疑存在张力,盆腔结肠并没有松弛地经过骶前区。考虑到直肠癌吻合常规使用直径28 mm或者29 mm的管型吻合器,荷包缝合放置抵钉座并进行吻合的过程占用了约3 cm肠管的长度,因此提出在Drp的基础上增加3 cm作为近切缘;在近端切缘确定后,所有病例术中测量肿瘤近切缘的距离均大于10 cm,本研究近端切缘平均长度为(16.4±3.2)cm;所有病例吻合后盆腔结肠松弛地经过骶前区,且无蜿蜒扭曲等过长表现,吻合口满意度明显增加。本研究回顾性分析的39例患者吻合后盆腔结肠无“悬空架桥”现象,吻合后无需再次游离近端结肠,无临床吻合口漏发生,手术流畅度及吻合满意度明显增加,初步证实了本方法能够作为标准操作流程使腹腔镜直肠癌手术达到精准吻合的目的。笔者团队希望本项技术改良能够作为腹腔镜直肠癌手术质量控制的一个重要环节,准确预测拟吻合近端结肠长度,通过实测标准化吻合流程,提高吻合质量来尽可能减少术后吻合口漏的发生风险。
综上所述,测量直肠残端或远切缘至骶骨岬的距离(Drp),能够促进腹腔镜直肠癌根治性切除术的精准吻合,具有很强的可操作性,客观上提高手术流畅性,增加吻合口满意度,临床实用价值较强,值得进一步研究与推广。

