磁性硅铁载铜吸附Hg0动力学机制及密度泛函研究*
周发山, 刁永发,杨炳文
(东华大学 环境科学与工程学院,上海 201620)
0 引 言
燃煤电厂排放的汞是全球汞污染排放的一个重要来源,在《重金属污染综合防治“十二五”规划》中,汞被列为重点管控的5种重金属之一[1]。燃煤烟气中汞主要以零价汞(Hg0)、二价汞(Hg2+)和颗粒汞(HgP)形式存在[2-4]。Hg2+和 HgP几乎可以完全被湿式脱硫装置和除尘设备捕获,而Hg0很难被现有的设备直接捕获[5-6]。目前研究成熟的一种干法Hg0捕集技术是在袋式除尘器上游烟气管道中注入吸附剂吸附Hg0,以达到控制痕量Hg0的目的[7]。
通过前期研究,利用Fe3O4@SiO2粒子、Cu0纳米颗粒及FeSi粉在300 ℃煅烧,制备出一种新型磁性吸附剂MagFeSi-Cu0[8]。研究发现MagFeSi-Cu0吸附剂具有和商业活性碳相当的脱汞效率,在150 ℃条件下汞吸附效率能达到90%,其中,FeSi中的非晶硅能促进Cu的负载从而提供更多的活性位点,但关于MagFeSi-Cu0吸附剂吸附Hg0的动力学吸附机制及Cu-Hg成键机理未有进一步研究。由于痕量Hg0的吸附过程是从反应物在MagFeSi-Cu0表面上的吸附开始的,吸附反应动力学可以准确的描述吸附过程,运用该手段可深入的研究吸附速率和吸附机制,并预测吸附过程的控制机制[9]。此外,采用密度泛函理论,从原子尺度上了解Hg0在Cu0原子表面的吸附机理,有助于深入了解Cu原子与Hg0原子之间的微观反应原理,为吸附剂的筛选和优化提供相应的理论基础。
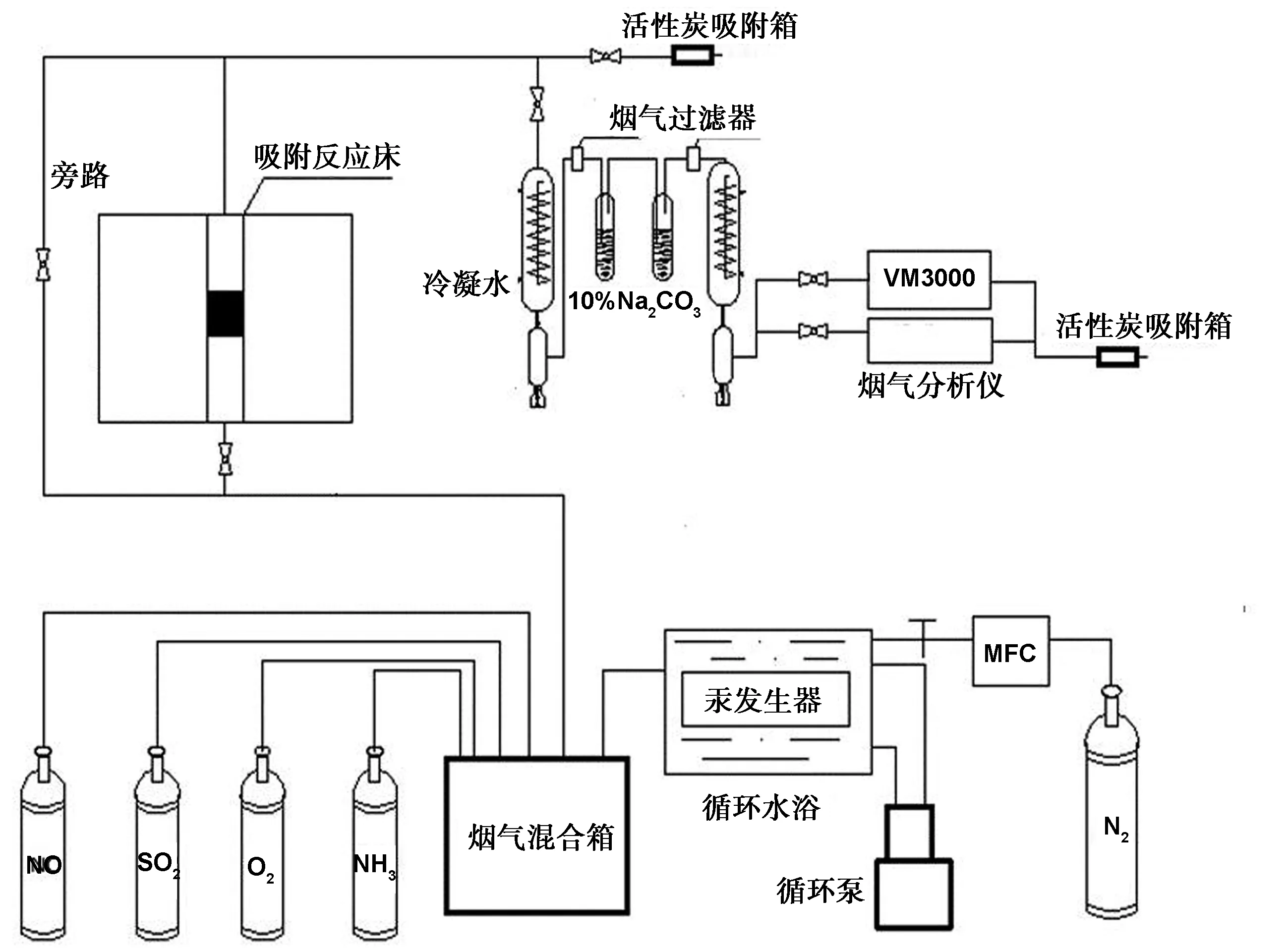
在Hg0与金属原子之间汞齐反应原子层级密度泛函研究方面,Steckel和Sasmaz等人[10-11]曾利用VASP密度泛函软件计算研究了单质Hg0在各种金属表面的吸附反应,考察的贵金属有Ag,Au,Cu,Ni,Pd 和 Pt。计算结果表明Hg与考察的6种金属都有较大的结合能,且Ag 由于本研究中MagFeSi-Cu0表面负载的纳米Cu0的金属结构都是面心立方,在研究原子吸附时常用的表面有(100)、(110)和(111)3种,其中(111)面属于六角密排晶系,一般情况下不会发生再构[13]。因此,在结合MagFeSi-Cu0吸附Hg0动力学机制的基础上,本研究将集中于讨论Hg0在Cu(111)表面的吸附能,电子轨道分布特征以及不同烟气温度下的吸附自由能的变化。 将3 g Fe3O4(<100 nm)溶解在含有90 mL去离子水中,然后逐滴添加1 ml TEOS。将所得混合物搅拌12 h,过滤并在50 ℃的空气循环烘箱中直接干燥以获得Fe3O4@SiO2黑色粉末。将0.2 mol/L的NaH2PO2溶液倒入75 ℃恒温的烧瓶中。通过加入H3PO4溶液将PH调节至1~2,然后在磁力搅拌下添加3 g硬脂酸(约0.01 mol)。在2 h内以每分钟40滴的速度将0.15 mol/L的CuSO4溶液加入到所制备的溶液中,然后过滤并在真空环境60 ℃下干燥12 h,以获得硬脂酸改性的纳米铜粉。以2∶3∶5的质量比混合铜粉,硅铁粉(<40 μm)和Fe3O4@ SiO2粉,并在300 ℃下煅烧1 h,以获得磁性吸附剂MagFeSi-Cu0。 固定床汞吸附系统如图1,总气流量为1.3 L/min,载汞氮气流量为10 mL/min。固定床反应器为处于管式炉中的石英玻璃管。实验过程中,将0.5 g的MagFeSi-Cu0均匀铺在石英管反应器内的石英棉上,待汞出口浓度稳定30 min后记录稳定后的汞入口初始浓度。 图1 吸附Hg0固定床实验系统原理图 吸附时间t处吸附剂中积累的汞吸附量(qt)通过以下公式计算[14]: 其中Q是气体的体积流量,m3;m是吸附剂的质量,g;C0和C分别是固定床反应器进口和出口处烟气中的汞浓度,μg/m3;qt是从吸附开始到t时刻这段时间内吸附剂单位累积汞吸附量,μg/g。 为了进一步了解MagFeSi-Cu0吸附Hg0中的铜汞齐作用机制,使用Gaussian16和Gaussview软件[15]进行计算,此外关于原子之间电荷转移相关分析采用Multiwfn3.6软件计算[16],并通过Shermo2.0.1软件分析不同烟气温度下Cu(111)表面Cu-Hg齐吸附自由能[17]。图2中描述的是吸附前后Hg0原子与Cu(111)晶胞计算模型。选取Cu(111)表面,真空层为2.0 nm。为了一方面减少体系的计算量,另一方面保证原子晶胞之间吸附能的稳定,模型中切取5层Cu(111)表面。 图2 Cu及Hg晶胞计算模型 通过汞吸附量实验考察固定床温度梯度和汞入口浓度对MagFeSi-Cu0脱汞的影响。在N2气氛下,以吸附剂载铜量20.4%为基础工况,分析固定床温度分别为80、150 和200 ℃工况下的汞吸附量随时间变化的规律,数据采集时间为100 min,结果如图3所示。 图3 不同温度下Hg0吸附与解析实验结果 从图3中可以看出,烟气温度由80 ℃升至150 ℃时,MagFeSi-Cu0的汞吸附量有所减弱,但减弱幅度并不明显,随后温度升至200 ℃时,吸附量较150 ℃时下降幅度较大。主要由于随着温度的升高,一方面Hg0分子的运动速率会加快,使Hg0在FeSi表面的有效碰撞增多从而提高了物质的反应速率,但同时由于铜汞齐极易受温度影响,容易发生汞的二次解析,致使Hg0在单质铜表面出现逃逸现象,特别是当温度达到并维持在200 ℃以后,吸附剂上的Hg0部分解析出来,降低了吸附剂的汞累积能力,从而导致单位汞吸附量较150 ℃时下降增幅明显。 目前研究吸附剂吸附过程的动力学模型主要有准二级动力学模型(Pseudo-second order)、颗粒内扩散模型(Weber&Morris)、Bangham模型和Elovich动力学模型[9],描述上面列出的动力学模型的方程式如下: (1)Weber及Morris模型: qt=kidt1/2+θ (1) 其中kid是粒子内扩散速率常数,θ是与边界层厚度成正比的常数。 (2)准二阶模型: (2) 其中k2代表吸附反应速率常数。 (3)Elovich模型 (3) 其中,α是与初始吸附速率有关的常数,β与可用于吸附的活性位点数量有关。 (4)Bangham模型 qt=ktα (4) 本研究采用这4种动力学模型从吸附动力学分析固定床温度梯度梯度下MagFeSi-Cu0对汞的动力学吸附机制。以150 ℃烟气条件下汞吸附量为拟合对象,分别与4种动力学模型进行拟合,得到结果如图4和表1所示。 图4 汞吸附动力学模型 表1 拟合动力学参数 由图4可知在烟气温度为150 ℃条件下Bangham模型的拟合度最高,这表明MagFeSi-Cu0的Hg0吸附过程是结合了吸附剂的外扩散及化学吸附的综合吸附过程[18]。Hg0通过微孔扩散转移到单质Cu0吸附位点,通过汞齐反应产生Cu-Hg齐,其中外扩散和汞齐吸附为主要的限制步骤。从表1的动力学模型拟合结果可以看出,在温度为80 ℃和150 ℃时,吸附剂汞吸附过程与3种吸附模型拟合度良好,拟合系数均在0.99以上,但当烟气温度达到200 ℃时,实验结果与准二阶模型和Elovich模型拟合度较差,但与Bangham模型拟合良好,说明此时吸附表面Hg0的扩散和吸附为主要的限制步。出现此现象主要因为随烟气温度升高,通过汞齐吸附方式存在于单质铜膜表面的Hg0分子运动加剧,脱离铜膜表面,导致吸附量大幅度下降。 2.3.1 Hg在Cu(111)表面吸附能研究 为了了解Hg0在Cu(111)表面Cu-Hg齐吸附反应的作用机制,使用Gaussian16和Gaussview密度泛函计算软件计算了Hg0在Cu晶胞表面吸附反应的吸附能。通过计算Hg0在Cu表面的吸附能来判断两者之间的相互作用的大小。吸附能(Ead)的值计算公式表示如下[19]: Ead=Eab-[Ea+Eb] 上式中,Eab表示的是吸附后整个体系的总能量,Ea和Eb分别表示吸附反应前吸附底物Cu(111)和吸附质Hg0的能量,Ead表示吸附体系的吸附能。Cu(111)表面Hg0吸附后所得结果如表2所示。 表2 Hg0在Cu(111)表面吸附能、电荷分布和转移电子数 根据表2可知,Hg0吸附后铜汞齐的吸附能为-0.534 eV,转移电子数为0.11,这与Steckel[11]等人的计算结果相一致。从Mulliken电荷分布可以看出,Hg在Cu(111)表面参与反应的主要在6s轨道和6p轨道,Hg的d 轨道没有参与表面的反应。 2.3.2 Hg在Cu(111)表面能态密度研究 为了更进一步地研究Hg0在Cu(111)表面吸附的成键细节,本文计算了Hg原子和Cu(111)表面铜原子的态密度。下图分别是Cu(111)晶胞表面Cu和Hg的分态密度图(DOS),结果如图5所示。 从图5可知,吸附后体系中的Hg0原子与Cu0原子之间的相互作用可以用Hg0原子的s-DOS及p-DOS分别与Cu0原子的s-DOS及p-DOS峰值重叠来解释[20]。Hg的s轨道与Cu的s轨道在-8.1 eV和-4.08 eV处均发生峰值重叠现象,此外,Hg的p轨道与Cu的p轨道在-1.36 eV处发生峰值重叠,这说明Hg与表面Cu原子轨道之间存在较强的相互作用。 图5 Hg在Cu(111)表面吸附后分态密度图 2.3.3 烟气温度对Cu(111)表面Hg0吸附能的影响 由于计算原子吸附过程电子能垒时完全忽略掉核的运动,因此采用更加严格的自由能垒来讨论不同烟气温度下Hg0原子在Cu(111)表面反应发生的难易程度。计算时使用Shermo软件计算所有反应物的自由能,得到在80~200 ℃下Cu-Hg的自由能垒,计算结果如表3所示。 表3 烟气温度对Hg0在Cu(111)表面的吸附能的影响 从表3可以看出,随着烟气温度的上升,Cu原子与Hg原子之间吸附能逐渐降低,从80 ℃时的-22.47 kJ/mol下降至200 ℃时的-13.96 kJ/mol。说明随着烟气温度升高,Cu-Hg齐稳定性逐渐减弱,最终造成Cu0纳米颗粒表面Hg0的脱附量逐渐增加,这也解释了MagFeSi-Cu0的汞吸附容量随着烟气温度升高而逐渐下降。 在实验研究了不同烟气温度对MagFeSi-Cu0汞吸附能力的影响的基础上,进一步结合了4种吸附动力学模型,分析了MagFeSi-Cu0汞吸附动力学机制。在此基础上,采用密度泛函理论集中讨论了Hg0在Cu(111)表面的吸附能,电子轨道分布特征以及不同烟气温度影响下吸附自由能的变化,分析结果如下: (1)从4种吸附动力学模型拟合度来看,描述Hg0在MagFeSi-Cu0表面吸附反应的Bangham方程的拟合度略高于准二级动力学模型和Elovich模型,这说明MagFeSi-Cu0脱汞的过程为表面Hg0扩散及铜汞齐吸附起主导作用。 (2)通过进一步原子层级密度泛函计算研究发现,Hg0在Cu(111)表面铜汞齐吸附能为-0.534 eV,Cu0原子与Hg0原子在S轨道和P轨道均产生了重叠峰。 (3)当烟气温度从80 ℃上升至200 ℃时,铜汞齐吸附能由-22.47 kJ/mol下降至-13.96 kJ/mol,也说明了随着烟气温度升高,Cu-Hg齐稳定性逐渐减弱。1 实验材料与方法
1.1 吸附剂制备
1.2 固定床汞吸附系统
1.3 Hg0在Cu(111)表面密度泛函计算模型

2 结果与讨论
2.1 汞吸附实验

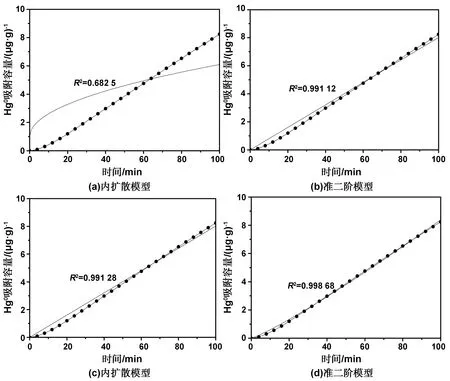
2.2 汞吸附动力学机制



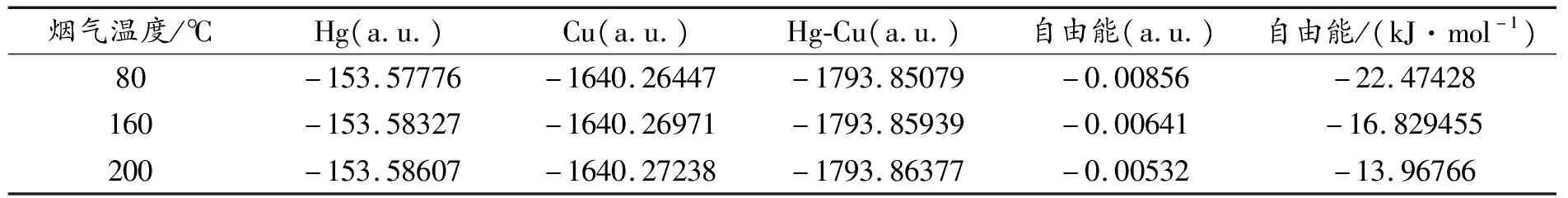
2.3 铜汞齐密度泛函作用机理


3 结 论

