营养膳食护理联合局部氧疗对跟骨骨折术免疫功能及切口愈合的影响
殷文珍 莫小燕 许翠霞 赵玉庆
近年来,随着交通、建筑等行业的发展,足踝部外伤的发生率逐年增高,其中跟骨骨折最为常见。跟骨骨折多由外力产生的高能量冲击损伤引起,而保守治疗的畸形愈合、骨性关节炎的发生率较高,因此临床上对有适应证的患者多选择手术治疗,其中针对SandersⅡ型及Ⅲ型患者切开复位内固定是最常用术式[1]。但由于跟骨解剖结构复杂,周围软组织菲薄,局部血供较差,切开复位内固定术后极易发生切口皮缘坏死、切口感染而致切口愈合不良,影响手术疗效,甚至可能影响患者的正常行走功能。研究发现[2],术后切口愈合不良与多种因素相关,其中局部组织缺血、缺氧及营养不足是其独立危险因素。因此,针对其危险因素,提出了营养膳食护理改善营养状况及局部氧疗改善局部缺氧症状,且在髋关节术后切口愈合等方面取得较好的临床疗效[3-4]。本研究探讨营养膳食护理联合局部氧疗对跟骨骨折术免疫功能及切口愈合的影响。
1 资料与方法
1.1 临床资料
选择2019年7月-2020年7月我科62例因跟骨骨折行内固定治疗的患者作为研究对象。纳入标准:年龄≥18岁;外伤史导致的X线明确显示的跟骨闭合性骨折,骨折时间<14d;Sanders分型Ⅱ型、Ⅲ型符合切开复位内固定手术治疗;术前无张力性水疱或血疱。排除标准:年龄<18岁;骨折时间>14d;合并病理性骨折;合并跟骨周围软组织坏死或开放性骨折;严重营养不良(白蛋白≤25g/L);合并自身免疫性疾病、下肢血管性疾病、恶性肿瘤;足踝部皮肤性疾病;不能配合戒烟;精神行为异常或认知功能障碍。所有患者自愿参与并签署知情同意书。采用随机数字表法分为观察组和对照组,各31例。观察组男性19例,女性12例;年龄≥60岁11例,<60岁20例;手术时间≥1.5h 12例,<1.5h 19例;术中植骨5例;骨折类型:Sanders Ⅱ型17例,Sanders Ⅲ型14例;体质量指数:≥24kg/m216例,<24kg/m215例;有糖尿病史10例。对照组男性22例,女性9例;年龄≥60岁13例,<60岁18例;手术时间≥1.5h 10例,<1.5h 21例;术中植骨3例;骨折类型:Sanders Ⅱ型14例,SandersⅢ 型17例;体质量指数:≥24kg/m214例,<24kg/m217例;有糖尿病史5例。两组临床资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法
对照组术后给予常规护理措施。观察组在常规护理的基础上给予营养膳食护理联合局部氧疗干预措施。
1.2.1营养膳食护理 (1)营养状况评估:由专业营养师及主管护师根据患者基本信息、检验结果及体质量指数对患者进行营养情况评估,同时了解患者日常饮食结构及饮食量。(2)制定膳食方案:根据患者的口味、忌口等个体情况制定相应的膳食方案,包括每日热量摄入量,脂肪、蛋白质、糖类的配比,蛋白质的来源等,并补充铁锌等多种微量元素及维生素。(3) 膳食方案的实施:核对膳食方案后向患者及家属详细讲解,并解决其疑问,以便更好的配合治疗。同时,记录患者每日饮食情况,鼓励其按照膳食方案进行饮食,出现消化不良、便秘等及时向医师及营养师反馈,根据情况调整食谱。
1.2.2局部氧疗 术后第一天切口换药后,在切口处放置一层薄纱块,将一次性延长管口置于切口中心,用透明敷料贴固定延长管后再覆盖2~3层纱块,并用薄棉垫及生物半透膜将其封闭,半透膜覆盖范围要大于棉垫范围,连接一次性延长管和切口治疗仪,用绷带包扎和固定,使局部形成高压氧舱的环境。切口治疗仪持续使用24h,7天为1个疗程,连续治疗1~2个疗程。使用过程中注意延长管不脱出、不折叠、检查主机电量,不可倒放。切口治疗仪可在温度10~40℃,湿度30%~80%的环境下运作,每2~3h巡视一次。
1.3 观察指标
比较两组引流时间、引流量、住院时间及切口愈合情况;于术后24h、48h、72h换药时采用红外线温度仪测量患肢切口1cm处及对侧相同部位皮肤温度,记录两者差值;于术后6h、24h及72h留取切口组织液,采用血气分析仪检测氧分压;于术前、术后7d、出院时清晨空腹抽取静脉血2ml,检测白蛋白(Alb)、血红蛋白(Hb)、转铁蛋白(TF)等营养指标及免疫功能指标(CD4+、CD8+、CD4+/CD8+)。切口愈合分为[5],甲级:切口愈合良好,无不良反应;乙级:切口处有红肿、硬结、血肿、皮肤发黑、积液等炎症反应,尚未化脓;丙级:切口处化脓,需要切开引流。乙级+丙级为切口愈合不良。
1.4 统计学方法
2 结果
2.1 两组术后引流时间、引流量及住院时间的比较,表1

表1 两组术后引流时间、引流量及住院时间的比较
2.2 两组切口愈合情况的比较,表2
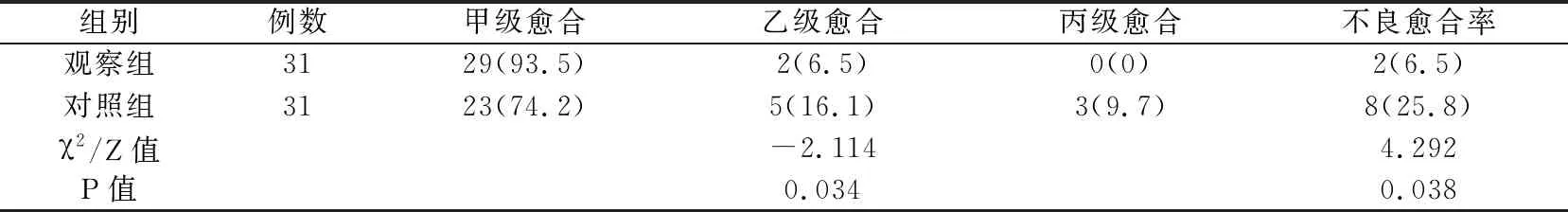
表2 两组切口愈合情况的比较 n(%)
2.3 两组切口组织液氧分压及皮肤温度差的比较,表3

表3 两组切口组织液氧分压及皮肤温度差的比较
2.4 两组营养状况的比较,表4

表4 两组营养状况的比较
2.5 两组免疫功能的比较,表5

表5 两组免疫功能的比较
3 讨论
跟骨对人体的站立、行走等均起到至关重要的支持作用,因此骨折后治疗的目的主要为尽可能恢复跟骨的高度及宽度,目前需要手术治疗的患者中切开复位内固定是最常用术式,但由于跟骨骨折多为冲击损伤造成,骨折后跟骨宽度增加,外侧壁突起,松质骨渗血多,极易导致局部软组织迅速肿胀而影响血液供应[6]。同时,手术作为二次叠加损伤可进一步加重该部位的营养及氧供应[7],不仅跟骨骨折的复位较为困难,且术后容易出现神经营养缺乏、水肿渗出、切口感染等并发症,引起术后切口愈合不良[8]。因此,在积极控制可能引起切口愈合不良的危险因素同时,采取相应的护理干预方式同样重要。
营养膳食护理是目前针对切口愈合不良而提出的一种全身管理的干预措施,目的是通过科学、合理的膳食管理提高机体营养摄入,保证切口愈合需要的氨基酸、蛋白质等营养成分[9]。局部氧疗是一种针对切口部位血液循环功能较低的局部干预措施,目的是通过改善切口部位的氧浓度,降低组织水肿,促进切口愈合[10]。本研究结果显示,观察组术后引流时间、引流量、住院时间少于对照组,不良愈合率低于对照组,而甲级愈合率明显高于对照组(P<0.05)。表明营养膳食护理联合局部氧疗明显缩短了术后切口愈合时间,且愈合率更高。
研究发现[11],组织修复包括炎症反应、肉芽组织生成及组织重塑三个阶段,切口局部缺氧可明显延长组织修复的第一阶段,即增加切口发生炎症反应的风险。本研究发现随着时间延长,两组切口组织液氧分压均逐渐升高,但观察组改善更明显。表明局部氧疗可以明显改善切口局部缺氧症状,进而可以促进切口组织的有氧代谢及肉芽组织的生成,缩短切口愈合时间。但有研究认为[12],切口愈合受多种因素影响,局部氧浓度的提高可以促进肉芽组织生成但并不能加速切口愈合,切口局部温度同样影响切口愈合,该研究认为切口局部温度升高可以促进局部氧气释放增加氧浓度,有利于切口愈合。本研究分析发现随着时间延长,两组切口皮肤温度差均逐渐降低,术后48h及72h观察组切口皮肤温度差低于对照组(P<0.05)。因此,切口局部温度在切口愈合中的作用尚需进一步探讨。
临床上手术不仅对机体是一种较大的创伤,且术后可引起机体对营养物质的需求增加,机体的营养状况是任何术后患者恢复最主要的物质基础[13-14],因此需要更明显的提高患者术后营养状况,为切口愈合提供有利条件。本研究结果显示,观察组术后7d及出院时Alb、Hb及TF均逐渐升高,且均高于对照组(P<0.05)。表明虽然术后常规要求患者及家属加强营养,但给予科学、合理、规范的营养膳食护理干预对患者营养的增加效果更明显,其不仅可以保证每日必须的营养摄入,且给予不同患者个性化的膳食方案可增加其临床依从性。此外,充足的营养亦是机体免疫功能的有利保障[15]。本研究结果显示,观察组术后7d及出院时CD4+及CD4+/ CD8+均高于对照组,CD8+低于对照组(P<0.05)。表明营养膳食护理联合局部氧疗明显提高机体细胞免疫水平。
综上所述,营养膳食护理联合局部氧疗不仅缩短了跟骨骨折术后切口愈合时间,且通过改善切口局部温度及氧浓度,增加机体营养状况及免疫功能,降低切口不良愈合率,提高切口甲级愈合率。

