离子液体及其双水相体系在萃取分离桑叶多糖中的应用
初正帅,彭效明,蔡青蔓,段阳,梁晓旭
(北京石油化工学院化学工程学院,北京 102600)
桑叶多糖具有降血糖、降血脂、抗氧化、免疫调节等多种功能,近代中医学家也常将桑叶配伍于中药复方中,应用于临床,且多获效。另外,植物多糖对体液免疫、细胞免疫、单核巨噬细胞、细胞因子等方面都具有调节作用。部分科学家发现近年桑叶多糖已成为植物活性成分研究领域的热点。桑叶多糖含有单糖(果糖、葡萄糖等)、低聚糖(蔗糖)、多糖(MPA-1、PMP-11、PMP-12等)[1-2]。
目前,桑叶多糖提取与分离常采用煎煮法、浸渍法、渗漉法、回流法等[3-9],在这些方法操作过程中常用甲醇、乙醇、丙酮、二氯甲烷、甲苯、乙醚等有机溶剂,但它们具有较强的挥发性或毒性,在生产过程中会引起环境污染。而离子液体具有不挥发、液程宽、溶解强、可设计调节等特性。将离子液体作为萃取剂,不仅对环境友好,而且能提高选择性,增加萃取化合物的范围,集合高效萃取和欲富集的优点。而将离子液体双水相体系运用到桑叶有效成分的萃取工作中更是一个很好的尝试。Gutowski等采用亲水性离子液体1-丁基-3-甲基咪唑盐酸盐和磷酸钾(K3PO4)首次提出了离子液体双水相体系这一概念[10]。离子液体双水相比较于传统双水相既为萃取营造了温和的环境,又避免了萃取过程中有机溶剂的使用,具备萃取率高、两相界面清晰、黏度低、绿色环保、操作简便等优点。因此近年来离子液体在分离天然活性物质方面被广泛研究[11-20]。
本文对离子液体和双水相体系在桑叶多糖提取工艺方面进行了研究,为桑叶多糖的有效开发,以及如何将离子液体应用在桑叶多糖的开发中奠定了基础。
1 材料与方法
1.1 材料与试剂
桑叶:北京市大兴区安定镇御林古桑园。
氢氧化钾、氢氧化钠、氯化钠、氯化钾(分析纯):北京化工厂;磷酸氢二钾、磷酸二氢钾(分析纯):北京北化精细化学品有限责任公司;无水碳酸钾、硫代硫酸钠、柠檬酸钠、硫酸铵(分析纯):天津市光复科技发展有限公司;蒽酮、无水碳酸钠(分析纯):天津市福晨化学试剂厂;硫酸(分析纯):北京兴青红精细化学品科技有限公司;葡萄糖标准品(纯度≥99%):北京世纪奥科生物技术有限公司;无水氯化钙(分析纯):国药集团化学试剂有限公司;磷酸二氢钠(分析纯):天津市天大化工实验厂。
1-丁基-3-甲基咪唑四氟硼酸盐、1-羟乙基-2,3-二甲基咪唑氟盐、1-丁基-3-甲基咪唑硝酸盐、1-丁基-3-甲基咪唑六氟磷酸盐、谷氨酸双三氟甲磺酰亚胺盐、1-丁基-3-甲基咪唑双三氟甲烷酰亚胺盐、羟乙基三甲基氯化铵、1-羟乙基-3-甲基咪唑氯盐、1-辛基-3-甲基咪唑六氟磷酸盐、1-庚基-3-甲基咪唑氯盐、1-辛基-3-甲基咪唑氯盐、1-戊基-3-甲基咪唑氯盐、1-癸基-3-甲基咪唑氯盐、1-己基-3-甲基咪唑六氟磷酸盐、1-己基-3-甲基咪唑氯盐(纯度≥99%,分析纯):中科院兰州化学物理研究所。
1.2 仪器与设备
CP224C电子天平:奥豪斯仪器(常州)有限公司;DT5-4B低速离心机:北京时代北利离心机有限公司;KH-500DB数控超声波清洗器:昆山禾创超声仪器有限公司;WE-2B玻璃仪器气流烘干器:(郑州)长城科工贸有限公司;UV2600紫外可见分光光度计:上海舜宇恒平科学仪器有限公司;DF-101S集热式磁力加热搅拌器:金坛市晶玻实验仪器厂。
1.3 方法
1.3.1 葡萄糖标准溶液的配制
准确称取105℃干燥至恒重的葡萄糖100 mg,混匀后用蒸馏水溶解并定容至100 mL。量取20 mL并定容至100 mL,得到浓度为0.2 mg/mL的葡萄糖标准品溶液,待用。
1.3.2 蒽酮试剂的配制
精密称取蒽酮0.2 g,加入浓硫酸100 mL,完全溶解后,置于棕色瓶内,现用现配。
1.3.3 标准曲线的绘制
依次量取葡萄糖标品 0、0.2、0.4、0.6、0.8、1.2、1.5 mg置于10 mL具塞试管中,加入4 mL现配的蒽酮试剂,100℃油浴加热10 min,冷却至室温25℃后,静置20 min,于620 nm下测定吸光度(葡萄糖浓度=标品浓度×所加标品体积/总体积;总体积=标品体积+蒽酮试剂体积)。
1.3.4 筛选合适的离子液体
称取一定质量的无机盐(以该无机盐0.01 mol计算)和1 g的离子液体混合于10 mL水中振荡后静置,观察是否有双水相形成;若无,则放入数控超声波清洗器中超声至有双水相形成,若超声时间超过105 min,则可表明无双水相形成(超声提取温度低,有利于萃取一些热不稳定的天然产物,在超声场的作用下,由于超声的空化作用,相间的传质速度更快,因而萃取效果更好)。
1.3.5 确定最优的离子液体浓度
在提取温度为80℃,提取时间为90 min,料液比为桑叶∶水=1∶17(g/mL)的条件下,于离子液体浓度 0~0.001 mol/mL范围内配制不同浓度溶液,在转速为2 500 r/min条件下离心3 min,量取离心后液体的体积并记录;用0.2 mL移液管量取离心后上清液0.1 mL,定容至10 mL容量瓶中;再用1 mL移液管量取定容后液体1 mL于试管中,加入4 mL配制的蒽酮溶液,封口,100℃油浴加热10 min,冷却(20 min左右)至室温25℃,于620 nm下测吸光度,比较吸光度值并确定最优的离子液体浓度。
1.3.6 单因素试验方法
以已知离子液体浓度配制的溶液为研究对象,以吸光度为指标,在单变量的情况下考察提取温度、提取时间、料液比对桑叶中多糖提取结果的影响[4]。在单因素的考察中,因为离子液体的存在,参比溶液的获得难度较大,故而双水相中更多考虑的是不同条件下的相对值,吸光度有负数出现,但不影响各个参数之间的定性趋势判断。
1.3.6.1 提取温度的影响
在提取时间为 90 min,料液比为桑叶∶水=1∶17(g/mL),最优离子浓度下,在不同温度下油浴加热,测其吸光度确定适宜温度;考察提取温度分别为60、70、80、90、100℃。
1.3.6.2 提取时间的影响
在料液比为桑叶∶水=1∶17(g/mL),适宜提取温度和最优离子液体浓度下,油浴加热不同时间,测其吸光度确定适宜的提取时间;考察提取时间分别为30、60、90、120、150 min。
1.3.6.3 料液比的影响
在已确定最优离子液体浓度、适宜提取温度和提取时间的试验条件下,测定不同料液比下吸光度确定适宜料液比;考察料液比分别为 1∶13、1∶14、1∶17、1∶20、1∶21(g/mL)。
1.3.6.4 响应面试验方法
根据单因素试验结果,采用三因素三水平的响应面分析设计,根据Box-Behnken中心组合试验设计原理优化工艺条件,并采用Design Expert软件进行响应面分析。试验因素与水平设计见表1。

表1 试验因素水平及编码Table 1 Level of experimental factors and coding
1.4 数据分析
采用Design-Expert 8.0软件进行试验设计,并进行数据分析。
2 结果与分析
2.1 葡萄糖标准曲线
以葡萄糖溶液浓度(X)为横坐标,以吸光度(Y)为纵坐标进行线性回归,得标准曲线如图1所示,线性方程为:Y=33.239X-0.276 5,R2=0.999 8。结果表明,葡萄糖浓度在0~0.06 mg/mL的范围内与吸光度呈良好的线性关系。

图1 葡萄糖标准曲线Fig.1 Standard curve of glucose
2.2 离子液体筛选
选择15种离子液体分别与不同的无机盐进行试验。选用的无机盐分别为磷酸氢二钾、无水氯化钙、氢氧化钾、磷酸二氢钾、氯化钠、硫酸铵、无水碳酸钾、硫代硫酸钠、柠檬酸钠、氯化钾、氢氧化钠、无水碳酸钠、磷酸二氢钠。依次进行超声波分层效果的试验,试验得出1-辛基-3-甲基咪唑氯盐、1-丁基-3-甲基咪唑六氟磷酸盐、1-己基-3-甲基咪唑六氟磷酸盐、1-丁基-3-甲基咪唑双三氟甲烷磺酰亚胺盐、1-丁基-3-甲基咪唑四氟硼酸盐这5种离子液体在加入大部分的无机盐后都可以发生分层现象,其中1-丁基-3-甲基咪唑四氟硼酸盐对氯化钠不发生分层现象,其它12种无机盐都可发生分层现象;1-己基-3-甲基咪唑六氟磷酸盐对13种无机盐都可发生分层现象,考虑经济效益,最终决定选用1-丁基-3-甲基咪唑四氟硼酸盐为本次试验合适的离子液体。
2.3 最优离子液体浓度
离子液体浓度对桑叶多糖提取效果的影响见图2。
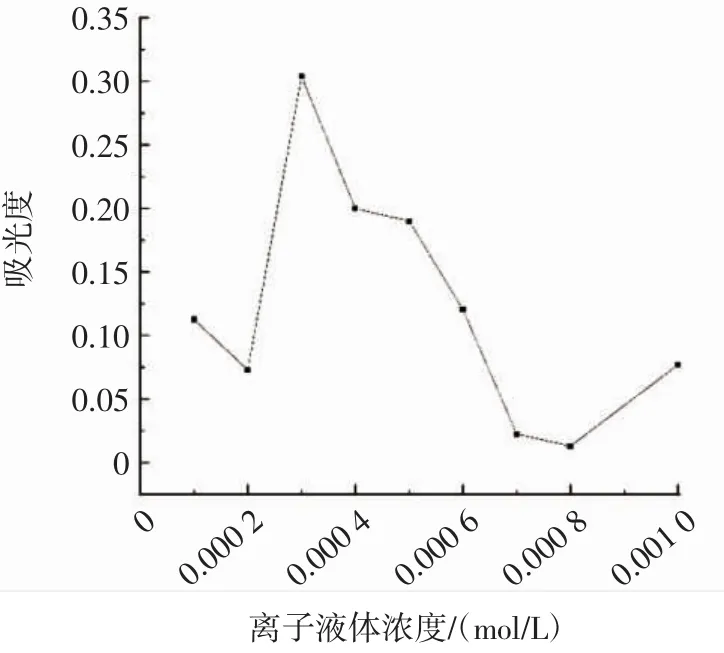
图2 离子液体浓度对桑叶多糖提取效果的影响Fig.2 Effect of ionic liquid concentration on polysaccharide extraction from mulberry leaves
由图2可得,离子液体浓度在0~0.000 8 mol/L范围内,吸光度随浓度的变化大致为先增大后减小,并在0.000 3 mol/L处达到最大值;由此可以确定最优离子液体浓度为0.000 3 mol/L。
2.4 单因素试验结果
2.4.1 提取温度的影响规律
提取温度对桑叶多糖提取效果的影响见图3。
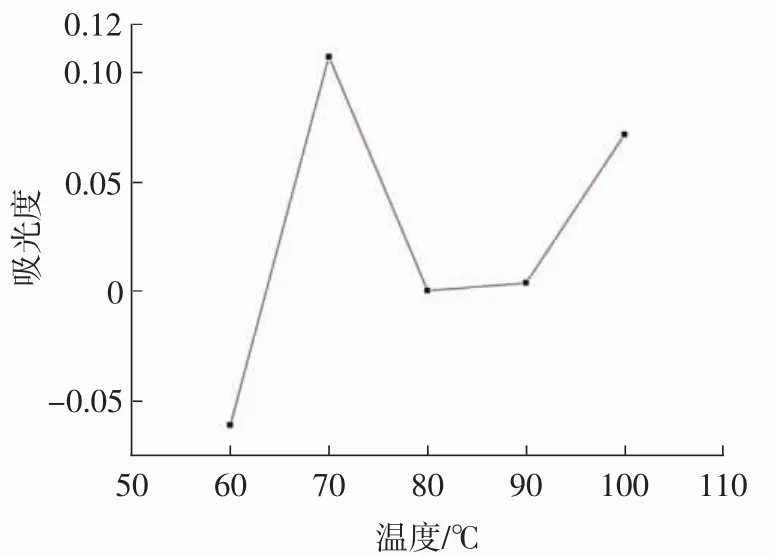
图3 温度对桑叶多糖提取效果的影响Fig.3 Effect of temperature on polysaccharide extraction from mulberry leaves
由图3可以看出不同温度下吸光度的变化关系。在60℃~80℃提取温度范围内,吸光度随温度的升高先增大后减小,并在70℃时达到最大;之后随着温度的上升,吸光度又回升,结合实际经济效益,初步得出最佳温度为70℃。
2.4.2 提取时间与吸光度的影响
提取时间对桑叶多糖提取效果的影响见图4。

图4 提取时间对桑叶多糖提取效果的影响Fig.4 Effect of extraction time on polysaccharide extraction from mulberry leaves
由图4可直观地看出当提取时间为120 min时,效果最好。
2.4.3 料液比与吸光度的影响
料液比对桑叶多糖提取效果的影响见图5。

图5 料液比对桑叶多糖提取效果的影响Fig.5 Effect of material liquid ratio on polysaccharide extraction from mulberry leaves
从图5纵坐标中可以看出在料液比为1∶17(g/mL)时,吸光度值相对最高,则料液比为1∶17(g/mL)时是提取多糖的最优值。
2.5 响应面试验结果
响应面设计见表2,回归模型方差分析见表3。0.474 07A-0.300 67B+0.940 88C+0.356 51AC-0.916 94A2-0.580 25B2。R2Adj=0.908 6、R2Pred=0.851 6 和信噪比为15.954值远大于4,回归方程拟合度和可信度均很高,能够很好地对吸光度进行预测,从而获得最佳多糖浓度提取方法。
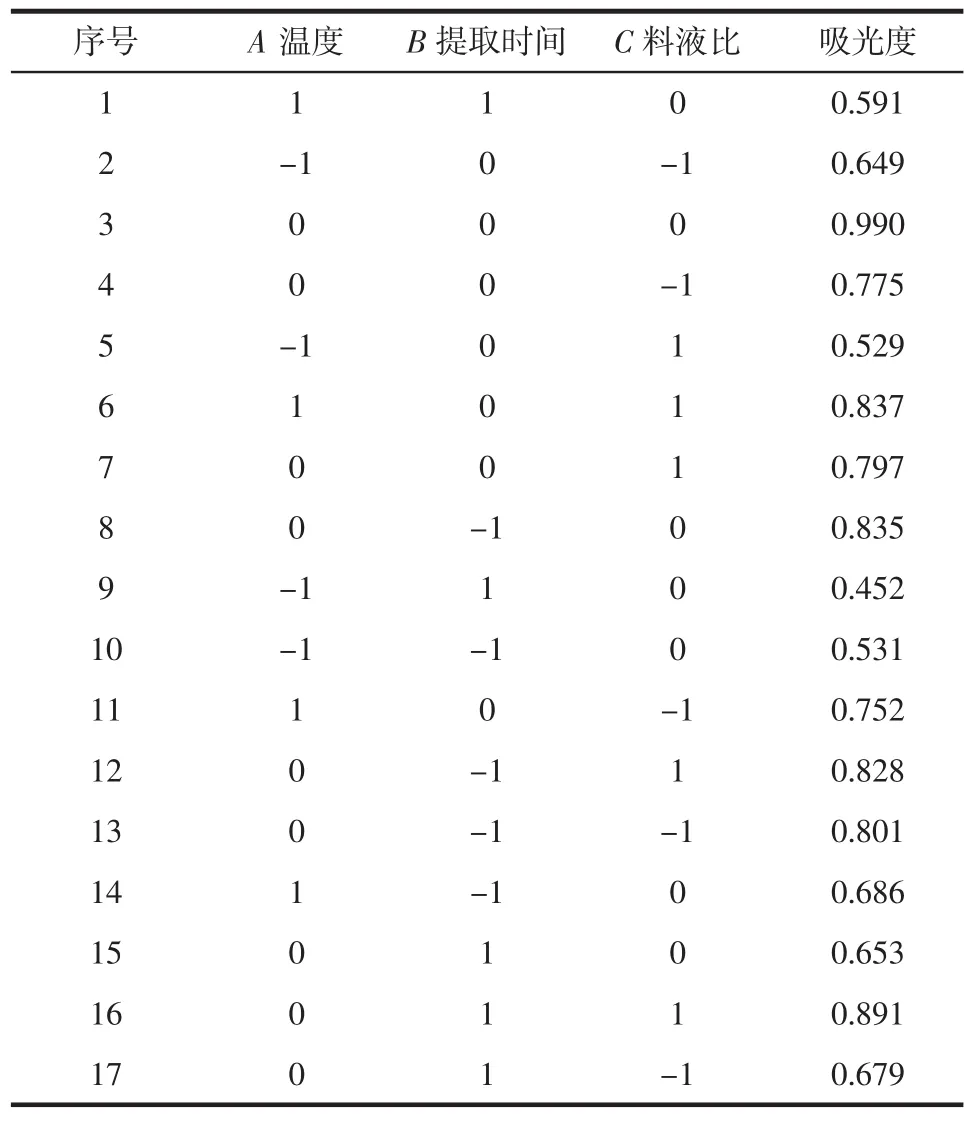
表2 响应面分析方案与试验结果Table 2 Response surface analysis scheme and test results
料液比、提取温度交互作用对多糖提取效果影响的响应面见图6。

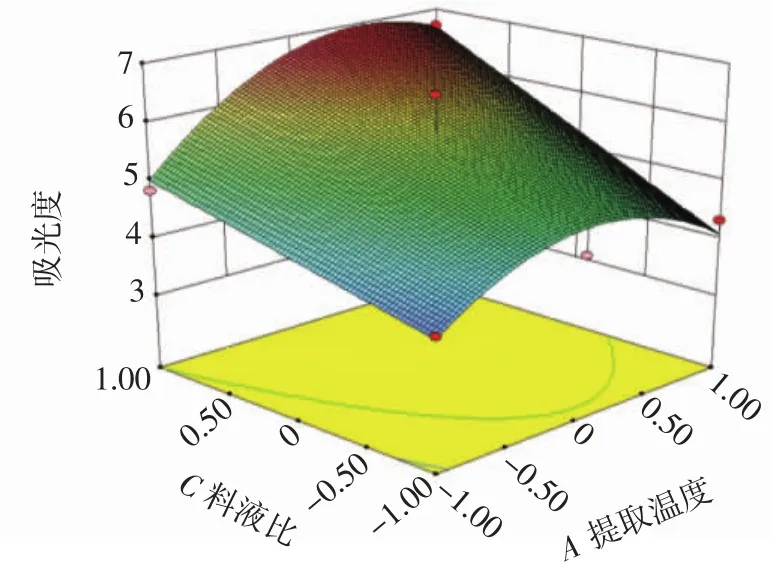
图6 料液比与提取温度交互作用对多糖提取效果影响的响应面Fig.6 Response surface and contour of the interaction of material-liquid ratio and extraction temperature on the extraction effect of polysaccharides
从图6可以看出,桑叶多糖的提取效果随着温度和料液比的提高而加大,这可能是由于温度和多糖分子内能之间的正相关的关系,但太高的温度亦会使多糖分子结构的破坏,料液比的提高将以更多的溶剂处理和成本高昂为代价,在一定范围之上将不可无限制的增加。根据Box-Behnken中心组合试验设计对多糖提取工艺条件进行优化,在模型取值范围内选择起始点作为最低点,将高值选择一个极大值,采用模型快速上升法进行优化,由此得到最佳的提取工艺条件为提取温度 76.3 ℃,料液比 1∶19.89(g/mL),提取时间为109.38min。根据实际,将参数调整为提取温度76℃、料液比 1∶20(g/mL)、提取时间 109 min,所得到的吸光度为0.836。进行验证试验,两次吸光度平均值为0.817,多糖提取率为6.77%,实测值与理论值无显著性差异,表明响应面分析得到的最佳工艺具有可信度。
3 结论
本试验通过筛选形成双水相现象较好的离子液体和盐并用溶剂浸提法对桑叶中多糖的提取工艺进行探究。通过用15种不同的离子液体与13种不同的无机盐的结合筛选,发现在桑叶多糖的提取体系中离子液体1-丁基-3-甲基咪唑四氟硼酸盐有很好的提取效果。而通过单因素试验和响应面设计最终确定了离子液体溶剂浸提法提取桑叶多糖的最佳工艺条件为离子液体的浓度0.000 3 mol/L,提取温度76℃,提取时间 109 min,料液比 1 ∶20(g/mL)。

