一例HIV窗口期样本三种试管核酸检测结果分析
帅敏 薛薇 黄超 邹晨 田智
血液核酸扩增技术是一种高灵敏度的血液传染病检测技术,能显著缩短病毒感染检测“窗口期”,检出病毒变异及免疫静默的感染者,降低输血传播病毒的风险[1]。自从血站实施核酸检测全覆盖以来,不同试管类型、离心温度和离心时间对核酸检测结果的影响,尤其是对HIV 核酸检测结果的影响尚不清楚。对HIV 强阳性样本而言,无论如何处理核酸都能检测出来,讨论意义不大。只有对HIV 窗口期样本的核酸检测结果进行分析才能看出试管类型、离心温度和离心时间对HIV 窗口期样本核酸检测结果的影响[2]。目前这方面一直缺少相关实验数据的说明,这主要是由于HIV 窗口期样本很难遇到。2018年8月初,检验科检测出一例HIV 窗口期样本(对拆分出的HIV 反应性样本都按窗口期样本来对待,后期结果证明该样本为HIV 窗口期样本),及时对同时留取的用三种类型真空采血管样本进行核酸检测,取得了相关检测数据,并及时完成对该样本的病毒载量检测。市疾控中心追踪三个月后再次采血进行WB 确认实验,确认结果为HIV 阳性[3]。现将对该HIV 窗口期样本的确认过程和三种不同处理模式的核酸检测结果进行回顾性分析,以探讨不同试管类型、离心温度和离心时间对HIV 窗口期样本核酸检测结果的影响。
1 材料与方法
1.1 样本来源与处理
1.1.1 样本来源
2018年7月30日按操作规程采集的无偿献血者样本,留取三管样本,第一管为带分离胶促凝的酶免检测样本,第二管为带分离胶EDTA-K2抗凝的核酸检测样本,第三管为EDTA-K2抗凝的血型检测样本(无分离胶),每管都留取5 mL 全血样本[4]。
1.1.2 样本处理
采样后对三份样本进行离心。带分离胶促凝样本,离心参数25℃,1 600 r/min,10 min;带分离胶EDTA-K2抗凝的核酸检测样本,离心参数5℃,1 600 r/min,20 min;EDTA-K2抗凝样本(无分离胶),离心参数25℃,1 600 r/min,5 min[5]。
1.2 仪器与试剂
KUBOT8420 常温离心机(日本,久保田商事株式会社)、ML-STAR8CH 全自动加样仪(瑞士,汉密尔顿)、FAME24/20 全自动酶联免疫分析仪(瑞士,汉密尔顿);DA3000、DA3500 核酸提取仪(中山大学达安基因股份有限公司)、smart32 核酸提取仪(中山大学达安基因股份有限公司);AFD9600 PCR 扩增仪(杭州,安杰思)、ABI7500 PCR 扩增仪(美国,ABI 公司)[6]。
常规血清学检测试剂:索灵HBsAg(批号D557910 效期20190205);新创HBsAg(批号2018045110 效期20190426);Ortho 抗-HCV(批号EXE285 效期20181221);科华抗- HCV(批号201801021 效期20190115);万泰抗-TP(批号N20180206 效期20190131);新创抗-TP(批号2018017501 效期20190102);万泰HIV 检测试剂,(批号I 20180205 效期20190131);伯乐HIV 检测试剂,(批号7J0409 效期20181121);科华ALT 速率法试剂,(批号20180112,效期20190107);核酸检测试剂:中山大学达安股份有限公司,批号2017003效期,20181120;病毒载量检测试剂:中山大学达安股份有限公司,批号2018004,效期20190514 蛋白印迹检测试剂:MP Diagnostics HIV BlOT 2.2 人类免疫缺陷病毒(HIV1+2 型)抗体检测试剂盒(免疫印迹法),批号AE8007,效期20191101;检测膜批号AB8C03049A,效期20200301。
1.3 方法
对该献血者样本进行血清学检测、8 混样核酸检测,单样本拆分检测[7]。确认该样本核酸检测结果为HIV 阳性后,对同时留取的3 种类型样本进行核酸单样本检测和HIV 病毒载量检测。三个月后由CDC 工作人员找到该献血者重新采集样本进行WB 确认实验[8]。
1.4 统计学分析
采用SPSS Statistics17.0 进行统计学分析;对离心温度、离心时间与核酸检测结果进行双变量相关分析,以P<0.05 为差异有统计学意义。
2 结果
2.1 血清学检测结果
该样本HBsAg、Anti-HCV、HIV-Ag/Ab、Anti-TP血清学检测结果均为阴性,ALT 结果正常。见表1。
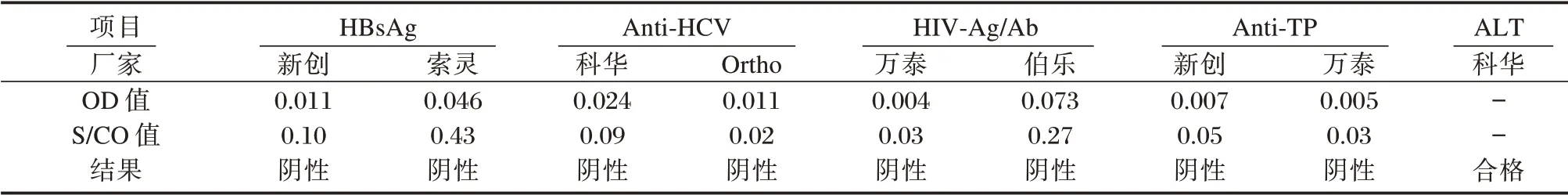
表1 HIV 窗口期样本血清学检测结果Table 1 serological test results of HIV window period samples
2.2 核酸检测结果
确定该样本核酸检测拆分结果为反应性结果后,第一时间马上对三种类型试管的样本进行核酸检测。见表2。

表2 HIV 窗口期样本三种试管的核酸检测结果Table 2 nucleic acid test results of three types test tubes of HIV window period samples
2.3 蛋白质免疫印迹(WB)确认结果
病毒载量检测结果HIV 阳性扩增,浓度为3.28×103IU/mL。市CDC 三个月后找到该献血者再次采样进行WB 确认实验,WB 确认结果为HIV-1 抗体阳性,检出条带有P24、gp41、P51、P66、gp120、gp160。见图1。

图1 WB 确认结果电泳图Figure 1 Electrophoretogram of WB confirmation results
离心5、10 和20 min 的核酸检测结果比较,差异无统计学意义(P>0.05)。离心温度5℃和25℃的核酸检测结果比较,差异无统计学意义(P>0.05)。Ct 值的均值x=32.62,标准差S=0.14,变异系数CV=0.44%,极差为0.36Ct 值。见表3。

表3 HIV 窗口期样本三种类型试管不同处理条件核酸检测结果对比Table 3 Comparison of nucleic acid detection results of three types of test tubes with different treatment conditions in HIV window period samples
3 讨论
通过对带分离胶抗凝、促凝和不带分离胶抗凝真空采血管HIV 窗口期样本核酸检测结果的分析,了解三种类型真空采血管不同离心时间、不同离心温度对窗口期HIV 样本核酸检测结果的影响。北京市血液中心的研究也表明“在不超过30℃的采血环境中,NAT 标本的现场保存,只需要和采集的血液一样保存即可,并在24 小时内离心处理,如此操作不会对HBV、HCB、HIV-1 弱阳性标本d2 的检测质量产生影响”[2]。虽然北京血液中心的研究是在不同厂家生产的带分离胶抗凝真空采血核酸检测结果之间进行,而本次的研究是在不同类型真空采血管核酸检测结果之间进行,但研究结果都表明用合适的条件处理核酸检测样本不会影响核酸检测的质量。
三种类型试管样本核酸检测Ct 值的极差是0.36,足量、无溶血、无脂血的三种类型试管的样本都可以用于核酸检测。HIV RNA 的浓度在血浆和血清中差别很小;有无分离胶对HIV 窗口期样本核酸检测结果影响很小,分离胶的主要作用是防止细胞破裂和溶血后对核酸检测的影响。足量无溶血的三种类型试管的样本都可以用于核酸检测,能够解决核酸检测5 mL 试管样本量在遇到拆分无效时面临的样本量不足的问题。混样检测需要的样本量在150~300 μL 之间,拆分样本量在960~1 600 μL 之间,正常的混样和拆分样本量仅需5 mL,个别拆分无效的样本可以用5 mL 带分离胶的促凝试管样本进行拆分。这样就不仅减少献血者血液的采集量,还减少8 mL 真空采血管成本的支出,也有利于实验室样本管理体系的标准化。以京津冀地区2018年14 个采供血机构检测数据显示,核酸混样检测有效批中pool 的无效率为0.2%(244/123697pool)[4],按6 样本混样计算约74 万份样本中只有1 464 份样本需要重新检测,而这其中只有拆分无效的样本才需要用到第二份5 mL 试管的样本。采用三种类型试管互备核酸检测和酶免检测的模式,可以节约大量采购8 mL 真空采血管的成本。
由于HIV 窗口期样本很难遇到,所以数据量较小,以上分析只是该例HIV 窗口期样本的分析结果。

