PD-1单抗治疗非小细胞肺癌相关不良反应及其与疗效的相关性分析
义维丽,赵文成,黄东宁,覃 莉,吴新天,周 斐,吴凤英
1.柳州市工人医院肿瘤科,广西 柳州 545005;2.同济大学附属上海市肺科医院肿瘤科,上海 200433
肺癌是发病率和死亡率最高的恶性肿瘤,2018年全球癌症统计数据显示,肺癌占全球恶性肿瘤总发病人数的11.6%,因肺癌死亡人数占癌症相关总死亡人数的18.4%[1]。在中国,肺癌发病率和死亡率均居第1位,严重威胁着人类健康[2]。约80%的肺癌为非小细胞肺癌(non-small cell lung cancer,NSCLC),多数患者初诊时已是晚期,近年来针对免疫检查点程序性死亡[蛋白]-1(programmed death-1,PD-1)/程序性死亡[蛋白]配体-1(programmed death ligand-1,PD-L1)抑制剂的免疫治疗给晚期肺癌的治疗带来了曙光。PD-1抑制剂如纳武利尤单抗(nivolumab)、帕博利珠单抗(pembrolizumab)已被证实能显著延长晚期NSCLC患者的生存期,均获批用于晚期NSCLC的标准二线治疗[3-5],pembrolizumab获批用于一线联合治疗或单药用于PD-L1表达>50%的NSCLC患者[6]。免疫治疗相对安全,但也可能发生免疫相关不良反应(immune-related adverse event,irAE),随着免疫治疗在临床中应用的增多,irAE也日益被重视。目前肺癌免疫治疗的irAE报道多见于大型的Ⅲ期临床研究,而这些大型的全球性临床研究多为高加索人种,而其中亚裔人群,尤其是中国人群的数据相对较少。另外,国内很多自主研发的免疫抑制剂安全性数据不详。因此,本研究汇总分析了同济大学附属上海市肺科医院使用单药PD-1抑制剂的irAE发生情况及其与免疫治疗效果的相关性。
1 资料和方法
1.1 研究对象
回顾性分析同济大学附属上海市肺科医院2015年6月—2019年1月接受抗PD-1抑制剂单药治疗的局部晚期及晚期NSCLC患者(包括入组临床研究及非临床研究的患者)。收集患者的临床基本特征、PD-1治疗的种类和方法,收集irAE的种类、发生时间、严重程度、处理和预后。irAE如皮肤反应、胃肠道反应、免疫性肝炎、内分泌系统毒性等分级、分类标准采用美国国家癌症研究所通用不良事件术语标准4.0版(Common Terminology Criteria for Adverse Events version 4.0,CTCAE v4.0)评估。
1.2 方法
收集疗效数据,疗效评估使用实体瘤疗效评价标准(Response Evaluation Criteria in Solid Tumors,RECIST)1.1版本,对评估为疾病进展(progressive disease,PD)的患者在4~8周后经RECIST评估再确认,收集客观缓解率(objective response rate,ORR)、疾病控制率(disease control rate,DCR)、无进展生存期(progression-free survival,PFS)。随访截至2019年6月1日。按有无irAE发生分为两组:irAE组及非irAE组。
1.3 统计学处理
使用SPSS 23.0软件,分析两组患者基线临床特征,年龄采用描述性统计分析及独立样本t检验。两分类变量如吸烟状态、性别。有效率ORR、DCR等采用Pearsonχ2检验。免疫治疗线数、病理学类型、放射治疗史等采用R×C表χ2检验分析。总人群及两组患者PFS采用Kaplan-Meier法和log-rank进行检验分析。单因素Kaplan-Meier法及多因素COX回归风险比例模型方法分析探讨irAE与患者PFS的相关关系,P<0.05为差异有统计学意义。
2 结果
2.1 人群基线特征
2015年6月—2019年1月,共109例患者接受了PD-1抑制剂单药免疫治疗,基线特征如下:中位年龄64岁(32~82岁),男女比例为89∶20,ECOG体能状态(performance status,PS)评分0、1、2分者分别为4、103、2例,吸烟或既往吸烟、从不吸烟者分别为69、40例,Ⅲ、Ⅳ期分别为20、89例,腺癌、鳞癌、NSCLC-非特指型(NSCLC-not otherwise specified,NSCLCNOS)、其他病理学类型分别为50、52、4、3例,免疫单药一线、二线、三线及以上患者分别为15、65、29例,接受免疫治疗药物种类分别为nivolumab、pembrolizumab、BGB-A317[百济神州(北京)生物科技有限公司PD-1单抗]、SHR1210(江苏恒瑞医药股份有限公司PD-1单抗)、IBI308[信达生物制药(苏州)有限公司PD-1单抗],患者数分别为25、60、17、3、4例。基因状态:野生型、未检测、EGFR突变、KRAS突变、BRAF突变为98、4、2、4、1例。PD-L1表达情况:阳性、阴性、未检测分别为11、8、90例,多数患者未检测PD-L1状态(90/109,82.5%),19例检测的患者中PD-L1阳性(≥1%)有11例(10例为Ⅳ期,1例为Ⅲ期,表1)。
2.2 抗PD-1免疫治疗irAE
irAE 发生情况:109 例患者中,63 例(57.8%)患者发生了irAE,其中43例(68.2%)发生了复合irAE,20例(31.8%)为单一irAE。最常见irAE为皮肤反应(29例,25.7%),其次分别为免疫性肝炎(18例,16.6%)、疲乏(16例,14.7%)、内分泌系统毒性(15例,13.8%)、免疫性肺炎(12例,11.0%)及胃肠道反应(10例,9.2%)等;皮肤血管瘤仅见于使用SHR1210患者。irAE的发生情况和严重程度见表2和图1。
发生时间:irAE多于治疗后4~30周出现,最常见于6~27周。不同irAE起始时间不一样:皮疹反应为18.9周(0.2~38.5周),瘙痒为28.5周(8.0~50.0周),免疫性肝炎为27.1周(4.0~67.1周),免疫性肺炎为28.2周(6.3~69.3周),内分泌系统毒性为26.6周(4.0~40.0周),消化系统毒性为6.1周(2.7~14.2周),疲乏为24.0周(0.2~45.0周)等(图2)。
治疗和预后:共17例患者使用了激素冲击治疗,主要用于肺炎、结肠炎、肾炎、关节炎等,其中4例免疫性肺炎和1例免疫性结肠炎患者缓解后永久停止使用抗PD-1治疗,免疫性肺炎患者中1例患者肺炎治疗降级后更换化疗方案,3例患者因肿瘤进展更换治疗方案,1例患者因肿瘤进展未继续抗肿瘤治疗。3例肺炎患者及肾炎、关节炎等患者治疗降级后继续使用抗PD-1治疗。
2.3 irAE的特殊情况
复合irAE:43例患者发生复合irAE,其中最为常见的是皮疹合并免疫性肝炎(16/43,37.2%),其次为皮疹合并乏力(10/43,23.3%),免疫性肝损伤合并甲状腺功能异常(6/43,13.9%),皮疹合并免疫性肺炎(5/43,11.6%),免疫性肝炎合并腹泻(5/43,11.6%)等。
严重irAE后再挑战患者包括:1例皮疹合并3级免疫性肺炎患者治疗降级后继续抗PD-1治疗,出现Ⅰ度皮疹,未再次出现免疫性肺炎;1例患者因无症状性淀粉酶、脂肪酶Ⅲ级升高,停药后缓解,后继续抗PD-1治疗,再次出现1/2级irAE,未出现严重irAE。另外,有3例免疫性肺炎(2例2级,1例1级)、2例肾炎(1例1级,1例2级)及2例关节炎(均为2级)患者后续继续使用抗PD-1治疗未见irAE加重,用药至PD。
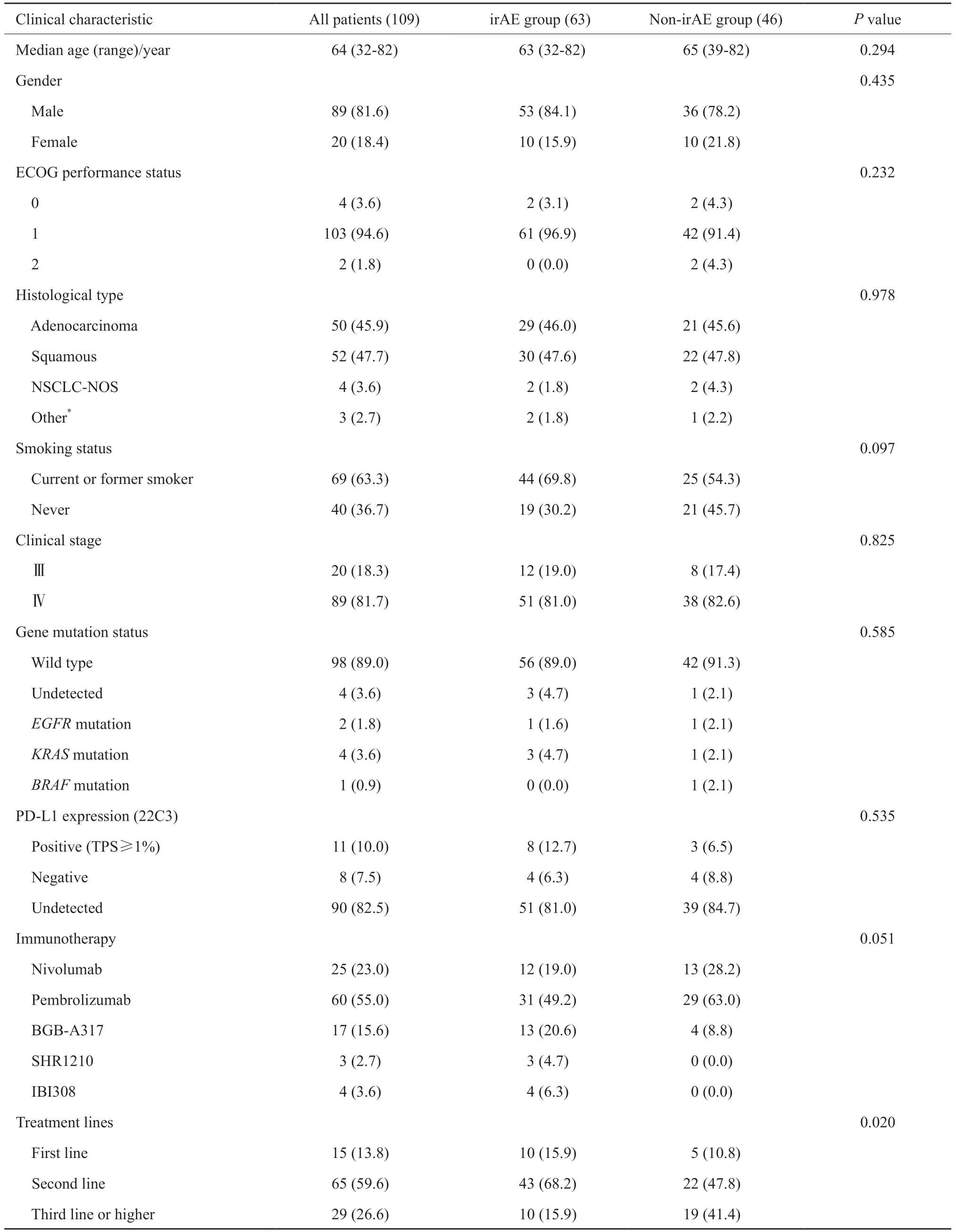
表1 总人群基线特征Tab.1 Clinical characteristics of the total population[n (%)]

表2 IrAE分类、分级Tab.2 The category and grade of irAE[n (%)]

图1 IrAE分类、分级Fig.1 The category and grade of irAE
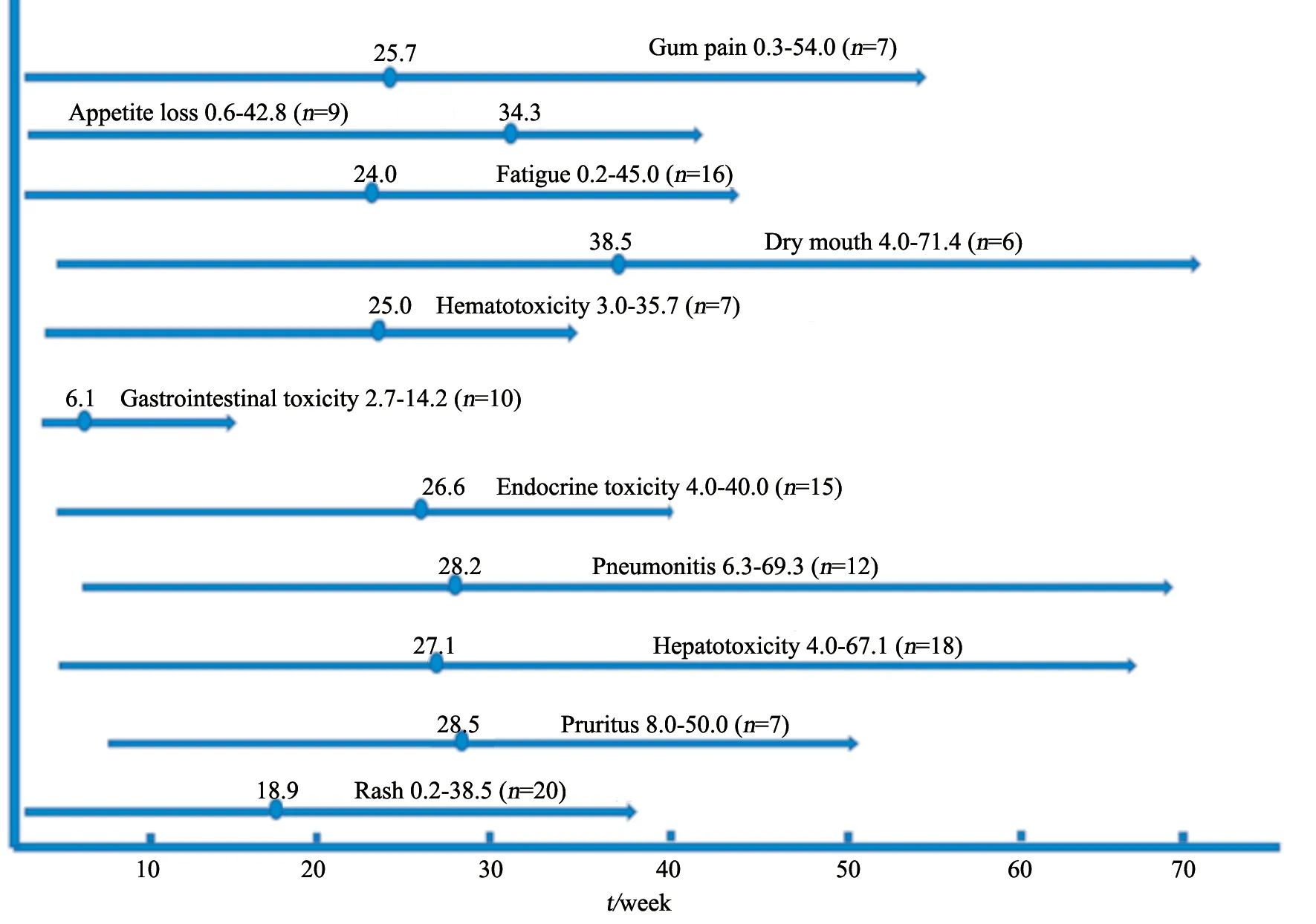
图2 不同irAE发生的中位时间Fig.2 Median time to onset irAE for different toxicities
2.4 irAE与抗PD-1治疗效果的相关性
截至随访日期,总人群ORR为24.7%,DCR为77.9%,irAE组对比非irAE组有较高的ORR及DCR(ORR:36.5%vs8.7%,P=0.001;DCR:85.7%vs67.4%,P=0.023,表3)。总人群中位PFS为4.6个月(95% CI:3.9~5.2个月)。irAE组和非irAE组中位PFS分别为8.7和3.5个月(HR=0.294,95% CI:0.184~0.469,P<0.001,图3~4)。单因素分析显示,免疫性肝炎(P=0.002)、皮肤反应(P<0.001)、口腔黏膜炎(P=0.003)及牙龈疼痛(P=0.02)与PFS预后相关;多因素分析提示,皮肤反应(P=0.014)与疗效呈正相关,中位PFS为12.7和4.3个月(HR=2.332,95% CI:1.184~4.595,P=0.014,表4,图5)。

表3 免疫治疗效果Tab.3 Response to immunotherapy[n (%)]

表4 免疫不良事件与PFS的关系Tab.4 Relationship between immune-related adverse events and PFS
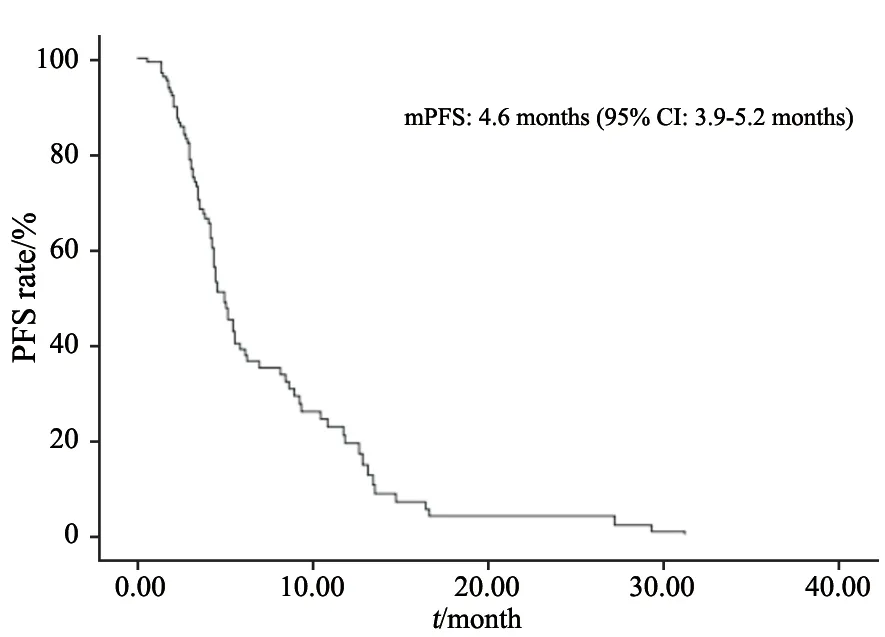
图3 总人群的PFSFig.3 PFS in total population

图4 irAE组及非irAE组患者的PFSFig.4 PFS for patients with and without irAE
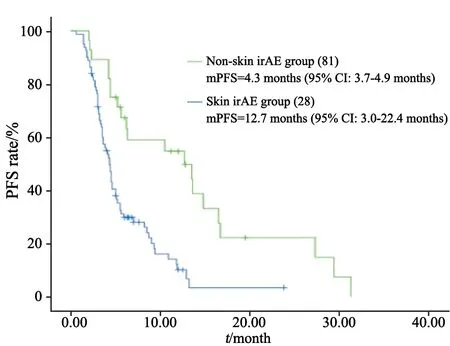
图5 有无皮肤irAE患者的PFSFig.5 PFS for patients with and without skin irAE
3 讨 论
PD-1/PD-L1抑制剂可阻断T细胞上的PD-1受体与其配体PD-L1之间的相互作用,从而恢复T细胞功能,增强T细胞对肿瘤细胞的杀伤能力[7-8]。然而过度激活的T细胞可以引起自身免疫介导的不良反应,对机体各系统组织产生免疫性损伤,称之为irAE。本研究分析了同济大学附属上海市肺科医院使用单药PD-1抑制剂免疫治疗的irAE发生情况,以及irAE的发生与疗效的相关性。
Pillai等[9]对晚期NSCLC行PD-1抑制剂治疗的12个研究共3 284例患者的irAE进行了meta分析,疲乏为最常见的irAE,发生率为19%,甲状腺功能减退发生率为6.7%,皮疹及腹泻发生率为9%,免疫性肺炎为4%,结肠炎、便秘、血液学毒性、免疫性肝炎等少见。Remon等[10]对晚期NSCLC患者PD-1抑制剂治疗irAE的发生进行了汇总,最常见的irAE为疲乏(20%左右)和皮肤反应(20%~40%);其次为免疫性肝炎、胃肠道反应、内分泌系统毒性等,少见irAE包括免疫性肺炎(约5%)、心脏毒性(<1%)、神经毒性(3.0%~6.1%)、血液学毒性(约2%)、胰腺毒性(0.6%~3.0%)、肾毒性(2%~3%)、眼毒性(<1%)等,并对常见irAE的发生时间进行了汇总,不同irAE发生的时间不一样,皮肤反应多发生于6.1周(0.1~100.0周),胃肠道毒性为4.9周(0.1~91.0周),内分泌系统毒性为12.2周(1.9~88.1周),免疫性肝炎为8.7周(0.1~131.0周),免疫性肺炎为30.3周(1.6~108.0周)。本研究中,皮肤反应(25.7%)最常见,其次为免疫性肝炎(16.6%)、疲乏(14.7%)、内分泌系统毒性(13.8%)等。irAE发生时间上,皮疹反应为18.9周(0.2~38.5周),瘙痒为28.5周(8.0~50.0周),免疫性肝炎为27.1周(4.0~67.1周),免疫性肺炎为28.2周(6.3~69.3周),内分泌系统毒性为26.6周(4.0~40.0周),消化系统毒性为6.1周(2.7~14.2周),疲乏为24.0周(0.2~45.0周)等,部分irAE发生时间比较长。本研究中,免疫性肝炎、肺炎的发生率相对较高,既往报道的数据多为临床研究数据的汇总分析,患者PS评分较好,而本研究包含了很多非临床研究患者,多线治疗的患者相对较多,irAE发生率相对较高。另外,中国为肝炎大国,虽然乙肝病毒抗原阴性,很多是慢性感染,导致免疫性肝炎的发生率略高于既往报道,可能是中国人群irAE谱中一个不一样的地方。本研究中3级以上irAE主要为免疫性肺炎,免疫性肺炎是一种相对少见但危及生命的irAE。Fujimoto等[11]回顾性分析nivolumab治疗15个中心615例晚期NSCLC患者的真实世界数据,10%的患者发生免疫性肺炎,5%的患者出现3级及以上免疫性肺炎。Nishino等[12]对包括黑色素瘤、NSCLC、肾癌等共4 496例患者使用PD-1抑制剂治疗后免疫性肺炎的发生进行meta分析,总人群发生率为2.7%,3级及以上肺炎发生率为0.8%,肺癌与黑色素瘤相比肺炎发生率为4.1%vs1.6%,3级及以上肺炎发生率为1.8%vs0.2%(P<0.001)。提示肺癌免疫性肺炎发生率高于黑色素瘤等其他肿瘤,可能原因为肺癌患者常暴露于吸烟和一些慢性肺损伤性疾病中,如慢性阻塞性肺部疾病等,导致免疫性肺炎发生率明显升高[13]。3级肺炎发生率高于相关临床研究,其可能原因:①中国很多肺癌患者为老年男性,长期吸烟,合并慢性支气管炎、慢性阻塞性肺病、甚至是陈旧性肺结核等慢性肺部疾病,导致免疫性肺炎发生率升高。②本研究人群包含较多非临床研究患者,后线治疗者较多,更能反应真实世界中肺炎发生率的情况。
本研究深入探索了irAE的发生与免疫治疗效果的相关性,发现irAE组患者免疫治疗效果明显优于非irAE组,多因素分析提示,皮肤irAE者较非皮肤irAE者预后好。Ricciuti等[14]回顾性分析了195例晚期NSCLC患者使用抗PD-1治疗的效果及与irAE发生率的关系,irAE组和非irAE组中位PFS分别为5.7和2.0个月(HR=0.41,95% CI:0.30~0.57,P<0.000 1)。Ali等[15]回顾性分析了40例使用nivolumab治疗的晚期NSCLC患者,发现皮肤irAE组和非皮肤irAE组ORR分别为42%和7%。Haratani等[16]回顾性分析了134例使用nivolumab治疗的晚期NSCLC患者的预后,发现有irAE组效果更好,中位PFS分别为9.2和4.8个月(P=0.04)。然而,目前irAE与免疫疗效之间的机制尚未阐明,先前有研究[17-18]表明,黑色素瘤患者治疗后容易出现白癜风,可能与黑色素瘤和正常黑色素细胞之间的共享抗原有关。NSCLC中皮肤irAE与疗效相关是否与共同抗原有关,尚待进一步研究。
本研究分析了中国晚期NSCLC患者使用单药PD-1抑制剂后irAE的发生情况、发生时间、处理及转归,探讨了irAE与免疫治疗效果的相关性,相较于国外临床研究数据,因中国人群既往的疾病谱与国外有所不同,同时本研究人群包含了使用BGB-A317、SHR1210、IBI308等国产PD-1单抗的患者等,本研究数据能更好地反映中国人群使用PD-1抑制剂的安全性和irAE发生率及与疗效的相关性等情况,数据更真实可靠。本研究也存在一定的局限性及不足,首先在非irAE组患者中,二线及后线以上治疗患者较irAE组偏多,这有可能令疗效评估出现偏倚,其次病例数不够多,尚待大样本研究进一步证实。
本研究发现肺癌患者PD-1单抗治疗后irAE多发生于6~27周,多为1~2级,皮肤irAE最多见,3~4级irAE多为免疫性肺炎,irAE发生与疗效相关,irAE患者相较于非irAE患者是否有着更好的疗效,irAE发生的机制以及有无预测irAE的标志物,尚需进一步研究探索。

