微创置管冲洗联合负压引流对肛周脓肿患者术后肛门疼痛和生理功能的影响
卢培东,王欣,徐洁,王丰艳
(青岛市市立医院西院区·青岛市第九人民医院,1.普外科;2.呼吸内科,山东 青岛 266002)
肛周脓肿多发于婴幼儿和20~40岁人群,男性发病率为女性3~4倍,患者多因肛周疼痛、红肿和硬结就诊。此病虽比较常见,但若诊治不及时,可引起肛瘘、坏死性筋膜炎,甚至脓毒血症。脓肿切开引流是目前治疗肛周脓肿的主要方法,手术操作简单,能迅速排出脓肿和缓解症状体征,但手术所致的创伤较大,创面愈合较慢、渗液多,患者术后的肛门疼痛明显,还可能影响肛门生理功能恢复[1]。近些年,微创外科理念深入人心,肛旁置管冲洗脓腔同时持续负压引流作为一种微创新疗法,逐渐受到临床重视。目前报道多侧重于对创面愈合和医疗费用的影响,而对患者术后肛门疼痛以及肛门生理功能的影响报道偏少[2]。本研究探讨上述微创新疗法对肛周脓肿患者术后肛门疼痛和生理功能的影响。
1 资料和方法
1.1 一般资料
选取2017年6月至2020年5月在青岛市第九人民医院普外科接受手术住院治疗的104例肛周脓肿患者。纳入标准:(1)患者主诉肛周红、肿、热、痛,排便时疼痛明显,入院就诊后经直肠指诊、超声和血常规等,确诊肛周脓肿;(2)患者年龄16~75岁,沟通交流能力良好;(3)经必要沟通讲解,均自愿接受手术住院治疗,对研究知情同意。排除标准:(1)化脓性汗腺炎、肛周疖肿及毛囊炎、骶前畸胎瘤或肛瘘等其他肛周肿块疾病者;(2)经沟通,倾向于选择药物治疗者;(3)肛周手术病史;(4)哺乳妊娠期妇女。利用随机数表法将104例肛周脓肿患者分成常规组和研究组,每组各52例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。研究已获医学伦理委员会审核通过。
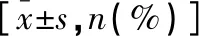
表1 两组肛周脓肿患者术前一般资料比较
1.2 方法
术前均完善专科相关检查,排除手术禁忌,借助肛门直肠腔内超声检查,了解脓肿大小、位置和深浅,均由资深普外科医师进行手术。
1.2.1 常规组 接受常规切开引流术,手术大都在局部麻醉下进行,但症状严重者选择全身麻醉。麻醉满意后,消毒铺巾,充分显露肛门部位。选择脓肿比较薄弱、波动感明显的病灶中央处作手术弧形切口,长度约3.0 cm,大弯钳扩张切口,充分引流出脓液,清除腔内坏死腐烂组织。根据Goodsall定律,从切口探入银质软探针,进入脓腔寻找内口位置,另一只手食指伸入肛内,帮助确定内口位置。低位脓肿者可直接切除感染内口,高位肛周脓肿者,需仔细观察脓腔大小,以及脓腔与肛门括约肌的位置关系,进行橡皮筋挂线处理,脓腔较大者,可作多切口对口引流。若术中探查未发现内口,脓腔切开引流,将脓肿充分排出即可。清理脓腔后给予0.5%甲硝唑注射液、生理盐水冲洗,冲洗后脓腔用凡士林纱布填塞,术毕。
1.2.2 研究组 接受肛旁微创置管冲洗联合负压引流,术前准备同常规组。选择脓肿比较薄弱、波动感明显的病灶中央处,用脓肿戳孔针进行穿刺,脓液流出表示脓腔穿刺位置准确。同样的手法在脓肿腔的边缘处进行戳孔穿刺,脓液从戳孔流出。用中弯钳适当扩张两个戳孔,直径约0.3 cm。从戳孔分别探入脓腔破隔器,充分清除腔内纤维隔、腐烂坏死组织。将两根14F导管从两个戳孔内植入脓腔,中央处戳孔导管植入深度需达到脓腔顶端,边缘处戳孔导管植入深度根据脓腔大小酌情选择,约0.5~1.0 cm。灌注生理盐水并确保引流通畅后,戳孔处缝合固定导管,采用0.5%甲硝唑注射液、生理盐水冲洗脓腔,至引流液清亮。负压引流前先探查内口,对内口进行修剪缝合处理,医用海绵封堵内口。裁剪医用泡沫敷料填入创腔,注意不留缝隙,缝合固定,半透明薄膜粘贴固定。连接三通管检查气密性,确认无漏气后,连接负压引流装置,负压值维持-200~-120 mmHg,监测体温和血象。
1.2.3 术后处理 术后使用抗生素3~5 d,开展健康教育,保持肛周清洁卫生,流质清淡饮食,排便时口服大便软化剂,每日温盐水坐浴等。常规组术后每日换药,研究组术后加强观察,确保引流通畅。院后保持联系方式进行随访,出院时叮嘱注意事项,嘱咐术后4周门诊复查。
1.3 研究指标
统计两组手术时间、出血量、创面愈合时间、住院时间及费用。术后采用视觉模拟疼痛评分量表(visual analogue scale,VAS)评估患者肛门疼痛度,VAS为患者自评,得分0~10分,依据主观疼痛感受选择适宜的分数,得分越高,表示肛门疼痛愈明显。术后4周门诊复查,参考Wexner评分量表[3]拟定肛门生理功能评价标准:(1) 正常:对大便、肠液、气体的控制正常;(2) 部分失禁:对固态成形大便控制尚可,但对稀便、肠液不能较好控制;(3)完全失禁:对固态大便、稀便、肠液、气体等均不能较好控制,需要使用卫生垫,生活方式改变。
1.4 统计学分析
2 结果
2.1 两组患者手术指标比较
研究组患者手术时间、创面愈合时间、住院时间和住院费用均短于或少于常规组(P<0.05),见表2。
表2 两组患者肛周脓肿患者手术指标比较
2.2 两组患者术后肛门疼痛比较
两组患者术前VAS评分比较,差异无统计学意义(P>0.05) ;术后1、3、5 d的VAS评分与术前比较,均明显下降(P<0.05),研究组术后1、3、5 d 的VAS评分低于常规组 (P<0.05)。见表3。
表3 两组患者术后肛门疼痛VAS评分比较
2.3 两组患者肛门生理功能比较
两组患者肛周脓肿患者均痊愈出院,术后4 周均复查,无中途失访病例,无复发和肛瘘发生。研究组肛门功能正常率高于常规组(P<0.05)。见表4。
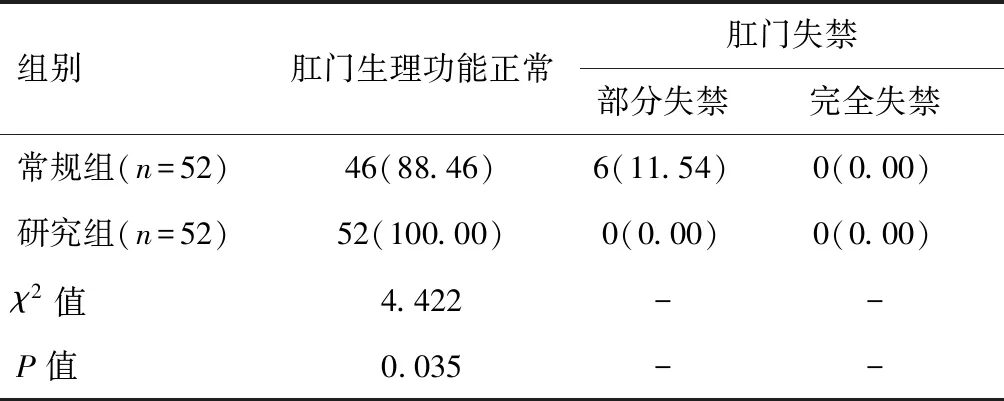
表4 两组术后肛门生理功能比较[n(%)]
3 讨论
肛周脓肿约占肛肠外科疾病的15%~30%,肛腺感染是主要致病因素,不良肛周卫生习惯、饮食不合理、长期便秘或腹泻者是高危发病人群[4]。脓肿切开引流是治疗肛周脓肿的有效手段,临床应用广泛,术者依据脓腔大小作手术切口,为充分引流出脓液,对切口扩张处理,切口长度较大,不仅创伤大、创面愈合慢,增加患者手术痛苦,而且易造成肛周软组织损伤,损伤括约肌,破坏肛门组织的完整性和自主生理功能,对患者日常生活和心理造成负面影响。已有报道[5-6]指出,高位肛周脓肿的脓肿范围大,位置较深,为确保引流通畅,需做多切口对口引流,创面愈合时间明显延长。如何减轻肛周脓肿患者的手术痛苦,保护肛门生理功能,需引起外科医师高度重视。
肛旁置管治疗肛周脓肿的最大优势在于微创,术者只需根据患者个体脓肿大小作2个戳孔即可,直径仅0.3 cm,操作步骤简单,节约手术时间,且无开放性切口,不破坏括约肌的完整性,保护肛门生理功能。负压封闭引流(vacuum sealing drainage,VSD)是近些年修复创面的物理技术,使用生物半透性膜封闭创面,在负压吸引作用下,借助敷料和引流管将创面的渗出物及时吸除,既防止脓液和分泌物在腔内堵塞引流,减轻水肿、污染,又能有效清除引流区的细菌,抑制细菌繁殖,促进脓腔内肉芽生长,缩小和修复脓腔,加快创面愈合[7]。Yusuke等[8]指出,使用腹部真空封闭引流术治疗危重患者腹部完全切口吻合口漏合并弥漫性腹膜炎的效果较良好,为临床治疗提供了新的选择。使用0.5%甲硝唑注射液、生理盐水冲洗脓腔,并给予VSD,能保持脓腔内相对清洁的局部环境,减少创面感染等并发症发生,促进创面愈合,同时减少术后换药和敷料更换次数,减轻医护工作负担。另外,高位肛周脓肿患者VSD后血清转化生长因子β(transforming growth factor β,TGF-β)和表皮细胞生长因子(epidermal growth factor,EGF)水平明显升高,促进创面血管形成和缩短愈合时间[9]。
本研究采用肛旁置管冲洗联合负压引流,取得较满意的效果。研究组手术时间、创面愈合时间、住院时间和住院费用均少于常规组,也印证了肛旁置管冲洗联合负压引流的临床优势和经济优势,与已有报道[10-11]相符。这可能是归因于VSD通过调节糖尿病患者血管内皮生长因子(vascular endothelial growth factor,VEGF)、超氧化物歧化酶(superoxide dismutase,SOD)和丙二醛(malondialdehyde,MDA)水平,能促进溃疡创面血管生成和改善机体氧化应激反应[12]。本研究还显示,研究组术后1、3、5 d肛门疼痛VAS评分均低于常规组,术后4 周复查时研究组无肛门失禁发生,常规组出现7例肛门部分失禁,表明肛旁置管冲洗联合负压引流不仅满足疾病治疗的需要,而且有效减轻患者疼痛应激,保护肛门功能,更符合微创外科的手术理念和人文理念[13]。刘洁等[14]报道,肛旁置管冲洗联合负压引流能降低肛周脓肿血清肿瘤坏死因子-α (tumor necrosis factor α,TNF-α)、白介素-6(interleukin,IL-6),减轻脓肿部位的炎性反应损伤,为创面愈合创造有利条件。
肛旁置管冲洗联合负压引流有以下要点:(1)根据患者脓腔大小戳孔,若患者脓腔较大,可选择2~4个戳孔,排除脓液和清除坏死组织后,冲洗彻底,直至引流液清亮,避免创面感染。(2)负压封闭引流前,需对内口进行封闭和明胶海绵封堵处理,确保创面清洁。(3)保证负压引流的气密性,若发生漏气,要及时更换生物半透膜。
综上,肛旁微创置管冲洗联合负压引流是治疗肛周脓肿的有效术式,能充分缓解症状体征,减轻术后肛门疼痛和保护肛门生理功能,更符合现代微创外科理念的发展趋势。

