SARS-CoV-2基因组RNA标准物质的研制
王 迪, 王志栋, 吴 枭, 牛春艳, 董莲华, 戴新华, 高运华
(中国计量科学研究院前沿中心,北京100029)
1 引 言
当前新型冠状病毒(SARS-CoV-2)对全球公共卫生安全造成了严重的威胁[1~5]。这种传染病于2020年初被大量发现,我国科学家在短时间内从患者体内分离出SARS-CoV-2病毒并进行了基因组测序,于2020年1月12日向世卫组织提供其基因组序列信息[6,7]。研究发现该病毒为一种β属的冠状病毒,遗传物质为线性单股正链的RNA。SARS-CoV-2基因组序列结构显示该基因组约29~30 kb,由12个蛋白编码区/开放读码框组成,其基因特征与SARS-CoV和MERS-CoV有一定区别,与蝙蝠SARS样冠状病毒(bat-SL-CoVZC45)同源性约为80%[8,9]。
目前对SARS-CoV-2感染患者尚无特定的治疗方法,及时筛查、早期诊断是缓解病情和阻止疫情进一步扩散的关键[10~13]。以“荧光定量PCR”为代表的核酸检测方法因高灵敏度、高特异性成为新冠病毒诊断的“金标准”[14~16]。目前国内研发生产SARS-CoV-2核酸检测试剂的企业就有100家以上,检测的靶基因主要为ORF1ab和N基因。然而据报道,采取荧光定量PCR方法阳性检出率较低。正如王辰院士所说:“并不是所有的病患都能检测出核酸阳性”。尽管多个因素会影响最终的检测结果,如样本采集和保存、病毒变异、仪器性能和人员操作等,但部分SARS-CoV-2荧光定量PCR试剂的质量问题也很可能是造成“假阴性”的重要原因。因此研制定值准确、稳定可靠的新冠病毒标准物质,加强对相关核酸检测试剂的验证评价和实验室的质量控制尤为重要。
本标准物质基于灭活的人源SARS-CoV-2病毒的基因组RNA样本,通过数字PCR方法对E、ORF1ab和N基因拷贝数浓度值进行了确定,并进行了其均匀性和稳定性验证。该标准物质涵盖了新冠病毒所有特征基因的全部序列,已用于新型冠状病毒核酸检测方法开发、相关试剂验证评价以及检测实验室质量控制和测量结果的量值溯源等工作。
2 材料与方法
2.1 材料与试剂
候选物为人源高度纯化的SARS-CoV-2病毒基因组RNA,RNA保存液和酵母RNA购自美国Thermo Fisher公司,引物和探针合成自上海Invitrogen生物技术公司,一步法反转录数字PCR试剂盒(One-Step RT-ddPCR Advanced Kit for Probes)购自美国Biorad公司。
2.2 仪器与设备
QX200数字PCR仪,购自美国Biorad公司;Light Cycle ®480-II荧光定量PCR仪,购自德国Roche公司;ABI QuantStudio 12 K Flex荧光定量PCR仪,购自美国Thermo Fisher公司;台式离心机和Milli-Q Advantage纯水仪,购自德国Millipore公司;CP225D电子天平,购自Sartorius公司。
2.3 方法
2.3.1 数字PCR定值方法
引物及探针序列采用世界卫生组织(WHO)和中国疾病预防控制中心(CDC)公布的序列。对探针浓度及PCR扩增温度进行了筛选优化,确定的扩增条件如下:45 ℃ 10 min,95 ℃ 3 min;95 ℃ 15 s,58 ℃ 30 s,40个循环;98 ℃ 10 min。具体序列参考WHO和中国CDC公布的SARS-CoV-2荧光定量PCR检测推荐的序列,见表1。
2.3.2 标准物质制备
1)标准物质贮存溶液目标基因拷贝数浓度的初步确定
取1 μL基因组RNA贮存溶液,用RNA存储缓冲液,进行10×梯度稀释,用数字PCR方法进行初步检验,确定贮存溶液的初始浓度和稀释比例。

表1 数字PCR的引物和探针Tab.1 Primers and probes used for digital PCR
2)标准物质的配制
综合标准物质候选材料的数量、浓度、数字PCR方法的线性范围,以及与实时荧光定量PCR方法的匹配性等因素,确定配制约103copy/μL和 102copy/μL两个浓度梯度的标准物质。
取适量基因组RNA贮存溶液,加入设定比例数量的RNA存储缓冲液(内含约1 mg/mL的酵母RNA),在冰水浴中充分震荡,充分混合均匀,配制成设定浓度的标准物质。然后在生物安全柜中分装到0.5 mL无RNA酶的冻存管中,每管50 μL。
2.3.3 标准物质的均匀性检验
按照国家计量技术规范JJF 1343—2012《标准物质定值的通用原则及统计学原理》中对标准物质均匀性评估的技术要求,从标准物质分装的初期、中期、末期随机抽取10管SARS-CoV-2基因组RNA标准物质,选择最小取样量为5 μL,采用数字PCR方法进行均匀性测定。每瓶重复检测3次,并采用方差分析法(F检验)对标准物质进行均匀性检验[17]。
2.3.4 标准物质的稳定性考察
由于应急所需,此标准物质当前只开展了短期稳定性考察。储存温度为4 ℃,分别在第0日、1日、3日、5日取样。每次每个储存温度随机选取2个样本,每个样本重复测量3测,采用数字PCR方法检测E、ORF1ab、N三个基因的浓度。
将特性量值(Y)与时间(X)绘制曲线并拟合,拟合直线斜率b1和斜率的不确定度s(b1)分别为:
(1)
(2)
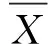
2.3.5 标准物质的定值
采用一步法反转录数字PCR方法对两种浓度标准物质进行定值。每种浓度标准物质抽取10个单元,每个单元取样5 μL,按照第2.2节中确定的检测方法分别对3种基因进行定量检测,每个单元重复测量3次。
3 结果与讨论
3.1 均匀性检验
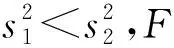
3.2 稳定性考察
按第2.3.4节中的方法,监测在4 ℃条件下标准物质E、ORF1ab和N基因浓度随时间的变化,来评价标准物质的短期稳定性,结果如图1。
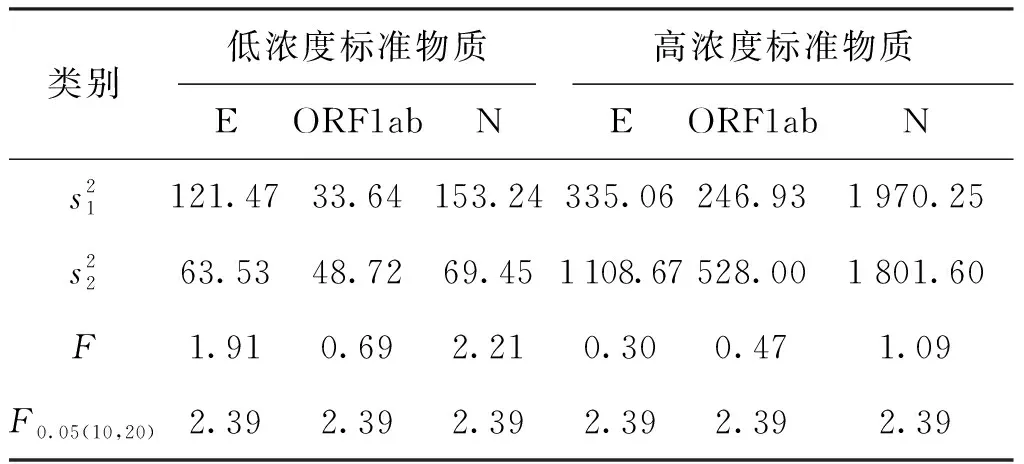
表2 两种标准物质均匀性检验Tab.2 Homogeneity of the two types of reference materials
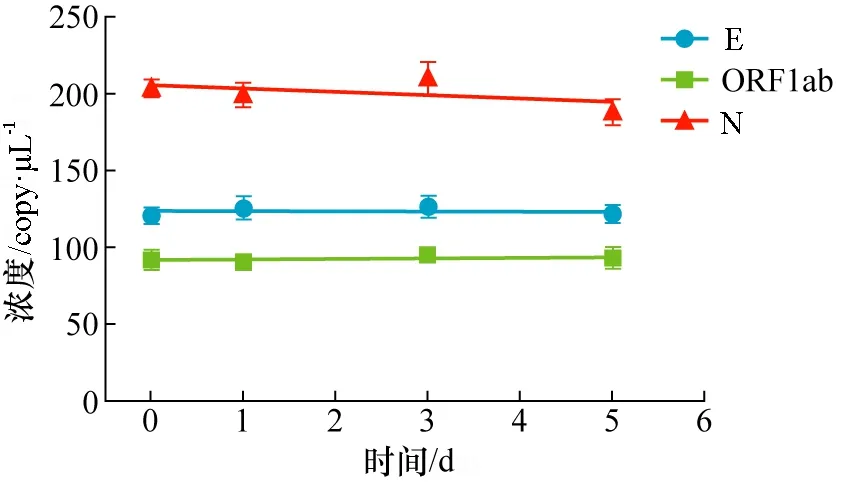
图1 标准物质的短期稳定性考察(4 ℃保存)Fig.1 Short-term stability of the reference material stored at 4 ℃
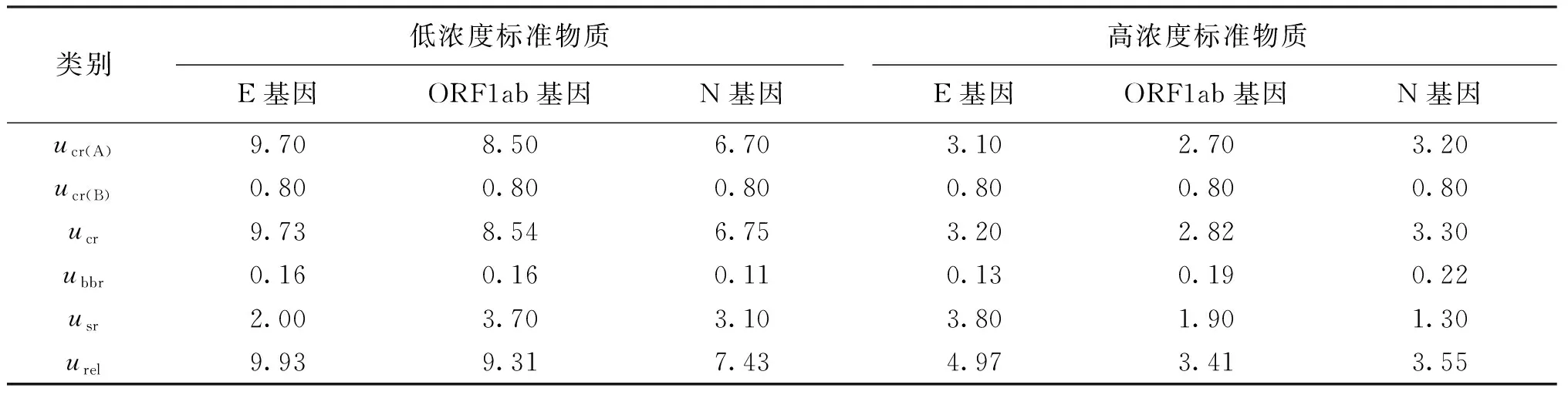
根据图1的拟合直线,计算斜率b1和s(b1),并查表得到置信水平0.95的t分布因子。结果如表3所示,3个基因均满足|b1| 表3 标准物质短期稳定性测试结果Tab.3 Short-term stability result of the reference material 由于应急所需,标准物质暂时未进行长期稳定性考察。但是根据CCQM P199 HIV-1 RNA比对中主导实验室提供的长期稳定性数据(可稳定保存8个月),可以预测本标准物质的稳定性,我们将会对该标准物质的长期稳定性持续进行监测。 按第2.3.1节中确定的检测方法,采用一步法逆转录数字PCR分别对E、ORF1ab和N基因进行定量检测。利用格拉布朗法和夏皮罗-威尔克法进行离群值检验和正态性分析后,所有定值数据均符合正态分布,定值数据没有异常值,数据均保留(见表4和表5),其中:SD表示标准偏差,RSD表示相对标准偏差。结果表明,在低浓度和高浓度标准物质中,3个基因的RNA浓度是不同的,其中N基因拷贝数最高,E基因居中,ORF1ab基因拷贝数最低。 表4 低浓度标准物质浓度的数字PCR定量结果 表5 高浓度标准物质浓度的数字PCR定值结果 标准物质定值结果的总不确定度由3个部分组成[18~20]。第1部分是标准物质定值方法的不确定度;第2部分是物质不均匀性所引起的标准不确定度;第3部分是物质在有效期内的不稳定性所引起的标准不确定度。表6为不确定度评定结果,合成相对标准不确定度为: (3) 式中:ucr为标准物质定值方法的相对不确定度;ubbr为物质不均匀性所引起的相对不确定度;usr为物质在有效期内的不稳定性所引起的相对不确定度。 (1)定值方法的不确定度包括了A类不确定度和B类不确定度。根据2种标准物质定值结果数据和测量次数,计算出每个标准物质的A类不确定度ucr(A);B类不确定度ucr(B)主要是仪器采集荧光信号时产生的不确定度(因仪器按照规定定期维护,该项忽略不计)和微滴体积引入的不确定度(0.8% )[21,22]。 (2)均匀性检验结果表明,标准物质在管间具有良好的均匀性。标准物质拷贝数值这一特性量值的均匀性引入的不确定度采用式(4)进行计算: (4) 式中ν为组内自由度。 (3)拷贝数浓度稳定性的不确定度贡献采用公式:us=s(b1)·X进行计算。 表6 不确定度评定Tab.6 Evaluation of measurement uncertainty (%) 全国标准物质管理委员会组织技术专家对研制的标准物质进行了技术评审,并报送国家市场监管总局批准,获得了国家标准物质证书,编号分别为GBW(E)091098和GBW(E)091099。 应用研制的标准物质,先后完成了对9种SARS-CoV-2病毒qRT-PCR检测试剂盒的性能评价。结果表明尽管不同试剂盒选择的靶基因检测区段存在差异,但以该标准物质为模板,这9种检测试剂盒均能扩增产生目标核酸片段,成功完成了性能评价工作。这说明该基因组RNA标准物质具有普遍适用性,可广泛应用于各类新冠相关核酸检测方法的开发,试剂的验证评价以及检测实验室的质量控制。这9种试剂盒的信息见表7。 针对新型冠状病毒标准物质缺乏的现状,研制了高低2种水平的新冠病毒基因组RNA标准物质。该标准物质具有新冠病毒完整的核酸序列,对不同核酸检测试剂盒具有普遍的适用性。利用研制的标准物质对9种SARS-CoV-2荧光定量PCR检测试剂盒的性能进行评价,证实了标准物质的适用性良好。同时研制的标准物质为新型冠状病毒核酸检测方法的开发、实验室质量控制以及测量结果的量值溯源等提供了重要的标准和计量技术支撑,为新型冠状病毒的检测奠定了一定的技术基础。 表7 qRT-PCR试剂盒信息Tab.7 qRT-PCR kit information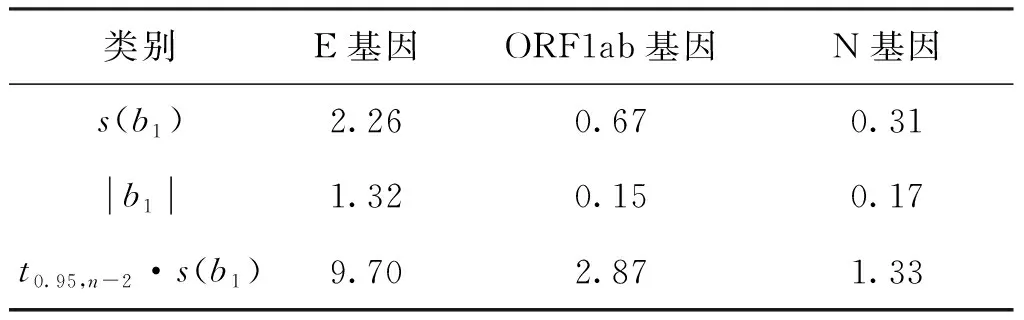
3.3 标准物质的定值
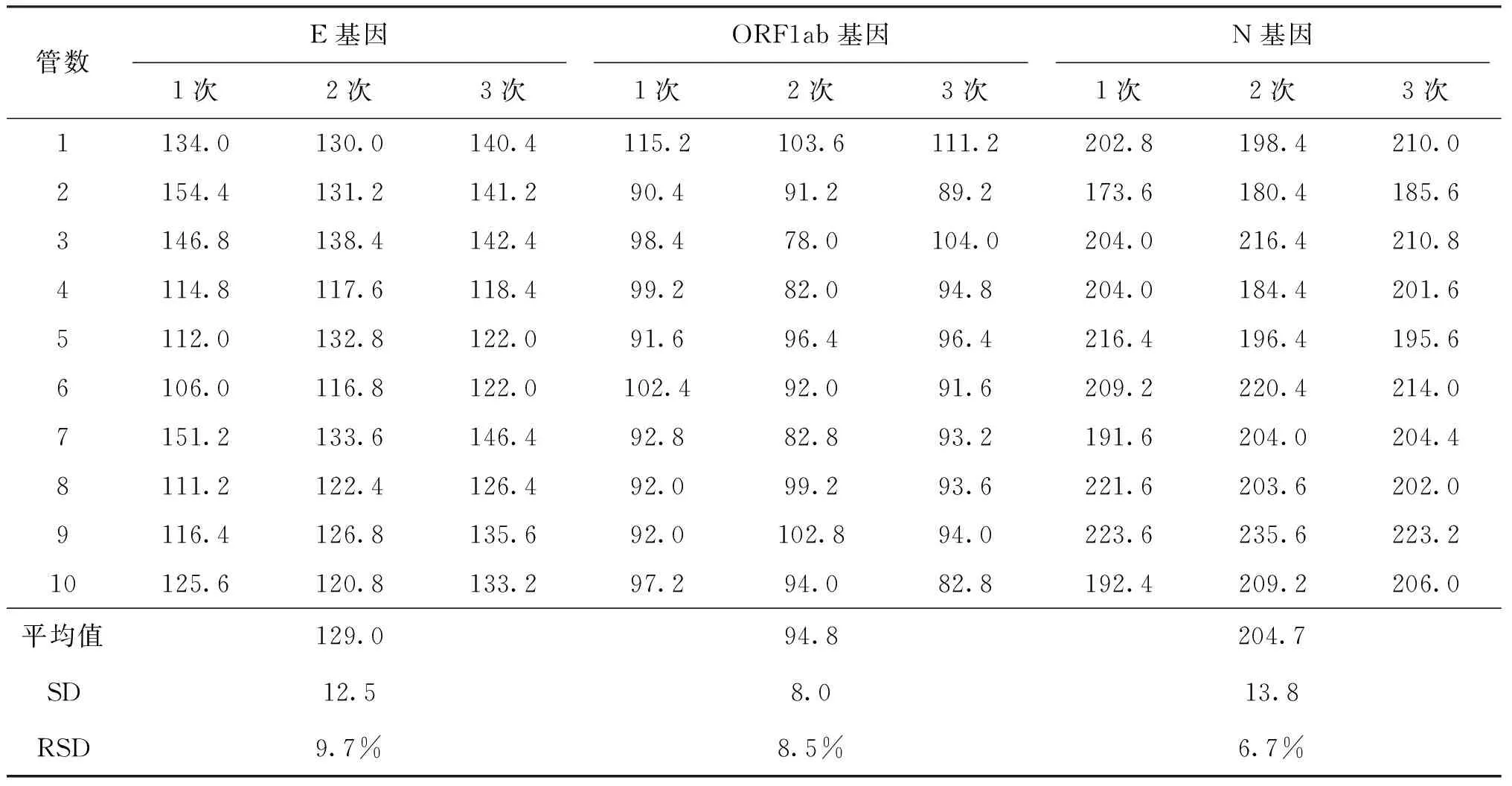
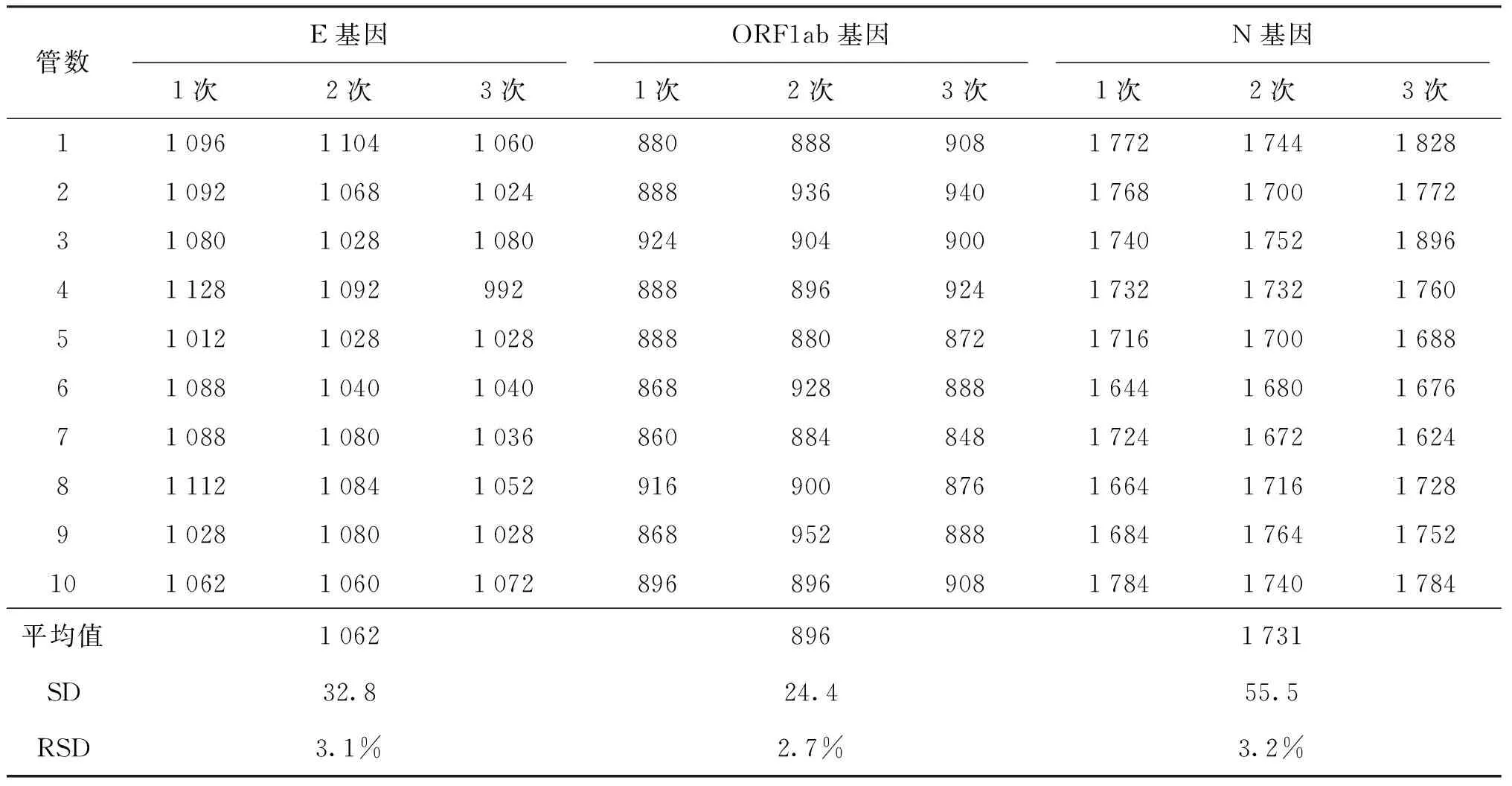
3.4 定值结果的不确定度评定
3.5 标准物质评审和应用
4 结 论