高龄高血压患者降压治疗的相关问题
安子玉 梁颖慧 秦明照
(1.首都医科大学第四临床医学院,北京100176;2.首都医科大学附属北京同仁医院老年医学科,北京100730)
高血压是心脑血管疾病重要的危险因素之一。随着人口老龄化程度的加重,年龄≥80岁高龄高血压患者比例增高。高龄高血压患者常伴有脑卒中、心力衰竭、肾衰竭和动脉粥样硬化性心血管疾病等并发症,是高龄患者的常见死亡原因之一。中国高龄老人高血压患病率为56.5%,而控制率为11.5%[1]。因此高龄高血压患者的降压治疗相关问题应得到社会的普遍关注。
高龄高血压患者以收缩压(SBP)升高为主,舒张压(DBP)不高甚至偏低,脉压增大;血压波动大;体位性低血压多见;并存多种心血管危险因素,靶器官损害和并发症多;常合并认知障碍、衰弱和多重用药;在合并疾病期状态,如盐和水摄入不足,更易出现容量衰竭,给高血压治疗带来困难[2]。在高龄高血压患者的治疗中,应充分考虑其特殊性。现就80岁以上高龄老年人的高血压降压治疗相关问题进行综述。
1 高龄老人的降压目标
高血压指南为高血压患者的诊断和治疗管理提供了重要依据。JNC 8[3]提出了新的降压目标,推荐年龄>60岁无糖尿病或慢性肾脏病的老年人降压目标为<150/90 mm Hg(1 mm Hg=0.133 3 kPa)。此前JNC 7的降压目标140/90 mm Hg已被普遍接受,所以当JNC 8设定更高的血压目标时,受到很多质疑。但此后各国发表的高血压指南中,高龄老人主流降压目标为<150/90 mm Hg。对于近年来高血压指南中所规定的老年及高龄老人的降压目标,总结于表1。
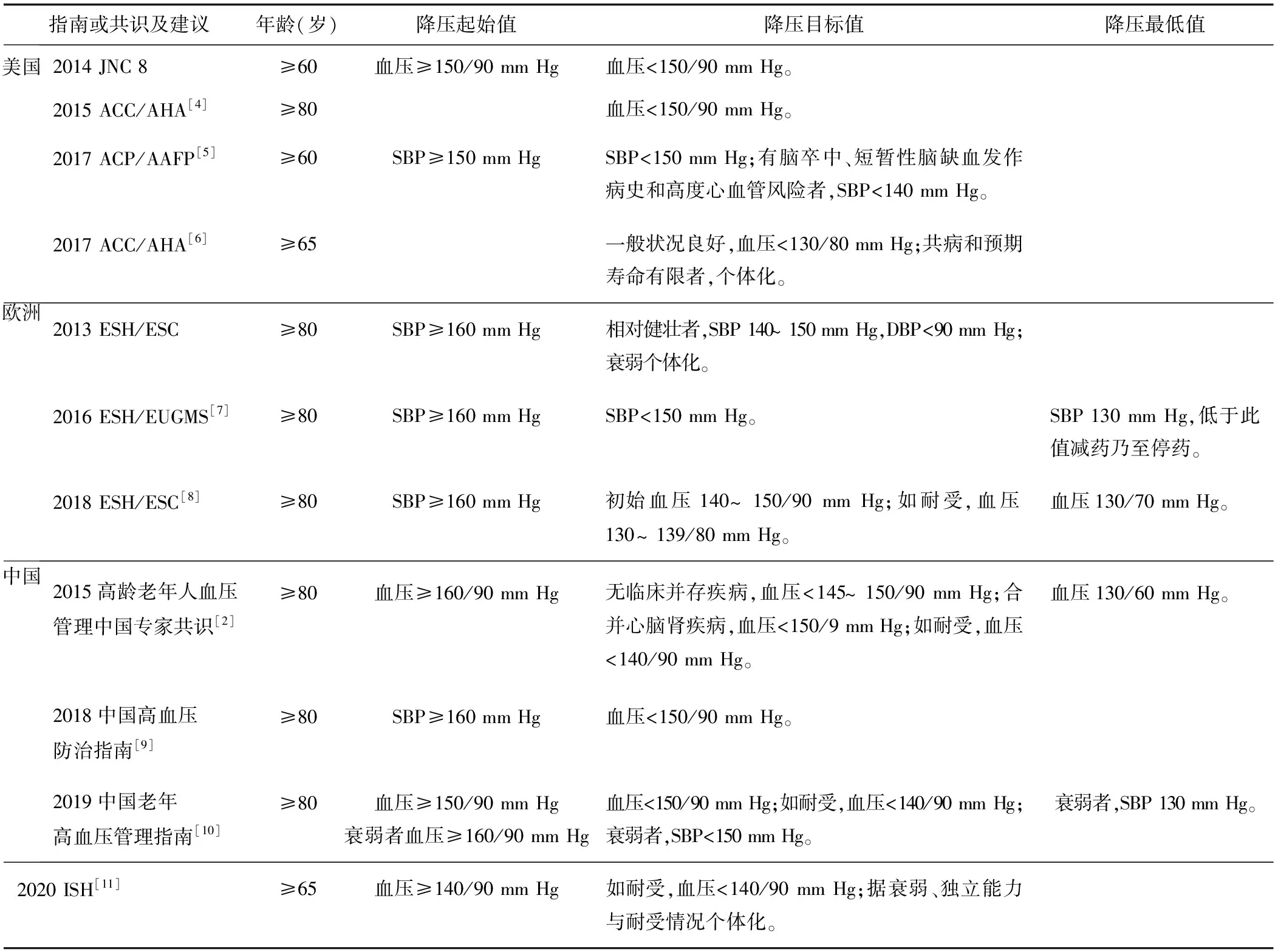
表1 国际及中国高血压指南共识——老年高血压降压目标
有人担心在老年人中更宽松的血压目标可能导致一些患者失去最佳治疗机会,但综合各国指南,虽然数值略有差异,但大多初始目标为血压<150/90 mm Hg,如可耐受进一步控制血压<140/90 mm Hg。中国2019年老年人血压管理指南[9]强调对于老年单纯收缩期高血压患者,当DBP<60 mm Hg,而SBP<150 mm Hg时,可先观察暂不用药物治疗;SBP为150~179 mm Hg时,可谨慎给予小剂量抗高血压药;如SBP≥180 mm Hg,需用抗高血压药。
高龄高血压降压目标是基于降压治疗随机对照试验结合流行病学观察研究及相关系统回顾和荟萃分析的结果来设立的,2016年美国收缩压干预试验(SPRINT)中,年龄≥75岁的老年人亚组分析[12]起到了关键性作用,但到目前为止各个研究结果并不一致,高龄老年高血压降压目标仍存在一些争议,还需进一步临床研究[13]。
2 高龄老人降压获益与风险
高龄老人患高血压后不经过及时治疗,心血管疾病的风险会有所增加[14],可能会产生一系列并发症。2018年中国老年健康影响因素跟踪调查结果显示,高龄老人中SBP为129 mm Hg的人群死亡风险最低,当SBP>154 mm Hg或<107 mm Hg时,全因死亡风险都会增高[15]。2020年英国一项前瞻性观察研究发现:SBP≥150 mm Hg时心血管疾病风险增加;血压140~160/80~90 mm Hg时全因死亡率最低,血压<130/80 mm Hg时全因死亡率增加62%;75岁以上衰弱老人及85岁以上的老人中,高血压反而与低死亡率相关[16]。因此高龄高血压患者降压治疗的获益与风险值得探讨。
SPRINT研究中,年龄≥75岁的老年人亚组分析发现,强化降压组(平均血压123/62 mm Hg)与标准降压组(平均血压135/67 mm Hg)相比,主要终点事件降低34%,心力衰竭风险下降38%,心血管死亡风险下降43%,全因死亡风险下降33%,总体不良反应及主观生活质量未观察到显著差异[12,17]。SPRINT研究表明其强化治疗血压值可能相当于传统诊室SBP<140 mm Hg[18]。但在该研究中强化治疗可能会导致急性肾损伤的风险增加[12-13],不过大多数急性肾损伤为轻度,随访追踪显示,大多数患者肾功能可完全恢复[19]。
但有不少的观察性研究表明,降压治疗中较低血压水平(SBP<130~140 mm Hg)可能导致死亡风险增加[20-21]。高龄人群血压和动脉僵硬度的预测价值研究发现在应用≥2种抗高血压药且SBP<130 mm Hg的患者,全因死亡相对风险为SBP>130 mm Hg的患者2倍[20],还有研究提示90岁老年高血压患者接受抗高血压药治疗较未治疗的病死率要高[22]。对高龄老人来说,严重伤害对死亡率和功能的影响与心血管事件相当,也有研究表明低DBP和脉压升高与老年高血压患者跌倒损伤的风险增加有关[23]。
关于认知方面,有观察性研究表明在年龄>60岁的群体中,SBP升高与痴呆无相关性[24],而较低的血压水平会加速高龄老人认知功能下降和加重痴呆的程度[25],因此降压治疗有可能增加相应风险。但随机对照试验的事后分析中,SPRINT高龄亚组强化降压治疗与标准治疗比较,虽未减少痴呆风险,但轻度认知功能障碍风险下降30%[17]。
随机对照与观察性研究结果之间存在差异,观察性研究中血压与不良事件、降压治疗与获益呈J型或U型曲线,甚至是反向关系,可能有以下原因:(1)随机对照试验对象较观察性研究对象相对健康,共病少[12]。(2)随机对照研究可能因获益而提前终结,可能夸大获益而低估风险。随机对照研究对受试者衰弱和认知状态等因素的建议往往取决于事后分析,证据强度不足。(3)存在不良健康状况的高龄老人常有广泛的动脉硬化基础,重要器官的血流灌注及自主调节功能障碍已较为显著,血压水平较低时可能导致灌注不足,一定程度的高血压是维持灌注的代偿机制[25]。(4)观察性研究中低血压与不良事件的关联一方面可能被其他因素混淆,另一方面可能存在反向因果关系。有研究表明,高龄患者的血压在死亡前2~3年有较明显的下降趋势,且与抗高血压药无关,这种情况下低血压可能是与衰弱相关的营养不良、体重减轻和心力衰竭等潜在合并症有关的风险指标,而不是不良事件的直接原因[26]。
3 衰弱高龄群体的降压治疗
高龄老人中,有部分人呈现衰弱状态。中国的高龄高血压患者有32.0%属于衰弱状态[27]。衰弱提示老年人生理年龄升高[21],它是多个生理系统累积衰退的结果。
观察性研究发现在衰弱高龄患者中,低血压(SBP<120~130 mm Hg或DBP<70 mm Hg)与主要心血管事件和死亡风险增加相关[16,26,28]。甚至有研究证明高龄患者中,传统心血管危险因素与高龄研究对象的死亡率无关,衰弱是此年龄组死亡的一个重要危险因素[29]。衰弱患者降压治疗可能不能获益,反而增加治疗相关风险,老年高血压患者并存衰弱者降压治疗依从性更差[30]。
虽然HYVET[31]和SPRINT[12]研究运用衰弱指数对受试者进行评估和事后分析,得出的结论是衰弱不影响降压治疗甚至是强化降压治疗的益处。但这些研究中衰弱患者多为轻度衰弱,中度衰弱有限,严重衰弱者很少[32],研究结果难以推及到中重度衰弱患者[33]。在SPRINT研究中衰弱与较高的晕厥、低血压以及跌倒风险相关[34]。
上述结果提示评估高龄老年人衰弱状态对血压管理的重要性。在为高龄老人治疗前,应尽可能准确地了解患者的功能和认知状况,用快速可行的方法对衰弱状态进行分层,识别纠正易诱发低血压发作的因素。医师应谨慎治疗,必要的情况下使用低剂量和单一药物,并严密监测治疗效果[8]。但高龄衰弱患者临床研究数据相对缺乏,无相对明确的分层标准,仍需进一步应用多种筛查进行评估,寻找简单、准确和可靠的方法来检测高龄老年人的生理年龄[35]。中国高龄老年人血压管理中国专家共识推荐制定降压方案前,对1年内非刻意节食情况下体重下降>5%或有跌倒风险的高龄老年高血压患者进行衰弱评估。衰弱筛查推荐采用FRAIL量表或步速测定,如有条件可进一步采用Fried衰弱综合征标准进行评估,以确定是否适合降压治疗[2,11]。
衰弱老年人降压目标应与普通高血压患者有所不同,但因缺乏直接随机对照研究的证据,合适的降压目标值尚不清楚。有学者建议,高龄高血压患者SBP≥160 mm Hg时应考虑开始治疗。如患者严重衰弱,目标SBP为160~190 mm Hg也可能合理[36]。如果联合降压治疗,SBP不应<130 mm Hg,否则应减药甚至停药。有研究[37]表明减药或停药与继续用药比较,血压有不同程度回升,而衰弱、认知、心肌梗死和全因死亡率等无明显差异,但这些研究都是短期和小规模研究,事件发生率低,研究证据强度低或极低。
总之,治疗高血压以防止心血管并发症和死亡是合理的,但高龄人群存在较大异质性,降压治疗的目标、获益和风险、衰弱和血压之间的关系等暂时还不能得出准确答案。未来研究需考虑如何更多和安全地纳入具有降压治疗获益风险不确定性人群,如衰弱、认知功能减退、共病和多重用药的高龄老年患者,或通过有价值的真实世界研究,以寻找管理高龄高血压患者最适合的策略。

