胶原多肽对白酒中4 种醛类物质的反应机理
刘 娴,黄张君,李 霞,廖学品,石 碧
(四川大学轻工科学与工程学院,皮革化学与工程教育部重点实验室,四川 成都 610065)
中国白酒是以粮谷为原料,酒曲为糖化发酵剂,经过固态、半固态或糖化发酵而成的蒸馏酒[1]。决定白酒风格和特征的微量成分占2%,目前已有超过2 000 种微量成分被检测出来,其中包括醛类、酯类、醇类、杂环类、萜烯类、芳香类、酮类、含氮化合物、酸类、硫类、缩醛类和内酯类[2]。
白酒发展的导向是健康与风味,2016年孙宝国团队首次提出健康白酒可以通过“内寻外加,自然强化”实现[3]。随着检测技术的发展,白酒中多种健康成分已成功实现了分离鉴定[4-6]。江南大学已经从白酒中检测出非挥发性脂肽类化合物地衣素和多肽,证实它们具有抗癌、抗病毒、溶纤、抑菌活性以及对白酒中挥发性成分具有选择性抑制作用[7-10]。而胶原多肽由于具有抗氧化、能够预防动脉硬化、抗衰老易吸收等作用,已被广泛应用于食品和化妆品行业[11]。白酒体系中适量的醛类挥发性成分可协调白酒的香气释放,但醛类物质过量便会导致白酒入口粗糙、口感不佳甚至产生刺喉的感受[12],其中,糠醛能够赋予白酒异香,但浓度过大时会呈现严重的辣味甚至焦苦味[13]。因此,胶原多肽与白酒体系中醛类物质的作用机理研究将为健康白酒的发展提供理论依据。
本实验以模拟白酒体系为研究对象,通过紫外光谱、荧光光谱以及三维荧光光谱研究了胶原多肽与白酒中糠醛、苯甲醛、乙醛、异戊醛的相互作用,并提出了它们之间的反应机制。然后通过顶空固相微萃取-气相色谱-质谱(headspace solid-phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)技术分析胶原多肽对浓香型白酒中醛类物质含量的影响,揭示胶原多肽对白酒中挥发性成分及醛类物质的影响规律。
1 材料与方法
1.1 材料与试剂
胶原多肽为实验室自制,平均分子质量3 000 Da;糠醛、异戊醛、乙醛、苯甲醛、正辛酸甲酯(以上均为色谱级,≥99.0%) 上海阿拉丁试剂有限公司;无水乙醇(色谱纯) 成都天润化工有限公司;浓香型白酒四川某酒业;纯水为实验室自制超纯水。
胶原多肽储备液:将0.4 g胶原多肽加入200.0 mL 52%(V/V)乙醇溶液中,配制成质量浓度2.0 g/L的胶原多肽储备液;醛类物质储备液:将糠醛、苯甲醛、乙醛和异戊醛分别用52%乙醇溶液稀释成2.0、2.0、10.0、10.0 g/L的储备液,于4.0 ℃低温贮藏备用。
1.2 仪器与设备
Lumina型荧光光度计、TSQ 9000 GC-MS/MS仪赛默飞世尔科技有限公司;UV-1800BPC紫外-可见分光光度计 上海美普达仪器有限公司;ZWY-2102C温控回旋立式双层振荡器 上海智城分析仪器制造有限公司;75 μm CAR/PDMS固相微萃取头 美国色谱科公司;VF-WAX ms(30 m×0.25 mm,0.25 μm)毛细管色谱柱美国安捷伦公司。
1.3 方法
1.3.1 紫外光谱分析
参考吴继红[9]的方法略有修改,将不同质量浓度的糠醛、苯甲醛、乙醛、异戊醛和固定质量浓度(10.0 mg/L)的胶原多肽于309 K反应1.0 h后,利用紫外-可见分光光度计对样品进行测定,紫外光谱的扫描范围为波长190~300 nm。
1.3.2 荧光光谱分析
参考饶震红等[14]的方法略有修改,在若干支50 mL比色管中分别加入5.0 mL胶原多肽储备液,将不同质量浓度的4 种醛类物质分别加入上述胶原多肽溶液中,配制得到一系列质量浓度梯度的混合溶液。将上述溶液充分混合并在3 种不同温度(293、301 K和309 K)反应1.0 h并进行荧光光谱分析。其中,激发波长设置为276 nm,发射波长为280~450 nm,激发和发射的狭缝宽度均为5.0 nm。
1.3.3 荧光猝灭机制的确定
为了研究糠醛、苯甲醛、乙醛和异戊醛对胶原多肽的猝灭机制,分别在293、301、309 K反应1.0 h后,通过Stern-Volmer方程[15]计算猝灭常数Ksv:

式中:F0和F为未添加猝灭剂和添加猝灭剂时的荧光强度;Ksv为猝灭常数;[Q]为猝灭剂的浓度;Kq为双分子猝灭过程速率常数;τ0为无猝灭剂时大分子的平均荧光寿命(10-8s)。
胶原多肽与醛类物质结合常数和结合位点数可以由双对数方程[16]计算:

式中:F0和F为未添加猝灭剂和添加猝灭剂时的荧光强度;Ka为结合常数;[Q]为猝灭剂的浓度;n为结合位点数。
1.3.4 相互作用力的确定
由Van’t Hoff公式[17]可以计算出反应熵变ΔS和焓变ΔH:

由式(2)~(4)可计算出结合常数Ka及结合位点数n,以及相互结合的热力学参数。
1.3.5 三维荧光光谱分析
分别取5.0 mL胶原多肽储备液于50 mL比色管中,固定胶原多肽含量,分别加入糠醛、异戊醛、乙醛和苯甲醛储备液,配制得到醛类物质的浓度分别为0.026 0、0.188 5 mmol/L和36.322 4 mmol/L,然后于309 K反应1.0 h后取适量的溶液于1.0 cm的石英比色皿内,在激发波长260~380 nm(增量为1.0 nm)、发射波长230~320 nm(增量5.0 nm)的条件下进行三维荧光分析,得到三维荧光光谱。
1.3.6 HS-SPME-GC-MS分析
将一定含量的胶原多肽加入250 mL浓香型白酒中,配制得到胶原多肽质量浓度分别为0.0、2.0、20.0、200.0 mg/L,25 ℃放置12 h后分析白酒成分。
HS-SPME条件:根据文献[9],将酒样酒度稀释成10%,取8 mL稀释后的酒样于20 mL顶空瓶中,每个样品瓶加入10 μL内标(正辛酸甲酯,最终质量浓度为0.093 8 mg/L),将样品瓶在35 ℃平衡10 min,并在35 ℃萃取45 min,搅拌速率500 r/min,每个样品重复萃取3 次。
GC条件:进样口温度270 ℃,载气为He,分流比为20∶1,升温程序:初始温度40 ℃,保持5 min,以4 ℃/min的速率升至100 ℃,再以6 ℃/min的速率升至230 ℃,保持10 min。
MS条件:采用电子电离源,电离能量为70 eV;离子源温度300 ℃;扫描范围m/z35~400;溶剂延迟时间3.50 min。
1.4 数据分析
所有实验重复3 次,采用Microsoft Office Excel 2010对实验所得数据进行处理及Origin 2018软件作图。
2 结果与分析
2.1 紫外光谱分析
紫外-可见吸收光谱能够简单、快速、有效地测定复合物的形成。当小分子化合物与蛋白质发生相互作用时,其紫外光谱图中吸收峰会产生明显变化[18]。本研究中,胶原多肽在波长198 nm处存在最大吸收峰,其与胶原多肽链上—C=O的n—π*跃迁有关[14]。

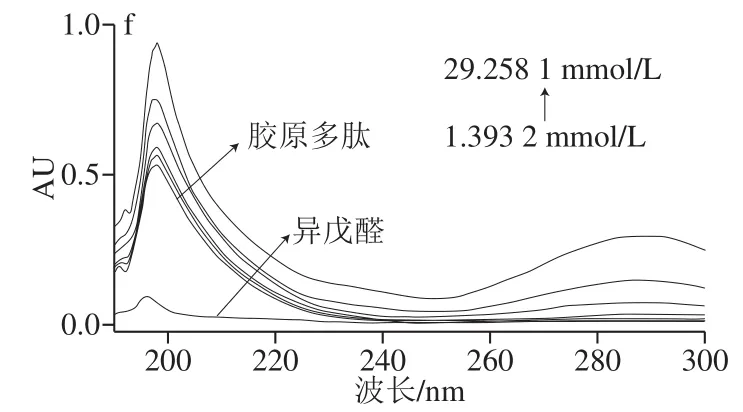
图 1 胶原多肽与不同浓度糠醛(a)、苯甲醛(b)、乙醛(c、d)和异戊醛(e、f)的紫外光谱图Fig. 1 UV absorption spectra of collagen peptide in the presence of different concentrations of furfural (a), benzaldehyde (b), acetaldehyde (c, d),and isovaleraldehyde (e, f)
如图1a、b所示,随着糠醛和苯甲醛浓度的逐渐升高,混合溶液在198 nm波长处的吸收峰均呈现增强现象。在糠醛-胶原多肽体系中,糠醛在224 nm波长处的峰随着糠醛浓度的增加产生红移现象;而在苯甲醛-胶原多肽体系中,苯甲醛浓度的升高使胶原多肽在198 nm波长处的吸收峰有明显红移的现象。上述结果表明,糠醛和苯甲醛这两种醛类物质能与胶原多肽产生相互作用[19]。在图1c、e中,当乙醛和异戊醛浓度较低时,紫外吸收峰未产生明显变化,说明低浓度的乙醛和异戊醛与胶原多肽未发生相互作用。继续增加乙醛和异戊醛浓度,如图1d、f所示,胶原多肽在198 nm波长处的吸收峰强度逐渐增大,并且乙醛-胶原多肽体系在280 nm波长左右和异戊醛-胶原多肽体系在290 nm波长左右出现一个新的吸收峰,且该吸收峰的强度也随着乙醛和异戊醛浓度的增加呈明显增强趋势,说明当乙醛和异戊醛的浓度较高时,能与胶原多肽发生反应并形成复合物。可能是胶原多肽的氨基与醛基反应生成—C=N—席夫碱结构,其反应机理如图2所示,通常生成席夫碱的反应是一个可逆反应,稳定性差,但由于芳香族醛具有一定的疏水性,能够与胶原多肽以疏水键结合,因此芳香族席夫碱比脂肪族席夫碱更稳定[20]。因此,糠醛与苯甲醛更容易与胶原多肽发生反应,而乙醛和异戊醛只有浓度较高时,才能与胶原多肽形成复合物,从而在紫外光谱中表现出明显的差异。白酒中乙醛浓度仅在3.405 2~6.810 4 mmol/L之间,异戊醛浓度范围鲜有报道,但应该远少于白酒中乙醛的浓度[13],所以在白酒中加入的胶原多肽基本上不会与乙醛和异戊醛进行反应。

图 2 醛-胶原多肽反应机理Fig. 2 Reaction mechanism between aldehydes and collagen peptide
普遍认为糠醛是白酒中的苦味物质之一[21],本研究表明白酒中加入胶原多肽可与糠醛结合,从而降低白酒的苦味。另一方面,胶原多肽中含有多种对人体有益的活性肽[22]。因此,在白酒中加入胶原多肽不仅可以减少苦味,还具有一定的保健功能。
2.2 荧光光谱分析
2.2.1 荧光猝灭光谱
荧光光谱能够反应小分子化合物和蛋白质之间结合环境的变化,因此被广泛应用于蛋白质与小分子之间相互作用的研究[23]。胶原多肽中主要由酪氨酸残基产生荧光。由图3可知,随着糠醛、苯甲醛、乙醛和异戊醛4 种醛类物质浓度的增加,胶原多肽的荧光产生明显的猝灭现象,但未出现红移或蓝移。

图 3 胶原多肽与不同浓度醛类的荧光光谱Fig. 3 Fluorescence spectra of collagen peptide with different concentrations of aldehyde
荧光猝灭分为静态猝灭、动态猝灭及动态静态结合猝灭。这些猝灭机制可以通过猝灭常数随温度变化和荧光寿命的变化进行区分。动态猝灭是猝灭剂分子与荧光分子的激发态分子之间产生相互碰撞而导致的荧光猝灭,温度越高,猝灭常数越大,故猝灭常数与温度变化呈正比。静态猝灭是猝灭剂分子与荧光分子在基态时生成不发荧光的复合物,其中,猝灭常数随着温度的升高而降低。动态静态结合猝灭是由于同一荧光基团受到碰撞和形成复合物而导致的,可以根据猝灭剂浓度的大小和变化趋势进行判断[24-25]。

表 1 胶原多肽分别与糠醛、苯甲醛、乙醛和异戊醛相互作用的Stern-Volmer常数Table 1 Stern-Volmer constants for the interactions of collagen peptide with furfural, benzaldehyde, acetaldehyde and isovaleraldehyde
由表1可知,当猝灭剂为糠醛和苯甲醛时,猝灭常数随着温度增高而降低,且Kq均远大于2×1010L/(mol·s),说明发生的是静态猝灭,胶原多肽与糠醛和苯甲醛生成了复合物[26]。当猝灭剂为异戊醛和乙醛时,猝灭常数随着温度升高而升高,且Kq均小于2×1010L/(mol·s),说明在此浓度范围内发生动态猝灭,乙醛和异戊醛与胶原多肽未形成复合物[27]。
2.2.2 相互结合的作用力分析
通过荧光实验结果分析可知,当猝灭剂为糠醛和苯甲醛时,胶原多肽与其结合形成了复合物。因此,本研究通过热力学计算对它们之间的结合作用力进一步分析。由图4可见,双对数方程拟合结果具有良好的线性关系,可由此得到结合常数Ka及结合位点数n。由表2可见,不同温度下苯甲醛与胶原多肽以及糠醛与胶原多肽的结合位点数约为1[17]。
大分子化合物和小分子化合物的结合力主要有4 种,分别为氢键、范德华力、疏水作用力、静电作用力。根据热力学规律可知,当ΔS<0和ΔH<0时,主要是氢键和范德华力;当ΔS<0和ΔH>0时,主要为静电作用力;当ΔS>0和ΔH>0时,主要为疏水作用力[28]。由表2可见,糠醛-胶原多肽体系和苯甲醛-胶原多肽体系的ΔG<0,且随着温度的升高而降低,说明糠醛和苯甲醛与胶原多肽的反应都是自发进行的。熵变与焓变均大于0,说明它们之间主要以疏水作用力相结合[29],这与紫外光谱的分析结果一致。
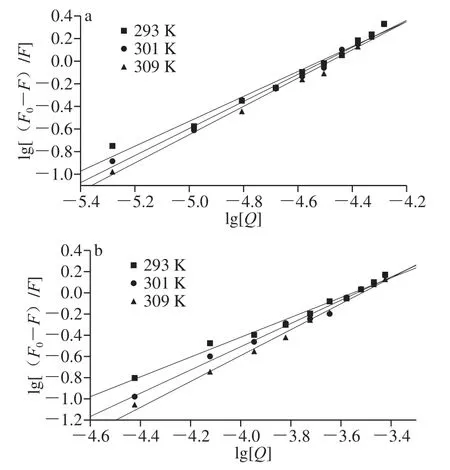
图 4 糠醛与胶原多肽混合体系(a)、苯甲醛与胶原多肽混合体系(b)在不同温度下的双对数方程Fig. 4 Double logarithmic plots for furfural-collagen peptide (a) and benzaldehyde-collagen peptide (b) at various temperatures
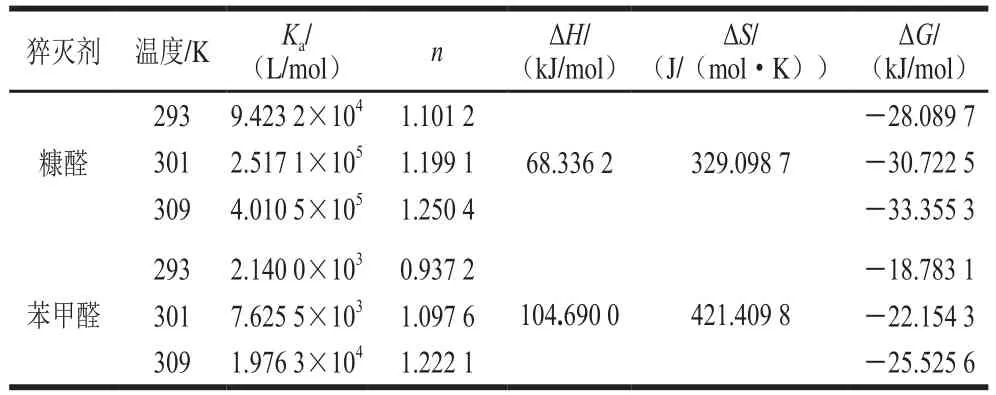
表 2 胶原多肽与糠醛和苯甲醛结合形成分子复合物的结合常数、结合位点数和热力学参数Table 2 Binding constants, number of binding sites and thermodynamic parameters of molecular complexes formed by the interactions of collagen peptide with furfural and benzaldehyde
2.3 三维荧光光谱
三维荧光可以更为直观地描述被测物质的荧光变化信息[30]。图5为胶原多肽中加入低(0.026 0 mmol/L)、中(0.188 5 mmol/L)和高(36.322 4 mmol/L)3 个浓度的糠醛、苯甲醛、乙醛和异戊醛前后的荧光变化等高线谱图,图中A(λem=λex)代表瑞利散射峰,Peak 1代表胶原多肽中酪氨酸残基特征荧光峰[31]。比较图5a~d,随着醛的加入Peak 1的荧光强度均有减弱的现象,说明它们之间能够发生相互作用。当糠醛浓度仅为0.026 0 mmol/L时,即可看到明显的荧光猝灭;当苯甲醛浓度为0.188 5 mmol/L时,能看到明显的荧光猝灭;当乙醛和异戊醛浓度高达36.322 4 mmol/L才可看到明显的荧光猝灭。因此,这4 种醛类物质对胶原多肽相互作用强弱顺序为:糠醛>苯甲醛>异戊醛>乙醛。三维荧光的分析结果进一步证明,胶原多肽能够与糠醛和苯甲醛发生明显的相互作用,而乙醛和异戊醛只有在高浓度下才可能与胶原多肽发生相互作用。
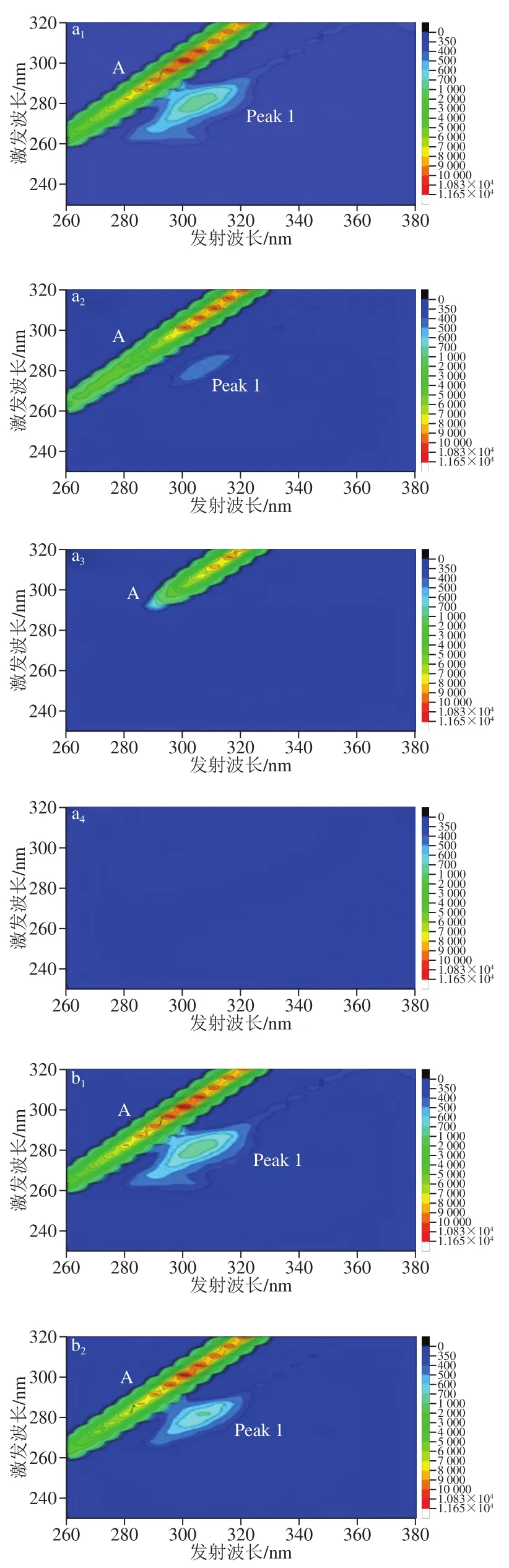
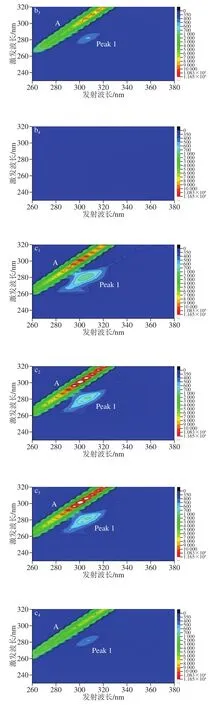
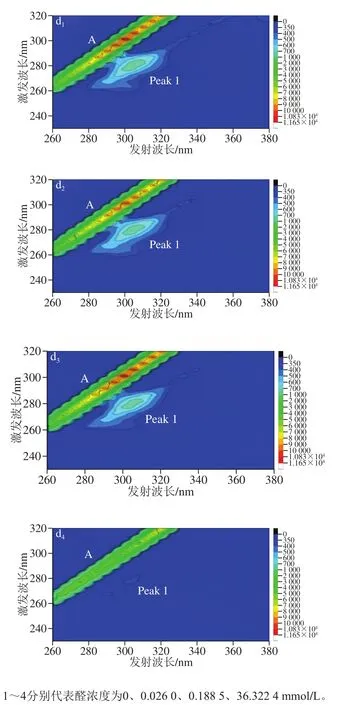
图 5 胶原多肽-醛溶液体系的三维荧光光谱Fig. 5 Three-dimensional fluorescence contour spectra of collagen peptide-aldehydes
2.4 胶原多肽影响白酒中挥发性成分的HS-SPME-GCMS分析结果
本研究目的主要是考虑健康酒即配制酒。模拟体系组成单一,能够准确的阐明反应过程;而真实白酒体系太过复杂,干扰因素太多,难于准确揭示胶原多肽与醛的反应机理,而发酵白酒中这几种醛是存在的,只是不同的发酵条件下含量不同而已[1]。因此,本实验在模拟体系的基础上,将不同含量的胶原多肽加入浓香型白酒中,采用HS-SPME-GC-MS分析技术定性和内标法定量,用真实体系验证上述模拟体系所得出的结果。
对实际的白酒体系,采用HS-SPME-GC-MS分析共定性出30 种挥发性物质,其中22 种酯类化合物、3 种醛类化合物、1 种醇类化合物、2 种烷烃类、1 种酸类和1 种酚类化合物。加入胶原多肽后,白酒中挥发性成分含量均有不同程度的降低。其中醛类化合物含量降低较为明显,当加入的胶原多肽质量浓度为200.0 mg/L时,3-糠醛的质量浓度从0.179 9 mg/L降低至0.144 6 mg/L,苯甲醛的质量浓度从0.506 8 mg/L降低至0.350 4 mg/L,这表明胶原多肽能够与醛类物质发生相互作用。
3 结 论
本实验通过建立模拟白酒体系,利用紫外光谱、荧光光谱和三维荧光光谱研究胶原多肽对糠醛、苯甲醛、乙醛和异戊醛的相互作用,并使用HS-SPME-GC-MS技术分析胶原多肽对实际的清香型白酒挥发性成分的影响。研究发现,胶原多肽与糠醛和苯甲醛之间以疏水作用力形成复合物,且温度越高,疏水键作用越强;胶原多肽与低浓度的乙醛和异戊醛作用力较弱,但在高浓度下可观察到明显的相互作用;胶原多肽能够显著降低实际白酒中醛类物质含量。上述研究将为健康白酒以及配制酒的发展提供理论依据。

