意大利蜜蜂同日龄不同职能工蜂上颚腺的转录组学分析
高 艳 杨振慧 李秋方 朱雅楠 梁立强 苏松坤* 聂红毅,2*
(1.福建农林大学 动物科学学院(蜂学学院), 福州 350002;2.福建农林大学 基因组与生物技术研究中心, 福州 350002;3.江西省养蜂研究所, 南昌 330052)
工蜂上颚腺呈一对大型囊状,分布于头部内表面两侧[1],主要合成和分泌脂肪酸以及蜂群报警激素相关的2-庚酮等信息素,其分泌的脂肪酸主要用于幼虫食物营养[2]。研究表明,上颚腺的组成和分泌量受蜜蜂级型和日龄等影响[3]。工蜂上颚腺能分泌蜂王浆成分中的ω-羟基酸及其相应的二酸[4],是蜂王浆中的主要脂质成分[3],其中,脂肪酸中的主要成分10-羟基-2-癸烯酸(10-hydroxy-2(E)-decenoic acid, 10-HDA)是蜂王浆所特有的成分,也是蜂王浆质量评价的重要参考标准[5]。
蜂王浆的分泌由哺育蜂哺育行为介导,因此,人们可以利用哺育蜂分泌蜂王浆饲喂幼虫的行为用于大量生产供人类食用的蜂王浆。蜂王浆由哺育工蜂的咽下腺和上颚腺共同分泌。为阐明上颚腺合成和分泌蜂王浆分子机制,前人已对不同发育日龄的上颚腺开展了大量的研究。黄少康等[6]利用HPLC测定0~30日龄意大利蜜蜂工蜂头部中10-HDA的含量,研究发现工蜂上颚腺中10-HDA含量随日龄增加呈逐渐上升的趋势,在10~20日龄间保持平衡,30日龄含量达到最高;转录组学分析不同级型意大利蜜蜂(蜂王、工蜂)上颚腺分泌物合成途径,发现细胞色素P450(CYP450)家族基因参与脂肪酸β-氧化和ω-氧化,其中CYP6AS8是工蜂中CYP450家族基因中表达量最高的基因,这一发现有助于阐明脂肪酸衍生的信息素生物合成的分子基础[7];Huo等[3]对不同发育日龄(刚出房工蜂、哺育蜂和采集蜂)的普通意大利蜜蜂和优良产浆意大利蜜蜂上颚腺进行蛋白组学分析,结果显示在哺育蜂阶段,特异性蛋白和高丰富的蛋白主要富集在物质转运和脂质合成相关的通路,推测哺育蜂上颚腺优先启动脂质合成中的高分泌活性以作为提供幼虫营养方面的来源,进而激活脂质合成维持所需的脂肪酸来源并最大限度地降低脂质降解以增加10-HDA合成,从而有助于提高蜂王浆的产量。前人已从转录组学和蛋白质组学等方面对不同日龄上颚腺展开研究,然而,上颚腺中蜂王浆合成和分泌的分子机制尚不明确。
为排除日龄因素对上颚腺蜂王浆合成和分泌分子机制的影响,本研究基于蜂群中工蜂劳动分工的可塑性[8-9],通过人工组建蜂群,收集3日龄工蜂(3 d)、10日龄哺育蜂(10 dN)、10日龄采集蜂(10 dF)、21日龄哺育蜂(21 dN)和21日龄采集蜂(21 dF),检测不同职能工蜂上颚腺中10-HDA含量,并采用RNA-seq技术全面筛选哺育蜂上颚腺中与蜂王浆合成分泌相关的差异基因(Differentially expressed genes, DEGs),为阐明上颚腺合成分泌蜂王浆分子机制提供大量有价值的信息,也为膜翅目昆虫中上颚腺功能的研究提供新的思路。
1 材料与方法
1.1 试验蜂种
本研究所用的“蜂强1号”意大利蜜蜂蜂种来自福建农林大学动物科学学院(蜂学学院)蜂场(隶属亚热带季风气候,119°30′ E, 26°08′ N,海拔600~1 000 m),样品于2017年10—11月采自福建农林大学动物科学学院(蜂学学院)教学蜂场。
1.2 主要仪器及试剂
荧光定量PCR仪(美国Bio-Rad公司)、高效液相色谱仪(LC-20A,日本株式会社岛津制作所)、色谱柱(4.6 mm×250 mm不锈钢柱,填充物不定形硅胶C18键合相,10 μm)、SPD-M20A二极管阵列检测器(日本株式会社岛津制作所)、体视显微镜1台、冷光源仪器1台;DEPC水(上海生工生物公司)、SYBR®Premix Ex TaqTMII (Tli RNaseH Plus)(TaKaRa公司)、甲醇(色谱纯,德国MECK基团有限公司)、无水乙醇(分析纯,国药集团化学试剂有限公司)、10-HDA标准品(纯度99.3%,上海安谱实验科技股份有限公司)、对硝基苯甲酯(分析纯,国药集团化学试剂有限公司)。
1.3 标记蜜蜂及收集样品
试验所用蜂群为正常健康的5群强群,每群蜂中至少含有2~3张即将出房的封盖子脾。在组建新的蜂群之前,去除封盖子脾上的蜜蜂,放于恒温恒湿培养箱(温度34.5 ℃,相对湿度60%)中,每隔 24 h 用不同颜色的记号笔在刚出房的蜜蜂胸部或腹部做好标记,连续标记5 d,每天标记刚出房工蜂数目为3 000~5 000头。标记后投入由1只蜂王、蜜粉脾各1张和1张幼虫脾组建的人工蜂群,其中幼虫脾置于中间位置,同时在边脾外侧插入隔板,纱盖上方盖上覆布,便于保温。每隔5 d,从原有蜂群中抽出小幼虫脾,替换组建蜂群中的封盖脾,以保证有充足的幼虫。
标记的工蜂发育到第3天时,直接收取工蜂作为3日龄工蜂(3 d);标记的工蜂发育至第10天和21天时,收集头部伸到有幼虫巢房且持续时间超过10 s的工蜂分别作为10日龄哺育蜂(10 dN)和21日龄哺育蜂(21 dN);在巢门口收集后足花粉筐中载有花粉的外勤蜂,将其分别作为10日龄采集蜂(10 dF)和21日龄采集蜂(21 dF)。按照这个要求,收集3 d、10 dN、10 dF、21 dN和21 dF共5组样本。
1.4 上颚腺的解剖
剪下工蜂头部并去除其触角,拨开口器后将手术用镊子穿过口器后翻转至反面朝上,放在自制蜡盘中,在体视显微镜下用手术刀将工蜂头部的几丁质外壳去除,沿着工蜂口器两边的上颚挑出上颚腺。
1.5 HPLC检测上颚腺中10-HDA的含量
取上述解剖后的5组样品,每组5对上颚腺,每组设置3个生物重复;上颚腺组织置于1.5 mL离心管中,加入50 μL甲醇充分研磨后,移至新的离心管中,加入100 μL内标溶液(对羟基苯甲酸甲酯溶液),定容至1 mL并摇匀,即得各组样本的上颚腺待测样品溶液。取10 μL 10-HDA标准溶液梯度溶液,注入色谱仪,测得10-HDA峰面积,每个样平行3次,基于峰面积的平均值与进样量进行线性拟合,得到10-HDA线性回归方程。根据内标法计算上颚腺中待测样品溶液中的10-HDA含量。
试剂(10-HDA标准溶液、内标溶液和水相溶液)配制、色谱条件参考文献[10-11]的操作。
1.6 上颚腺中蜂王浆合成和分泌相关DEGs的表达水平分析
1.6.1试验组样品cDNA文库构建及Illumina测序
3 d的3个生物学重复分别为3 d_1、3 d_2和3 d_3; 10 dN的3个生物学重复分别为10 dN_1、10 dN_2和10 dN_3; 10 dF的3个生物学重复分别为10 dF_1、10 dF_2和10 dF_3; 21 dN的3个生物学重复分别为21 dN_1、21 dN_2和21 dN_3; 21 dF 的3个生物学重复分别为21 dF_1、21 dF_2和21 dF_3。委托北京诺禾致源生物有限公司开展总RNA质量控制、cDNA文库构建和Illumina测序。本研究15个RNA-seq测序的数据已上传NCBI SRA (https:∥submit.ncbi.nlm.nih.gov/subs/sra/SUB8031156/overview),SRA数据编号为SUB8031156。RNA-seq测序数据分析采用西方蜜蜂参考基因组(Amel_4.5),其链接为:https:∥www.ncbi.nlm.nih.gov/assembly/GCF_000002195.4/。
1.6.2哺育蜂上颚腺中蜂王浆合成和分泌相关DEGs的筛选及表达水平分析
根据FPKM(Fragemnts Per Kilobase of exon model per Million mapped reads)值法计算每个基因在5组样本中的表达量。利用DESeq2软件分析差异基因,将校正后的P<0.05作为筛选差异基因的标准,其中log2Fold change>0和log2Fold change<0分别作为筛选上调和下调DEGs的标准[12]。
筛选与上颚腺中蜂王浆合成分泌密切相关的DEGs的标准如下:DEGs在10 dN上颚腺中的表达量显著高于3 d和21 dN;DEGs在10 dN上颚腺中的表达量显著高于10 dF;DEGs在21 dN上颚腺中的表达量显著高于21 dF;DEGs在10 dN与 21 dN 上颚腺中的表达量无显著差异。将10 dN与3 d之间产生的DEGs记为10 dN vs 3 d组,10 dN与21 dF之间产生的DEGs记为10 dN vs 21 dF组,10 dN与10 dF之间产生的DEGs记为10 dN vs 10 dF组,21 dN与21 dF之间产生的DEGs记为21 dN vs 21 dF组,10 dN与21 dN产生的DEGs为10 dN vs 21 dN组。通过韦恩图分析:10 dN vs 3 d与10 dN vs 21 dF、10 dN vs 10 dF、21 dN vs 21 dF 交集产生共有DEGs(共有DEGs包括调控蜂王浆合成分泌相关,也包括日龄发育等相关);为减少日龄发育的影响,从上述4组交集共有DEGs中去除10 dN vs 21 dN与其交集产生的DEGs,即为哺育蜂上颚腺中与蜂王浆合成分泌密切相关的DEGs。
通过clusterProfiler R软件包和基因本体(GO)条目将关键差异表达基因DEGs映射到GO数据库中,利用BLAST软件将筛选得到的DEGs与KEGG数据库比对,P<0.05表示显著性富集。利用诺禾Novogene售后工具平台(https:∥magic.novogene.com/public/customer/main#/tool_rna/add_tool)对DEGs进行KEGG pathway富集分析。
1.6.3DEGs的实时荧光定量PCR(Quantitative real-time PCR)验证
利用Primer Premier 6为随机选取的6个DEGs设计特异性引物(表1),其中以actin(NM_001185146.1)作为内参基因。反应体系:SYBR Premix Ex Taq Ⅱ(TaKaRa公司,日本)5 μL,正/反向引物(2 μmol/L) 2 μL,模板(500 ng/μL) 2 μL,ddH2O补充至10 μL。PCR扩增程序分为3步:95 ℃预变性30 s;95 ℃变性5 s,60 ℃退火30 s,共40个循环;最后一步为溶解曲线分析:65 ℃开始,每5 s上升0.5 ℃,直至上升到95 ℃。在荧光定量PCR仪(Bio-Rad公司,美国)完成反应程序后,采用2-ΔΔCt法[13]计算上颚腺DEGs的相对表达量。
1.7 数据分析
采用SPSS 20.0软件中单因素方差分析(One-way ANOVA)不同职能工蜂上颚腺10-HDA含量的差异显著性以及qPCR中ACFS2、Mrjp1、Mrjp2、Mrjp3、Mrjp4和Mrjp7基因在不同样本中表达量的差异显著性(P<0.05表示差异显著,P<0.01表示差异极显著),结果用平均值±标准误表示。
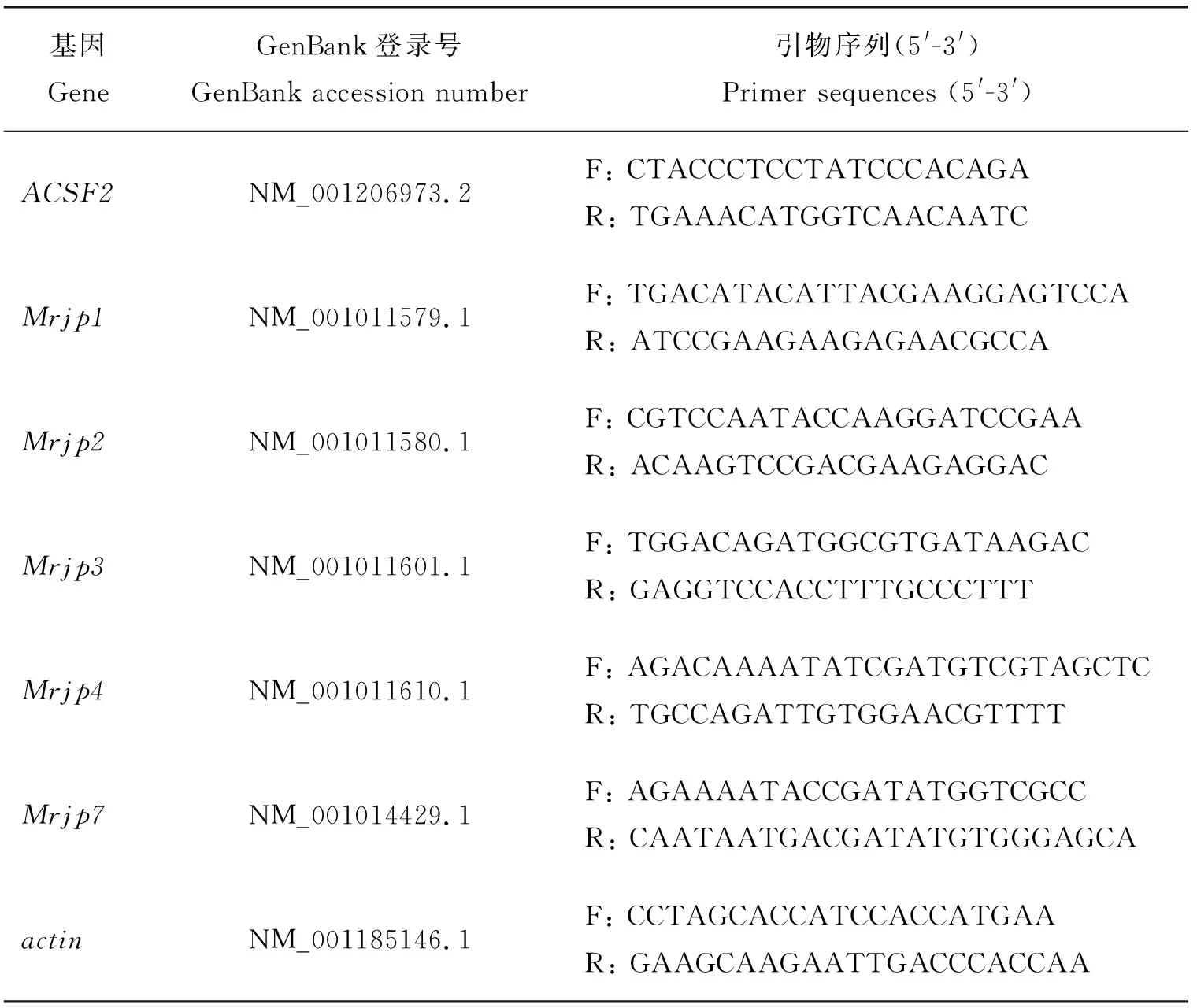
表1 引物信息Table 1 Primer information
2 结果与分析
2.1 工蜂上颚腺中10-HDA的含量测定
HPLC测定3 d、10 dN、10 dF、21 dN和21 dF上颚腺中10-HDA含量。发现3 d上颚腺的 10-HDA 含量最低(0.002 5±0.000 85 mg),10 dN上颚腺中10-HDA的含量为0.019 2±0.007 78 mg,21 dF上颚腺的10-HDA含量最高(0.041 5±0.005 97 mg);随着日龄增加,上颚腺中10-HDA的含量随之增加,其中21 dN和21 dF上颚腺中10-HDA的含量均显著高于3 d(P<0.05),21 dF上颚腺中10-HDA的含量显著高于10 dN(P<0.05);在相同日龄(10日龄和21日龄)的哺育蜂和采集蜂中,本研究发现采集蜂上颚腺中10-HDA含量均高于同日龄哺育蜂,但差异不显著(图1)。
2.2 不同职能工蜂上颚腺测序文库的质控
过滤低质量reads后,每个文库产生约4 049~8 775万个clean reads,与西方蜜蜂基因组匹配率为76.49%~90.63%。RNA-seq测序有效读段数为35 871 395~67 116 890,样本的单一匹配率均在72%以上,Q30值也均在87.8%以上(表2),说明RNA-seq数据质量较好,测序数据可靠性高。
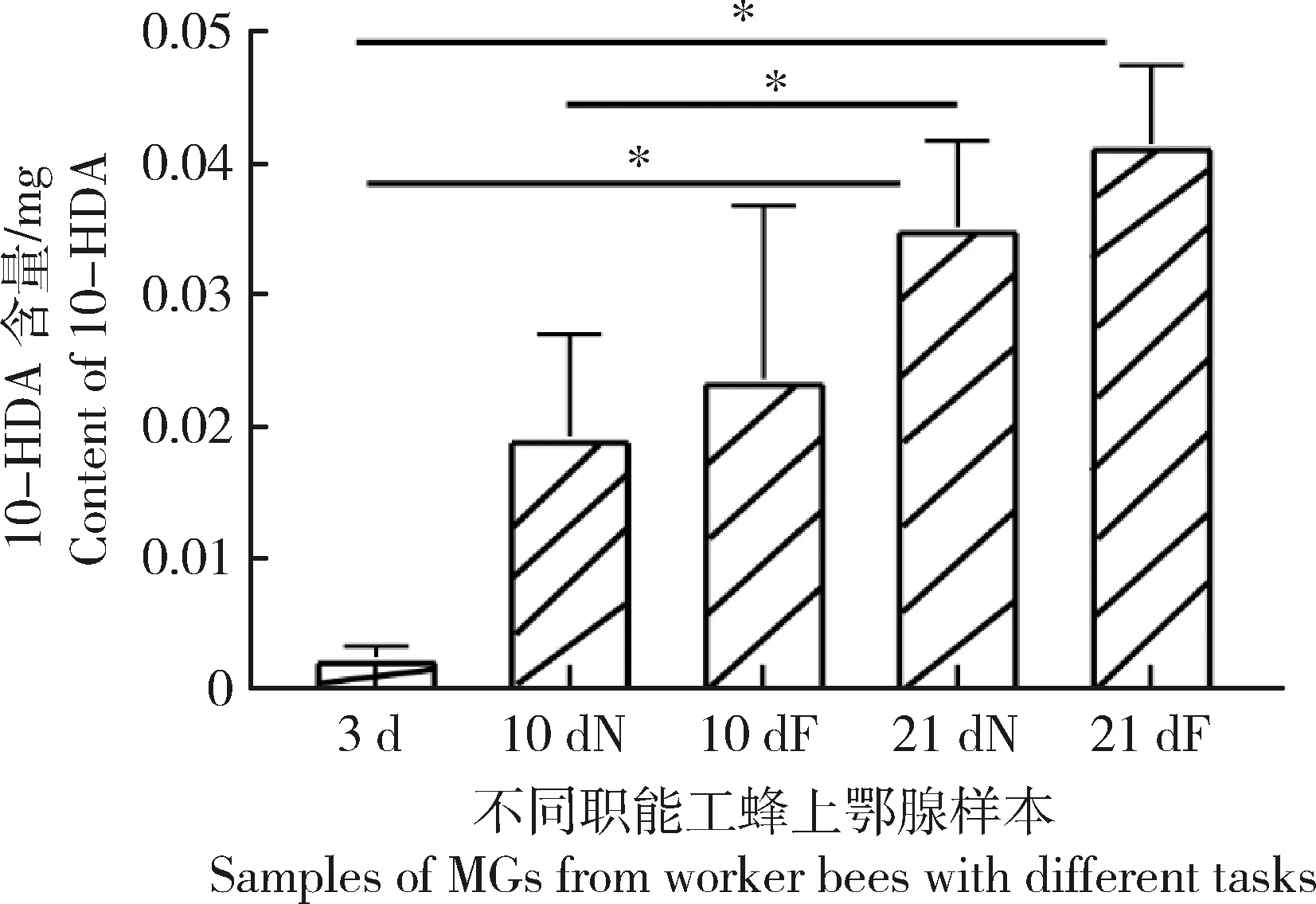
图中数据为平均值±标准误,*P<0.05Data in the figure are mean±SE, *P<0.05图1 不同职能工蜂上颚腺10-HDA含量Fig.1 Contents of 10-HDA in the MGs of worker bees at different developmental ages
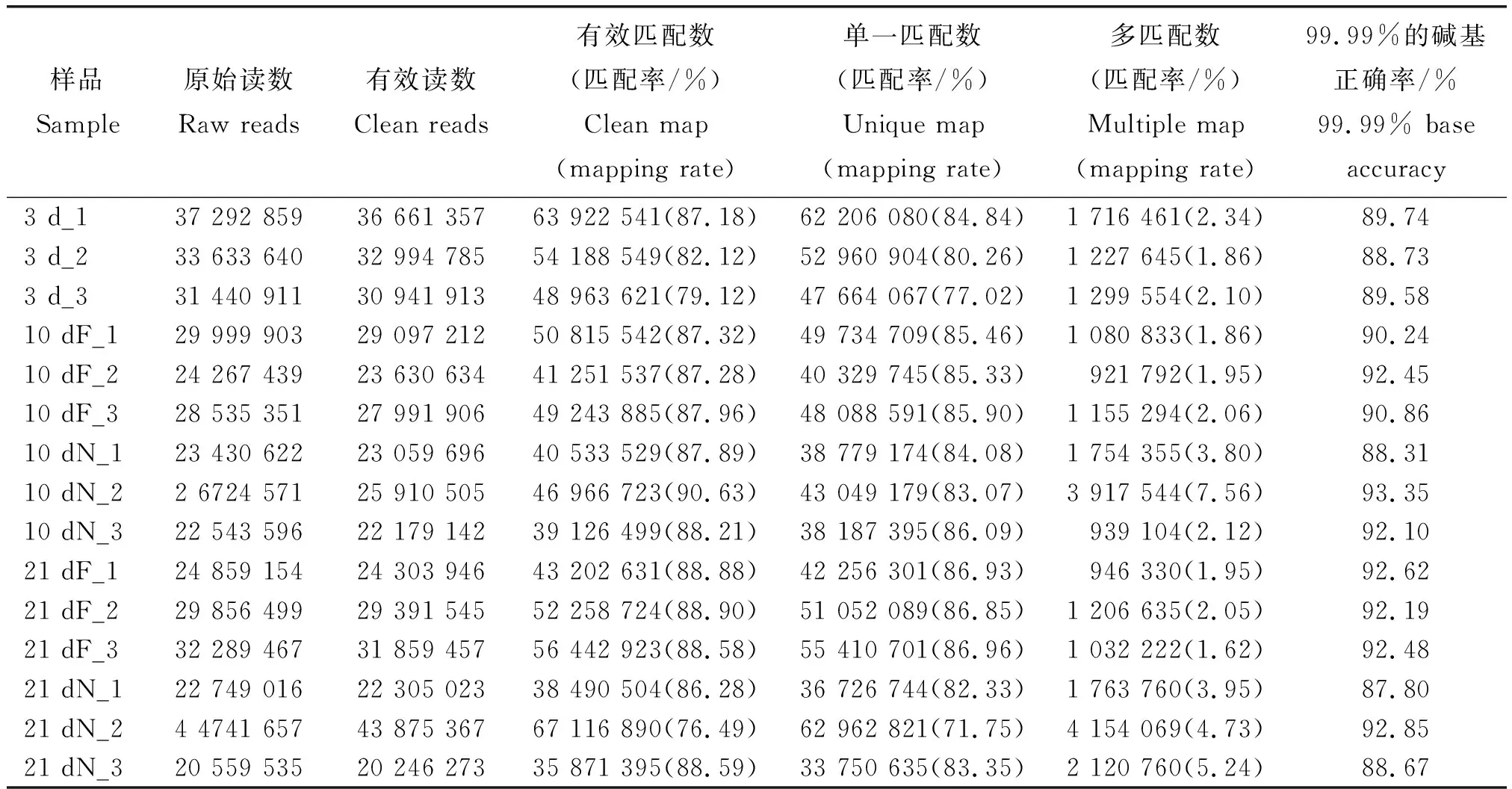
表2 上颚腺15个文库RNA-seq数据总览Table 2 Overview of RNA-seq data from 15 libraries in MGs
2.3 相同日龄哺育蜂和采集蜂上颚腺中Mrjps的表达谱
上颚腺是蜂王浆合成和分泌的重要外分泌腺体,因此,通过RNA-seq研究了相同日龄哺育蜂和采集蜂Mrjps的表达模式(图2)。Mrjps均表现出相似的表达模式,即这些基因在10 dN上颚腺中的表达量远高于3 d、10 dF和21 dF,并且21 dN上颚腺中表达量也高于同龄采集蜂,暗示它们可能在蜂王浆蛋白的合成中起关键作用。在这些基因中,Mrjp1表达量最高,该基因在3 d、10 dN、10 dF、21 dN 和21 dF上颚腺中的FPKM值分别为201.59、40 997.05、387.54、63 157.08和399.08;Mrjp8和Mrjp9表现出相对较低的表达水平(FPKM<43.33)。
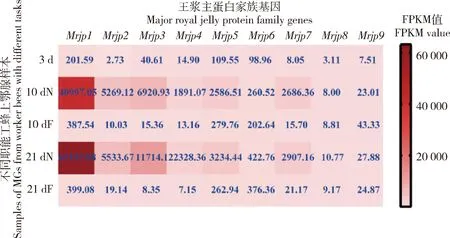
图2 Mrjps在5组工蜂上颚腺中的转录组数据表达谱Fig.2 Expression profiles of Mrjps in the MGs from five samples of worker bees
2.4 筛选上颚腺中蜂王浆合成分泌相关的DEGs
由图3可看出,10 dN vs 3 d有381个DEGs;10 dN vs 21 dF有568个DEGs;10 dN vs 10 dF有374个DEGs;21 dN vs 21 dF有664个DEGs,将这4组进行交集得到67个共有DEGs,这67个DEGs可能与调控蜂王浆合成和分泌及日龄发育等相关。
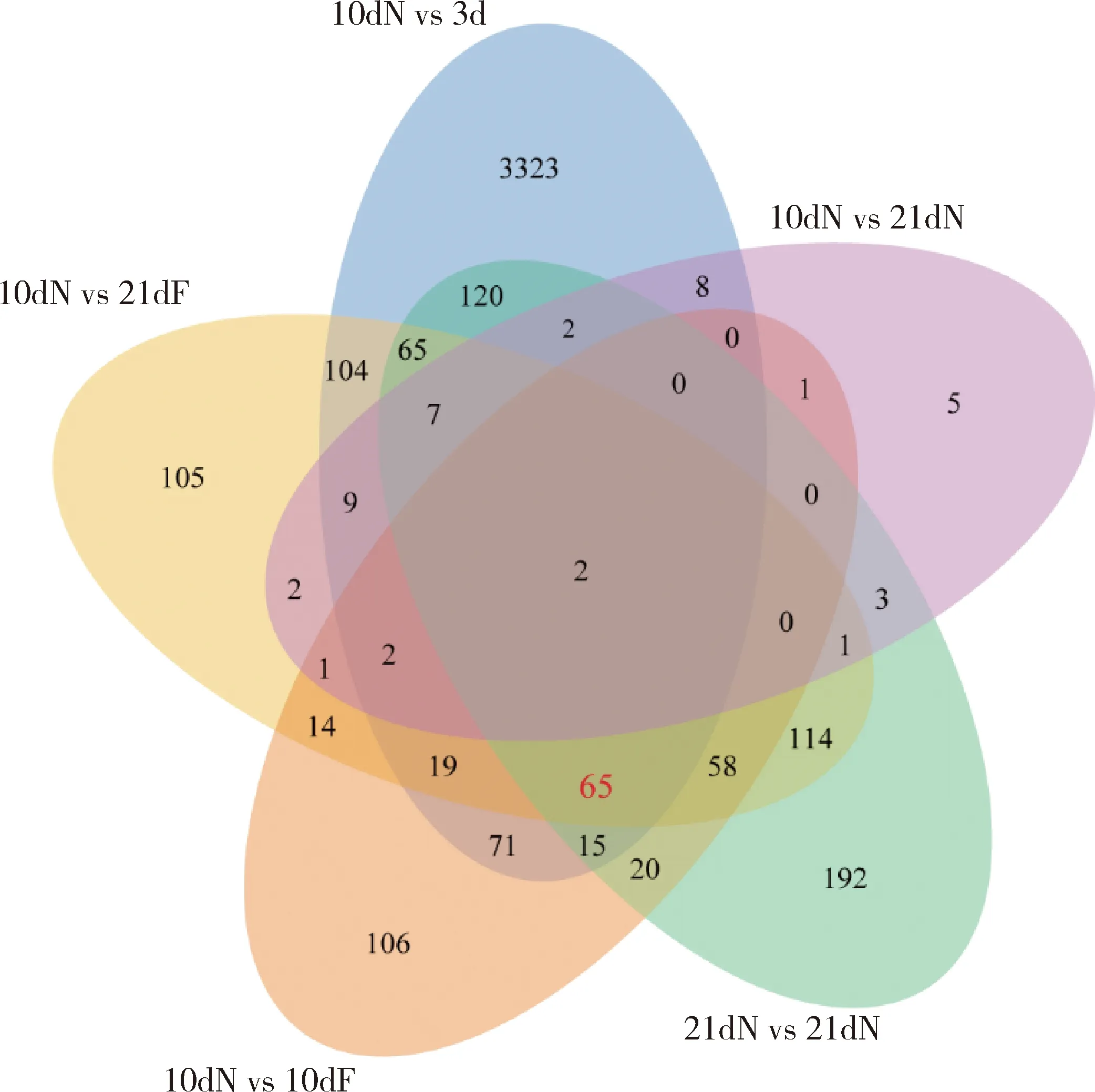
图3 上颚腺中筛选蜂王浆合成分泌相关DEGs韦恩图Fig.3 Venn diagram of DEGs related to synthesis and secretion of royal jelly in MGs
为减少日龄因素的影响,去除10 dN vs 21 dN与67个DEGs交集产生的2个DEGs,最后得到严格筛选条件下与蜂王浆合成与分泌密切相关的65个DEGs(图3)。在这些基因中,只有46个DEGs在10日龄哺育蜂上颚腺中的表达量显著高于3 d、10 dF 和21 dF上颚腺中表达量,同时这些基因在21日龄哺育蜂上颚腺中的表达量也显著高于21 dF中的表达量,符合筛选上颚腺中蜂王浆合成和分泌相关DEGs的标准;相反,11个DEGs在哺育蜂上颚腺中则均呈显著下调表达(表3)。
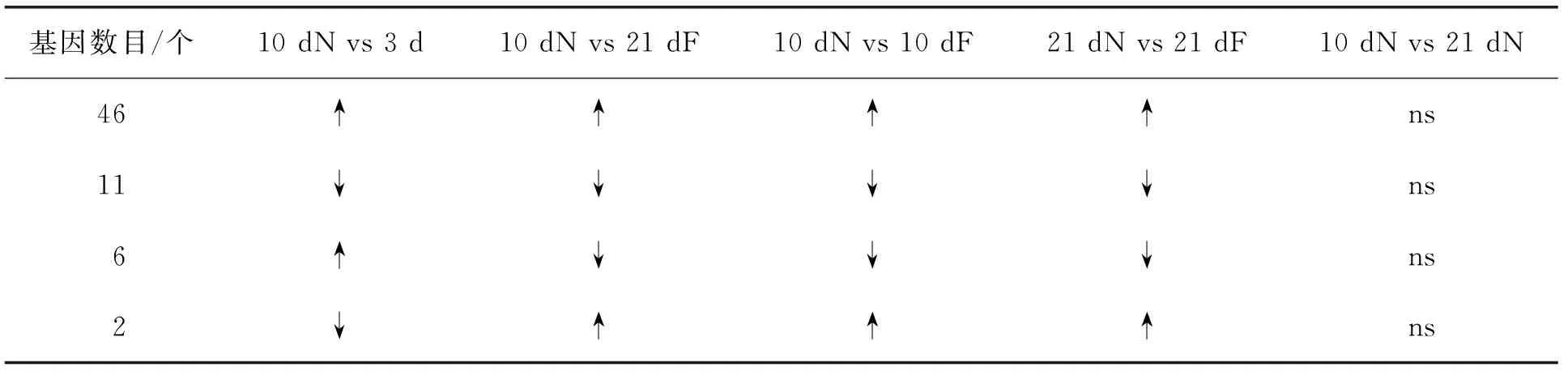
表3 5组样本中上颚腺65个DEGs的差异性分析Table 3 Analysis of significance of 65 DEGs in MGs among 5 groups of honeybee samples
2.5 哺育蜂上颚腺中上调DEGs的GO分析
46个上调DEGs的GO富集表明,在生物学进程中,上调DEGs富集在蛋白质均聚、蛋白质寡聚、大分子复合物组装、大分子复合物亚基组织、细胞组分组装、跨膜运输、细胞组分生物发生、氧化还原过程、蛋白质复合物组装和蛋白质复合物生物发生等;在分子功能上,上调DEGs富集在染色体部分、染色体、胞外区、非膜界细胞器、胞内非膜界细胞器、胞内细胞器部分、细胞器部分、细胞核、大分子复合体和胞内膜界细胞器等;在细胞组分方面,上调DEGs富集在与血红素结合、四吡咯结合、DNA结合、连接酶活性、形成碳氮键、气味结合、酸性磷酸酶活性、丝氨酸型肽酶活性、丝氨酸水解酶活性和磷氧裂解酶活性、氧化还原酶活性(图4(a))。在上调DEGs中没有显著的GO富集,但是这些DEGs中一些基因参与了蛋白磷酸化过程。
2.6 上调DEGs的KEGG分析
上调DEGs共富集32条KEGG,其中包括缬氨酸/亮氨酸/异亮氨酸代谢、脂肪酸延伸、脂肪酸代谢、β-丙氨酸代谢、脂肪酸降解、碳代谢、精氨酸和脯氨酸代谢、丙酸新陈代谢、甘油酯新陈代谢、过氧物酶体、视黄醇新陈代谢、抗坏血酸和藻酸盐代谢、其他多糖降解、药物代谢-细胞色素P450、戊糖和葡萄糖醛酸酯的相互转化、丁酸代谢、细胞色素P450对异生源代谢、药物代谢-其他酶、果糖和甘露糖代谢、鞘脂代谢。而缬氨酸/亮氨酸/异亮氨酸降解、脂肪酸延伸、脂肪酸代谢、β-丙氨酸代谢、脂肪酸降解、碳代谢均呈显著性富集,这些通路与蛋白质代谢、脂肪酸代谢有关,暗示上颚腺中相关基因可能参与了蛋白质和脂肪酸的生物合成(图4(b))。
2.7 Real-time PCR验证RNA-seq数据可靠性
为进一步验证RNA-seq结果,随机选择6个DEGs(ACFS2、Mrjp1、Mrjp2、Mrjp3、Mrjp4和Mrjp7),并使用qPCR进行了验证。结果表明,qPCR检测的6个DEGs的表达模式与转录组数据中DEGs的表达模式一致(图5),表明上颚腺RNA-seq的数据是可靠的。
3 讨 论
本文比较了不同职能工蜂上颚腺中10-HDA的含量,同时使用RNA-seq对相同日龄哺育蜂和采集蜂的上颚腺进行了系统分析。

(a)上调DEGs的GO富集分类;(b)上调DEGs的KEGG富集通路。(a)、(b)只列出了GO和KEGG富集功能上排名前30和20位的通路(a) GO enrichment classification of up-regulated DEGs; (b) KEGG enrichment pathway of up-regulated DEGs. a and b only list the top 30 and 20 pathways in GO and KEGG enrichment function, respectively.图4 上调DEGs的GO和KEGG功能富集分析Fig.4 GO and KEGG functional enrichment analysis of up-regulated DEGs
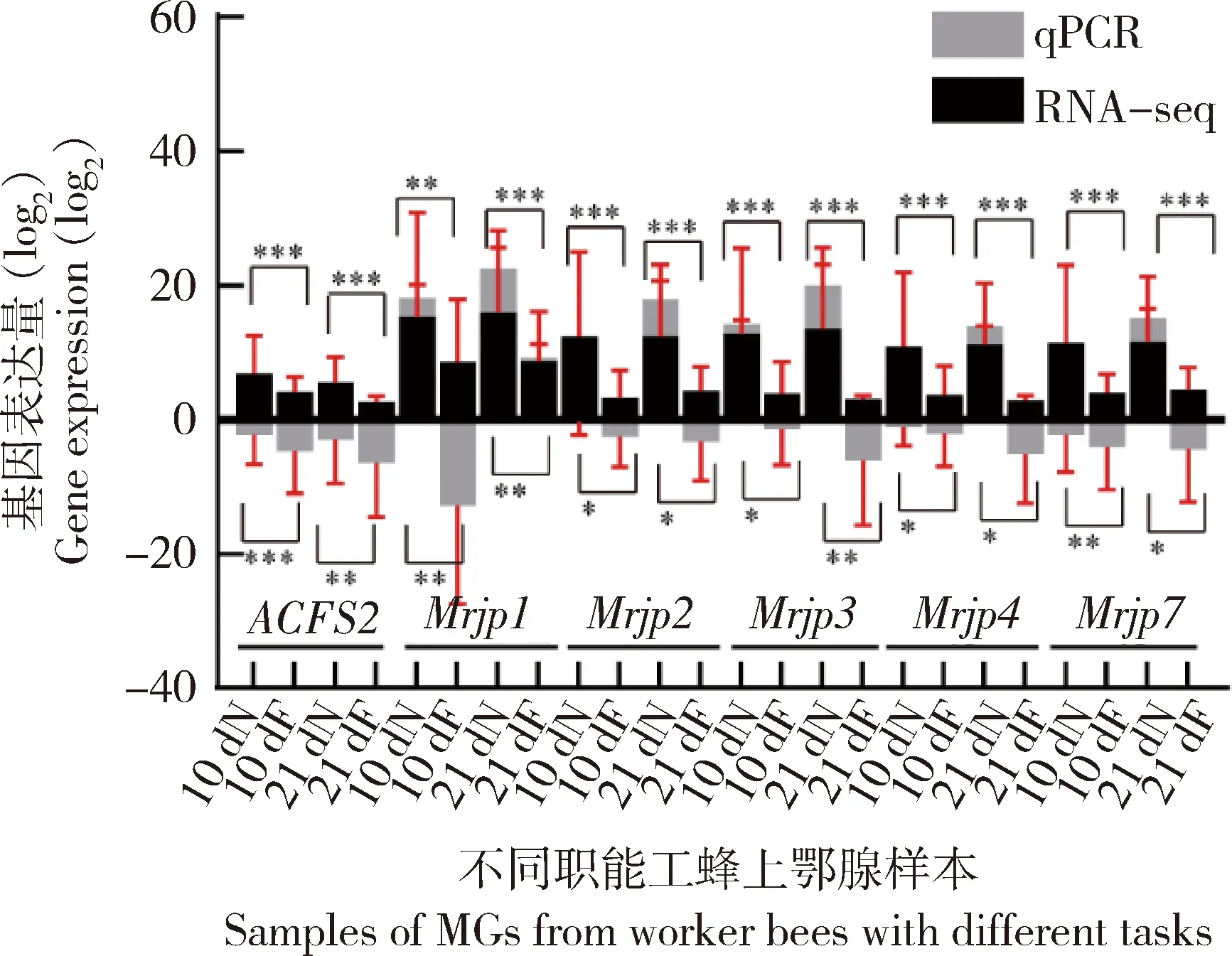
从左到右依次为ACFS2、Mrjp1、Mrjp2、Mrjp3、Mrjp4和Mrjp7 6个基因在样本10 dN、10 dF、21 dN和21 dF中的表达量,其中黑色柱状图表示RNA-seq数据中基因的FPKM值,灰色表示qPCR数据中基因的相对表达量,纵坐标均为相应取过以2为底的对数数值。图中数据为平均值±标准误,*P<0.05; **P<0.01; ***P<0.001。Note:The expression levels of ACFS2, Mrjp1, Mrjp2, Mrjp3, Mrjp4 and Mrjp7 six genes in the samples 10 dN, 10 dF, 21 dN, 21 dF were shown from left to right; The black bar graph represents the FPKM value of the gene in the RNA-seq data, and the gray bar represents the relative expression of genes in the qPCR data; The ordinates are the corresponding logarithmic values with a base of 2. Data in the figure are mean±SE, *P<0.05; **P<0.01; ***P<0.001.图5 上颚腺中转录组数据的qPCR验证Fig.5 qPCR validation of transcriptome data in MGs
3.1 上颚腺中10-HDA的分泌规律以及Mrjps表达趋势分析
在3日龄、10日龄和21日龄工蜂的发育过程中,发现工蜂上颚腺中10-HDA含量总体呈逐渐上升的趋势,至21日龄达最高,但同日龄条件下,采集蜂上颚腺中10-HDA的含量高于哺育蜂。黄少康等[6]利用HPLC对0~30日龄意蜂工蜂头部的10-HDA进行测定,结果发现工蜂上颚腺中10-HDA含量随日龄总体呈逐渐上升的趋势,在10~20日龄间保持平衡,30日龄含量达到最高,这与本研究结果基本一致,推测可能是由于哺育蜂的哺育行为致使腺体分泌物中部分10-HDA进入蜂王浆中。
在本研究中,上颚腺中的Mrjp1-9表现出一种日龄依赖性的表达谱,从第3天到第10天(哺育蜂阶段)转录丰度增加,随后第21天(采集蜂阶段)转录丰度下降;与此同时,10/21日龄的哺育蜂上颚腺的Mrjps表达量高于相应的采集蜂。Mrjp1-4和Mrjp7在哺育蜂上颚腺中大量表达(FPKM>2 000),可能也是构成蜂王浆蛋白的主要成分。其中,5个基因(Mrjp1、Mrjp2、Mrjp3、Mrjp4和Mrjp7)符合上颚腺中与蜂王浆合成和分泌相关基因的筛选标准。与10/21 dF相比,这些基因在哺育蜂上颚腺中的表达量明显上调。
3.2 上颚腺中脂肪酸的生物合成分泌相关的上调DEGs
一般认为蜂王浆中的脂质成分主要由上颚腺分泌[4]。上颚腺的主要功能是分泌脂肪酸和一些信息素。脂肪酸生物合成主要包括最佳前体-硬脂酸的合成、脂肪酸羟基化、脂肪酸链的缩短和末端羟基化修饰[2,7,14]。
硬脂酸可以从食物中摄入后,直接进入上颚腺,也可以短链脂肪酸为原料,在上颚腺中从头合成[40,44]。硬脂酸经过ω-羟基化得到ω-羟化硬脂酸,ω-羟化硬脂酸经过一系列β-氧化和功能化修饰得到主要分泌物10-HDA[14]。
脂肪酸合成酶是工蜂上颚腺的一种特异性蛋白,也是催化内源性脂肪酸合成的关键酶。工蜂上颚腺以短链脂肪酸为原料,从头合成一种长链软脂酸的过程需要脂肪酸合成酶的催化[15]。本研究发现编码脂肪酸合成酶的基因LOC412815在哺育蜂和采集蜂阶段的表达量均较高,但该基因在采集蜂阶段的表达量稍微高于哺育蜂阶段;前人研究结果发现上颚腺中脂肪酸合成酶的表达会影响10-HDA含量的变化[16],本研究发现10-HDA在采集蜂上颚腺中的表达量高于哺育蜂,这一结果也说明了LOC412815在采集蜂阶段的表达量高于哺育蜂。
通过KEGG途径分析,发现3个上调DEGsLOC411662(2-烯酰基辅酶A还原酶)、LOC408291(3-酮酰基-CoA硫解酶)、LOC409150(烯酰辅酶A水合酶)明显富集在脂肪酸延伸通路上,暗示这3个基因可能参与了硬脂酸的生物合成过程。
研究表明,CYP6家族成员中的CYP6AS8和CYP6AS11参与了昆虫脂肪酸羟基化[7]。本研究发现CYP6AQ1在筛选的DEGs中呈上调表达,暗示该基因可能在上颚腺分泌物的生物合成中发挥重要作用,并可能参与了上颚腺中脂肪酸信息素前体的羟基化。
羟基化后,通过β-氧化对脂肪酸碳链进行缩短过程。本文的研究结果表明,5个上调DEGs,乙酰辅酶A合成酶(ACSF2)、乙酰辅酶A脱氢酶(LOC408567)、烯酰辅酶A水合酶(LOC409150)、羟烷基辅酶A脱氢酶(LOC725274)、酮脂酰辅酶A硫解酶(LOC408291)均是参与脂肪酸β-氧化过程的关键酶。脂肪酸β-氧化过程中,一种关键酶—脂酰CoA脱氢酶在其中起到了催化氧化的作用,本研究在富集的脂肪酸降解通路中发现了LOC725274编码的3-羟烷基酰基-CoA脱氢酶Ⅱ型这一基因,此外这一氧化过程也需要通过一种电子传递中间体而完成。电子转移黄素蛋白β(Electron transfer flavoprotein subunit beta, ETF-β),是与脂肪代谢相关的酶类,作为脂酰CoA脱氢酶的电子受体,通过ETF脱氢酶将电子转移给主要的呼吸链,参与脂肪酸β氧化过程[17],在转录组数据中发现LOC410308基因编码的ETF-β在哺育蜂阶段的表达量要高于同日龄的采集蜂阶段。
此外,3-酮脂酰CoA硫解酶(LOC408291)催化脂肪酸β-氧化循环中的硫解反应,与脂质的合成、降解以及能量的产生有关[18-19]。在筛选得到的DEGs中发现,相对于采集蜂阶段,LOC408291在哺育蜂阶段呈高量表达。
本文比较了KEGG通路中脂质代谢的相关基因,包括脂质降解通路中编码相关酶的基因(烯酰辅酶A水合酶LOC409150、乙酰辅酶A脱氢酶LOC408567、3-酮脂酰辅酶A硫解酶LOC408291)的表达水平在DEGs中均呈上调。载脂蛋白是昆虫体内重要的脂质转运蛋白,值得注意的是,上调DEGs中编码载脂蛋白-III的基因A4呈大量表达,这与Wu等[7]的研究结果基本一致。GO功能富集发现,在生物过程中,A4与脂质转运和脂质定位相关,在分子功能中与脂质结合相关,推测载脂蛋白可能在上颚腺的脂肪酸运输方面发挥作用。
脂肪酸的合成均经过羟基化、β-氧化和功能集团修饰,羟基化和β-氧化是合成脂肪酸及其衍生物的重要通路。本研究发现在上调DEGs中参与羟基化(CYP6AQ1)和β-氧化(ACSF2、LOC408567、LOC409150、LOC725274和LOC408291)的关键基因,推测这些基因在工蜂上颚腺合成10-HDA等相关脂肪酸衍生物方面发挥重要作用。
3.3 其他重要的DEGs
在昆虫中,气味结合蛋白(Odorant binding proteins, OBPs)和化学感觉蛋白(Chemosensory proteins, CSPs)在运载疏水性气味分子和信息素穿过淋巴液的信号传导中发挥重要作用[20-21]。有研究表明,一些OBPs在上颚腺中高量表达,暗示其可能参与了信号化学物质的溶解和释放[22]。OBP14在蜂群成员(蜂王、工蜂和雄蜂)的上颚腺中含量丰富,相对于幼蜂和老年蜂,其在内勤蜂中含量最高,OBP14与单萜类结构有较好的亲和性[22];OBP21在老年蜂上颚腺中含量丰富,并与法尼素结合,法尼素是一种吸引蜂群的信息素[22]。此外,在上调DEGs中,也检测到Obp14、Obp17和Obp21,其中Obp21的表达最为丰富。对于社会昆虫而言,蜜蜂的嗅觉系统对于嗅觉线索的检测和辨别至关重要,这是蜂群社会中成员间主要的协调合作方式,对于蜂群的交流至关重要[23]。CSP3已显示与哺育所产生的大型脂肪酸和酯衍生物特异性结合[21],从而影响了哺育蜂的行为[24]。虽然OBPs和CSPs可以与多种配体结合,但它们更倾向于传递不同气味的蜜蜂信息素,且具有较高的结合力[23]。
脂肪酸代谢通路中的相关DEGs以及一些气味结合分子的相关基因在上颚腺中均呈上调表达,推测可能哺育蜂需要提供蜂群食物中所需的关键性脂肪酸物质(10-HDA)和蜂群成员间交流的脂肪酸信息素,因此,相对于采集蜂,同日龄哺育蜂分泌脂肪酸的能力更强。
4 结 论
基于蜂群内社会性劳动分工的可塑性,本研究通过组建人工蜂群的方法获得相同日龄哺育蜂和采集蜂(10日龄和21日龄),测定了不同职能工蜂上颚腺中10-HDA含量变化趋势,发现10-HDA含量总体随日龄逐渐上升至21日龄达最高,但同日龄条件下,采集蜂上颚腺中10-HDA的含量高于哺育蜂。运用转录组学对相同日龄哺育蜂和采集蜂的上颚腺进行系统分析,筛选得到46个与上颚腺中蜂王浆合成和分泌相关的差异基因,发现这些基因主要富集于蛋白质代谢、脂肪酸代谢和能量代谢等方面。本研究是在排除日龄因素的影响下,对上颚腺中基因表达变化模式进行全面分析,为研究上颚腺中蜂王浆合成和分泌的分子机制提供大量有价值的信息,也为膜翅目昆虫中上颚腺的功能研究提供一个新的视角。