新型甾体类吡唑并[1,5-a]嘧啶化合物的合成
范宁娟,李璐琦,汤江江
(1.西北农林科技大学 a.生命科学学院;b.生命科学大型仪器共享平台;c.化学与药学院,陕西 杨凌 712100)
甾体化合物是一类天然生物活性物质。含杂环修饰的甾体化合物,特别是在甾体骨架D-环引入含氮杂环后的甾类衍生物,具有抗癌[1-4]和酶抑制[5]等活性。吡唑并[1,5-a]嘧啶基衍生物有良好的生物活性[6],可作为抗血吸虫剂[7]、抗肿瘤药物[8-9],以及治疗睡眠障碍药物[10]。
雄烯二酮是一种重要的甾体激素,在性生理机能表达中扮演了重要角色[11]。随着甾体化学的不断发展,研究人员发现雄烯二酮类衍生物还具有其它生物活性,如抑制某种酶的作用[12-13]、细胞毒活性[14-16]等。
本文以雄烯二酮为原料,制得16E-苯亚甲基甾体衍生物(1);1和3-氨基吡唑反应合成了D-环吡唑并[1,5-a]嘧啶基修饰的雄烯二酮类衍生物(2,Scheme 1),收率达72%,其结构经1H NMR,13C NMR和HR-MS(ESI)表征。

Scheme 2

Scheme 1
1 实验部分
1.1 仪器与试剂
XT-4型熔点仪;Bruker Advance III 500 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);AB SCIEX TripleTOF® 5600型高分辨液质联用仪。
1按文献方法[17]合成;雄烯二酮,纯度98%;其余所用试剂均为分析纯。
1.2 2的合成
将10.372 g(1 mmol)溶于5 mL无水乙醇中,加入叔丁醇钾0.224 g(2 mmol)和3-氨基吡唑0.083 g(1 mmol),搅拌下回流反应6 h。冷却至室温,减压浓缩,粗产物加入45 mL乙酸乙酯和15 mL水,萃取,有机层用饱和氯化钠溶液(15 mL)洗涤,无水硫酸钠干燥,浓缩,粗产物经硅胶柱层析(洗脱剂:二氯甲烷/甲醇=40/1,V/V)纯化得淡黄色固体20.313 g,收率72%,m.p.178~180 ℃;1H NMR(500 MHz,CDCl3)δ:1.13~1.19(m,1H),1.23(s,3H,18-H),1.33(s,3H,19-H),1.63~1.71(m,3H),1.98~2.08(m,4H),2.33~2.42(m,2H),2.51~2.55(m,1H),2.64~2.74(m,2H),6.09(s,1H,4-H),6.27(dd,J=1.5 Hz,10.0 Hz,1H,2-H),6.65(d,J=2.2 Hz,1H,3′-H),7.10(d,J=10.0 Hz,1H,1-H),7.54~7.59(m,3H,Ar-H),7.76(d,J=7.8 Hz,2H,Ar-H),8.01(d,J=2.2 Hz,1H,2'-H);13C NMR(125 MHz,CDCl3)δ:17.51,18.86,22.57,28.93,32.60,32.94,32.97,34.78,43.60,45.99,52.52,54.68,96.23,119.76,124.32,127.87,128.63,129.59,130.23,130.48,142.15,143.76,149.27,155.19,168.03,173.81,186.18;HR-MS(ESI)m/z:Calcd for C29H30N3O{[M+H]+}436.2383,found 436.2339。
2 结果与讨论
2.1 2的合成反应机理
以催化剂叔丁醇钾为例,分析了2的合成反应机理,结果见Scheme 2:在叔丁醇钾作用下,3-氨基吡唑与化合物1中的α,β-不饱和酮片段脱去一分子水生成亚胺A;A在碱性环境中去质子化转变为B;B的互变异构体C发生分子内的内迈克尔加成反应得到中间体D;D经芳构化得到目标产物2。
2.2 催化剂对反应的影响
以甲醇钠作为碱性催化剂,2收率仅23%(Entry 1),即使延长反应时间至12 h,收率也没有明显提升(Entry 2)。在证实了2的结构后,考察了其它催化剂对收率的影响,结果见表1。以氢氧化钾作为碱性介质,在乙醇中反应6 h的收率只有12%(Entry 3),如果碱换成叔丁醇钠或叔丁醇钾,反应6 h后的环化收率分别增至62%和72%(Entry 4~5),延长叔丁醇钾的反应时间至12 h,收率变化不大(Entry 6),可见大位阻碱有利于环化反应的发生。需要指出的是,如果无碱性介质参与反应,则关环反应不能进行(Entry 7)。
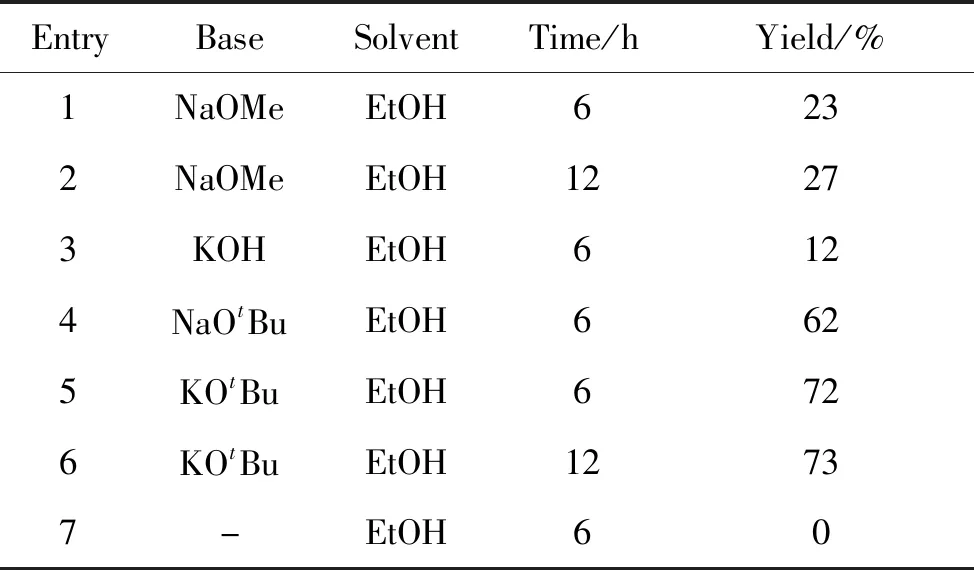
表1 催化剂对2收率的影响Table 1 Effect of catalysts on the yield of 2
以雄烯二酮为原料,合成了D-环吡唑并[1,5-a]吡啶基修饰的雄烯二酮类衍生物。该方法具有收率较高、操作简便等优点,为合成此类甾体类衍生物提供了参考。

