虎尾轮根化学成分及其体外抗肾间质纤维化活性
李 南
(河南中医药大学,河南郑州 450046)
虎尾轮根为豆科兔尾草属植物猫尾射Uraria crinita(L.)Desv.ex DC 的根[1]。主要分布于河南、云南、湖北、广东等省。味甘性温,入肾、肺、胃三经,在民间广泛应用,具有益肾强腰,理气化痰的功效。主治腰背酸痛、遗精、气滞痰饮。《泉州本草》 载有“益肾滋肝,治肾虚遗精”。其主要化学成分为黄酮、香豆素、有机酸、三萜、多糖、甾体类[2-3]。王燕燕等[4]研究表明其具有拮抗肾阳虚小鼠生殖器官萎缩、抗疲劳、增强免疫力、提高小鼠应激能力的作用。为阐明虎尾轮根抗肾间质纤维化的物质基础,寻找抗肾间质纤维化活性天然化合物。本研究对虎尾轮根乙醇提取物的化学成分进行研究,从中分离得到16 个化合物,除化合物3 外,均为首次从虎尾轮根中分离得到。化合物2、4~5、7~8、11~12、14 对肾间质纤维化指标有不同程度的抑制作用。本研究丰富了虎尾轮根化学成分的资源库,以期为后续对其肾间质纤维化的研究提供参考。
1 材料
Bruker AV 400 型核磁共振波谱仪(瑞士Bruker 公司);Sephadex LH-20(美国Pharmacia 公司);OHAUS CP214 型电子天平(奥豪斯仪器有限公司);柱色谱硅胶(100~200、300~400 目,青岛海洋化工厂);GF254薄层硅胶板(青岛海洋化工厂);UPLC-T5291 型高分辨质谱仪(美国Agilent 公司);胶原纤维Ⅳ、Ⅲ型前胶原蛋白、层粘连蛋白(美国Gibco 公司);ZK-31D 型暗箱式紫外分析仪(上海电光仪器厂);RET1200 型暗箱式紫外分析仪(上海顾村电光仪器有限公司);ADP440 型旋转蒸发器(英国Bellingham Stanley 公司);RE-3506A 型旋转蒸发器(上海亚荣生化仪器厂);SephadeX LH-20(美国GE Pharmacia 公司)。噻唑蓝(MTT,美国Amresco 公司);DMEM培养基(美国Gibco 公司);二甲基亚砜(DMSO,上海阿达玛斯试剂有限公司);顺铂(上海麦克林试剂公司,批号C18151213)。提取分离所用溶剂均为分析纯。
虎尾轮根采自河南省郑州市,经河南中医药大学赵献敏副教授鉴定为虎尾轮Uraria crinita(L.)Desv.ex DC 的根,标本收藏于河南中医药大学药学院标本室。
2 提取与分离
取干燥虎尾轮根36.4 kg,加入95%乙醇加热回流提取3 次(时间分别为2、2、1 h),提取液混合后,经减压浓缩回收溶剂,得虎尾轮根提取物8.6 kg。将提取物超声溶解与水中,依次用石油醚、二氯甲烷、丙酮、正丁醇萃取,取上述萃取物浓缩得到石油醚部分(Fr.A,273.5 g)、二氯甲烷部分(Fr.B,251.6 g)、丙酮部分(Fr.C,172.4 g)、正丁醇部分(Fr.D,273.5 g)。将Fr.B 用硅胶柱色谱进行分离,以石油醚-乙酸乙酯(100 ∶0~80 ∶20~50 ∶50~20 ∶80~0 ∶100)梯度洗脱,通过薄层硅胶板分析,合并相同组分,得到Fr.B-1~Fr.B-9。Fr.B-2 过硅胶色谱柱,以石油醚-乙酸乙酯(100 ∶0~60 ∶40~40 ∶60~0 ∶100)梯度洗脱,得到11 个组分Fr.B-2-1~Fr.B-2-11。Fr.B-2-2 经硅胶柱色谱分离得化合物1(16 mg)。Fr.B-2-5 经Sephadex LH-20 分离得到化合物4(26 mg)、8(23 mg);Fr.B-2-9 经重结晶得到化合物3(29 mg)。Fr.B-7 过硅胶色谱柱,以石油醚-乙酸乙酯(80 ∶20~50 ∶50~20 ∶80)梯度洗脱,得到9 个组分 Fr.B-7-1~Fr.B-7-9。Fr.B-7-3 经Sephadex LH-20 分离得到化合物2(24 mg)、7(27 mg);Fr.B-7-5 经重结晶得到化合物11(23 mg)。将Fr.C 用硅胶柱色谱进行分离,以石油醚-乙酸乙酯(80 ∶20~50 ∶50~20 ∶80)梯度洗脱,通过薄层硅胶板分析,合并相同组分,得到Fr.C-1~Fr.C-11。Fr.C-3 经Sephadex LH-20 反复纯化得化合物5(19 mg)。Fr.C-4 经硅胶色谱柱分离,以二氯甲烷-甲醇(100 ∶0~70 ∶30~30 ∶70~0 ∶100)梯度洗脱,得到8 个组分Fr.C-4-1~Fr.C-4-8,Fr.C-4-2经硅胶色谱柱分离,以二氯甲烷-甲醇(50 ∶50)洗脱,得化合物 15(22 mg);Fr.C-4-5 经Sephadex LH-20 分离得化合物14(26 mg)、16(34 mg)。Fr.C-6 经硅胶色谱柱分离,以二氯甲烷甲醇(100 ∶0~70 ∶30~30 ∶70~0 ∶100)梯度洗脱,得到10 个组分Fr.C-6-1~Fr.C-6-10,Fr.C-6-2经硅胶色谱柱分离,以二氯甲烷-甲醇(10 ∶90~90 ∶10)梯度洗脱,得化合物6(22 mg)、10(25 mg);Fr.C-6-4 经重结晶得化合物9(24 mg)、12(22 mg);Fr.C-6-7 经Sephadex LH-20 分离得化合物13(32 mg)。
3 结构鉴定
化合物1:黄色粉末(丙酮),ESI-MS m/z:223.4 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:7.79(1H,d,J =2.4 Hz,H-5′),7.36(1H,d,J =2.4 Hz,H-7′),6.58(1H,dd,J =8.4,2.4 Hz,H-6′),5.06(1H,d,J =8.4 Hz,H-1′a),4.39(1H,m,H-5),4.35(1H,d,J =8.4 Hz,H-1′e),4.05(2H,q,J =8.4 Hz,H-2″),2.42(2H,m,H-3),2.09(2H,m,H-4),1.42(3H,t,J =7.5 Hz,H-3″);13C-NMR(150 MHz,DMSO-d6) δ:172.6(C-2),29.5(C-3),24.2(C-4),61.6(C-5),49.6(C-1′),179.3(C-2′),148.5(C-3′),151.7(C-5′),114.5(C-6′),122.4(C-7′),169.5(C-1″),63.7(C-2″),14.8(C-3″)。以上数据与文献[5]基本一致,故鉴定为divaricataester A
化合物2:黄色粉末(丙酮),ESI-MS m/z:296.3 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:6.95(2H,d,J =8.4 Hz,H-2″,6″),6.85(1H,d,J =2.4 Hz,H-3),6.68(2H,d,J =8.4 Hz,H-3″,5″),6.08(1H,d,J =2.4 Hz,H-4),4.43(2H,t,J =8.4 Hz,H-1′),4.17(2H,s,H-6),3.52(2H,q,J =8.4 Hz,H-7),3.15(2H,t,J =8.4 Hz,H-2′),1.18(3H,t,J =8.4 Hz,H-8);13C-NMR(150 MHz,DMSO-d6)δ:133.1(C-1),1252.6(C-3),109.7(C-4),140.9(C-5),64.2(C-6),65.4(C-7),14.6(C-8),180.6(C-9),41.3(C-1′),36.8(C-2′),128.6(C-1″),129.7(C-2″),114.2(C-3″),153.1(C-4″),114.2(C-5″),129.7(C-6″)。以上数据与文献[6]基本一致,故鉴定为pyrrolezanthine-6-ethyl ether。
化合物3:无色针晶(甲醇),ESI-MS m/z:443.1 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:13.16(d,5-OH),11.17(d,7-OH),6.79(d,J =8.4 Hz,H-6′),6.73(d,J =8.4 Hz,H-5′),5.97(2H,d,J =2.4 Hz,H-6,H-8),5.91(2H,s,-OCH2O-),4.47(dd,J =10.2,8.4 Hz,H-2),4.41(dd,J =5.6,8.4 Hz,H-2),4.29(dd,J = 10.2,8.4 Hz,H-3),3.39(s,-OCH3);13C-NMR(150 MHz,DMSO-d6) δ:69.5(C-2),48.1(C-3),196.5(C-4),163.2(C-5),97.1(C-6),167.1(C-7),94.8(C-8),162.7(C-9),102.6(C-10),1119.5(C-1′),140.5(C-2′),138.2(C-3′),150.2(C-4′),100.8(C-5′),124.1(C-6′),101.7(-OCH2O-),60.2(-OCH3)。以上数据与文献[7]基本一致,故鉴定为5,7-二羟基-2′-甲氧基-3′,4′-亚甲基二氧异黄酮。
化合物4:无色粉末(丙酮),ESI-MS m/z:235.9 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:8.24(1H,d,J =2.4 Hz,H-6),8.06(1H,dd,J =8.4,2.4 Hz,H-4),7.12(1H,d,J =2.4 Hz,H-3),6.58(1H,s,H-8),4.05(3H,s,2-OCH3),2.57(3H,s,H-2′),2.31(3H,s,H-10),1.95(3H,s,H-11);13C-NMR(150 MHz,DMSO-d6) δ:157.2(C-1),129.8(C-2),125.3(C-3),134.5(C-4),129.1(C-5),133.4(C-6),197.3(C-7),110.9(C-8),163.4(C-9),29.1(C-10),26.1(C-11),191.8(C-1′),19.7(C-2′),55.7(-OCH3)。以上数据与文献[8]基本一致,故鉴定为dehydroespeleton。
化合物5:无色结晶(丙酮),ESI-MS m/z:435.1 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:5.36(1H,t,J =8.4 Hz,H-6),5.08(1H,m,H-11),4.93(1H,d,J =2.4 Hz,H-12),3.48(1H,m,H-3),0.98(3H,d,J =8.4 Hz,H-21),0.87(3H,s,H-19),0.79(3H,d,J =8.4 Hz,H-26),0.75(3H,d,J =2.4 Hz,H-27),0.73(3H,t,J =8.4 Hz,H-29),0.72(3H,s,H-18);13C-NMR(150 MHz,DMSO-d6)δ:38.2(C-1),32.5(C-2),72.3(C-3),41.7(C-4),141.3(C-5),122.5(C-6),24.9(C-7),51.7(C-8),50.9(C-9),36.2(C-10),130.2(C-11),137.2(C-12),41.6(C-13),57.2(C-14),23.6(C-15),29.1(C-16),55.4(C-17),11.9(C-18),20.3(C-19),35.8(C-20),18.5(C-21),40.6(C-22),26.1(C-23),45.6(C-24),28.7(C-25),20.3(C-26),18.6(C-27),23.1(C-28),11.7(C-29)。以上数据与文献[9]基本一致,故鉴定为pleuchiol。
化合物6:白色形粉末(甲醇),ESI-MS m/z:373.2 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:8.13(2H,d,J =8.4 Hz,H-2″,6″),8.09(2H,d,J =8.4 Hz,H-2′,6′),7.58(2H,dd,J =8.4,2.4 Hz,H-4′,4″),7.41(4H,m,H-3′,5′,3″,5″),6.08(2H,m,H-5,6),6.05(1H,ddd,J =8.4,2.4,2.4 Hz,H-4),5.73(1H,ddd,J =10.2,8.4,2.4 Hz,H-3),5.08(1H,d,J =8.4 Hz,H-7α),5.04(1H,d,J =8.4 Hz,H-7β),4.72(1H,d,J =8.4 Hz,H-2);13C-NMR(150 MHz,DMSO-d6) δ:134.8(C-1),69.5(C-2),75.3(C-3),123.7(C-4),1249.3(C-5),125.2(C-6),65.1(C-7),130.2(C-1′),130.1(C-2′),129.5(C-3′),132.6(C-4′),129.5(C-5′),130.1(C-6′),167.2(C-7′),129.3(C-1″),130.2(C-2″),129.7(C-3″),132.1(C-4″),129.7(C-5″),130.2(C-6″),167.2(C-7″)。以上数据与文献[10]基本一致,故鉴定为1,6-desoxypipoxide。
化合物7:白色粉末(丙酮),ESI-MS m/z:290.2 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:9.31(1H,s,4′-OH),7.48(2H,d,J =8.4 Hz,H-2,6),7.41(1H,dd,J =8.4,2.4 Hz,H-4),7.39(1H,d,J =8.4 Hz,H-7′),7.36(2H,dd,J =8.4,2.4 Hz,H-3,5),6.92(2H,d,J =2.4 Hz,H-2′,6′),6.72(2H,d,J =2.4 Hz,H-3′,5′),6.57(1H,d,J =8.4 Hz,H-8′),5.68(1H,s,NH),3.29(2H,t,J =8.4 Hz,H-8),2.72(2H,t,J =8.4 Hz,H-7);13CNMR(150 MHz,DMSO-d6) δ:134.3(C-1),128.7(C-2),130.1(C-3),131.6(C-4),130.1(C-5),128.7(C-6),33.6(C-7),39.7(C-8),130.4(C-1′),130.2(C-2′),114.6(C-3′),156.2(C-4′),114.6(C-5′),130.2(C-6′),139.4(C-7′),121.7(C-8′),164.7(C-9′)。以上数据与文献[10]基本一致,故鉴定为p-coumaroyl-β-phenethylamine。
化合物8:白色粉末(丙酮),ESI-MS m/z:483.7 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:7.51(1H,d,J =8.4 Hz,H-7‴),7.12(1H,brs,H-2‴),6.91(1H,d,J =8.4 Hz,H-6‴),6.73(1H,d,J =8.4 Hz,H-5‴),6.57(2H,brs,H-2,5),6.49(1H,dd,J =8.4,2.4 Hz,H-6),6.27(1H,d,J =8.4 Hz,H-8‴),4.32(1H,d,J =8.4 Hz,H-1′),4.18(1H,d,J =8.4 Hz,H-1″),2.72(2H,m,H-7);13C-NMR(150 MHz,DMSO-d6) δ:131.2(C-1),117.3(C-2),146.2(C-3),144.5(C-4),115.7(C-5),119.6(C-6),34.8(C-7),69.4(C-8),102.6(C-1′),72.3(C-2′),77.6(C-3′),68.2(C-4′),76.2(C-5′),68.3(C-6′),104.6(C-1″),73.5(C-2″),76.9(C-3″),69.2(C-4″),76.5(C-5″),60.8(C-6″),125.8(C-1‴),115.6(C-2‴),146.1(C-3‴),149.2(C-4‴),117.2(C-5‴),122.3(C-6‴),145.3(C-7‴),114.1(C-8‴),167.3(C-9‴)。以上数据与文献[11]基本一致,故鉴定为isolugrandoside。
化合物9:黄色粉末(丙酮),ESI-MS m/z:462.7 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:9.26(1H,brs,7-OH),6.93(1H,d,J =10.2 Hz,H-6′),6.72(1H,d,J =8.4 Hz,H-5),6.61(1H,d,J =2.4 Hz,H-3′),6.51(1H,dd,J =10.2,2.4 Hz,H-5′),6.31(1H,dd,J =8.4,2.5 Hz,H-6),6.20(1H,d,J =2.4 Hz,H-8),4.08(1H,dq,J =8.4,2.4 Hz,H-2β),4.02(1H,t,J =8.4 Hz,H-2α),3.27(1H,m,H-3α),3.76(3H,s,2′-OCH3),2.75(1H,dd,J =8.4,2.4 Hz,H-4β),3.72(3H,s,-OCH3),2.68(1H,ddd,J =10.2,8.4,2.4 Hz,H-4α);13C-NMR(150 MHz,DMSO-d6) δ:70.2(C-2),30.6(C-3),29.8(C-4),128.4(C-5),107.6(C-6),160.2(C-7),103.6(C-8),157.1(C-9),113.7(C-10),119.5(C-1′),155.2(C-2′),99.2(C-3′),158.3(C-4′),105.3(C-5′),128.2(C-6′),55.6(-OCH3),55.1(-OCH3)。以上数据与文献 [12]基本一致,故鉴定为紫苜蓿烷。
化合物10:无色结晶(丙酮),ESI-MS m/z:295.2 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:12.41(1H,brs,5-OH),9.83(1H,br s,4′-OH),6.79(1H,d,J =8.4 Hz,H-6′),6.40(1H,d,J =2.4 Hz,H-3′),6.28(1H,dd,J =8.4,2.4 Hz,H-5′),5.68(2H,brs,H-6,8),4.46(1H,t,J =8.4 Hz,H-2α),4.30(1H,dd,J =8.4,2.4 Hz,H-2β),4.09(1H,dd,J =8.4,2.4 Hz,H-3β),3.72(3H,s,7-OCH3);13CNMR(150 MHz,DMSO-d6) δ:69.4(C-2),45.2(C-3),196.2(C-4),163.2(C-5),96.5(C-6),163.8(C-7),96.2(C-8),163.4(C-9),100.2(C-10),113.6(C-1′),159.1(C-2′),99.5(C-3′),157.6(C-4′),106.3(C-5′),129.2(C-6′),55.2(-OCH3)。以上数据与文献[12]基本一致,故鉴定二氢木豆异黄酮。
化合物11:黄色粉末(丙酮),ESI-MS m/z:409.3 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:7.51(1H,d,J =8.4 Hz,H-7),7.40(1H,d,J =2.4 Hz,H-2),7.31(1H,d,J =2.4 Hz,H-2′),7.18(1H,s,H-7′),6.95(1H,dd,J =8.4,2.4 Hz,H-6′),6.92(1H,dd,J =8.4,2.4 Hz,H-6),6.68(1H,d,J =8.4 Hz,H-5′),6.62(1H,d,J =8.4 Hz,H-5),6.51(1H,d,J =8.4 Hz,H-8);13C-NMR(150 MHz,DMSO-d6)δ:127.6(C-1),108.6(C-2),149.2(C-3),144.2(C-4),112.8(C-5),121.8(C-6),148.3(C-7),117.2(C-8),167.6(C-9),55.4(3-OCH3),123.7(C-1′),113.2(C-2′),147.1(C-3′),139.4(C-4′),115.1(C-5′),124.2(C-6′),148.2(C-7′),139.6(C-8′),165.2(C-9′),55.4(3′-OCH3)。以上数据与文献[13]基本一致,故鉴定为8-O-4-dehydrodiferulic acid。
化合物12:白色晶体(丙酮),ESI-MS m/z:244.1 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:7.22(1H,dd,J =8.4,2.4 Hz,H-3),6.08(1H,dd,J =8.4,2.4 Hz,H-4),5.93(1H,dt,J =8.4,2.4 Hz,H-5),5.62(1H,d,J =8.4 Hz,H-2),5.51(1H,dqt,J =10.2,8.4,2.4 Hz,H-9),5.41(1H,dtq,J =10.2,8.4,2.4 Hz,H-8),3.22(2H,dd,J =8.4,2.4 Hz,H-2′),2.23(4H,m,H-6,7),1.79(1H,seqt,J =8.4 Hz,H-3′),1.57(3H,brd,J =8.4 Hz,H-10),0.87(6H,d,J =8.4 Hz,H-4′,5′);13CNMR(150 MHz,DMSO-d6) δ:165.8(C-1),119.5(C-2),139.7(C-3),129.3(C-4),144.7(C-5),33.4(C-6),29.1(C-7),130.6(C-8),127.3(C-9),13.8(C-10),47.2(C-2′),28.3(C-3′),19.6(C-4′,5′),19.6(C-5′)。以上数据与文献[14]基本一致,故鉴定为8,9-dehydropellitorine。
化合物13:白色粉末(丙酮),ESI-MS m/z:332.1 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:7.68(1H,d,J =8.4 Hz,H-7),7.57(2H,m,H-2,6),7.35(3H,m,H-3,4,5),6.47(1H,d,J =8.4 Hz,H-8),5.08(d,J =8.4 Hz,2.4H,H-α),4.51(d,J =8.4 Hz,2.4H,Hβ);13C-NMR(150 MHz,DMSO-d6) δ:136.4(C-1),130.8(C-2),132.4(C-3),32.9(C-4),132.4(C-5),130.8(C-6),1147.3(C-7),119.2(C-8),169.1(C-9),99.1(C-1′),75.2(C-2′),78.2(C-3′),71.6(C-4′),75.1(C-5′),64.6(C-6′),93.6(C-1″),75.7(C-2″),74.1(C-3″),69.5(C-4″),72.1(C-5″),64.6(C-6″)。以上数据与文献[15]基本一致,故鉴定为6-O-(E)-肉桂酰基-α/β-D-吡喃葡萄糖苷。
化合物14:白色粉末(丙酮),ESI-MS m/z:369.3 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:8.06(1H,d,J =8.4 Hz,H-4),7.60(1H,d,J =8.4 Hz,H-5),6.79(1H,d,J =8.4 Hz,H-6),6.31(1H,d,J =2.4 Hz,H-4′),6.30(1H,d,J =8.4 Hz,H-3),4.40(1H,d,J =8.4 Hz,H-3′),1.92(6H,s,-COCH3×2),1.38(3H,s,2′-CH3),1.29(3H,s,2′-CH3);13C-NMR(150 MHz,DMSO-d6) δ:1160.2(C-2),111.5(C-3),145.1(C-4),130.2(C-5),114.2(C-6),157.1(C-7),106.8(C-8),154.2(C-9),111.6(C-10),9.7(-COCH3× 2,-CH3),78.4(C-2′),71.8(C-3′),60.3(C-4′),23.6(-CH3),25.1(-CH3),170.1(-COCH3×2,-C =O)。以上数据与文献[16]基本一致,故鉴定为trans-3′,4′-diacetylkhellacton。
化合物15:白色粉末(甲醇),ESI-MS m/z:366.8 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:7.61(1H,dd,J =8.4,2.4 Hz,H-6),7.50(1H,d,J =2.4 Hz,H-2),7.20(1H,d,J =8.4 Hz,H-5),5.02(1H,d,J =8.4 Hz,glc-1),3.92(3H,s,3-OCH3),3.79(3H,s,-OCH3),3.61(1H,dd,J =8.4,2.4 Hz,H-glc-6a),3.51-3.34(5H,m,H-glc-2,3,4,5,6b);13CNMR(150 MHz,DMSO-d6) δ:126.1(C-1),117.2(C-2),153.1(C-3),149.6(C-4),113.1(C-5),125.0(C-6),169.1(C-7),101.7(Cglc-1),74.8(C-glc-2),79.2(C-glc-3),70.8(C-glc-4),77.5(C-glc-5),61.8(C-glc-6),56.5(3-OCH3),53.2(-OCH3)。以上数据与文献[17]基本一致,故鉴定为3-甲氧基-4-O-β-D-吡喃葡萄糖基苯甲酸甲酯。
化合物16:黄色粉末(甲醇),ESI-MS m/z:476.3 [M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:12.62(1H,s,6-OH),8.09(1H,s,H-4),7.43(1H,s,H-3),6.93(1H,s,H-7),2.75(3H,s,H-11),2.62(3H,s,H-13);13C-NMR(150 MHz,DMSO-d6) δ:154.1(C-2),107.4(C-3),126.9(C-4),120.6(C-5),159.6(C-6),99.7(C-7),162.4(C-8),121.6(C-9),203.6(C-10),26.8(C-11),187.5(C-12),25.8(C-13)。以上数据与文献[18]基本一致,故鉴定为euparone。
4 体外抗肾间质纤维化活性筛选
采用MTT 法[19]测试化合物1~16 体外抗肾间质纤维化指标(胶原纤维Ⅳ、Ⅲ型前胶原蛋白,层粘连蛋白)的活性,阳性对照物为顺铂。取胶原纤维Ⅳ、Ⅲ型前胶原蛋白,层粘连蛋白稀释(均分别稀释为20、60、180 μg/mL 3 个质量浓度),每个质量浓度设置3 个复孔,放置于96 孔板中,在37 ℃恒温箱中培养12 h,分别加入化合物 1~ 16(质量浓度分别为 50、150、450 μg/mL),顺铂。在DMEM 培养基中培养48 h后,每孔加入15 μL MTT 溶液染色,继续孵育3.0 h,然后加入500 μL DMSO,混合均匀后,在360 nm 波长处测定吸光度,计算细胞抑制率。采用SPSS 20.0 统计软件,计算目标化合物的IC50值。结果表明化合物5、8 对胶原纤维Ⅳ、Ⅲ型前胶原蛋白,层粘连蛋白具有一定的体外抑制作用。化合物11、14 对胶原纤维Ⅳ、Ⅲ型前胶原蛋白,具有一定的体外抑制作用。化合物2、7 对Ⅲ型前胶原蛋白具有一定的体外抑制作用。化合物4、12对胶原纤维Ⅳ,层粘连蛋白具有一定的体外抑制作用。其他化合物没有明显的体外抗肾间质纤维化活性。见表1。
表1 各化合物体外抗肾间质纤维化IC50值(,μg/mL,n=3)Tab.1 IC50values of anti-renal interstitial fibrosis for various compounds in vitro(,μg/mL,n=3)
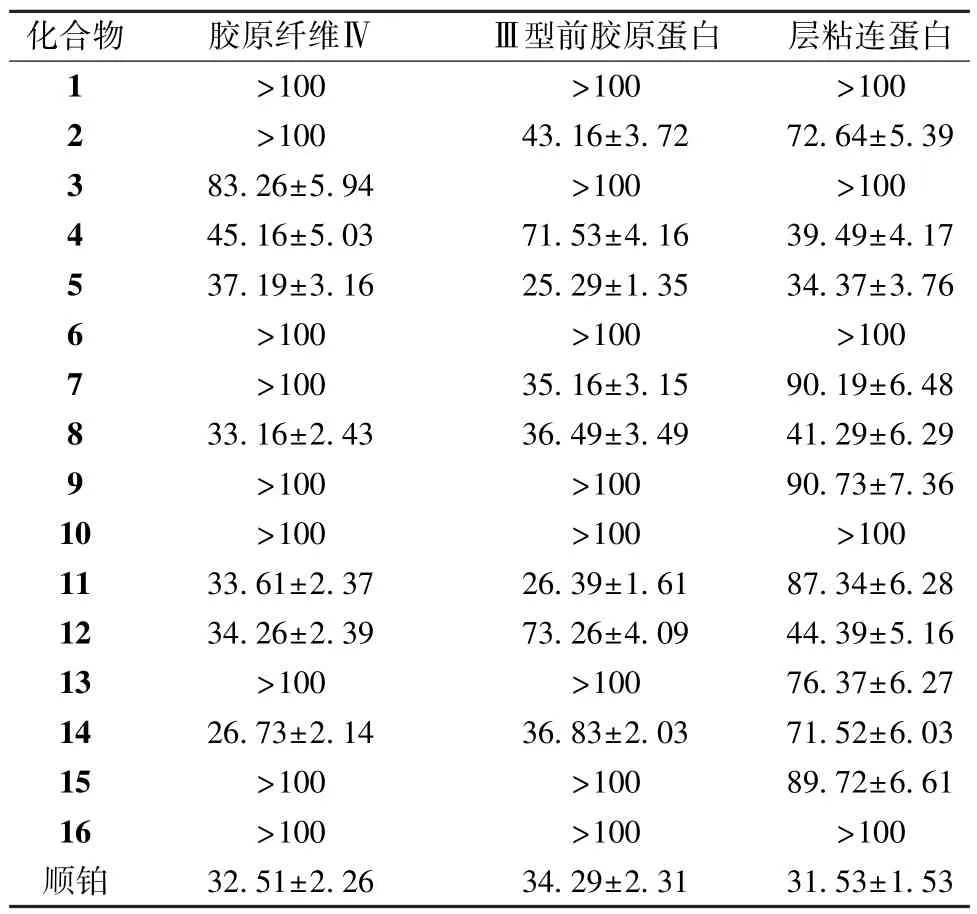
表1 各化合物体外抗肾间质纤维化IC50值(,μg/mL,n=3)Tab.1 IC50values of anti-renal interstitial fibrosis for various compounds in vitro(,μg/mL,n=3)
5 讨论
虎尾轮根为民间常用药,具有广阔的应用前景。本研究从虎尾轮根中分离得到16 个化合物,除化合物3 外,均为首次从虎尾轮根中分离得到,其中化合物1、4、6、7、9、11、15 为首次从兔尾草属植物中分离得到。通过对虎尾轮根体外抗肾间质纤维化活性进行筛选,化合物5、8 对胶原纤维Ⅳ、Ⅲ型前胶原蛋白,层粘连蛋白具有一定的体外抑制作用,化合物2、4、7、11、12、14 对部分肾间质纤维化指标有不同程度的抑制作用。本研究结果丰富了虎尾轮根化学成分的物质基础,表明虎尾轮根具有较大的抗肾间质纤维化开发潜力,以期对抗肾间质纤维化新药的研发提供一定的帮助。

