肥厚型梗阻性心肌病中二尖瓣处理策略的研究进展
朱昌盛、王生伟、唐兵,王水云审校
肥厚型心肌病(HCM)是一种常见的单基因显性遗传性心脏病,是青少年猝死的最常见病因[1]。在成年人群中HCM 的发病率在0.2%左右,典型特征为非对称性室间隔异常肥厚[2-3]。约有70%的HCM患者会发生左心室流出道梗阻进展成肥厚型梗阻性心肌病(HOCM)[4-5]。左心室流出道梗阻和二尖瓣收缩期前向运动(SAM)是HOCM 患者典型的血流动力学表现。对于药物治疗无效的HOCM,室间隔心肌切除术是目前治疗的金标准[6-8]。近年来随着影像学技术的进展,二尖瓣及瓣下装置异常得到了更广泛和深入的认识,逐渐被看作是HOCM 这一疾病的重要组成部分[9-10]。因此,这也直接引起了关于HOCM 外科治疗理念和策略的新变化[11-12]。本文旨在回顾总结HOCM 合并二尖瓣异常相关文献,希望能为这一类患者手术策略的选择提供有益参考。
1 左心室流出道梗阻、SAM 和二尖瓣反流的机制
HOCM 中左心室流出道、SAM 和二尖瓣反流相互关联、相互影响[13]。除了室间隔基底部肥厚本身所致的左心室流出道狭窄外,SAM 是HOCM 中左心室流出道梗阻的最常见原因[14]。尽管SAM 很早就被报道,但其发生机制一直以来充满争议。最近的研究表明,SAM 的发生不能全部用文丘里效应(Venturi effect)来解释[1-15]。Sherrid 等[15]研究显示,在SAM 开始发生时虽然文丘里效应客观存在,但是其强度不足以产生SAM,因为此时通过左心室流出道的血流速度和正常对照无差异。研究者从而推断血流推力是SAM 始发的主要动力。Ro 等[14]则运用一种新的超声技术——矢量流成像(Vector flow mapping)证实了血流推力在SAM 始发时的启动作用。95%的HOCM 可见左心室收缩早期血流撞击突起的二尖瓣叶引发SAM,此外在SAM 发生前后血流撞击二尖瓣叶的夹角均超过60°,意味着此过程中文丘里效应很小。
上述研究不仅解释了文丘里效应和血流推力在室间隔肥厚所致左心室流出道狭窄产生SAM 引发左心室流出道梗阻的血流动力学机制,实际上提示了突入左心室流出道的二尖瓣本身也参与其中。事实证明确实如此。一方面某些HOCM 患者尽管接受室间隔心肌切除术治疗消除室间隔肥厚,仍然会有残余SAM;另一方面非HOCM 患者如二尖瓣病变的患者也会发生SAM。心脏超声和磁共振成像技术在HOCM 的广泛应用和不断进步,使研究者逐渐认识到二尖瓣及瓣下装置异常在左心室流出道梗阻中具有的重要作用[11,16-18]。HOCM 中的二尖瓣异常可归纳为瓣叶冗长、乳头肌异常(包括增粗、前移)和异常腱索均可导致或加重SAM、二尖瓣反流,甚至乳头肌异常本身可以导致中部梗阻[19]。
综上所述,HOCM 中左心室流出道梗阻、SAM和二尖瓣反流是由多因素参与的复杂的综合体,其手术矫治可能也涉及多方面。
2 二尖瓣处理策略
以梅奥诊所为代表的观点是足够的心肌切除疏通左心室流出道后基本可消除SAM 相关的二尖瓣反流从而避免二尖瓣手术[20]。但是上述结论建立的前提是这一大组HOCM 患者中合并二尖瓣固有病变的比例仅为8.1%(162/1 993)。换言之,在不合并二尖瓣固有病变,足够的室间隔心肌切除可消除SAM相关二尖瓣反流。在174 例同时行二尖瓣手术患者中,133 例(76.4%)为二尖瓣修复,且远期生存率优于二尖瓣置换。
Bogachev-Prokophiev 等[21]报道了比较合并二尖瓣异常的HOCM 接受室间隔心肌切除术患者同期二尖瓣修复术和置换术疗效的随机对照试验研究结果,证实了前述结论。该研究共纳入88 例合并二尖瓣异常的HOCM 患者,随机分为两组,一组接受二尖瓣修复术(n=41),另一组接受二尖瓣置换术(n=47)。二尖瓣置换组总体死亡率显著高于二尖瓣修复组;两组免除二尖瓣重度反流率相似。另外二尖瓣置换组血栓栓塞率更高。因此,Bogachev-Prokophiev 等得出结论,HOCM 合并二尖瓣异常所致二尖瓣重度反流需行二尖瓣手术者首选二尖瓣修复。
3 二尖瓣修复技术
如前所述HOCM 中左心室流出道梗阻、SAM 和二尖瓣反流发生机制尽管充满争议,但是随着认识的逐渐加深,关于HOCM 中二尖瓣处理的理念和策略也在与时俱进,并应用到各自的临床实践,下文将介绍几种在HOCM 中联合应用的二尖瓣成形技术。
3.1 二尖瓣前叶加宽
荷兰鹿特丹伊拉斯莫斯医学中心在HOCM 合并二尖瓣前叶面积>12 cm2患者中实施室间隔心肌切除术联合二尖瓣前叶加宽,并相继报道了近远期结果[22-24]。具体操作为纵行切开二尖瓣前叶,然后将一块长3 cm×2.5 cm 的自体心包片连接二尖瓣中央部分(图1)[25]。Kofflard 等[24]比较了8 例接受室间隔心肌切除联合二尖瓣前叶加宽与12 例仅接受室间隔心肌切除患者的早期疗效,结果显示前者术后二尖瓣SAM、二尖瓣反流、心功能改善均较后者的更好。该报道的明显不足之处是样本数太少。van der Lee C 等[23]于2003 年报道了29 例HOCM 患者接受这一手术方式的中期结果,平均随访时间3.4 年。90%的患者术后SAM 消失或仅为轻微,97%的患者术后二尖瓣反流消失或为微量。围术期仅有1 例因自体心包片裂开需紧急再次手术。无病例死亡与起搏器植入。但是该研究缺乏对照组,无法判断与仅接受室间隔心肌切除患者相比,其疗效孰优孰劣。最近,Vriesendorp 等[22]报道了室间隔心肌切除术联合二尖瓣前叶加宽在98 例HOCM 患者中的远期疗效。平均随访时间8.3 年的结果显示,该手术方式消除或减轻SAM 和二尖瓣反流具有良好的持久性,生存率和性别、年龄匹配的健康荷兰人相似。
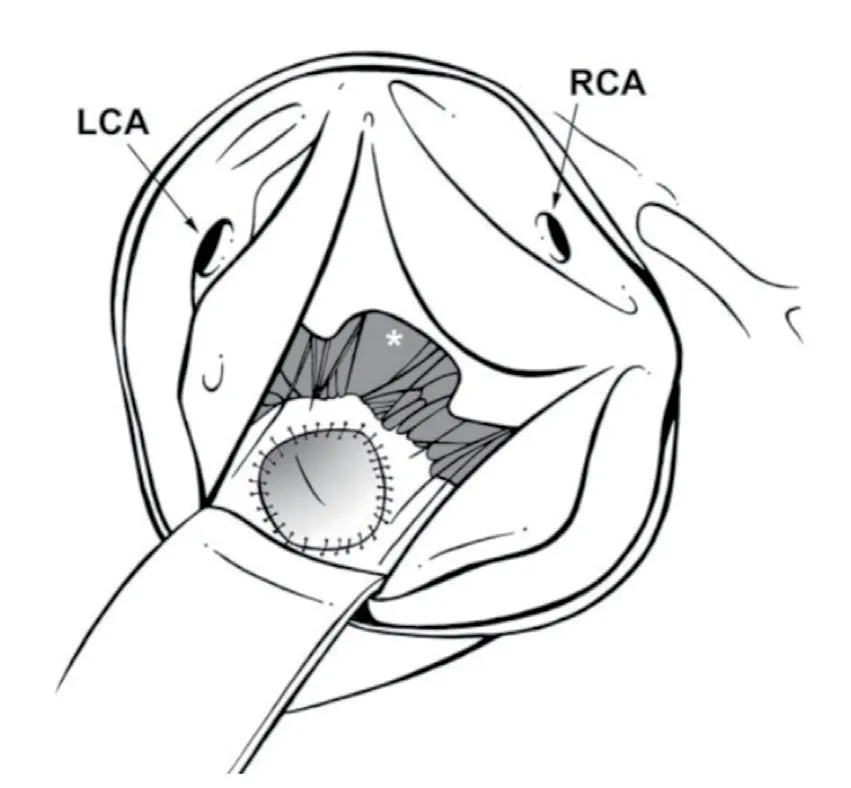
图1 二尖瓣前叶自体心包片加宽示意图
Dulguerov 等[26]在二尖瓣前叶加宽的基础上进一步联合后叶部分切除以使二尖瓣叶对合平面进一步后移(图2),降低SAM 和二尖瓣反流发生率。平均随访3.5 年,无1 例死亡。但是样本量较小,仅有16例患者。因此需要大样本量、长期随访来进一步证实。
3.2 切除-折叠-松解
圣卢克-罗斯福医学中心Balaram 等[27-29]自1997 年开始采用切除-折叠-松解术式治疗HOCM合并二尖瓣前叶和乳头肌前移患者(图3)。截至2011 年,这一中心已采用该手术方式治疗了82 例HOCM 患者,无早期死亡,左心室流出道梗阻、SAM 和二尖瓣反流显著改善。最新报道的82 例HOCM 患者与仅接受室间隔心肌切除组相比年龄较小,但左心室流出道压差更高,二尖瓣前叶长度也更长(平均37 mm),平均随访5.6 年,5 年、10 年生存率分别为98%、92%[29]。尽管Balaram 等的报道显示HOCM 合并二尖瓣前叶和乳头肌前移患者接受切除-折叠-松解术式近远期疗效良好,但是选择合适患者很重要。另外仍需真正的随机临床试验比较合并二尖瓣前叶和乳头肌异常患者分别接受两种术式的结果进一步验证这一术式的疗效与持久性。
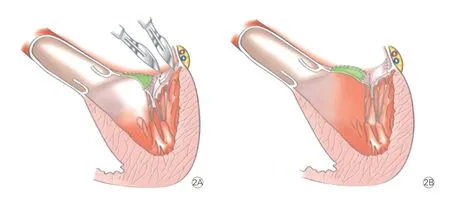
图2 二尖瓣前叶加宽联合后叶部分切除

图3 切除-折叠-松解术式示意图
3.3 腱索切除
意大利热亚那国立研究中心在39 例轻度室间隔肥厚(≤19 mm)HOCM 患者中采用室间隔心肌切除联合腱索切除并报道了术后早期结果[30]。通过术中超声和直视下探查连接到二尖瓣叶游离缘内侧的增粗、粘连或纤维化的腱索予以切除(图4)。术后血流动力学明显改善。仅有1 例术后依然为持续性重度反流,无围术期死亡。与同时期25 例轻度室间隔肥厚(≤ 19 mm)仅接受室间隔切除术HOCM 患者相比,无1 例二尖瓣环植入或二尖瓣置换,术后左心室流出道压差更低。另外,后者术后二尖瓣中到重度以上反流更多。接受室间隔切除联合腱索切除组二尖瓣前叶-瓣环比、对合面积更大提示二尖瓣叶复位到了正常的靠后的位置,研究者认为这是该组术后流出道压差更低、反流更少的直接证据。该研究的明显不足之处是随访时间太短、样本量相对小,因此需要大样本量、长期随访进一步证实。尽管如此,上述研究确实为HOCM 中轻度肥厚这一特殊人群提供一种避免室间隔穿孔、降低起搏器植入率同时有效消除梗阻与二尖瓣反流的新方法。
3.4 乳头肌重定位
克利夫兰诊所的Kwon 等[31]报道了22 例HOCM 患者接受乳头肌重定位(图5)伴或不伴室间隔心肌切除的早期结果,无围术期死亡,仅1 例因定位乳头肌的缝线撕脱需再次手术。该组患者与仅接受室间隔心肌切除组相比,室间隔相对较薄,但术前流出道压差相似,术后血流动力学改善相似,早期效果良好。此外,乳头肌重定位组术后无1 例发生严重的传导阻滞,永久起搏器植入率低。

图4 二尖瓣异常腱索切除示意图

图5 乳头肌重定位技术的手术模式图
4 小结
综上所述,行室间隔心肌切除时所联合的二尖瓣成形术本质上是针对不同二尖瓣反流机制的个体化治疗。由于目前对于HOCM 中SAM、二尖瓣反流的发生机制尚有争议,不同研究者及相关研究单位对于潜在机制认识不同,以及临床实践经验的不同,相继采用了各具特色的手术方式。尽管手术方式不同,最终都达到了消除或减轻左心室流出道梗阻、SAM 和二尖瓣反流的目的。由此提示,HOCM 中左心室流出道梗阻、SAM 和二尖瓣反流的机制可能确实是涉及到多方面的因素。因此,需要进一步研究明确各因素在HOCM 的左心室流出道梗阻、SAM 和二尖瓣反流确切机制中发挥的作用,惟其如此才能有的放矢,实现基于机制的综合性精准治疗。
利益冲突:所有作者均声明不存在利益冲突

