妙用塑料瓶 改进中学化学实验
江苏省南通市海门区正余初级中学(226153) 陆春华
塑料瓶是日常生活中的常见用品,它具有透明、密封、质软等优点。将塑料瓶应用于中学化学实验改进中,可以将教材中原本枯燥、乏味的实验变得生动、有趣,能更好地帮助学生理解和掌握化学知识,提高学习效果。笔者根据中学化学实验教学的实际情况,例举了塑料瓶在中学化学实验中的改进应用。
1 稀释浓H2SO4实验装置
1.1 实验用品
注射器、胶皮管、玻璃管、塑料瓶、墙纸刀片、pH试纸、小烧杯、培养皿、浓H2SO4、水等。
1.2 实验装置
新设计的实验装置如图1所示。
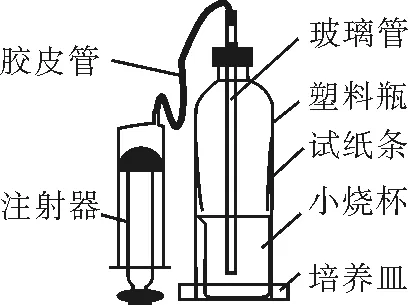
图1 稀释浓H2SO4实验装置
1.3 实验步骤
(1)取一个剪去底部的塑料瓶,用烧红的墙纸刀片在距瓶底8 cm处沿瓶身四周烫6个小孔。
(2)用一端烧红的玻璃管对准塑料瓶盖中间位置,烫出1个小孔。
(3)将pH试纸从瓶身的小孔处穿入瓶内,将其固定在塑料瓶内壁。
(4)取一长短合适的胶皮管,套在玻璃管的一端,胶皮管的另一端固定在注射器尖嘴部位。
(5)向小烧杯中注入适量的浓H2SO4,并把小烧杯放在培养皿上,用剪去底部的塑料瓶放在小烧杯上面。
(6)用注射器通过胶皮管向浓H2SO4中注入水。
(7)烧杯中产生许多雾气,液滴飞溅,pH试纸上出现很多斑点。
1.4 几点说明
(1)实验现象非常明显,给学生带来很强的视觉冲击力。
(2)玻璃管既可以用来向浓H2SO4中注入水,也可用来搅拌,使浓H2SO4与H2O混合得更加充分,释放出更多的热量,现象越发明显。
(3)材料易得,加工也很方便,具有很好的推广性。
(4)实验结束以后,要及时清洗装置,防止被浓H2SO4腐蚀。
2 自制固、液体反应发生装置
2.1 实验用品
塑料瓶、弹簧夹、乳胶管、玻璃导管、石灰石、稀盐酸等。
2.2 实验装置
新设计的实验装置如图2所示。

图2 自制固、液体反应发生装置
2.3 实验步骤
(1)在2只塑料瓶盖各钻1个小孔,再分别连接1根短玻璃导管,用玻璃胶将其密封。剪去塑料瓶b的中下部,在距离塑料瓶a底部约1 cm处钻1个小孔,将其与1根短玻璃导管连接,也用玻璃胶将其密封。用乳胶管连接去底的塑料瓶b和塑料瓶a,关闭弹簧夹B,给瓶a拧上瓶盖,在玻璃导管上连接乳胶管,并关闭弹簧夹A。
(2)制取气体,拧开a的瓶盖,向a中加入固体,盖上瓶盖,向b中加入液体,打开A和B,液体流入a中,与固体接触,反应发生了。
(3)关闭A,打开B,液体回流到b中,抬高a的高度或降低b的高度,均可使液体迅速回流到b中,反应很快就停止了,若还想让反应再次进行,可以将b瓶抬高或将a瓶降低。
(4)若需要更换液体药品,可以在液体全部流入b时,关闭B,将b中废液倒出,再向b中加液体药品,打开B,让液体药品流入a中,反应又开始了。
2.4 几点说明
(1)本实验装置适用于块状固体和液体反应制取气体,如实验室制取H2和CO2。
(2)塑料瓶是生活中常见的废弃物,利用塑料瓶进行实验,可以很好地把化学与生活紧密的联系在一起。
3 验证CO2与碱溶液反应实验装置
3.1 实验用品
塑料瓶、饱和烧碱溶液、饱和石灰水、水、二氧化碳气体、注射器、稀盐酸等。
3.2 实验装置
新设计的实验装置如图3~5所示。

图3 CO2与碱反应

图4 将稀盐酸注入反应后的A、B两瓶

图5 变瘪的A、B两瓶又重新鼓起来
3.3 实验步骤
(1)取A、B、C 3只大小、形状一样的塑料瓶,并分别收集满CO2气体,再分别向其中注入等体积的饱和NaOH溶液、饱和Ca(OH)2溶液和水,并将3只塑料瓶振荡相同的次数,发现A瓶变瘪程度最明显,B瓶略有变瘪,C瓶几乎无明显现象,实验现象如图3所示。由此可知,CO2能与NaOH、Ca(OH)2溶液发生反应,且与NaOH反应程度更为明显。此外,还可由Ca(OH)2溶液与CO2作用有白色沉淀生成、NaOH与CO2反应使瓶子变瘪程度更大等现象分析可知,检验CO2用Ca(OH)2溶液,吸收CO2用NaOH溶液。
(2)再分别用2支一样规格的注射器分别吸取等量的稀盐酸,再分别向上述反应后的A、B 2瓶注入等体积、等浓度的稀盐酸,发现瓶内都有气泡出现,变瘪的A、B 2瓶口又重新鼓起来,如图4、5所示,则说明CO2与碱溶液的确发生了反应。
3.4 几点说明
(1)根据塑料瓶变瘪的程度来设计对比实验,借助产生的可视化现象,化“隐性”为“显性”,说明CO2与碱溶液发生了反应。
(2)由于溶液中均含有H2O,且CO2能溶于水,用此设计实验时,巧妙地避免了由于水的存在而造成的对实验的干扰,并排除了这一可能。
4 气体溶解度受外界因素影响实验装置
4.1 实验用品
塑料瓶、冷水、白醋、纯碱、大碗、沸水等。
4.2 实验装置
新设计的实验装置如图6所示。
4.3 实验步骤
(1)向一塑料瓶中注入约300 mL冷水,再注入50 mL白醋,振荡、使其混合均匀,再向塑料瓶中加入2 g纯碱,发现塑料瓶中立刻出现大量气体(Na2CO3+2CH3COOH=H2O+2CH3COONa+CO2↑),实验现象如图6(a)所示。

(a)
(2)用拇指堵住塑料瓶口,如图6(b)所示,瓶中压强变大,此时瓶中仍在产生气泡。待反应结束时,移开拇指,发现塑料瓶中又开始出现大量气泡(CO2气体)。这是因为移开拇指后,瓶中压强变小,原先溶解在水中的CO2气体不断逸出,则说明温度不变时,压强变小,气体溶解度下降。
(3)待步骤(2)结束,水中不再有CO2气体逸出时,将塑料瓶放入一盛有2/3容积沸水的大碗中,如图6(c)所示。此时,塑料瓶内温度升高,瓶内就有大量气泡产生,则说明当压强不变时,温度升高,气体溶解度下降。
4.4 几点说明
(1)材料易得,所选塑料瓶、白醋、大碗均是日常生活用品。
(2)操作简便,适合学生分组实验,提高了学生的动手操作能力,培养了学生学习化学的兴趣。
5 钠和水反应实验装置
5.1 实验用品
塑料瓶、剪刀、乳胶管、水槽、坩埚钳玻璃管、弹簧夹、注射针(截去尖端部位)、铁架台、钠等。
5.2 实验装置
新设计的实验装置如图7所示。

图7 钠和水反应实验装置
5.3 实验步骤
(1)取1个大小合适的塑料瓶、剪去瓶底,在塑料瓶盖上打1小孔,插入玻璃管后密封,再连接夹有弹簧夹的乳胶管和注射针。
(2)将塑料瓶固定在铁架台上,使塑料瓶底浸入水中2 cm(玻璃管下端套一合适的塑料管,当弹簧夹关闭时,即使装置浸入水中,水也不会倒流入玻璃管,当打开弹簧夹时,H2能顺利排出)。
(3)关闭弹簧夹,将塑料瓶倾斜浸没在水中,将瓶中空气排尽。如图7所示,将塑料瓶固定在铁架台上。
(4)用坩埚钳将一小块钠迅速放在塑料瓶口的下方,钠和水反应,迅速脱离坩埚钳,钠开始熔化,并悬浮于塑料瓶内的水面上。
(5)待完全反应后,将塑料瓶尽可能下移至水面下方固定,再把弹簧夹打开,将气体点燃,气体燃烧产生淡蓝色火焰,则说明生成了H2。
5.4 几点说明
(1)由于钠熔化时会有少许钠粘在塑料瓶内壁,极易造成塑料瓶壁破裂,因此本实验最好选用瓶壁较厚的塑料瓶。
(2)为防止熔化的钠导致塑料瓶破裂,可在塑料瓶内壁涂一层植物油。
(3)钠的用量不宜过多,过多可能会引起爆炸。实验中钠的质量最好不要超过0.2 g。
6 分子运动实验装置
6.1 实验用品
塑料矿泉水瓶、塑料吸管、注射器、烧杯、棉签、酚酞溶液、浓氨水等。
6.2 实验装置
新设计的实验装置如图8所示。

图8 分子运动实验装置
6.3 实验步骤
(1)在吸管上交叉插5根棉签,在棉签上各滴加2滴酚酞溶液。将吸管放入广口塑料瓶中,拧紧瓶盖。
(2)用注射器抽取2 mL浓NH3·H2O,并从塑料瓶底将其注入,不一会儿,棉签由下往上依次变红。
(3)若将塑料瓶底置于热水中进行实验,棉签变色更快(也可另取一套相同的实验装置放在冷水中进行实验,两组实验同时进行,更具说服力)。
(4)实验结束后,清洗实验装置,以便下次再用。
6.4 几点说明
(1)实验现象十分明显,证明分子在不断运动的同时,还可以证明温度越高,分子运动速率越快。
(2)材料易得,成本低,在不影响实验效果的前提下还能更好的培养学生动手操作能力。
7 铜和稀硝酸反应实验装置
7.1 实验用品
塑料瓶、橡皮塞、铜丝、稀HNO3等。
7.2 实验装置
新设计的实验装置如图9、10所示。

图9 将铜丝插入橡皮塞中部
7.3 实验步骤
(1)取1个容积为200 mL的塑料瓶,找1个与塑料瓶口匹配的橡皮塞,取1根长短合适的铜丝,将其一端拧成螺旋状,另一端插入橡皮塞口径较小一侧的中部,如图9所示。
(2)向塑料瓶中加入约半瓶稀HNO3,用手慢慢挤压塑料瓶(一定要慢,防止稀HNO3溢出)外壁,使稀HNO3液面缓慢上升至离瓶口1 cm处。
(3)用插有铜丝的橡皮塞迅速塞紧瓶口,铜丝与稀HNO3在塑料瓶内发生反应,发现瓶内有无色气体产生,溶液由无色慢慢变为绿色,变瘪的塑料瓶又重新鼓起,瓶内液面逐渐下降,铜丝与稀HNO3分离,反应停止。
(4)再将塑料瓶放倒,铜丝与稀HNO3又重新反应,瓶内液体颜色越来越深,且仍有无色气体生成,塑料瓶体积慢慢变大,如图10所示。
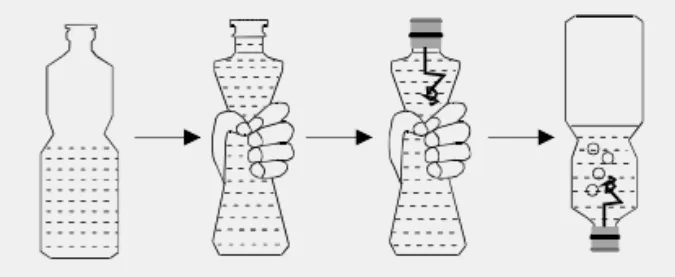
图10 铜丝与稀HNO3反应
(5)再把塑料瓶倒放过来,使瓶口向上,缓缓松开橡皮塞,使少许NO逸出,迅速将橡皮塞塞紧,发现瓶内有红棕色气体出现。
7.4 几点说明
(1)本实验装置简易,操作简便。塑料瓶是日常生活用品,适合实验器材缺乏的学校开展实验教学时使用,也适用于学生家庭实验。
(2)塑料瓶可变性强,可以很好地将瓶中空气排尽,防止NO被氧化,更能清晰地看到NO是一种无色气体。
(3)本实验装置的密封性好,生成的NO几乎没有逸出,避免了环境污染。
(4)本实验装置可以重复多次使用,具有很好的推广性。
(5)实验结束后,切不可将稀HNO3久置于塑料瓶中,否则塑料瓶会被腐蚀,影响下次实验。
8 结语
改进化学实验,可以提高学生的学习兴趣,激发学生学习化学的潜能。选用塑料瓶来改进中学化学实验变废为宝,材料易得,操作简便,装置经过清洗后可多次使用。

