银杏达莫注射液溶血试验方法研究及结果评价
葛丽萍,颜 皓,韩 峰
(内蒙古药品检验研究院,内蒙古 呼和浩特 010010)
中药注射剂是我国医药产业重要的组成部分,其药理药效以及安全性研究越来越受到药学研究人员的重视。银杏达莫注射液为心脑血管扩张药,用于预防和治疗冠心病、血栓栓塞性疾病。考虑到中药制剂的成分复杂,尤其一些中药注射剂,由于含有溶血成分或是杂质等,易引起过敏、溶血等严重不良反应。因此,本实验通过两种不同检测方法对其安全性指标进行考察,为保证中药注射剂临床使用安全和制剂质量的可控性提供依据。
1 试验试剂、动物及仪器
1.1 受试检品:银杏达莫注射液
厂家:A制药股份有限公司,B药业股份有限公司,C制药有限公司
规格:5mL,10mL
1.2 试剂:氯化钠注射液,规格:100mL
厂家:青州尧王制药有限公司
1.3 实验动物:家兔
来源:北京市海淀区兴隆实验动物养殖场,合格证编号:SCXK(京)2011-0006。
饲料来源:北京科澳协力饲料有限公司,证号:SCXK(京)2005-0007。
1.4 仪器
UV-2550 紫外分光光度计(厂家:岛津)SKP-01型电热恒温培养箱(厂家:湖北黄石市医疗器械厂)DL-5000型离心机(厂家:菲恰尔)
1.5 实验环境:内蒙古药品检验药检院药理动物实验室
使用许可证号:SYXK(蒙)2011-001
2 实验方法
2.1 体外试管溶血法[1](试管观察法)
2.1.1供试品溶液配制:量取5mL银杏达莫注射液加入至100mL0.9%氯化钠注射液中,摇匀,作为供试品溶液。
2.1.2取兔血,放入含玻璃珠的三角烧瓶中振摇10分钟,加入0.9%氯化钠溶液约10倍量,摇匀,离心15分钟,除去上清液,沉淀细胞再用0.9%氯化钠溶液按上述方法洗涤2~3次,至上清液不显红色。将所得红细胞用0.9%氯化钠溶液配成2%的混悬液,供试验用。
2.1.3取洁净试管7只, 1~5号管为供试品管,6、7号管分别为阴性、阳性对照管。各管依次加入2%红细胞悬液、0.9%氯化钠溶液、纯化水、供试品溶液(见表1),混匀后,置37℃恒温箱中温育,开始每隔15分钟观察1次,1小时后,每隔1小时观察1次,观察3小时。

表1 试剂加入量
2.1.4结果判断标准
若试验中的溶液呈澄明红色,管底无细胞残留或少量红细胞残留,表明有溶血发生;如细胞全部下沉,上清液体无色澄明,表明无溶血发生[1]。
2.1.5试验结果
对94批次银杏达莫注射液进行溶血检验,结论均为合格。
2.2 改进的溶血性试验[2](分光光度法)
2.2.1供试品溶液配制:同1.1。
2.2.2同1.2。
2.2.3取洁净试管12只,进行编号,1~5号管为供试品管,6~10号管为供试品对照管,11、12号为阴性、阳性对照管。按下表所示依次加入2%红细胞悬液、0.9%氯化钠溶液或纯化水、受试物,混匀后,置37℃恒温箱中进行温育3小时。

表2 试剂加入量
2.2.4将上述各管溶液,1100 转/分钟离心5分钟。
2.2.5结合指导原则,以纯化水为空白,选取545nm波长处检测上述各管的吸光度(OD)值。
2.2.6溶血率按照下式进行计算:溶血率=(A供试品试验管-A供试品对照管-A阴性对照管)/(A阳性对照管-A阴性对照管)×100%
2.2.7结果判断标准
溶血率>5%表明有溶血发生。
2.2.8实验结果:见表3。
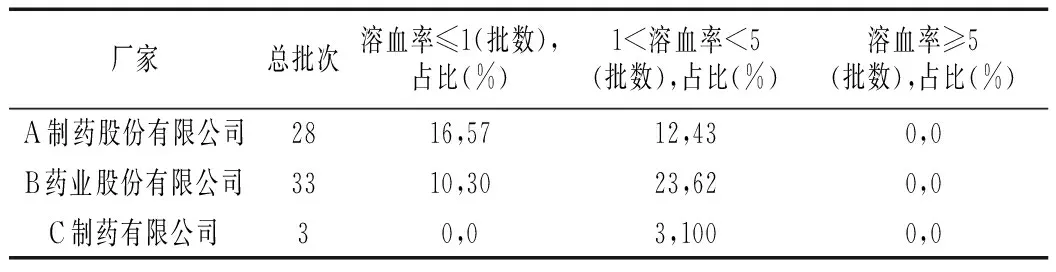
表3 实验结果
3 结果分析总结
根据溶血率判定标准,上述检测的64批银杏达莫注射液的溶血率均小于5%,全部合格。其中,检测A药业股份有限公司样品28批,占检测总量43.75%;检测B制药股份有限公司样品33批,占检测总量51.56%;检测C制药有限公司样品3批,占检测总量4.69%。检测结果中溶血率≥1%的样品共有37批,其中A药业股份有限公司样品占29.73%;B制药股份有限公司样品占62.16%;C制药有限公司样品占8.57%。
在对94批银杏达莫注射液进行完常规体外试管溶血法(试管观察法)检测后,并得出全部合格的结论后,又从其中选取了64批样品(包括本次抽检的3个厂家及其不同规格的产品)并采取了改进的体外溶血性试验法(分光光度法)进行验证,使得本次银杏达莫注射液的溶血试验检测更为准确,数据更为详实。通过分光光度法检测结果的比较,可以看出,B、C企业产品的溶血偏高的占比较大,存在一定的安全风险,有必要加强产品质量控制。
分光光度法与常规方法比较,操作比较复杂,但可以作为常规方法有效补充,可以更直接准确地反映制剂对血细胞的影响。当采用常规法测定的结果有疑问时,可采用分光光度法作为辅助方法,帮助对结果进行更为精确的判断。

