HPLC法同时测定葡萄糖酸钙锌口服溶液中盐酸赖氨酸与苯甲酸钠的含量
李梓莹
葡萄糖酸钙锌口服溶液是以苯甲酸钠为防腐剂,由葡萄糖酸钙、葡萄糖酸锌和盐酸赖氨酸组成的复方制剂,临床多用于治疗因缺钙、缺锌引起的疾病,包括佝偻病、小儿生长发育迟缓、食欲缺乏、厌食症等[1]。其中盐酸赖氨酸为人体必需氨基酸,可促进钙吸收,增加骨结合蛋白的含量,促进身体生长发育,还对脑组织缺血、缺氧性疾病有保护作用,可调节体内氮代谢平衡[2]。目前盐酸赖氨酸的测定方法多为衍生化[3]或梯度洗脱[4]的高效液相色谱法(HPLC),存在操作繁琐、分析时间长、衍生物试剂不易得到等问题。苯甲酸钠价廉易得,但其毒副作用随着其广泛应用也日渐突出,比如具有纺锤体毒剂的作用,存在基因遗传毒性[5]、导致染色体断裂,对哺乳动物骨髓细胞具有致突变作用[6],可能影响动物受精过程,存在生殖毒性,有轻度的积蓄作用等[7],大量饮用含苯甲酸钠防腐剂的饮料会刺激胃肠道,影响钙的吸收,诱发急性荨麻疹、血管性水肿,导致大脑严重萎缩[8-10]。国外已经开始禁止苯甲酸钠的使用,但国内仍在食品和药物制剂中作为防腐剂被广泛使用[4]。
《中国药典》暂未收载葡萄糖酸钙锌口服溶液这一品种剂型,且无相关文献收载有关葡萄糖酸钙锌口服溶液中苯甲酸钠的量的控制测定方法。鉴于苯甲酸钠的量会影响该药的吸收及疗效,甚至有可能产生严重的毒副作用,临床上该药除成人外也用于婴幼儿,婴幼儿多体弱,故检测葡萄糖酸钙锌口服溶液中苯甲酸钠含量十分必要。本文建立HPLC分析方法,同时测定葡萄糖酸钙锌口服溶液中盐酸赖氨酸和苯甲酸钠的含量,并进行相关的方法学研究及考察,操作快捷简便、专属性强,测定结果准确、可靠、稳定。现报道如下。
1 仪器与试剂
1.1 仪器 Agilent 1260型高效液相色谱仪Chemstation色谱工作站,美国安捷伦科技有限公司,MT5型电子天平,梅特勒托利多仪器有限公司(精度:0.001 mg)。
1.2 试药 盐酸赖氨酸对照品(中国食品药品检定研究院,批号:140673-201509),苯甲酸钠对照品(中国食品药品检定研究院,批号:100433-201702);葡萄糖酸钙锌口服溶液(由湖北福人金身药业有限公司、澳洛(中国)制药有限公司、湖北午时药业股份有限公司提供),乙腈为色谱纯,德国默克公司;磷酸、磷酸氢二钾、辛烷磺酸钠为分析纯,水为纯化水。
2 方法与结果
2.1 色谱条件 色谱柱:Agilent Zobarx C18(250 mm×4.6 mm,5 μm);流动相K2HPO4缓冲液(取K2HPO42.2822 g,加水溶解并稀释至1 000 ml,用H3PO4调pH值至4.8,加1.08 g辛烷磺酸钠)—乙腈(90∶10),流速1.0 ml/min,检测波长203 nm,柱温40 ℃,进样量10 μl。
2.2 溶液的制备
2.2.1 供试品溶液的制备:取本品3 ml(约相当于盐酸赖氨酸30 mg),置100 ml量瓶中,加水定容至刻度,摇匀。
2.2.2 对照品溶液的制备:取盐酸赖氨酸对照品6 mg、苯甲酸钠对照品1 mg,置20 ml量瓶中,加水超声溶解并定容至刻度,摇匀,制成每毫升中约含0.3 mg/ml盐酸赖氨酸及0.05 mg/ml苯甲酸钠的溶液。
2.2.3 阴性空白溶液的制备:取处方量辅料,加水搅拌溶解,加入处方量葡萄糖酸钙、葡萄糖酸锌搅拌溶解后加水定容至最终体积;取上述溶液3 ml,置100 ml量瓶中,加水定容至刻度,摇匀,作为阴性空白溶液。
2.3 检测限及定量限
2.3.1 检测限:检测限溶液配制:分别取盐酸赖氨酸线性1溶液、苯甲酸钠线性1溶液逐步稀释。以S/N=3计算,盐酸赖氨酸检测限为4.211 μg/ml,苯甲酸钠检测限为0.0754 μg/ml。
2.3.2 定量限:分别取盐酸赖氨酸线性1溶液、苯甲酸钠线性1溶液,作为各自组分的检测限溶液。以S/N=10计算,盐酸赖氨酸定量限为20.39 μg/ml,苯甲酸钠定量限为0.1142 μg/ml。
2.4 耐用性试验 本文考察3种不同厂牌和型号的色谱柱:(1)Agilent Zobarx C18(250 mm×4.6 mm,5 μm)(2)Kromasil C18(250 mm×4.6 mm,5 μm)(3)Inersil ODS-3 C18(250 mm×4.6 mm,5 μm)主成分峰形均良好(盐酸赖氨酸理论塔板数均≥7 000,苯甲酸钠理论塔板数均≥4 000),且能达到较好的分离效果,表明该方法耐用性较好。
2.5 线性关系考察
2.5.1 盐酸赖氨酸线性范围:取盐酸赖氨酸对照品50.397 mg,置25 ml量瓶中,加水溶解后,加水定容至刻度,摇匀,作为对照品贮备溶液。再精密量取3、3、1、3、3、3 ml分别置200、100、20、20、10、5 ml量瓶中,加水定容至刻度,摇匀,即得线性试验用系列浓度的溶液。按浓度从小到大的顺序取各溶液分别进样10 μl,注入液相色谱仪,记录色谱图。以峰面积(Y)对浓度(X)进行线性回归,线性方程为Y=3.47650×102X-0.3784,相关系数r=1.0000(n=6)。结果表明,盐酸赖氨酸浓度在0.03~1.21 mg/ml范围内,呈良好的线性关系。
2.5.2 苯甲酸钠线性范围:取苯甲酸钠对照品6.174 mg,置25 ml量瓶中,加水溶解后,加水定容至刻度,摇匀,作为对照品贮备溶液。再精密量取2、2、2、2、2、4 ml分别置50(再精密量取1 ml置25 ml量瓶)、250、50、10、5、5 ml量瓶中,加水定容至刻度,摇匀,即得线性试验用系列浓度的溶液。按浓度从小到大的顺序取各溶液分别进样10 μl,注入液相色谱仪,记录色谱图。以峰面积(Y)对浓度(X)进行线性回归,线性方程为Y=5.07706×104X+1.41985×101,相关系数r=1.0000(n=6)。结果表明,苯甲酸钠浓度在0.39~196.98 μg/ml范围内,呈良好的线性关系。
2.6 系统专属性试验 分别精密量取供试品溶液、对照品溶液、阴性空白溶液各10 μl注入液相色谱仪,记录色谱图,结果均无干扰。见图1、图2、图3。
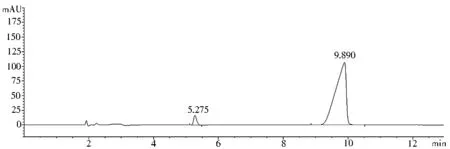
图1 对照品溶液HPLC图(盐酸赖氨酸保留时间为5.3 min,苯甲酸钠保留时间为9.8 min)
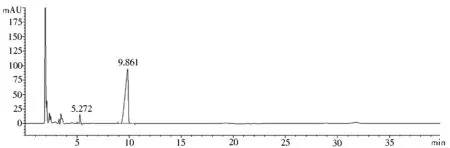
图2 供试品溶液HPLC图
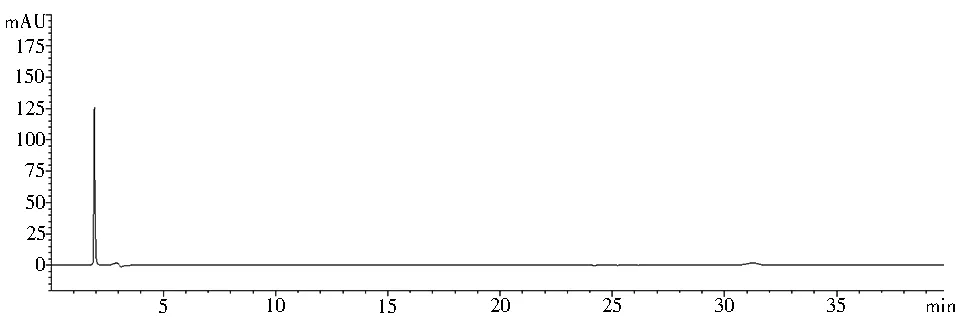
图3 阴性空白溶液HPLC图
2.7 破坏性试验 (1)酸破坏:取本品3 ml,置100 ml量瓶中,加0.1 mol/L盐酸2 ml,室温放置1 h后加0.1 mol/L氢氧化钠溶液2 ml中和,加水定容至刻度,摇匀。(2)碱破坏:取本品3 ml,置100 ml量瓶中,加0.1 mol/L氢氧化钠溶液2 ml,室温放置1 h后加0.1 mol/L盐酸2 ml中和,加水定容至刻度,摇匀。(3)氧化破坏:取本品3 ml,置100 ml量瓶中,加30%过氧化氢溶液1 ml,室温放置1 h,加水定容至刻度,摇匀。(4)光破坏:取本品3 ml,置100 ml量瓶中,254 nm照射15 min,加水定容至刻度,摇匀。(5)高温破坏:取本品3 ml,置100 ml量瓶中,沸水浴30 min,放冷,加水定容至刻度,摇匀。样品在高温与氧化条件不稳定,易产生降解产物。见图4。
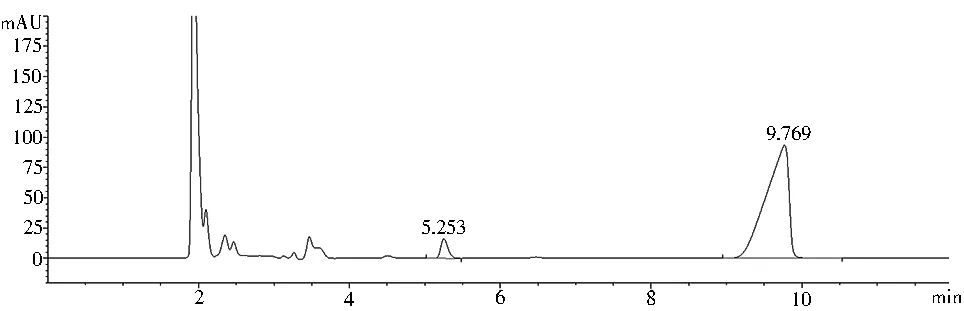
A
2.8 精密度实验 分别取盐酸赖氨酸线性4溶液、苯甲酸钠线性4溶液,连续重复进样10 μl(n=6),测定峰面积的RSD%分别为0.4%、0.2%。
2.9 稳定性实验 取供试品溶液于室温放置,分别于0、5、10、12、18 h进样10 μl,样品中盐酸赖氨酸与苯甲酸钠峰面积基本保持不变,RSD%分别为0.9%、0.2%,即样品在18 h内稳定。
2.10 加样回收实验
2.10.1 盐酸赖氨酸回收率实验:精密量取样品3 ml,置10 ml量瓶中,加水定容至刻度,摇匀,作为供试品贮备溶液。分别精密称取盐酸赖氨酸对照品1.8、3、4.2 mg各3份,置20 ml量瓶,分别精密加入供试品贮备溶液1 ml,加水定容至刻度,摇匀,经0.45 μm滤膜滤过,取续滤液各10 μl注入液相色谱仪,盐酸赖氨酸含量测定的平均回收率为101.06%,RSD%为0.8%。
2.10.2 苯甲酸钠回收率实验:分别精密称取苯甲酸钠对照品2.5、4、5.5 mg各3份,置200 ml量瓶,分别精密加入样品3 ml,加水定容至刻度,摇匀,经0.45 μm滤膜滤过,取续滤液各10 μl注入液相色谱仪,苯甲酸钠含量测定的平均回收率为100.27%,RSD%为0.7%。
2.11 样品测定结果 见表1。
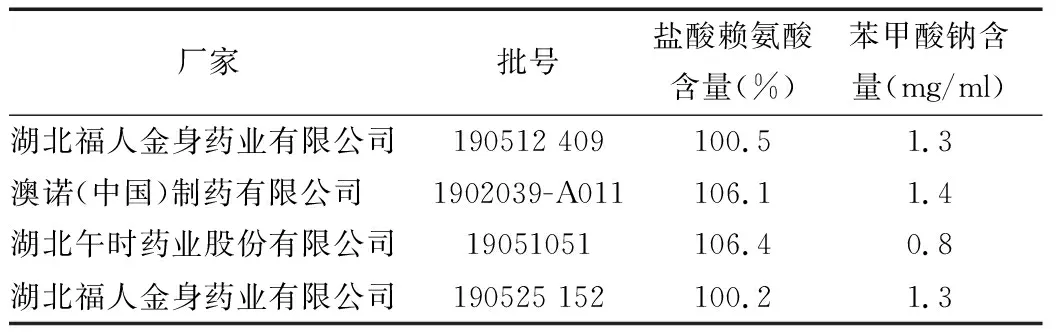
表1 样品中盐酸赖氨酸及苯甲酸钠含量测定结果 (n=4)
3 讨 论
3.1 波长选择 用DAD检测器对各自对照品进行扫描,结果葡萄糖酸钙、葡萄糖酸锌、盐酸赖氨酸无最大吸收,苯甲酸钠除226 nm有最大吸收外另无最大吸收,选择末端吸收203 nm与226 nm检测苯甲酸钠,峰形无明显变化,峰面积基本一致,考虑要同时测定盐酸赖氨酸及苯甲酸钠的含量,故选择末端吸收203 nm作为测定波长。由于葡萄糖酸钙、葡萄糖酸锌光谱图均一致,为葡萄糖酸的响应图谱,故不考虑在选定的色谱条件下同时测定这两种组分的含量,只考察这两种组分在选定的色谱条件下对方法是否存在干扰。
3.2 流动相中有机相类别的选择及是否应添加离子对试剂 由于甲醇截止波长为205 nm,盐酸赖氨酸及苯甲酸钠均需采用末端检测波长,为了减少溶剂对检测的干扰,改为用乙腈作为有机相洗脱。同时参考文献,由于盐酸赖氨酸含有2个伯氨基、1个羧基,极性较大, 单纯采用磷酸二氢钾溶液和乙腈为流动相时难以保留,过早出峰导致检测存在误差,无法定量作其含量测定的检查。在流动相中添加适量的离子对试剂,可以使其保留能力明显改善,延迟其出峰时间,使其能准确积分定量。
3.3 柱子类型的选择 参照葡萄糖酸钙锌口服溶液YBH37212005标准中盐酸赖氨酸含量的测定方法进行试验。采用氨基键合硅胶为填充剂的色谱柱,以0.05 mol/L磷酸二氢钾溶液—乙腈溶液(乙腈—水(10∶1)(30∶70)为流动相,流速为1.0 ml/min,检测波长为203 nm,柱温为40 ℃。试验表明,苯甲酸钠在该色谱条件下,较早出峰,与溶剂峰、葡萄糖酸钙、葡萄糖酸锌重叠在一起。经多种调试,苯甲酸钠峰均未能与溶剂峰、葡萄糖酸钙、葡萄糖酸锌峰完全分离,分离度达不到要求无法准确积分定量,故放弃选用氨基键合硅胶为填充剂的色谱柱。参考文献[2-3,11],无论是衍生化方法还是梯度方法,多用C18柱做盐酸赖氨酸的含量测定检查,故选用C18柱进行试验。
3.4 流动相pH值的选择 参照葡萄糖酸钙锌口服溶液YBH02122016标准中苯甲酸钠含量测定测定方法进行试验。以0.05 mol/L磷酸二氢钾溶液—甲醇(70∶30)为流动相,流速为1.0 ml/min,检测波长为224 nm,柱温为30 ℃。在该色谱条件下,葡萄糖酸钙、葡萄糖酸锌、盐酸赖氨酸与溶剂峰均有部分重叠,无法完全分离,而苯甲酸钠峰形良好,可以避免样品中其他成分及辅料的干扰。0.05 mol/L磷酸二氢钾溶液pH值为4.8,故参考该标准,用磷酸调pH值至4.8,同时试验用磷酸调节pH值至6.5、3.5的情况,考察流动相pH值的影响。pH值为4.8时,盐酸赖氨酸与苯甲酸钠峰形良好,出峰时间适中(图1)。pH值为6.5时,盐酸赖氨酸与苯甲酸钠峰形良好,但苯甲酸钠出峰时间过早与溶剂峰、辅料峰才刚达到分离度1.5(苯甲酸钠保留时间为2.3 min,盐酸赖氨酸保留时间为5.1 min(图5),故不采用该pH条件。pH值为3.5时,苯甲酸钠保留时间为31.4 min,考虑到样品中还有辅料峰在苯甲酸钠峰后出峰,分析时间过长,分析效率低(图6),故不采用该pH条件。综合考虑溶剂峰、辅料峰的干扰、分析时间的长短、峰形是否良好,最后确定流动相pH值为4.8。
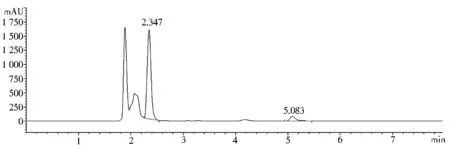
图5 用磷酸调pH值至6.5为流动相的供试品溶液HPLC图
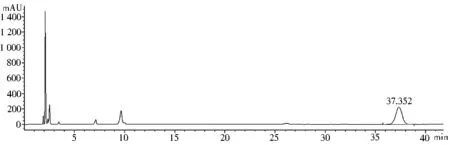
图6 用磷酸调pH值至3.5为流动相的供试品溶液HPLC图
4 结 论
实验结果表明,采用HPLC法同时测定葡萄糖酸钙锌口服溶液中盐酸赖氨酸和苯甲酸钠的含量,精密度良好,有较高的准确度,可以避免样品中其他成分及辅料的干扰,操作简便,灵敏度高,测定结果准确,线性范围及回收率等均符合系统适用性要求,可快速有效检测葡萄糖酸钙锌口服溶液中盐酸赖氨酸和苯甲酸钠的含量,从而保证样品的质量,保障患者用药安全。

