O/W型山苍子精油微乳的制备及其性能研究
程 晨,司红燕,王宗德,廖圣良,邹晨阳,王 鹏
(江西农业大学 林学院;国家林业草原木本香料(华东)工程技术研究中心,江西 南昌 330045)
山苍子(Litseacubeba(Lour.) Pers.)是我国特有的香料植物资源之一,山苍子精油年产量达4 000余吨[1]。山苍子精油不仅具有柠檬的香气[2],而且还具有抑菌、抗氧化、抗炎抗癌以及杀虫等多种生物活性[3-5],在医药、农业、食品和化妆品等领域有广阔的应用前景。但是,目前我国山苍子精油资源的深加工利用率较低,长期以出口初级山苍子精油为主,主要是由于山苍子精油的水溶性低和易挥发等特点降低了其生物利用度,限制了山苍子精油的应用以及其整个产业的发展[6-8]。目前将山苍子精油微胶囊化和微乳化是提高其生物利用度最常用的2种方法。但微胶囊技术存在操作繁琐、成本较高、产品粒径较大等问题,而微乳是由油相、水相、表面活性剂和助表面活性剂按照一定比例自发形成的各向同性的热力学稳定体系[9],具有粒径小且均匀、外观澄清透明、制备简单以及各项性能稳定等特点。因此将山苍子精油制成水包油(O/W)型微乳,不仅可以提高山苍子精油的水溶性、降低其挥发性,而且能够降低成本,提高其深加工利用率和经济价值。而关于山苍子精油微乳方面的研究还鲜有报道。本研究以山苍子精油为油相,探究制备O/W型山苍子精油微乳的制备条件并对其性能进行测试分析,以期提高山苍子精油的水溶性,降低其挥发性,进一步提高其应用价值,为山苍子精油高附加值产品的开发提供理论支撑。
1 实 验
1.1 试剂与仪器
山苍子精油(柠檬醛质量分数69.21%),采购于江西省大坑乡山苍子精油提取工厂。聚氧乙烯蓖麻油-35(CremopHor EL-35),德国巴斯夫公司;聚氧乙烯蓖麻油-30(EL-30),江苏省海安石油化工厂;曲拉通X-100(Triton X-100),聚乙二醇400(PEG-400),以上试剂均为化学纯。2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(ABTS),98%,阿拉丁试剂公司;无水乙醇、甘油、1,2-丙二醇、无水硫酸钠、2,6-二叔丁基对甲酚(BHT)、吐温-80(Tween-80),分析纯。
DDS-307电导率仪,上海仪电科学有限公司;多角度粒度及高灵敏度Zeta电位仪,美国布鲁克海文公司;双光束紫外可见分光光度计,北京普析通用仪器有限责任公司;NDJ-8S数字旋转黏度计;7694E顶空进样器、7890B-5977A气相色谱-质谱(GC-MS)联用仪,美国安捷伦科技有限公司。
1.2 山苍子精油微乳的制备
1.2.1微乳拟三元相图的绘制 利用传统的三元相图可观察三组分体系中3个变量对整个体系结构的影响,而超过3个变量的体系则无法分析。绘制拟三元相图是在三元相图的基础上加以改进,通过合并变量使实际的变量变成3个,从而达到可以分析各变量对整个组分体系的影响的目的[10]。
山苍子精油微乳体系包含4个组分,表面活性剂、助表面活性剂、山苍子精油和去离子水。采用加水法制备山苍子精油微乳,先将表面活性剂与助表面活性剂按一定比例搅拌均匀,再将两者混合物与山苍子精油分别按照9 ∶1、8 ∶2、7 ∶3、6 ∶4、5 ∶5、4 ∶6、3 ∶7、2 ∶8、1 ∶9的质量比进行混合,表面活性剂、助表面活性剂和山苍子精油的总质量为5 g。将3种成分充分搅拌均匀后,边搅拌边缓慢滴加去离子水。通过观察体系的外观形态变化,即整个体系由浑浊变为澄清透明再到浑浊的变化点,确定山苍子精油微乳形成的临界点。根据确定的临界点,以山苍子精油、去离子水和混合表面活性剂(表面活性剂与助表面活性剂的混合物)为拟三元相图的三个顶点,利用Origin 2017软件绘制拟三元相图,确定山苍子精油微乳的区域,然后用 AutoCAD(2008)计算微乳区域的面积占拟三元相图总面积的比例。
1.2.2微乳制备条件的优化
1.2.2.1表面活性剂的筛选 固定制备温度为25 ℃,选择Tween-80、EL-30、EL-35和Triton X-100这4种无毒的非离子表面活性剂来制备山苍子精油微乳,分别将这4种表面活性剂与助表面活性剂无水乙醇按质量比2 ∶1的比例混合均匀作为混合表面活性剂,绘制拟三元相图,比较微乳区域面积的大小,确定最佳表面活性剂。
1.2.2.2助表面活性剂的筛选 固定制备温度为25 ℃,助表面活性剂分别选取PEG-400、无水乙醇、1,2-丙二醇和丙三醇,将优选的表面活性剂分别和这4种助表面活性剂以质量比2 ∶1的比例均匀混合,绘制拟三元相图,比较各微乳区域面积的大小。
1.2.2.3Km值的筛选 固定制备温度为25 ℃,选取选优之后的表面活性剂/助表面活性剂用于制备微乳。表面活性剂/助表面活性剂的质量比(Km)值分别选取0.5、1、2和3,绘制拟三元相图,比较各微乳区域面积的大小。
1.2.2.4制备温度的筛选 选取优选之后的表面活性剂/助表面活性剂用于制备微乳。在Km值为2的条件下,分别在15、25、35和45 ℃下制备山苍子精油微乳,绘制拟三元相图,比较各微乳区域面积的大小。
1.2.2.5正交试验 根据单因素试验的结果,进一步选取表面活性剂类型、助表面活性剂类型、Km值和制备温度的3个较优水平,设计4因素3水平的正交试验。通过极差分析,获得山苍子精油微乳的最佳制备条件。
1.3 O/W型山苍子精油微乳性能分析
1.3.1微乳类型测定 采用电导率仪测定微乳体系的电导率,当电导率上升时,微乳为油包水(W/O)型;当电导率由最高值开始下降时,微乳为水包油(O/W)型[11]。
1.3.2微乳稳定性
1.3.2.1标样1的制备 以Triton X-100为表面活性剂,无水乙醇为助表面活性剂,Km值为1,混合表面活性剂与油质量比(S/O)值为9 ∶1,含水率为70%(以微乳总质量计,下同),制得O/W型山苍子精油微乳,记为标样1。
1.3.2.2温度稳定性测试 取等量的山苍子精油微乳分别放入15、25、35和45 ℃的恒温水浴锅里静置20 min,观察其外观形态,如果外观形态无分层或浑浊现象,表示微乳稳定,反之则不稳定。
1.3.2.3离心稳定性测试 在室温下,取等量的山苍子精油微乳分别在1 000、2 000、3 000和4 000 r/min的转速下离心20 min,观察其外观形态。如果外观形态无分层或浑浊现象,表示微乳稳定,反之则不稳定。
1.3.3微乳物理性质 室温下,分别采用多角度粒度及高灵敏度Zeta电位仪、电导率仪、pH计测试微乳标样1的粒径、多分散系数(PDI)、电导率和pH值,均循环测定3次。
1.3.4微乳水溶性 室温下,准确称取等量的山苍子精油、山苍子精油微乳标样1、去离子水置于3个相同的玻璃器皿中。加入相同量、相同浓度的水溶性染料亚甲基蓝水溶液,静置1 min,通过观察亚甲基蓝水溶液在3种不同溶液中的扩散速度来分析微乳水溶性。
1.3.5微乳缓释性 利用GC-MS,通过静态顶空气相色谱法测试山苍子精油微乳标样1和山苍子精油中主成分柠檬醛的含量,对比精油和微乳在同等时间挥发出来的气体内的柠檬醛含量变化,从而对微乳的缓释性进行分析。GC条件:色谱柱为HP-5MS弹性石英毛细管柱(30 m×250 μm×0.25 μm);程序升温,60 ℃(保持16 min),以5 ℃/min升至180 ℃,以10 ℃/min升至240 ℃(保持10 min);进样口温度250 ℃;载气He,载气流速1.4 mL/min;分流进样,分流比100 ∶1。MS条件:级杆温度选择150 ℃;选用EI离子源,电子能量为70 eV;离子源温度设置为230 ℃;传输线温度250 ℃;扫描范围33~400 u。顶空进样条件:平衡室温度为35 ℃,定量环温度为40 ℃,传输线温度为45 ℃,进样量为1 mL。
1.3.6微乳抗氧化性
1.3.6.1DPPH自由基的清除率 配置48 mg/L的DPPH自由基(DPPH·)溶液,避光保存待用。取5 mL 不同浓度的山苍子精油乙醇溶液、山苍子精油微乳标样1乙醇溶液、混合表面活性剂水溶液乙醇溶液、BHT乙醇溶液分别各自加入5 mL的DPPH·储备液中,混合均匀后,于室温下避光反应30 min,在515 nm处测定吸光度值(Ai)。以无水乙醇作为空白调零,以5 mL对应浓度的测试溶液加上5 mL无水乙醇作为对照(Aj)。5 mL无水乙醇加5 mL DPPH·储备液的吸光度值为(Ac)。各组分别做3次平行试验,取平均值。DPPH·清除率按下式计算:
YDPPH·=[1-(Ai-Aj)/Ac]×100%
式中:YDPPH—DPPH·清除率,%;Ai—各样品和DPPH·反应的吸光度值;Aj—各样品和无水乙醇反应的吸光度值;Ac—无水乙醇和DPPH·反应的吸光度值。
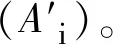

2 结果与讨论
2.1 山苍子精油微乳的制备条件
2.1.1表面活性剂的影响 以山苍子精油为油相,去离子水为水相,无水乙醇为助表面活性剂,Km值为2,分别考查了4种不同的表面活性剂对微乳体系形成的影响,绘制的拟三元相图见图1。

a.EL-30;b.EL-35;c.Tween-80;d.Triton X-100图1 不同表面活性剂形成的拟三元相图Fig.1 Quasi-ternary phase diagram formed with different surfactants
在4种表面活性剂中,当以Triton X-100为表面活性剂时所形成的微乳区域面积最大,所以选择Triton X-100为最佳表面活性剂。比较3种形成微乳面积较大的表面活性剂的链长发现,EL-30(30)和EL-35(35)亲水链长相差不大,所形成的微乳区面积也几乎相等,具有最小的亲水链长的Triton X-100(10)形成的微乳区域面积最大。而Tween-80疏水链长18,微乳面积也最小。这可能是因为对于山苍子精油微乳体系而言,所用的表面活性剂的亲水链越短,空间位阻越小,油相分子就能更好地与表面活性剂结合,乳化效率更高,相界面层更加稳定,所以形成的相图中微乳区域面积大[12]。
2.1.2助表面活性剂的影响 以山苍子精油为油相,去离子水为水相,Triton X-100为表面活性剂,Km值为2,比较4种不同助表面活性剂制备微乳的情况,拟三元相图见图2。
助表面活性剂的主要作用是降低界面张力和体系黏度,并在一定程度上调节表面活性剂的亲水亲油平衡值[13]。一般而言,当助表面活性剂的链长越短时,其相对分子质量越小,越能与表面活性剂更好融合,从而降低界面张力,促使微乳形成[14]。由图2可知,4种助表面活性剂形成的微乳面积由大到小的排序为无水乙醇>1,2-丙二醇>PEG-400>丙三醇,所以无水乙醇是制备山苍子精油微乳最优的助表面活性剂。

a.PEG-400;b.无水乙醇 absolute ethanol;c.丙三醇 glycerol;d.1,2-丙二醇 1,2-propanediol图2 不同助表面活性剂形成的拟三元相图Fig.2 Quasi-ternary phase diagram formed with different cosurfactants
2.1.3Km值的影响 以山苍子精油为油相,去离子水为水相,Triton X-100为表面活性剂,无水乙醇为助表面活性剂,绘制4种不同Km值的拟三元相图见图3。

a.0.5;b.1;c.2;d.3图3 不同Km值形成的拟三元相图Fig.3 Quasi-ternary phase diagram formed with different Km values
在Km值为0.5~3范围内,形成微乳的面积随着Km值的增大而增大。此外,虽然Km=3时比Km=2时形成的微乳区面积略大,但当Km值为3时,在形成微乳过程中会产生较多的凝胶相,黏度过高,而且表面活性剂越多,对人体产生的刺激越大,也更加容易产生泡沫,不利于后期产品的运输。因此,Km值选取为2作为制备山苍子精油微乳最优Km值。
2.1.4温度的影响 在山苍子精油微乳制备体系中,选取的Triton X-100为非离子表面活性剂,温度对非离子表面活性剂的乳化作用有较大的影响。因此,在以山苍子精油为油相,去离子水为水相,Triton X-100为非离子表面活性剂,无水乙醇为助表面活性剂,Km值为2的条件下,进一步探讨了温度对微乳制备条件的影响,不同温度下的拟三元相图见图4。

a.15 ℃;b.25 ℃;c.35 ℃;d.45 ℃图4 不同温度形成的拟三元相图Fig.4 Quasi-ternary phase diagram formed under different temperatures
在15~45 ℃温度范围内,微乳的面积随着温度的上升呈现先增加后减小的趋势,在25 ℃下形成的微乳面积最大。
2.2 山苍子精油微乳制备条件的优化
在单因素试验的基础上,利用正交试验进一步对山苍子精油微乳的制备条件进行优化,试验结果如图5和表1所示。

图5 正交试验形成的拟三元相图Fig.5 Quasi-ternary phase diagram formed by orthogonal experiment
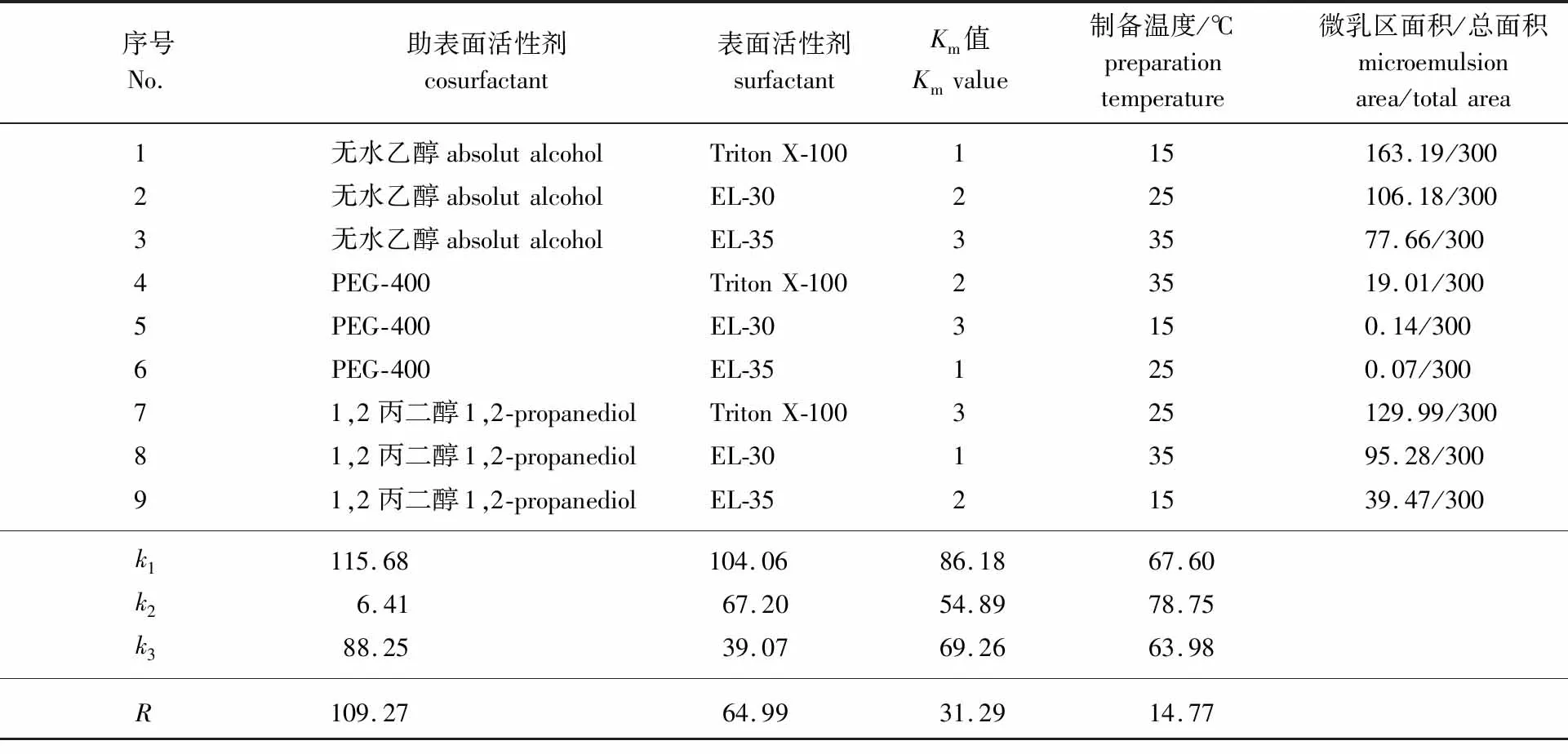
表1 正交试验结果Table 1 The results of orthogonal experiment
由表1可知,助表面活性剂的极差(R)最大,表明在山苍子精油微乳制备过程中,助表面活性剂对微乳的制备影响最大,其次为表面活性剂和Km值,最后为制备温度。因此,微乳的最佳制备条件为:表面活性剂为Triton X-100,助表面活性剂为无水乙醇,Km值为1,制备温度为25 ℃。在最佳条件下制备出的微乳区面积/总面积为154.65/300。
2.3 O/W型山苍子精油微乳的性能测试分析
2.3.1微乳类型测定 电导率在一定程度上能反映微乳的相行为及结构特征,当微乳处于W/O状态时,随着水分子的增多,导电粒子碰撞增多,电导率逐渐升高;当微乳处于双连续状态时,微乳中的既有W/O微粒,也有O/W微粒,电导率升高速度变慢,达到最大值;当微乳处于O/W状态时,随着含水率的增多,微乳滴不断被稀释,电导率下降[15-16]。采用正交试验得到的最佳条件来制备山苍子精油微乳,当混合表面活性剂与油的质量比(S/O)为7 ∶3、8 ∶2、9 ∶1时能制备出可无限稀释微乳,因此在室温下测量这3个比例形成的微乳的电导率随着含水率变化的值,结果见图6。

图6 不同混合表面活性剂和山苍子精油质量比微乳的电导率-含水率曲线图Fig.6 Curve of conductivity-water content of microemulsions in different proportion of the essential oil and surfactants
根据图6可知,当S/O为7 ∶3、8 ∶2且含水率在10%~70%时,微乳的电导率随含水率的增加而逐渐升高,表明此时微乳是W/O型山苍子精油微乳;当含水率为70%时电导率达到最大值,随后随着含水率的增加,微乳的电导率下降,这说明当含水率大于70%时所形成的微乳为O/W型山苍子精油微乳。同理可得,对于S/O为9 ∶1的山苍子精油微乳而言,含水率大于60%形成的微乳为O/W型山苍子精油微乳。
2.3.2微乳的稳定性
2.3.2.1温度稳定性 表面活性剂的性能会随着温度而变化,微乳的性能也会随温度而改变,因此,温度对微乳的储存至关重要。以Triton X-100为表面活性剂,无水乙醇为助表面活性剂,Km值为1,制备O/W型山苍子精油微乳,微乳外观随温度变化的情况如表2所示。

表2 O/W型山苍子精油微乳随温度变化情况1)Table 2 State of O/W type L.cubeba oil microemulsion at different temperatures
由表2可知,对于S/O为7 ∶3和8 ∶2的微乳而言,当含水率在70%~90%时,微乳在温度高于35 ℃时均会出现浑浊的现象,表明S/O为7 ∶3和8 ∶2的微乳的储存温度应小于35 ℃。对于S/O为9 ∶1的微乳而言,当含水率在60%~80%时,微乳储存在15~45 ℃均澄清透明,表现出较好的温度稳定性,这也揭示了随着微乳体系中表面活性剂比例的增大,微乳的温度稳定性增强。
2.3.2.2离心稳定性 在微乳的温度稳定性实验结果的基础上,选择温度稳定性良好的试样进一步测试其离心稳定性。微乳本身并不是一个永久稳定体系,它在储藏的过程会发生颗粒聚集,产生分层现象。因此通过离心法探究它出现该现象的快慢,以此来考察标样1微乳体系的稳定性。
在经过不同转速的离心实验之后,标样1从外观上看均没有明显变化,都是澄清透明,无分层或浑浊现象,表明标样1的离心稳定性良好。
2.3.3微乳的理化性质 在25 ℃下,利用粒径分析仪测定标样1的平均粒径为13.43 nm,多分散系数(PDI)为0.125,电导率为83 mS/m,pH值为5.82。

a.去离子水deionized water;b.山苍子精油微乳microemulsion of L.cubeba oil;c.山苍子精油L.cubeba oil图7 标样1的水溶性测试Fig.7 Water solubility test results of standard sample 1
2.3.4微乳的水溶性 以去离子水和山苍子精油为对照,通过观察亚甲基蓝水溶液在山苍子精油微乳标样1中的扩散速度来测其水溶性,结果见图7。一般而言,亚甲基蓝水溶液在溶液中的扩散速度与受试溶液的水溶性成正相关关系,扩散速度越快则表明受试溶液的水溶性越好。由图7可知,与山苍子精油相比,水溶性染料亚甲基蓝水溶液在山苍子精油微乳标样1中的扩散速度更快,这说明将山苍子精油制备成微乳能显著地增强山苍子精油的水溶性。
2.3.5微乳的缓释性 根据图8可知,在3~12 h内,山苍子精油挥发气体中的柠檬醛峰面积显著高于山苍子精油微乳标样1,并且随着时间的变化,精油挥发气体中的柠檬醛含量越来越多,而微乳挥发气体中的柠檬醛含量没有明显变化,说明将山苍子精油制备成山苍子精油微乳可以有效地提高其缓释性。

图8 2种不同溶液的柠檬醛峰面积Fig.8 Peak area of citral in two different solutions图9 4种不同溶液的DPPH·清除率Fig.9 DPPH· clearance of four different solutions图10 4种不同溶液的·ABTS+清除率Fig.10 ·ABTS+ clearance of four different solutions
2.3.6微乳的抗氧化性
2.3.6.1DPPH·的清除率 DPPH·法是研究抗氧化性较为简单常用的一种方法,一般测试样品的抗氧化性越强,DPPH·清除率就越大。山苍子精油、山苍子精油微乳标样1、混合表面活性剂和BHT的DPPH·清除能力如图9所示。由图可知,不同质量浓度下的混合表面活性剂水溶液的DPPH·清除率为0,说明混合表面活性剂没有抗氧化活性;山苍子精油微乳标样1的DPPH·清除率随着质量浓度增加而增大,表明山苍子精油微乳标样1的抗氧化活性随着质量浓度的增加而增强,且在微乳中发挥抗氧性的成分是山苍子精油。与标样1中含有相等精油量的山苍子精油,在10~30 g/L质量浓度范围内的DPPH·清除率均低于标样1,质量浓度30 g/L时标样1和山苍子精油的DPPH·清除率为95%和44.79%,说明将山苍子精油制备成微乳可以显著提高其抗氧化性。将其与市售的BHT相比,山苍子精油微乳标样1在30 g/L的质量浓度下对DPPH·清除率与BHT相差不大,说明山苍子精油微乳在DPPH·抗氧化性上有较大的应用前景。
2.3.6.2·ABTS+的清除率 通过测定吸光度的减少量可计算出·ABTS+清除率,进而体现出被测样品的抗氧化活性。山苍子精油、山苍子精油微乳标样、混合表面活性剂、BHT的·ABTS+清除能力如图10所示。由图可知,山苍子精油微乳标样1的·ABTS+清除率随着质量浓度增加而增大,表明山苍子精油微乳标样1的抗氧化活性随着质量浓度的增加而增强;不同质量浓度下的混合表面活性剂水溶液的·ABTS+清除率随着质量浓度的增加而缓慢增加,说明混合表面活性剂对微乳的抗氧化活性起到增强作用;与标样1中含有相等精油量的山苍子精油,在10~30 g/L质量浓度范围内的·ABTS+清除率均比标样1低,质量浓度30 g/L时,标样1和山苍子精油·ABTS+清除率为54.7%和16.4%,说明将山苍子精油制备成微乳可以显著提高其对·ABTS+抗氧化性。但是将其与市售的BHT相比,山苍子精油微乳标样1的抗氧化性还是略显不足,与其他抗氧化活性高的精油成分复配,可能是解决这一问题的途径之一。
3 结 论
3.1在25 ℃下,以Triton X-100为表面活性剂,无水乙醇为助表面活性剂,Km值为1,采用加水法能成功制得O/W型山苍子精油微乳。在S/O值为9 ∶1,且含水率为70%的条件下制得的微乳缓释性能较强,温度小于45 ℃时温度稳定性好,1 000~4 000 r/min时离心稳定性较好。
3.2山苍子精油微乳液标样1的平均粒径为13.43 nm,PDI为0.125,电导率为83 mS/m,pH值为5.82。经测试发现山苍子精油微乳标样1的水溶性显著优于精油本身,表明将山苍子精油微乳化有助于提高其水溶性;在相同时间内,标样1中柠檬醛的挥发量小于精油,表明微乳的缓释性更优。
3.3抗氧化活性实验结果表明:在10~30 g/L质量浓度范围内,山苍子精油微乳标样1比山苍子精油表现出更高的DPPH·和·ABTS+清除率,说明将山苍子精油制备成微乳液可以显著提高其抗氧化性。

