基于CT数据的术前3D重建在胸腔镜下近肺门处良性肿瘤摘除术的应用价值
左涛,赵轲,陈治国,徐迪,陈宝钧
(华中科技大学同济医学院附属武汉中心医院 胸外科,湖北 武汉430014)
肺良性肿瘤是指发生在肺实质或支气管内的良性肿瘤,主要有炎性假瘤、肺错构瘤、肺硬化性血管瘤等。其发病率远较肺部恶性肿瘤低,但部分肺良性肿瘤不断生长,甚至可能发生恶变,且通过非手术方法常难与恶性肿瘤相鉴别[1-3]。因此外科手术是肺良性肿瘤诊断和治疗的最确切的手段。为尽可能减少切除正常肺组织,切除方式以局部切除是为首选。外周型肿块可选择楔形切除术,而近肺门处病变行肺叶切除损失过多肺组织,并加重了患者的经济和身体负担。
随着数字医学迅猛发展,3D重建技术已经被广泛应用于骨科、口腔科、普外科等临床科室[4-6]。胸外科也开始有初步的应用,主要应用于肺段切除或穿刺活检[7-9]。肺门的血管、支气管解剖变异较多,手术难度大。三维计算机血管扫描成像技术重建肺血管、支气管,可清晰地呈现肺部解剖结构,有助于近肺门处良性肿瘤的精准切除。本文回顾性分析与总结华中科技大学同济医学院附属武汉中心医院开展的基于CT数据的术前3D重建在胸腔镜下近肺门处良性肿瘤摘除术,拟为其临床应用提供相关可行性分析及理论依据。
1 资料与方法
1.1 一般资料
选取2017年1月1日—2019年1月1日华中科技大学同济医学院附属武汉中心医院胸外科就诊的肺门区良性肿瘤患者18例,分为研究组12例和对照组6例。研究组术前经胸部增强CT 检查后建立3D 重建模型,并在3D 模型指导下行胸腔镜下近肺门处良性肿瘤摘除术。对照组3D重建,直接行胸腔镜下肿瘤摘除术。所有患者纳入标准:①位于肺门处<5 cm的肿瘤,临床考虑良性可能性大;②以下至少满足1条:患者有咳嗽、胸闷、咳血等临床表现;病灶不能完全除外恶性可能;复查过程中病灶增大;③无法行肺楔形切除术或行肺楔形切除术损伤肺叶或肺段支气管、动静脉;④病灶距离肺表面≤2 cm。排除标准:①术前明确诊断为恶性或临床考虑恶性可能性大的;②术中发现肿块与肺组织粘连紧密。
患者中男性11 例,女性7 例;年龄45~76 岁。术前诊断均考虑良性肿瘤,其中左上肺5例,左下肺3 例,右上肺5 例,右中叶1 例,右下肺4 例。合并高血压4 例,糖尿病2 例,冠状动脉粥样硬化性心脏病1 例。有吸烟史10 例。术前评估心肺功能,行头部磁共振、腹部B 超、骨扫描等检查排除手术禁忌。肿瘤与支气管邻近的患者行纤维支气管镜检查或超声支气管镜检查排除气道侵犯。
1.2 影像资料获取
所有患者应用双源CT扫描仪(Deft-nition,德国西门子公司)行胸部增强CT 检查。取仰卧位,双手置于头顶,于肱正中静脉或前臂静脉内以5 ml/s的速率注入非离子型对比剂(碘氟沙醇)约60 ml,然后以相同的速率注入30~40 ml 生理盐水冲洗。注入对比剂后约16~20 s后开始追踪肺动脉性三期扫描,即肺动脉期、肺静脉期和延迟期,扫描范围从胸廓入口平面至肋膈角平面。扫描参数为:管电压120 kV,有效管电流约150~180 mAs,准直器厚度0.6 mm,重建层厚0.625 mm。机器内置三维后处理软件处理重建后图像。见图1。
1.3 3D重建图像获取及入路规划
将CT 扫描数据以DICOM 格式导入INCOOL 3D+软件(杭州英库医疗科技公司)。利用分割工具中的动态区域,使用软件中的分割功能模块,即可获得胸部3D 重建模型(见图2)。若模型表面粗糙可适当给予光滑处理,从任意角度旋转、调整模型颜色及透明度能更好地显示肿块与周围结构之间的位置关系。根据3D重建图像,分析肺结节与肺门处肺血管及肺段支气管位置、结构关系(见图3~5),预先规划手术方式和避让路线(见图6)。以肿瘤为圆心,术前明确其各个方向的血管、支气管走向,并做好记录。测量其距胸膜表面最近且无血管、气管通行的路径。

图1 近肺门肿瘤的CT表现

图2 3D重建模型

图3 肿瘤与肺动脉位置关系的3D重建图像

图4 肿瘤与肺静脉位置关系的3D重建图像
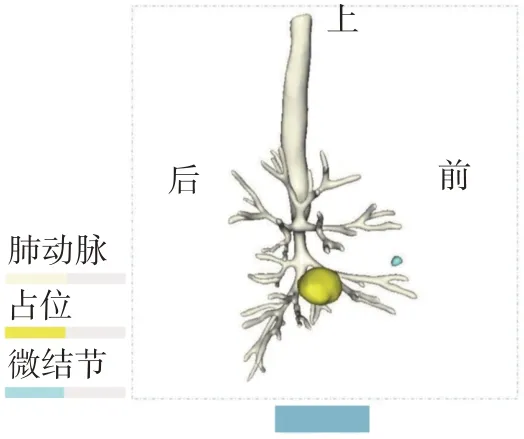
图5 肿瘤与肺段支气管的位置关系的3D重建图像

图6 结节周围少血管、气管区及规划手术入路
1.4 手术过程
双腔气管插管全身麻醉,健侧单肺通气。采用单操作孔胸腔镜手术方式:嘱麻醉医师单肺通气后,取第7或8肋间腋中线行1 cm切口为观察孔,腋前线第4肋间取2 cm切口为操作孔。人工气胸后,彻底塌陷肺组织。对照CT图像,以卵圆钳探查高度可疑肺门处,发现类圆形可活动的肿瘤即为病灶。游离肿瘤附近肺门组织,对照术前3D 重建图像,整个术中均注意保护肿瘤附近肺动脉、肺静脉、支气管。探查肿瘤表面肺组织最菲薄处无血管、气管结构后,电刀切开肿瘤表面脏层胸膜,钝性剥离直至瘤体,沿肿瘤的包膜分离。对于术前认为有恶性可能的,可应用9 F头皮针对肿瘤进行穿刺活检,术中快速冰冻切片排除恶性后再继续手术。肿瘤基底部有明显血管蒂时用血管夹夹闭处理后切断,否则仅用电刀处理。完整摘除肿瘤后立即送快速病理学检查除外恶性肿瘤。肺创面如有出血,采用喷凝模式止血。为避免损伤肺血管,或引发大出血、肺淤血或肺栓塞,尽量不缝合肺创面。温盐水冲洗,膨肺检查无明显出血及漏气,留置28 F胸管后关胸。
2 结果
手术切除肿瘤经病理学检查排除恶性肿瘤。研究组患者均得到完整、清晰的3D 重建模型,医生根据重建模型分析肺肿瘤与肺门处肺血管及段支气管位置、结构关系。手术过程顺利,手术时间(40.3±8.9)min,术中出血(60.5±10.7)ml,无中转开胸;术后病理:肺错构瘤6例,硬化性肺泡细胞瘤5例,神经鞘瘤1例。术后并发症咯血2例,肺漏气1例,无死亡及严重并发症发生。对照组手术时间(45.7±12.1)min,术中出血(240.9±90.7)ml。术后病理:肺错构瘤3例,神经鞘瘤1 例,炎症假瘤1 例。术中中转开胸1 例,修补肺动脉。术后并发咯血1例,肺漏气1例,肺栓塞1例,肺内巨大血肿1例,其中肺内巨大血肿行二次手术切除肺叶。研究组手术时间短于对照组(P<0.05),并发症发生率低于对照组(P<0.05)。全部患者术后随访半年均无复发。见图7、8。

图7 手术切除肿瘤的大体标本
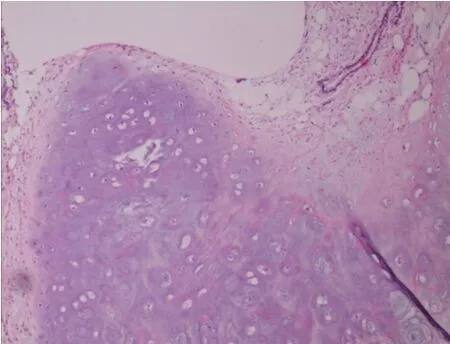
图8 错构瘤术后病理切片
3 讨论
随着低剂量CT 平扫的在我国的普及,肺结节的检出率明显增加。大部分结节考虑为良性,无需手术。但部分肺良性肿瘤不断生长,有恶变的可能,需通过外科手术进行诊断和治疗。相比肺叶切除而言,良性肿瘤的部分切除可最大限度地保留正常的肺组织,使患者术后获取更好的生活质量。尤其对高龄、心肺功能差等患者,部分切除可减少相关并发症。然而对于近肺门的良性肿瘤,行肺段切除手术复杂、费用高昂,行楔形切除损伤肺门区重要结构,甚至常常被迫中转开胸或选择肺叶切除术。此时,胸腔镜下肺良性肿瘤的摘除术是最优的手术方式。
而数字医学的发展,使基于影像学数据的3D 重建技术为快速、精准、高效地制造个性化模型提供解决方案[10]。通过该技术能以立体化的角度全面系统地观察肺门的局部解剖结构,深入而完善地了解肺门内各组织的形态、数量、分布、毗邻关系、个性化变异、肿瘤血供等,使手术医师在术前能对手术的术式、入路、切除范围等进行全面细致的设计和评估,力求在达到切除目的的同时避免损伤肺血管、支气管等重要结构,使手术更加精确、安全、微创。
本研究通过术前3D 重建,明确肿瘤和各组织的关系,术中操作顺利,无大出血等并发症出现。且肺良性肿瘤,尤其是错构瘤和硬化性血管瘤,一般具有完整的包膜,与周围正常疏松的肺组织有明显界限,而且多无大的血管供血,因而摘除术安全、可靠[11-12]。通过术前3D 辨认肺血管方位后,能明显减低重要结构的损伤,从而降低相关术后并发症的发生率。本文研究组术后无死亡及肺梗死、肺栓塞、支气管胸膜瘘等严重并发症发生。术中如无法确定预定切除部位的胸膜下是否有大血管存在时,可应用卵圆钳夹持5 F头皮针,接5 ml注射器,带负压抽吸胸膜下组织,结合3D 图像,确认入路安全后开始电刀游离。未通过3D 重建的患者,手术具有一定盲目性,容易损伤周围血管,甚至可能中转开胸或形成肺内血肿。
综上所述,通过基于CT 数据的术前3D 重建技术,参考肺血管、支气管和肿瘤重建图像,为胸腔镜下近肺门处良性肿瘤摘除术的术前规划、术中指导提供一种个性化的方法,使手术更加安全、精准。

