太子神悦胶囊提取工艺研究及方法验证
左明明,胡时先,朱美霞,陈婷
(新疆华春药业医药研究院,新疆 乌鲁木齐 830000)
太子神悦胶囊为国家五类新药,处方由太子参、葛根、淫羊藿三味药材组成,具有补肾填精、温补肾阳之功效,用于治疗中轻度抑郁症。太子神悦胶囊处方君药太子参(RadixPseudostellariae)为石竹科植物孩儿参的干燥块根,具有生津润肺,益气健脾的功效。现代药效学研究表明,太子参具有抗疲劳、抗应激、增强耐氧能力等作用[1-3]。研究表明,太子参药材有效部位为多糖成分,小分子糖和低聚糖,如葡萄糖、蔗糖、麦芽糖等[4-5]。余煊[6]对太子神悦胶囊的作用机制研究表明:太子神悦和其成分淫羊藿苷单体能够有效提高五羟色胺(5-HT)合成限速酶色氨酸羟化酶II(TPH2)的表达,进而升高脑内5-HT胺含量。宋宇昕[7]针刺结合太子神悦胶囊治疗心脾两虚型郁证的临床疗效研究表明:根据中医症候疗效判定标准,针药组总有效率为90%。
本实验主要研究了太子神悦胶囊处方药材提取工艺,确定最佳提取工艺参数,开展工艺验证,为太子神悦胶囊制剂批量规模生产奠定基础。
1 仪器与材料
1.1 仪器
高效液相色谱仪(Waters 515系,996 PDA检测器),调温电热套(上海予英仪器有限公司),RE旋转蒸发仪(上海亚荣生化仪器),十万分之一电子天平(北京赛多利斯仪器系统有限公司),DHG电热恒温鼓风干燥箱(常州金坛良友仪器有限公司),UV-1800紫外可见分光光度计(北京普析通用仪器有限公司),752紫外光栅分光光度计(上海精密科学仪器有限公司),万分之一电子天平(上海中生科技有限公司),HH-8数显恒温水浴锅(常州国华电器有限公司),SHZ-D(III)双表双抽循环水真空泵(郑州市亚荣仪器有限公司),ZF-6(ZF-1)三用紫外分析仪(上海精密仪器仪表有限公司)。
1.2 材料
原料:太子参葛根淫羊藿。溶剂:水、食用乙醇。试药:苯酚(AR),浓硫酸(AR),乙腈(色谱纯)。对照品:淫羊藿苷对照品,葛根素对照品,D-无水葡萄糖(中国药品生物制品检定所)。
2 方法
2.1 太子神悦胶囊太子参药材提取工艺研究
2.1.1 综合得分计算方法
综合得分:D=A×0.4+B×0.6
A:干膏量/最大干膏量×100;B:干膏中有效成分含量/最大干膏有限成分含量×100。
2.1.2 太子参多糖含量测定法
标准曲线的制备[8],结果标准曲线为:Y=6.321 3x+0.021 2(R2=0.999 6),葡萄糖在0.057 6~0.192 mg/mL之间线性关系良好。按照标准曲线的方法检测样品含量,计算多糖提取率。
2.1.3 太子参药材多糖含量测定
精密称取太子参样品粗粉0.5 g,用80%乙醇提取1 h,过滤,药渣用饮用水90 ℃提取2 h,过滤,药渣加蒸馏水洗涤数次,洗液并入滤液,蒸馏水定容于100 mL容量瓶中。再取50 mL加蒸馏水定容于100 mL备用,以硫酸苯酚法检测。
2.1.4 单因素试验
2.1.4.1 提取溶剂的选择
太子参主要有效成分为多糖物质,根据相关文献[8-9],太子参提取溶剂采用纯化水、20%乙醇、50%乙醇以及75%乙醇,进行单因素试验:取4份太子参药材各60 g,破碎后置2 000 mL原底烧瓶中,分别加入20倍量纯化水、20%乙醇、50%乙醇以及75%乙醇回流提取3次,2 h/次。合并滤液。以出膏率和总多糖含量为指标计算综合得分。试验结果见表1。

表1 提取溶剂单因素试验结果表
2.1.4.2 料液比的影响
以饮用水为提取溶剂,取4份60 g量太子参药材置2 000 mL圆底烧瓶中,分别加入8倍量、12倍量、15倍量及20倍量饮用水。提取3次,2 h/次,合并滤液,取样。以出膏率和总多糖含量为指标计算综合得分。试验结果见表2。
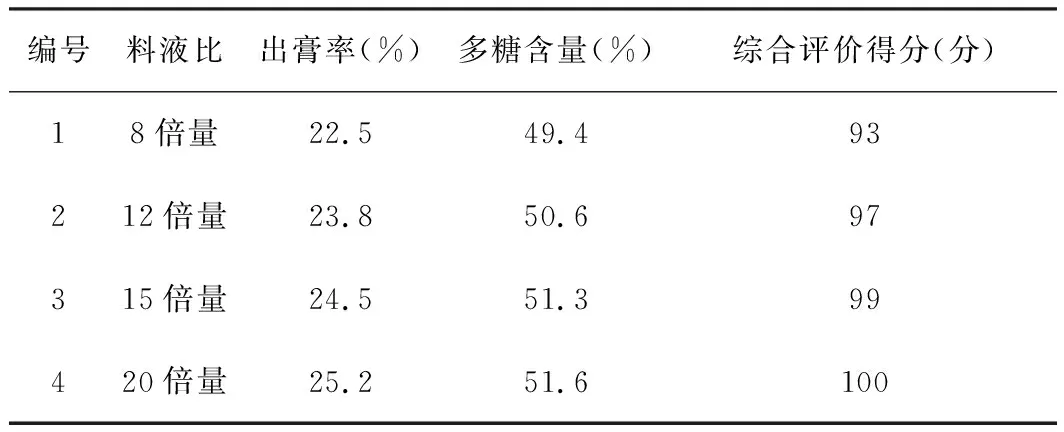
表2 太子参提取料液比单因素试验结果表
2.1.4.3 提取时间的影响
以饮用水为提取溶剂,取4份60 g量太子参药材置2 000 mL圆底烧瓶中,加入20倍量饮用水。提取时间分别为1 h、2 h、3 h、4 h,提取3次,合并滤液,取样。以出膏率和总多糖含量为指标计算综合得分。试验结果见表3。
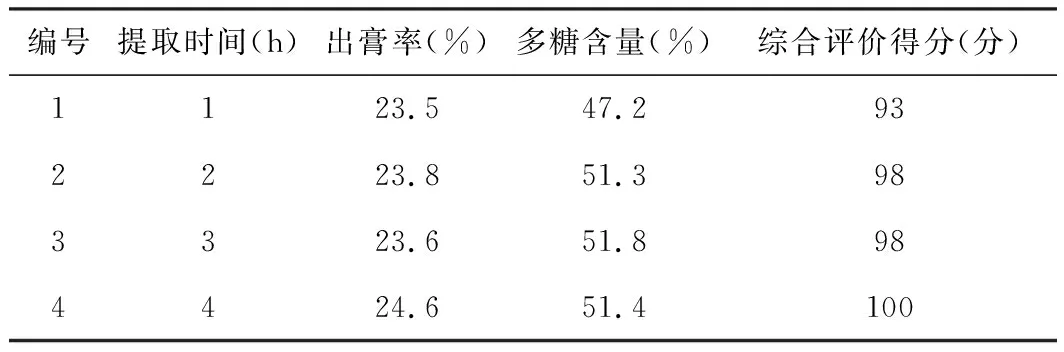
表3 太子参提取次数单因素试验结果表
2.1.4.4 提取次数的影响
以饮用水为提取溶剂,取4份60 g量太子参药材置2 000 mL圆底烧瓶中,加入20倍量饮用水。分别提取1、2、3、4次,2 h/次,合并滤液,取样。以出膏率和总多糖含量为指标计算综合得分。试验结果见表4。
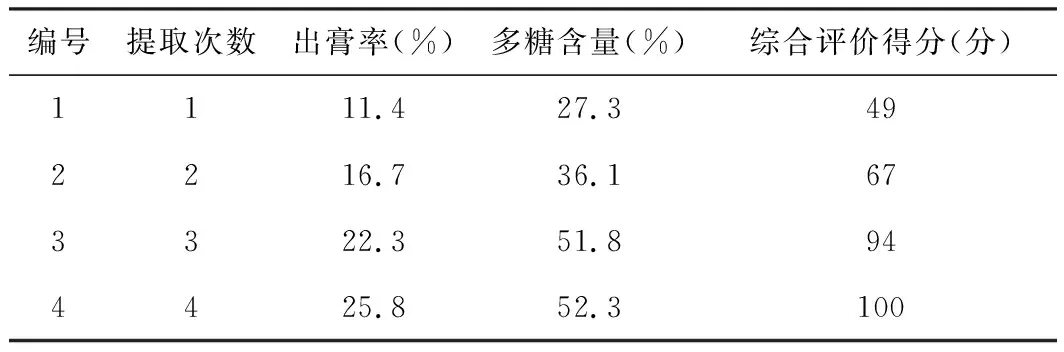
表4 太子参提取次数单因素试验结果表
2.1.5 正交试验
根据太子神悦胶囊太子参提取单因素实验结果,选料液比、提取时间、提取次数3个因素,采用L9(34)正交试验,对太子参药材提取工艺进行考察,确定太子参多糖提取的最佳工艺。实验因素与水平如表5所示。

表5 正交试验因素水平表
2.1.6 正交试验结果
以提取液干膏率和多糖含量为评价指标,计算综合评价得分。由表6可知,影响太子参多糖提取的各因素主次顺序:提取次数>料液比>提取时间。 太子参最佳工艺为A1B2C2,即料液比为8倍量,提取次数3次,提取时间3 h。由表7方差分析表明,因素B为显著因素,随着提取次数增加,所得干膏总量增加,但有效部位太子参多糖含量逐渐降低。因此,确定太子参药材提取的最佳工艺为:取太子参,加入8倍量的饮用水提取3次,3 h/次。
2.1.7 太子参多糖提取最佳工艺验证
根据太子参多糖提取正交试验结果,以确定的最佳提取工艺开展三批小试验证。即:取太子参药材60 g,破碎后置1 000 mL圆底烧瓶中,加入8倍量的饮用水提取3次,3 h/次。
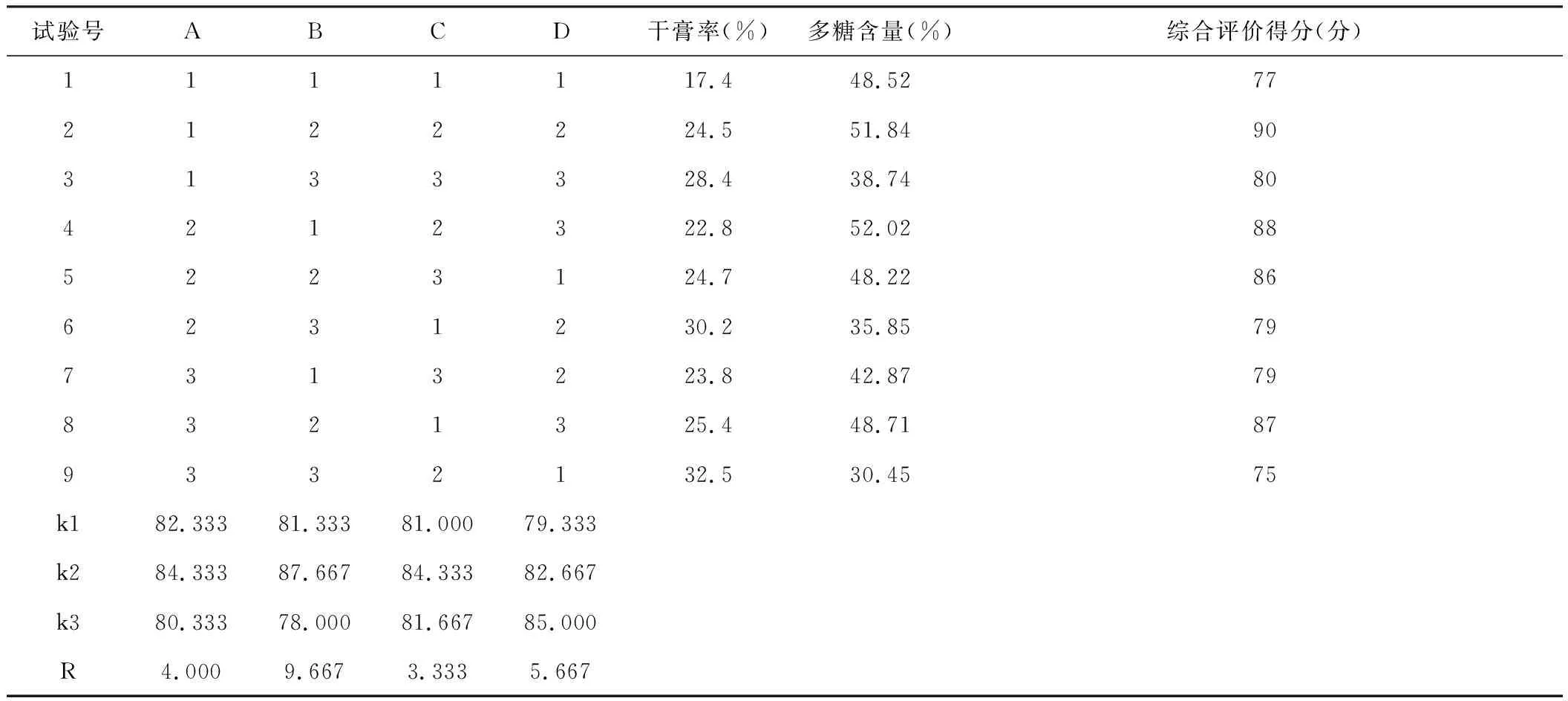
表6 太子参提取正交试验结果表
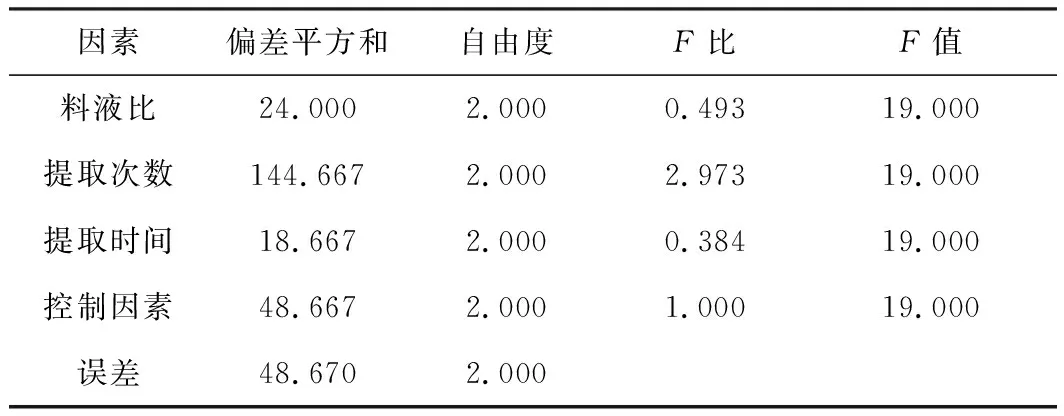
表7 太子参提取正交试验方差分析表
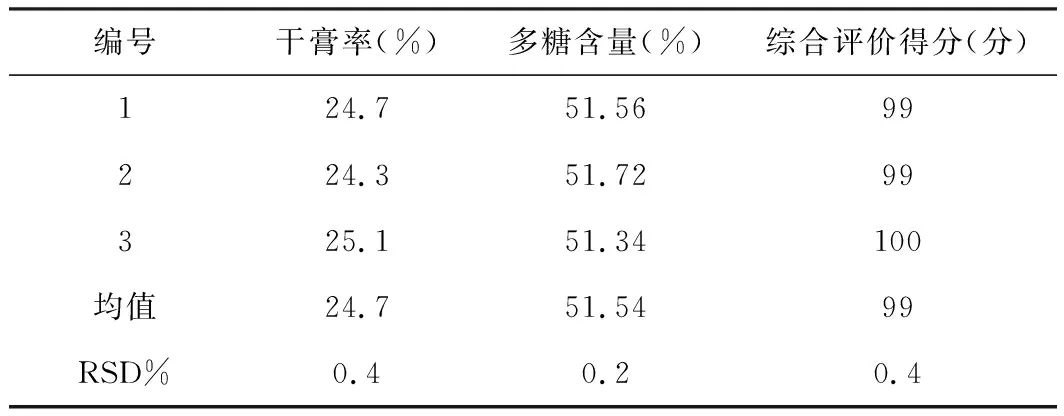
表8 太子参提取工艺验证
试验结果表8显示,三批工艺验证试验太子参提取液干膏率均值24.7%,多糖含量均值51.54%,RSD%<1,实验结果平行。证明太子参药材提取工艺稳定可行。
2.2 太子神悦胶囊葛根、淫羊藿提取工艺研究
2.2.1 综合得分计算方法
综合得分:F=A×0.2+B×0.2+C×0.2+D×0.4
A:干膏量/最大干膏量×100;B:干膏中葛根素含量/干膏最大葛根素含量×100;C:干膏中总黄酮含量/干膏最大总黄酮含量×100(干膏总黄酮含量以葛根素计);D:干膏中淫羊藿苷含量/干膏最大淫羊藿苷含量×100
2.2.2 葛根素含量测定法
照高效液相色谱法(《中国药典》2010年版一部附录VI D)测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂。乙腈-0.5%磷酸水(10∶90)为流动相;检测波长为250 nm;柱温45 ℃。理论塔板数按葛根素峰计算应不低于3 000。
对照品溶液的制备:精密称取葛根素对照品加甲醇制成每1 mL含80 μg的葛根素溶液。
供试品溶液的制备:取原料药粉末约32 mg,精密称定,置100 mL量瓶中,加80%乙醇,超声处理2~5 min,摇匀并定容至刻度。用微孔滤膜(0.45 μm)滤过,取滤液,即得。
测定法:分别精密吸取对照品溶液和供试品溶液各5 μL,分别注入液相色谱仪,测定,即得。
2.2.3 总黄酮含量测定法(以葛根素计)
照品溶液的制备:精密称取葛根素对照品适量,加无水乙醇制成1 mL中含葛根素0.1 mg的溶液。
标准曲线的制备:精密吸取葛根素对照溶液0.2、0.4、0.6、0.8、1.0 mL,分别置于10 mL容量瓶中,用无水乙醇溶解并定容至刻度,摇匀。以无水乙醇作为空白在紫外分光光度计250 nm处测定吸收度,绘制标准曲线,得到回归方程。
样品的测定:取原料药粉末,精密称定10 mg,置50 mL容量瓶中,各加入80%乙醇溶解并定容至刻度,摇匀。再精密吸取1 mL,置25 mL容量瓶中,加80%乙醇 稀释至刻度,摇匀。照标准曲线制备项下的方法,测定吸收度,根据回归方程计算供试品溶液中总黄酮的含量,即得。
2.2.4 淫羊藿苷含量测定法
照高效液相色谱法(《中国药典》2010年版一部附录VI D)测定。
色谱条件与系统适用性试验:用十八烷基硅烷键合硅胶为填充剂。乙腈-水(27∶73)为流动相;检测波长为270 nm;柱温30 ℃。理论塔板数按淫羊藿苷峰计算应不低于1 500。
对照品溶液的制备:精密称取淫羊藿苷对照品适量加甲醇制成制成浓度为0.154 mg/mL的淫羊藿苷溶液。
供试品溶液的制备:取原料药粉末约64 mg,精密称定,置10 mL量瓶中,加入80%乙醇超声处理5~10 min,摇匀并定容至刻度,经微孔滤膜(0.45 μm)滤过,滤液备用。
测定法:分别精密吸取对照品溶液和供试品溶液各10 μL,注入液相色谱仪,测定,即得。
2.2.5 单因素试验
2.2.5.1 提取溶剂的选择
太子神悦胶囊处方药材葛根、淫羊藿主要提取的有效部位为黄酮类化合物及苷类化合物,根据两类化合物特点设计采用30%乙醇、60%乙醇、80%乙醇以及95%乙醇为提取溶剂。通过单因素试验确定两味药材最佳乙醇提取浓度。
试验方法:取葛根药材40 g,淫羊藿药材20 g,混合后置2 000 mL原底烧瓶中,分别加入20倍量30%乙醇、60%乙醇、80%乙醇以及95%乙醇回流提取3次,2 h/次。合并滤液。以出膏率、总黄酮含量、葛根素含量、淫羊藿苷含量为指标计算综合得分。试验结果见表9。

表9 提取溶剂单因素试验结果表
2.2.5.2 料液比的影响
以80%乙醇为提取溶剂,取葛根药材40 g,淫羊藿药材20 g,混合后置2 000 mL原底烧瓶中,分别加入8倍量、12倍量、15倍量及20倍量80%乙醇。提取3次,2 h/次,合并滤液,取样。以出膏率、总黄酮含量、葛根素含量、淫羊藿苷含量为指标计算综合得分。试验结果见表10。
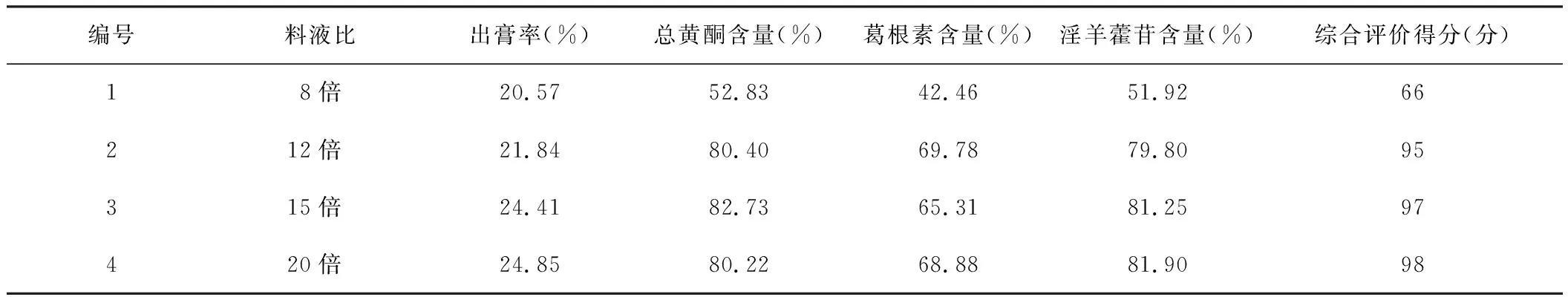
表10 料液比单因素试验结果表
2.2.5.3 提取时间的影响
以80%乙醇为提取溶剂,取葛根药材40 g,淫羊藿药材20 g,混合后置2 000 mL原底烧瓶中,加入20倍量80%乙醇提取,提取时间分别为1 h、2 h、3 h、4 h,提取3次,合并滤液,取样。以出膏率、总黄酮含量、葛根素含量、淫羊藿苷含量为指标计算综合得分。试验结果见表11。
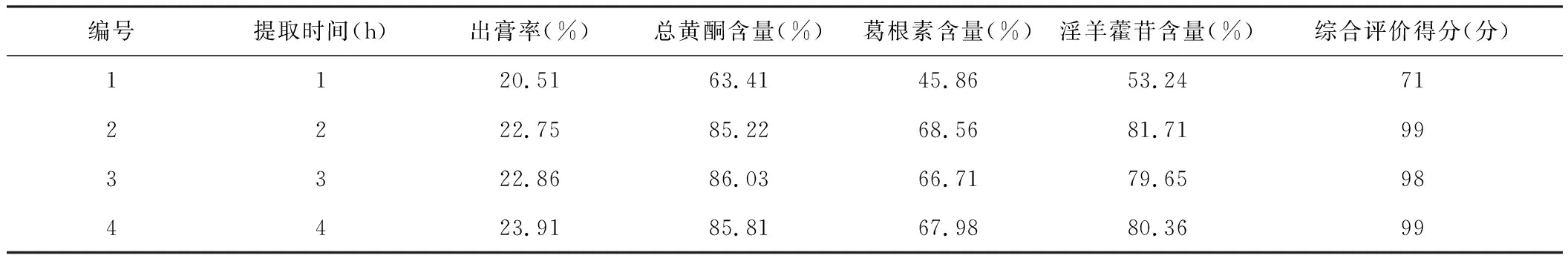
表11 料液比单因素试验结果表
2.2.5.4 提取次数的影响
以80%乙醇为提取溶剂,取葛根药材40 g,淫羊藿药材20 g,混合后置2 000 mL原底烧瓶中,提取次数分别为1次、2次、3次、4次,合并滤液,取样。以出膏率、总黄酮含量、葛根素含量、淫羊藿苷含量为指标计算综合得分。试验结果见表12。

表12 提取次数单因素试验结果表
2.2.6 正交试验
根据太子神悦胶囊葛根、淫羊藿提取单因素试验结果,选料液比、提取时间、提取次数3个因素,采用L9(34)正交试验,对葛根、淫羊藿药材提取工艺进行考察,确定葛根、淫羊藿提取的最佳工艺。试验因素与水平如表13所示。

表13 正交试验因素水平表
2.2.7 正交试验结果
以提取液出膏率、总黄酮含量、葛根素含量、淫羊藿苷含量为评价指标,计算综合评价得分。由表14可知,影响太子参多糖提取的各因素主次顺序:提取次数>料液比>提取时间。葛根、淫羊藿最佳工艺为A2B3C1,即料液比为12倍量,提取次数3次,提取时间1 h。由表15方差分析表明,因素B为显著因素,A、C为不显著因素。因此,确定葛根、淫羊藿药材提取的最佳工艺为:取处方比例葛根、淫羊藿药材,加入12倍量的饮用水提取3次,1 h/次。
2.3 葛根、淫羊藿提取最佳工艺验证
根据葛根、淫羊藿提取正交试验结果,以确定的最佳提取工艺开展三批小试验证。即:取葛根药材40 g,淫羊藿药材20g,混匀后置1 000 mL圆底烧瓶中,加入12倍量的饮用水提取3次,1 h/次。
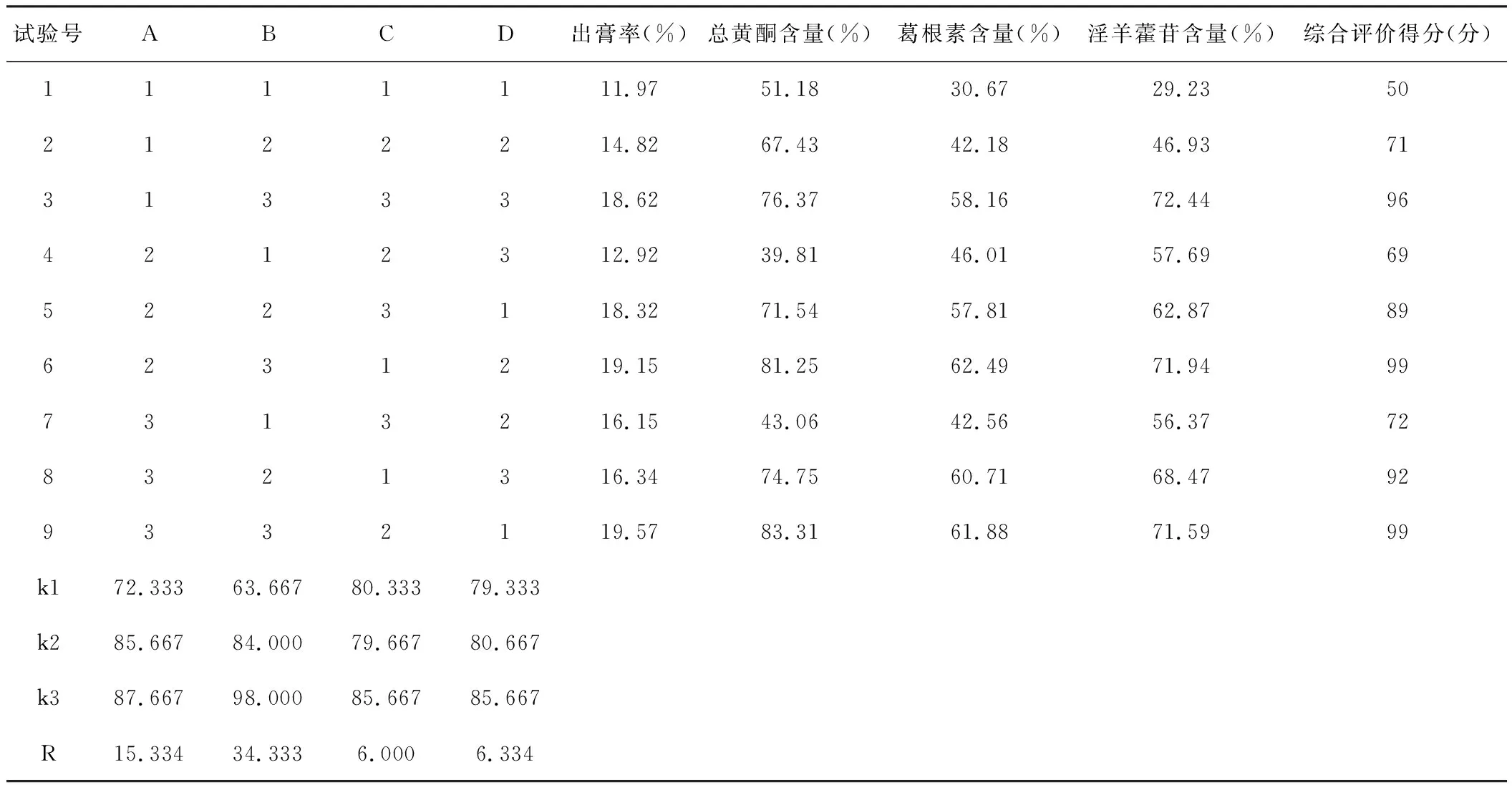
表14 葛根、淫羊藿提取正交试验结果表
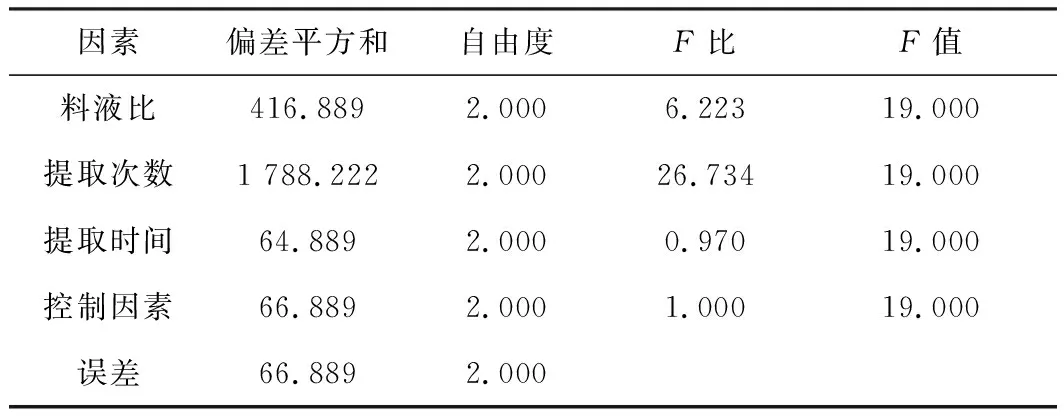
表15 葛根、淫羊藿提取正交试验方差分析表
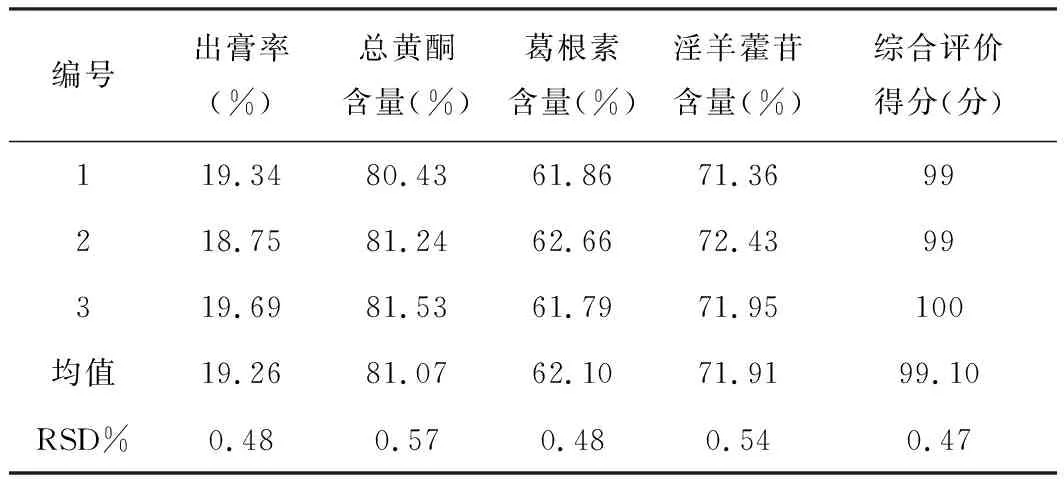
表16 葛根、淫羊藿提取工艺验证结果表
试验结果表16显示,三批工艺验证试验总黄酮(以葛根素计)含量均值81.07%,葛根素含量均值62.10%,淫羊藿苷含量均值71.91%,RSD%<1,实验结果平行。证明葛根、淫羊藿药材提取工艺稳定可行。
3 结果
3.1 太子神悦胶囊太子参药材提取工艺
结果表明,太子参药材最佳提取纯化工艺如下:取处方量太子参药材,加8倍量饮用水提取3次,3 h/次,提取液过滤后合并滤液,滤液在80 ℃,0.08 MPa条件下减压浓缩至相对密度约为1.18~1.19(50 ℃)。
3.2 太子神悦胶囊葛根、淫羊藿药材提取工艺
结果表明,葛根、淫羊藿药材最佳提取纯化工艺如下:取处方量葛根和淫羊藿药材,加入12倍量的80%乙醇,回流提取3次,每次1 h,合并滤液,减压浓缩(60 ℃,0.06 MPa),至相对密度约为1.03~1.04(50 ℃)。
4 小结与讨论
太子神悦胶囊的适应症是用于治疗中轻度抑郁症,为国家五类新药研发项目,目前已完成三期临床试验,即将取得生产批件,上市销售。太子神悦胶囊中间品制备工艺是否可行关系到药品成品质量的均一性、稳定性。太子神悦胶囊中间品制备工艺经过单因素试验、正交试验、生产工艺小试验证、中试验证及规模生产验证,关键生产工艺参数不断优化、细化。结果表明太子神悦胶囊中间品制备工艺稳定、可行,具备规模生产的条件,为产品上市后规模化生产奠定基础。

