氯化钙-无花果蛋白酶-猕猴桃蛋白酶体系对兔肉肌原纤维蛋白结构的协同作用
李明奇,贺稚非,2,李少博,李冉冉,瞿 丞,李洪军,2,*
(1.西南大学食品科学学院,重庆 400716;2.西南大学重庆市特色食品工程技术研究学院,重庆 400716)
肉的嫩度是影响肉制品品质的重要特性,肉中肌原纤维蛋白(myofibrillar protein,MP)是决定肉品嫩度的主要因素之一[1]。在诸多嫩化手段中,嫩化剂被认为是一种经济有效安全的嫩化方法,其作用机理多样,其中氯化钙与外源蛋白酶是常见的嫩化剂;高浓度的钙离子可以激活钙蛋白酶使细胞骨架蛋白降解[2],另一方面钙离子引起的电荷间的排斥作用会导致Z盘的机械性断裂,使肌动蛋白失去稳定性,从而MP解聚失去完整性,肉制品嫩度因此得到改善[3];外源蛋白酶中常见的有木瓜蛋白酶、猕猴桃蛋白酶和无花果蛋白酶等从植物中提取的酶制剂,外源酶通过水解MP,破坏肌肉纤维结构,从而提高肉制品的嫩度[4]。虽然木瓜蛋白酶是目前被广泛使用的酶制剂,但其存在过度嫩化而使肉制品表面发黏的现象[5];猕猴桃蛋白酶和无花果蛋白酶是近几年被广泛研究的2 种酶制剂,据前人实验显示,这2 种酶的嫩化效果更温和,且最适酶解温度较低,猕猴桃蛋白酶在35~45 ℃,无花果蛋白酶在45~55 ℃[6-7],在此温度范围内嫩化可以保护肉制品色泽。
兔肉具有高蛋白、低脂肪、低胆固醇的营养特点,蛋白质量分数高达20%,每100 g兔肉可提供900 kJ的热量,其中80%由蛋白质提供,可见兔肉是一种健康优质的蛋白来源[8]。但是兔肉在热加工后失水严重,肉质变硬,口感发柴[9]。目前在利用嫩化剂嫩化兔肉方面,已证明氯化钙、无花果蛋白酶和猕猴桃蛋白酶组成的复配嫩化剂可以显著降低兔后腿肉的剪切力和蒸煮损失[10],但在蛋白质水平上进一步研究复配体系对MP的协同降解作用却鲜有报道。在本研究中,利用已得到的嫩化剂最优配比处理兔后腿肉,观察处理后的兔肉中MP相关指标随嫩化时间的变化,以肌原纤维蛋白小片化指数(myofibrillar fragmentation index,MFI)、MP溶解度、可溶性蛋白含量(soluble protein content,SPC)、MP表面疏水性以及十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE)为指标判断MP结构的变化,同时与等量的氯化钙、猕猴桃蛋白酶、无花果蛋白酶3 种单一嫩化剂处理兔后腿肉所得的蛋白质指标变化情况作对比,分析此过程中各组指标的变化趋势,以期研究复配嫩化剂中各组分之间在降解MP时的协同作用机理,为嫩化剂的复配形式提供更多理论依据和参考。
1 材料与方法
1.1 材料与试剂
选择70 日龄伊拉公兔20 只(购自重庆市阿兴记原种兔养殖基地),每只体质量3~3.5 kg,屠宰去皮后,取后腿,置于装有冰袋的采样箱中运回实验室,在4 ℃下过夜排酸,然后放置于-18 ℃环境下贮藏。
猕猴桃蛋白酶(105U/g,食品级) 广州馨之味食品配料商城;无花果蛋白酶(105U/g,食品级) 山东一品食品配料有限公司;氯化钙(食品级) 河南万邦实业有限公司;磷酸二氢钾、磷酸氢二钾(均为食品级) 河南华悦化工产品有限公司;氯化镁、氢氧化钠、SDS、三羟甲基氨基甲烷(tris(hydroxymethyl)methyl aminomethane,Tris)、β-巯基乙醇、考马斯亮蓝R-250、甲醇、冰醋酸 重庆市钛新化工有限公司;酒石酸钾钠 宁波大川精细化工有限公司;乙二胺四乙酸二钠(ethylenediaminetetraacetic acid disodium salt,EDTA-2Na) 成都市科龙化工试剂厂;溴酚蓝(bromophenol blue,BPB) 北京鼎国生物技术有限责任公司;上述试剂均为分析纯;牛血清蛋白(生化试剂)成都市科龙化工试剂厂;SDS-PAGE凝胶配制试剂盒范德(北京)生物科技有限责任公司;RealBand蛋白预染Maker 北碚区文鼎试验设备经营部。
1.2 仪器与设备
UV-2450紫外分光光度计 日本岛津公司;电泳仪伯乐生命医学产品(上海)有限公司;FA2003分析天平上海精密科学仪器有限公司;HH-6富华数显恒温水浴锅金坛市富华仪器有限公司;WT-1插入式温度计 江苏省精创电气股份有限公司;Avanti J-30I冷冻离心机美国贝克曼库尔特公司;XHF-D内切式匀浆机 宁波新芝生物科技股份有限公司;722型可见分光光度计 上海元析仪器有限公司;F-2500荧光分光光度计 日本日立公司。
1.3 方法
1.3.1 样品嫩化处理
将兔后腿肉从-18 ℃的冰箱中取出,置于4 ℃条件下解冻12 h,剔除腿骨以及表面可见脂肪和结缔组织后,将其分为大小均匀,每块质量约20 g的肉块,每100 g肉为一组,将各组实验样品分别置于100 mL质量浓度为35 mg/L的复配嫩化剂(氯化钙、无花果蛋白酶、猕猴桃蛋白酶分别以质量浓度18、11、6 mg/L复配)、氯化钙、无花果蛋白酶、猕猴桃蛋白酶溶液中(磷酸缓冲液调节至pH 8),于30 ℃水浴条件下浸泡处理,以第0、30、60、90、120、150、180分钟为取样点进行指标测量,上述复配嫩化剂比例及嫩化条件已经由响应面及正交试验优化得出[10]。
1.3.2 MP的提取
参考Wang Zhaoming等[11]的方法稍作修改,将嫩化后的兔肉进一步切成块状并用绞肉机绞成肉糜,用于提取MP。将25 g肉糜置于100 mL 0.01 mol/L的磷酸盐缓冲液中(pH 7.0,0.1 mol/L NaCl,0.002 mol/L MgCl2,0.001 mol/L EDTA-2Na),5 000 r/min均质30 s后,5 000 r/min、4 ℃离心30 min,去除上清液,重复上述过程3 次后,取沉淀与100 mL 0.01 mol/L的磷酸盐缓冲液(0.1 mol/L NaCl,pH 6.25)混合,5 000 r/min均质30 s。5 000 r/min、4 ℃离心15 min后,将沉淀与100 mL的磷酸盐缓冲液(0.01 mol/L ,pH 6)混合,5 000 r/min均质30 s后用双层纱布过滤。最后,滤液再次6 000 r/min、4 ℃离心15 min,所得沉淀即为MP,置于4 ℃冰箱保存不超过24 h。
1.3.3 MFI的测定
参考王兆明[12]的方法并作适当修改,剔除可见结缔组织后称取4.00 g肉样并绞碎,加入10 倍体积提取液(0.1 mol/L KCl,0.018 mol/L K2HPO4,0.007 mol/L KH2PO4,0.001 mol/L EDTA-2Na,0.001 mol/L MgCl2,pH 7.0,4 ℃),冰浴条件下5 000 r/min均质1 min后5 000 r/min、4 ℃离心30 min,重复上述操作2 次后,在沉淀中加入15 mL上述冰浴MFI提取液并均质30 s后用单层纱布过滤,所得滤液即为MP提取液。用双缩脲法测定MP提取液中蛋白质量浓度,再用上述MFI提取液调整MP质量浓度至0.5 mg/mL,在540 nm波长处测定吸光度,MFI计算如式(1)所示:
pH值能够反映肌肉内部游离氢离子和氢氧根离子浓度,所以作为一项比较重要的指标来评价水产品的品质[23]。由表6可知,处理条件不同的海螺肉在4 ℃贮藏20天,pH值不相同。pH值会随着海螺贮藏时间的增长而呈现出先降再升的趋势。兰洋的研究验证了兔肉微冻保鲜技术中pH值都先下降后上升,宋华静等[24]在研究微冻保鲜技术中鲜猪肉的pH值变化时也有类似的发现。红茶处理的海螺肉在第15天达到最低pH值。红茶处理后海螺肉样的pH值均略低于未处理的海螺肉。pH值上升速度越快表明样品腐败变质水平越高。本实验表明红茶处理在一定程度上延长了海螺肉的货架期。

式中:A540nm为540 nm波长处测定吸光度;200为吸光系数。
1.3.4 蛋白质溶解度的测定
参考Agyare等[13]的方法作适当修改。将提取出的MP用磷酸盐缓冲液(0.6 mol/L NaCl,0.05 mol/L Na2HPO4,pH 6.2),冰浴条件下2 800 r/min均质0.3 min,制成蛋白质质量浓度为2.5 mg/mL的溶液。然后在4 ℃条件下放置1 h后4 500 r/min、4 ℃离心15 min,用双缩脲法测定上清液中MP的浓度,空白为磷酸盐缓冲溶液。溶解度计算如式(2)所示:

1.3.5 SPC的测定
参照罗海波[14]的方法作适当修改。取兔肉4 g,经绞肉机绞碎,加入10 倍体积提取液(0.007 mol/L KH2PO4,0.018 mol/L K2HPO4,0.001 mol/L EDTA-2Na,0.1 mol/L KCl,0.001 mol/L MgCl2,pH 7.0,4 ℃),冰浴条件下均质处理1 min后5 000 r/min、4 ℃离心30 min,用双缩脲法测定上清液中SPC。
1.3.6 MP表面疏水性
参考Chelh等[15]的方法。用0.02 mol/L的磷酸盐缓冲液(pH 6,0.6 mol/L NaCl)将MP稀释至5 mg/mL,取1 mL稀释液与0.2 mL质量浓度为1 mg/mL的BPB溶液混合,对照组加入1 mL磷酸盐缓冲液和0.2 mL的BPB溶液。25 ℃下置于摇床混合均匀,10 min后2 000 r/min、4 ℃离心15 min,取上清液并用10 倍体积,浓度为0.02 mol/L磷酸盐缓冲液(pH 6)稀释,在595 nm波长处测定吸光度。MP表面疏水性计算如式(3)所示:

1.3.7 蛋白质SDS-PAGE
1.4 数据处理
数据均采用IBM SPSS Statistics 17.0分析处理,取置信度95%(P<0.05,差异显著),采用Origin 2017进行图形绘制。
2 结果与分析
2.1 MFI随嫩化时间的变化
MFI的定义是长度为1~4 个肌节的肌原纤维占全部肌原纤维的比例,可作为表征嫩度的重要指标,MFI值越大,说明肌节中肌动球蛋白的降解程度越大,肌肉嫩度越好[16]。由图1可知,随着嫩化处理的进行,4 个处理组的MFI均呈现增加趋势,在0~60 min内,只有氯化钙组的增长不显著(P>0.05),在第60分钟,蛋白酶组的MFI显著高于复配组(猕猴桃蛋白酶组为75.31f 0.99,无花果蛋白酶组为77.12f 0.79,复配组为73.28f 0.12)(P<0.05),氯化钙组最低(53.66f 1.28),在90~150 min,氯化钙组和无花果蛋白酶组MFI显著增大(P<0.05),猕猴桃蛋白酶组无显著增长(P>0.05),同时复配组的MFI显著增加且后期一直在4 组中保持最大值(P<0.05)。表明在0~90 min之间,复配组MFI显著增长的原因主要由无花果蛋白酶和猕猴桃蛋白酶在蛋白表面的降解作用引起;在90~150 min内,氯化钙的离子作用导致Z盘断裂,MP结构逐渐失去稳定性,促使蛋白质展开,暴露更多酶解位点,进而使蛋白酶的酶解作用增强,且这种协同增效降解作用具有一定持续性和稳定性。

图1 MFI随嫩化时间的变化Fig.1 Changes in MFI with tenderization time
2.2 溶解度随嫩化时间的变化
MP溶解度可以与肌球蛋白粗丝解聚程度呈正相关[17]。由图2可知,4 种嫩化剂处理后的兔肉MP溶解度总体呈现先上升后下降的趋势,复配组溶解度在0~90 min内为最大值且增长速度最快,从(13.99f 0.49)%增加到(52.38f 0.65)%,此后继续增长,在第150分钟达到最大值(53.75f 0.36)%,蛋白酶组的溶解度在0~120 min显著上升,第90分钟无花果蛋白酶组溶解度达到最大值(39.54f 0.36)%,第120分钟猕猴桃蛋白酶组溶解度达到(56.59f 1.38)%,氯化钙组在嫩化前期增长趋势平缓,90~120 min内溶解度显著增加并达到最大值(48.44f 0.27)%,2 种蛋白酶的降解程度有一定差异,这可能是因为在30 ℃时猕猴桃蛋白酶活性比无花果蛋白酶活性高引起的[6]。上述现象表明嫩化初期,复配组溶解度的增加主要由蛋白酶对MP的降解作用导致的,后复配组溶解度的进一步增加是由蛋白酶和氯化钙的共同作用所致,氯化钙增加离子强度,引起电荷间排斥,减小蛋白之间的静电相互作用力,加强蛋白质和水的作用,从而使MP之间的分散性更好[18]。在120~150 min内,氯化钙组和蛋白酶组均呈下降趋势,一方面在高浓度的氯化钙组中蛋白质之间由于疏水作用力重新聚集,溶解度降低[19],另一方面在酶作用下降解产生的小分子蛋白质会重新聚集成大分子蛋白质,导致溶解度降低[20];但是复配组无显著变化(P>0.05)。这可能是因为复配组中的蛋白酶将MP降解后,一定浓度的氯化钙可参与小分子蛋白周围水化层的形成,阻碍小分子蛋白质的重新聚集[18]。上述现象均表明复配嫩化剂可以在短时间内使MP降解成小分子蛋白质,提高溶解度,且这种协同嫩化作用比单一嫩化剂更稳定持久。
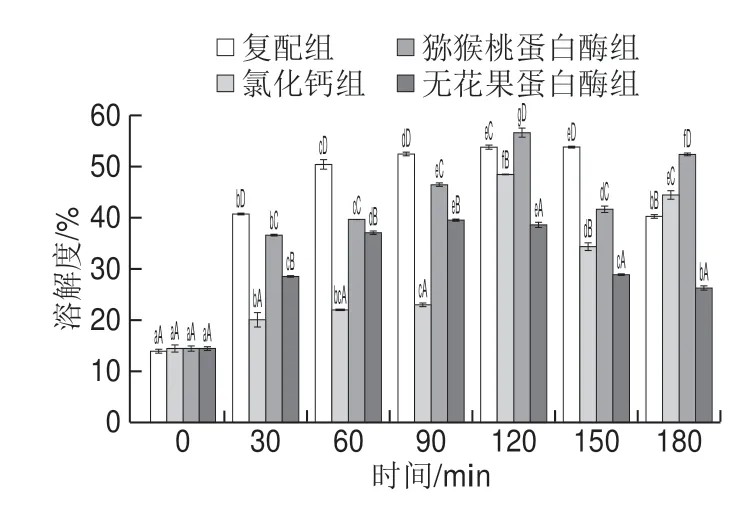
图2 溶解度随嫩化时间的变化Fig.2 Changes in myofibrillar protein solubility with tenderization time
2.3 SPC随嫩化时间的变化
肉的可溶性蛋白主要由肌浆蛋白和肌红蛋白等水溶性蛋白组成[21],同时,MP被降解后也会增加SPC[13],由图3可知,4 种嫩化剂处理下的兔肉中SPC随时间总体呈现下降趋势,中间略有波动,这主要是因为在浸泡嫩化处理过程中,位于细胞液中的一部分水溶性蛋白进入嫩化液中[8],同时由于嫩化剂对MP的降解作用,会增加肉中SPC,因此肉中SPC是一个动态变化的过程,总体而言,流失于溶液中的SPC比降解产生的量大。4 组中氯化钙组的SPC最少,在0~120 min内,其值下降幅度最大,从(7.26f 0.21)mg/mL下降到(4.27f 0.04)mg/mL,表明由MP解聚所产生的小分子蛋白量较少,说明氯化钙在这段时间内降解MP的速度比其他3 组慢,后氯化钙组SPC有小幅度增长,表明120 min后,氯化钙降解MP的速率略大于可溶性蛋白流失于溶液中的速度,直至二者达到动态平衡;2 个蛋白酶组的SPC虽然总体呈波动下降趋势,但2 组的SPC始终高于氯化钙组和复配组,且下降幅度也较小,猕猴桃蛋白酶组和无花果蛋白酶组在第180和150分钟分别达到最小值(6.21f 0.10)mg/mL和(6.06f 0.08)mg/mL,这是由于蛋白酶降解MP产生的小分子蛋白质补充了流失于溶液中的可溶性蛋白。复配组SPC在第120分钟达到最小值为(5.61f 0.24)mg/mL,可见在复配组中,氯化钙使MP结构松散,蛋白酶可充分与作用位点结合,产生大量可溶性蛋白,但同时可能因为一部分可溶性蛋白由于蛋白结构变疏松,更容易流失于溶液中,所以复配组SPC介于氯化钙组和蛋白酶组之间。上述现象表明在降解早期,复配成分中的蛋白酶对SPC的增加起主要作用,在第90分钟时,复配组与2 个蛋白酶组的差异不明显,可以推测2 种蛋白酶复合使用其特异性比单一使用更小,降解作用更好,因为复配组中总蛋白酶的含量比单一酶组的含量少。而在120 min后氯化钙与蛋白酶的协同作用显著,使复配组中SPC开始增加。

图3 SPC随嫩化时间的变化Fig.3 Changes in SPC with tenderization time
2.4 表面疏水性随嫩化时间的变化
表面疏水性反映蛋白质中疏水性残基在蛋白表面的分布情况,其变化可以反映出蛋白质表面疏水性氨基酸残基的相对含量,从而表征蛋白质表面性质及结构的变化情况[22],表面疏水性越大,表明MP表面疏水性基团越多。由图4可知,复配组、氯化钙组、猕猴桃蛋白酶组的表面疏水性随处理时间延长呈先增加后减小的趋势,无花果蛋白酶组表面疏水性一直增加,说明4 种嫩化剂均引起MP分子展开,蛋白质构象变得疏松,稳定性下降,原本聚集在非极性环境的蛋白质内部的疏水性基团暴露到外部极性环境中,导致表面疏水性基团含量增加,从而表面疏水性增加[7],后期表面疏水性降低,其原因可能是大量暴露的疏水性基团导致MP表面疏水作用力增加,蛋白质又聚集起来,从而降低了表面疏水性,这与MP溶解度所反映的情况一致。其中氯化钙组比蛋白酶组的表面疏水性大,在第120分钟达到最高值(118.43f 0.86)μg,一方面氯化钙的离子作用较强,使肌球蛋白结构疏散而展开[12],另一方面钙离子可以降低非极性基团转移到水中所需要的自由能,促进疏水基团的暴露[18];蛋白酶组则是通过降解作用使MP结构发生变性而引起折叠打开,分子结构伸展,暴露疏水性残基,后期被分解的小分子蛋白质又重新聚合折叠[23],其中猕猴桃蛋白酶在第90分钟达到最大值(77.73f 1.11)μg,无花果蛋白酶最大值为(66.32f 0.58)μg,这种差异可能是由于2 种蛋白酶的作用位点不一致,对MP表面疏水基团的影响程度不同,同时可以看出复配组的表面疏水性比其他组高,在第150分钟达到(124.38f 0.54)μg,说明蛋白酶和氯化钙复配使用对MP结构的改变比单独使用时更显著,复配组中的3 种嫩化剂有更好的协同作用,氯化钙使蛋白质结构最大化展开,2 种蛋白酶分别利用自己不同的底物特异性降解MP,促使折叠进一步展开,蛋白质结构发生更大程度的变化,暴露出更多的疏水性氨基酸残基。
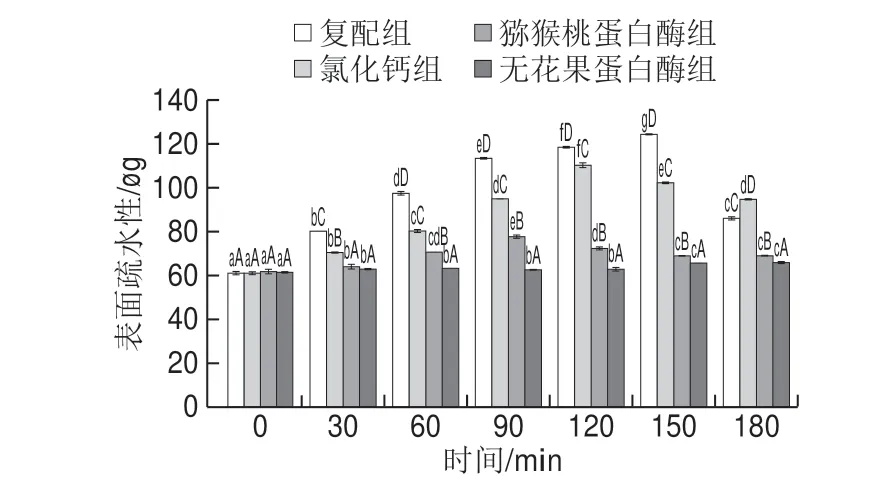
图4 表面疏水性随嫩化时间的变化Fig.4 Changes in surface hydrophobicity with tenderization time
2.5 SDS-PAGE随嫩化时间的变化
由图5可知,未经处理时(0 min),最明显的蛋白条带主要集中在180~245、140~180、100 kDa及75 kDa左右、30~45 kDa和低于25 kDa的区域。随嫩化时间的延长,4 组不同嫩化剂处理下的MP均发生了一定的变化。从图5A可以看出,复配组中180~245 kDa条带明显变细,颜色变淡,这主要是由肌球蛋白重链(myosin heavy chain,MHC)降解导致的,肌球蛋白是肌肉中重要的结构蛋白,占MP的45%左右,MHC的分子质量约200 kDa,它的降解与肉品嫩度呈显著正相关[24],此外100 kDa左右的C蛋白和15 kDa左右的肌球蛋白轻链(myosin light chain,MLC)在第90分钟时有明显的降解现象,其条带浓度降低并在后期逐渐消失,位于30~45 kDa的数条条带也明显变淡,但位于30 kDa左右的原肌球蛋白和45 kDa左右的肌动蛋白条带没有显著变化。从图5B可以看出,氯化钙组中140~245、30、45 kDa及75 kDa左右的条带无明显变化,100 kDa左右的C蛋白条带在30~90 min内变浅,后期颜色有所加深,只有分子质量在15~25 kDa及30~45 kDa之间的蛋白有显著的降解现象,表明氯化钙对蛋白的降解作用是有限的。从图5C可以看出,猕猴桃蛋白酶组中180~245 kDa的条带在30~120 min内明显变细变浅,但在第150分钟时条带又有所增粗,表明猕猴桃蛋白酶对MHC有显著降解作用,这与Liu等[25]的结果一致,但后期可能随着嫩化的进行,被降解的蛋白质由于相互作用力又重新聚集在一起,此外,75 kDa左右蛋白条带在第30分钟左右就基本消失,但是其他蛋白条带并没有明显的变化,表明猕猴桃蛋白酶的特异性较高。从图5D可以看出,无花果蛋白酶组中,140~180、100 kDa左右、30~45 kDa以及25 kDa以下的蛋白条带明显变细变浅,而其他条带无明显变化,表明无花果蛋白酶对MLC、C蛋白的降解作用强烈。总体而言,复配组的MHC条带变化程度比其他3 组更大,降解最显著,且在最后条带没有发生显著的增粗现象,说明2 种蛋白酶和氯化钙复合对蛋白质的降解作用比单独使用效果更明显且更稳定,同时也可以说明在复配成分中起降解蛋白作用的主要以2 种蛋白酶为主,并且这2 种蛋白酶对蛋白的降解具有不同的特异性,所以复合使用时可以结合的作用位点更广,降解作用更显著,结合其他指标也可以推测氯化钙的作用主要是使蛋白质结构失去稳定性从而展开暴露出更多的酶结合位点,使酶解作用更充分。
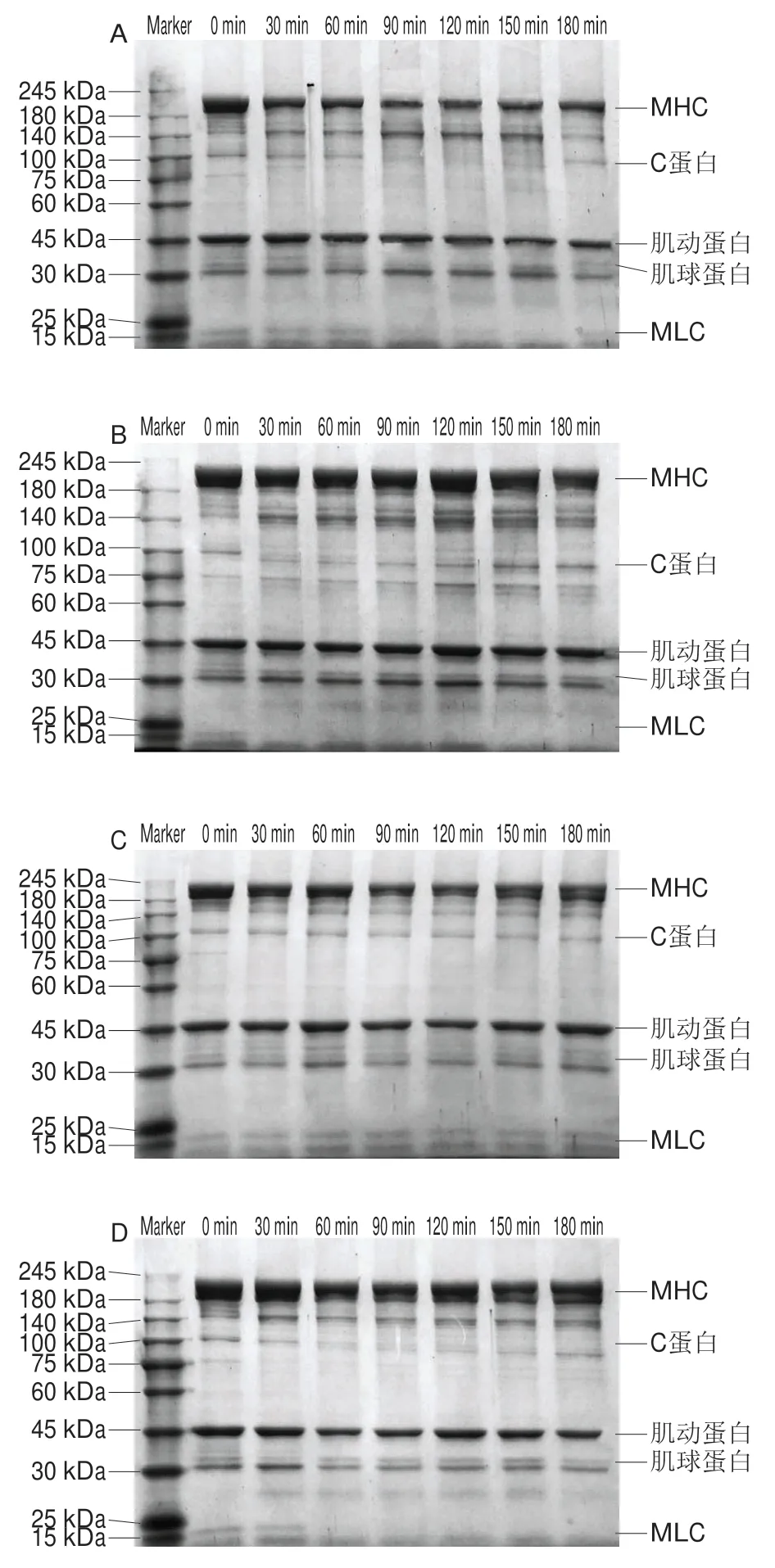
图5 SDS-PAGE随嫩化时间的变化Fig.5 Changes in SDS-PAGE pattern with tenderization time
3 讨论与结论
选取复配组MFI不再发生显著变化(P>0.05)的时间节点为实验终点,因为研究对象为复配嫩化剂对兔肉的协同嫩化机理,而MFI可作为反映MP降解程度和肉品嫩化程度的指标[26]。实验结果表明,复配嫩化剂可以更显著提高MFI,这表明复配组在相同时间内对MP的降解和对肉品嫩度的提高比其他组更明显。电泳图谱也进一步说明复配组具有更高的嫩化效率,可以看到在嫩化至第90分钟时,复配组中大分子蛋白质条带已经明显变浅变窄。蛋白质表面疏水性先增加后减小的变化趋势表明,在嫩化过程中,MP结构先展开后聚集,复配组疏水性最高,说明复配组蛋白质展开程度最大,暴露出了更多的疏水性氨基酸残基,氯化钙组比其他2 种单一酶组更能有效提高表面疏水性,说明氯化钙在复配嫩化剂中的作用主要以改变蛋白质结构为主,而且关于氯化钙通过改变蛋白结构,提高蛋白表面疏水性的研究也早有报道[27],推测其机理一方面由于氯化钙静电相互作用,即增加电荷间排斥作用,使Z盘机械性断裂[28],另一方面,因为在动物死后,m-蛋白酶比μ-蛋白酶保留时间更久[29],故外源Ca2+也可通过激活m-钙蛋白酶,作用于部分骨架蛋白和肌钙蛋白T,使蛋白质结构失去稳定性[30],但钙蛋白酶的降解作用有限,对肌球和肌动蛋白的作用不明显,这与电泳图谱中观察到的氯化钙组发生变化的条带主要以肌钙蛋白T为主相一致。MP溶解度和肌原纤维降解度呈正相关[31],复配组的溶解度最高,其次为2 种蛋白酶,同时SPC可以反映出流失到嫩化剂中的水溶性蛋白含量和肌原纤维被降解所产生的可溶性小分子蛋白质之间的动态关系,氯化钙组的溶解度和SPC显著低于2 个单一酶组,表明蛋白酶在复配嫩化剂中的主要作用以降解MP为主,电泳图谱还表明了2 种酶具有不同的酶解特异性。
复配嫩化剂的组成成分有一定协同作用,根据指标变化判断机理是氯化钙使MP结构松散并展开,暴露出更多酶结合位点,使2 种酶的降解作用更强烈,同时2 种蛋白酶的特异性不同,结合使用可以使降解作用更广泛,降解效率更高。

