2-取代-7-溴-1,2-二氢酞嗪的合成
杨 帆,王咏琪,黎 阳,张 帅,康 慨,仝红娟,2*
(1.陕西国际商贸学院医药学院,陕西 西安 712046;2.陕西省中药绿色制造技术协同创新中心,陕西 西安 712046)
酞嗪类化合物作为一种重要的含氮杂环类化合物,具有广泛的生物活性,如抗痉挛[1]、抗细胞毒素[2]、抑菌[3-4]、抗癌[5]、抗炎[6]等,可作为强心药[7]、血管弛缓药[8],在有机合成及药物合成领域具有重要的研究价值,是药物合成领域的研究热点。酞嗪类化合物的合成方法较多,但存在诸多问题,如过渡金属的使用、催化剂用量大且价格昂贵、后处理繁琐等[9]。1,2-二氢酞嗪是重要的酞嗪类衍生物,目前有关其合成的报道较少[10]。
作者以4-溴-2-甲基苯腈为原料,经溴代、还原得到化合物4-溴-2-(溴甲基)苯甲醛(Ⅱ),再与4-取代苯肼反应得到2-取代-7-溴-1,2-二氢酞嗪(Ⅰ),通过1HNMR和ESI-MS对目标化合物结构进行表征,并考察物料比、催化剂种类及用量、Na2CO3用量、反应溶剂、反应温度、反应时间对目标化合物收率的影响,优化合成条件。合成路线如图1所示。
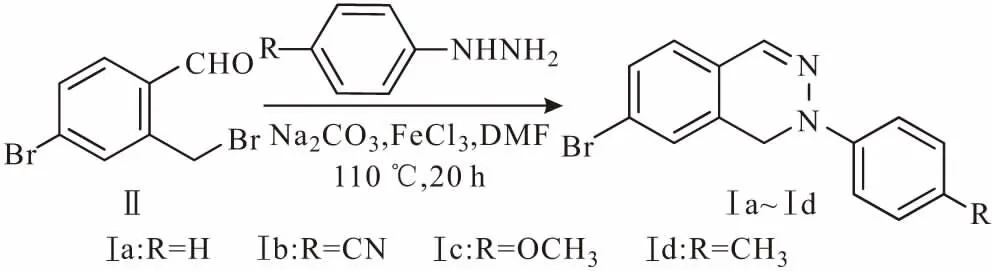
图1 2-取代-7-溴-1,2-二氢酞嗪的合成路线
1 实验
1.1 试剂与仪器
4-溴-2-(溴甲基)苯甲醛,按文献[11]方法合成;苯肼、4-氰基苯肼、4-甲氧基苯肼、4-甲基苯肼均为分析纯,阿达玛斯试剂有限公司;柱层析硅胶(300~400目),试剂级,青岛海洋化工厂。
AV300型核磁共振仪(CDCl3为溶剂,TMS为内标),德国Bruker公司;RE-52AA型旋转蒸发仪,上海亚荣生化仪器厂;SHB-Ⅲ型循环水式多用真空泵,郑州长城科工贸有限公司;Ultima Global Spectrometer型质谱仪(ESI源),美国Waters公司。
1.2 合成方法
在50 mL装有回流冷凝管的三口瓶中加入552 mg(2.0 mmol)4-溴-2-(溴甲基)苯甲醛(Ⅱ)、2.2 mmol 4-取代苯肼、636 mg(6.0 mmol)碳酸钠、32 mg(0.2 mmol)三氯化铁和20 mLN,N-二甲基甲酰胺(DMF),110 ℃下搅拌20 h,TLC监测反应结束后,降至室温,然后加入60 mL乙酸乙酯稀释,依次进行水洗涤(2×50 mL)、饱和食盐水洗涤(2×50 mL),合并有机相,无水硫酸钠干燥,减压浓缩,柱层析分离纯化(洗脱剂V石油醚∶V乙酸乙酯=10∶1),得到目标化合物Ⅰ2-取代-7-溴-1,2-二氢酞嗪。
2 结果与讨论
2.1 目标化合物的表征
将4-溴-2-(溴甲基)苯甲醛(Ⅱ)分别与4种4-取代苯肼反应,合成得到4种目标化合物Ⅰa、Ⅰb、Ⅰc、Ⅰd,其表征数据如下:
2-苯基-7-溴-1,2-二氢酞嗪(Ⅰa):淡黄色固体,收率83%。1HNMR(300 MHz,CDCl3),δ:7.44(dd,J=8.2 Hz、1.8 Hz,1H),7.42(s,1H),7.38(t,J=8.4 Hz,2H),7.33(br,1H),7.30(d,J=8.4 Hz,2H),7.09(d,J=8.4 Hz,1H),7.06(t,J=8.7 Hz,1H),4.74(s,2H);ESI-MS,m/z:[M+H]+287.05。
2-(4-氰基苯基)-7-溴-1,2-二氢酞嗪(Ⅰb):白色固体,收率68%。1HNMR(300 MHz,CDCl3),δ:7.46~7.44(m,1H),7.42(s,1H),7.39(t,J=8.4 Hz,2H),7.35~7.30(m,2H),7.30(d,J=7.8 Hz,1H),4.71(s,2H);ESI-MS,m/z:[M+H]+312.07。
2-(4-甲氧基苯基)-7-溴-1,2-二氢酞嗪(Ⅰc):淡黄色固体,收率89%。1HNMR(300 MHz,CDCl3),δ:7.45~7.43(m,1H),7.43(s,1H),7.38(t,J=8.3 Hz,2H),7.33~7.29(m,2H),7.18(dd,J=7.6 Hz、1.6 Hz,1H),7.13(d,J=7.8 Hz,1H),6.98~6.95(m,2H),4.74(s,2H),3.80(s,3H);ESI-MS,m/z:[M+H]+317.06。
2-(4-甲基苯基)-7-溴-1,2-二氢酞嗪(Ⅰd):淡黄色固体,收率88%。1HNMR(300 MHz,CDCl3),δ:7.44~7.42(m,1H),7.41(s,1H),7.39(t,J=8.4 Hz,2H),7.33~7.30(m,2H),7.19~7.16(m,2H),4.76(s,2H),2.31(s,3H);ESI-MS,m/z:[M+H]+301.08。
2.2 合成条件优化
以2-苯基-7-溴-1,2-二氢酞嗪(Ⅰa)的合成为模型反应,考察合成条件(物料比、催化剂种类及用量、Na2CO3用量、反应溶剂、反应温度及反应时间)对目标化合物Ⅰa收率的影响。
2.2.1 物料比对目标化合物Ⅰa收率的影响
考虑原料成本因素,选择苯肼过量。以FeCl3为催化剂、N,N-二甲基甲酰胺为反应溶剂,在FeCl3用量n(FeCl3)∶n(化合物Ⅱ) 为 0.10∶1、Na2CO3用量n(Na2CO3)∶n(化合物Ⅱ)为3.0∶1、反应温度为110 ℃、反应时间为20 h的条件下,考察物料比(化合物Ⅱ与苯肼物质的量比)对目标化合物Ⅰa收率的影响,结果见表1。

表1 物料比对目标化合物Ⅰa收率的影响
由表1可知,当物料比n(化合物Ⅱ)∶n(苯肼)为1∶1.0时,目标化合物Ⅰa的收率为78%;增加苯肼用量至n(化合物Ⅱ)∶n(苯肼)为1∶1.1时,收率提高到83%;继续增加苯肼用量至n(化合物Ⅱ)∶n(苯肼)为1∶1.2、1∶1.3时,收率变化较小。因此,确定最佳物料比n(化合物Ⅱ)∶n(苯肼)为1∶1.1。
2.2.2 催化剂种类及用量对目标化合物Ⅰa收率的影响
在确定了物料比n(化合物Ⅱ)∶n(苯肼)为1∶1.1后,固定Na2CO3用量n(Na2CO3)∶n(化合物Ⅱ)为3.0∶1、N,N-二甲基甲酰胺为反应溶剂、反应温度为110 ℃、反应时间为20 h,考察催化剂种类及用量对目标化合物Ⅰa收率的影响,结果见表2。
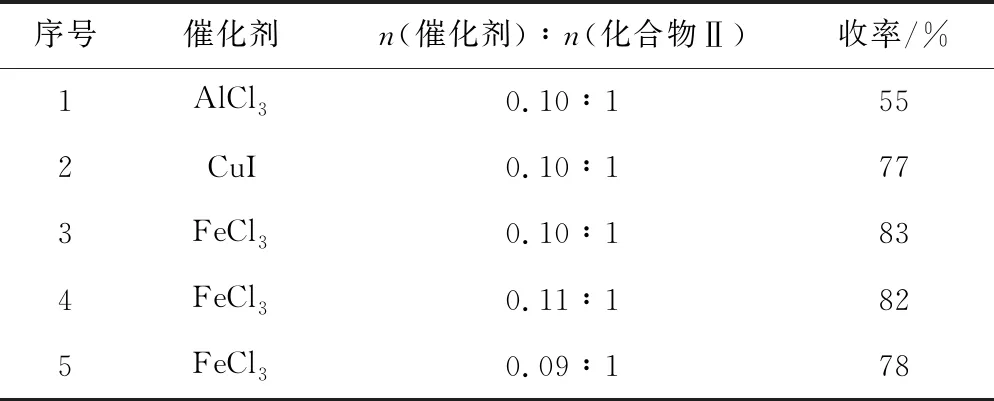
表2 催化剂种类及用量对目标化合物Ⅰa收率的影响
由表2可知,3种催化剂AlCl3、CuI、FeCl3均能催化该反应的进行,在其用量n(催化剂)∶n(化合物Ⅱ)为0.10∶1时,目标化合物Ⅰa的收率分别为55%、77%、83%,FeCl3的催化活性最高。进一步对FeCl3用量进行考察发现,增加FeCl3用量n(FeCl3)∶n(化合物Ⅱ)至0.11∶1时,目标化合物Ⅰa的收率没有明显变化;而减少FeCl3用量n(FeCl3)∶n(化合物Ⅱ)至0.09∶1时,收率明显降低。因此,确定催化剂为FeCl3,其最佳用量n(FeCl3)∶n(化合物Ⅱ)为0.10∶1。
2.2.3 Na2CO3用量对目标化合物Ⅰa收率的影响
在确定了物料比n(化合物Ⅱ)∶n(苯肼)为1∶1.1、催化剂FeCl3用量n(FeCl3)∶n(化合物Ⅱ)为0.10∶1后,固定N,N-二甲基甲酰胺为反应溶剂、反应温度为110 ℃、反应时间为20 h,考察Na2CO3用量对目标化合物Ⅰa收率的影响,结果见表3。

表3 Na2CO3用量对目标化合物Ⅰa收率的影响
由表3可知,当Na2CO3用量n(Na2CO3)∶n(化合物Ⅱ)为2.0∶1时,目标化合物Ⅰa的收率仅65%;增加Na2CO3用量n(Na2CO3)∶n(化合物Ⅱ)至3.0∶1时,收率提高到83%;继续增加Na2CO3用量,收率开始降低,当Na2CO3用量n(Na2CO3)∶n(化合物Ⅱ)增至4.0∶1时,收率降为80%。因此,确定Na2CO3最佳用量n(Na2CO3)∶n(化合物Ⅱ)为3.0∶1。
2.2.4 反应溶剂对目标化合物Ⅰa收率的影响
在确定了物料比n(化合物Ⅱ)∶n(苯肼)为1∶1.1、催化剂FeCl3用量n(FeCl3)∶n(化合物Ⅱ)为0.10∶1、Na2CO3用量n(Na2CO3)∶n(化合物Ⅱ)为3.0∶1后,固定反应温度为110 ℃、反应时间为20 h,考察反应溶剂对目标化合物Ⅰa收率的影响,结果见表4。

表4 反应溶剂对目标化合物Ⅰa收率的影响
由表4可知,以甲苯和二氧六环为反应溶剂时,目标化合物Ⅰa的收率较低,分别为61%和57%;以乙腈和N,N-二甲基甲酰胺为反应溶剂时,收率较高,其中,以N,N-二甲基甲酰胺为反应溶剂时的收率最高,达到83%。因此,确定N,N-二甲基甲酰胺为反应溶剂。
2.2.5 反应温度对目标化合物Ⅰa收率的影响
在确定了物料比n(化合物Ⅱ)∶n(苯肼)为1∶1.1、催化剂FeCl3用量n(FeCl3)∶n(化合物Ⅱ)为0.10∶1、Na2CO3用量n(Na2CO3)∶n(化合物Ⅱ)为3.0∶1、N,N-二甲基甲酰胺为反应溶剂后,固定反应时间为20 h,考察反应温度对目标化合物Ⅰa收率的影响,结果见表5。

表5 反应温度对目标化合物Ⅰa收率的影响
由表5可知,在反应温度为90 ℃时,目标化合物Ⅰa的收率为56%;升高反应温度,收率逐渐提高,当反应温度升至110 ℃时,收率提高到83%;继续升高反应温度,收率反而稍有降低。因此,确定最佳反应温度为110 ℃。
2.2.6 反应时间对目标化合物Ⅰa收率的影响
在确定了物料比n(化合物Ⅱ)∶n(苯肼)为1∶1.1、催化剂FeCl3用量n(FeCl3)∶n(化合物Ⅱ)为0.10∶1、Na2CO3用量n(Na2CO3)∶n(化合物Ⅱ)为3.0∶1、N,N-二甲基甲酰胺为反应溶剂、反应温度为110 ℃后,考察反应时间对目标化合物Ⅰa收率的影响,结果见表6。

表6 反应时间对目标化合物Ⅰa收率的影响
由表6可知,在反应时间为16 h时,目标化合物Ⅰa的收率为74%;随着反应时间的延长,收率逐渐提高,在反应时间为20 h时,收率提高到83%;继续延长反应时间,收率变化不大。因此,确定最佳反应时间为20 h。
3 结论
以4-溴-2-(溴甲基)苯甲醛(Ⅱ)为原料,分别与4种4-取代苯肼反应得到4种2-取代-7-溴-1,2-二氢酞嗪化合物。以2-苯基-7-溴-1,2-二氢酞嗪(Ⅰa)的合成为模型反应,确定最优合成条件如下:物料比n(化合物Ⅱ)∶n(苯肼)为1∶1.1、催化剂FeCl3用量n(FeCl3)∶n(化合物Ⅱ)为0.10∶1、Na2CO3用量n(Na2CO3)∶n(化合物Ⅱ)为3.0∶1、N,N-二甲基甲酰胺为反应溶剂、反应温度为110 ℃、反应时间为20 h,在此条件下,化合物Ⅰa的收率可达到83%。该方法具有底物和催化剂价廉易得、收率高、后处理简单等优点。

