基于建模教学发展化学高阶思维的教学研究
李金燕 杨剑 钟奕玲 罗一帆 许旋
摘要:以“电解原理之放电顺序的探究”为素材,从学生已学的惰性电极电解氯化铜溶液的分析模型进阶到通过惰性電极电解氯化钠溶液的探究,从离子放电顺序的视角完善电解池认识模型,再通过创设“净水器推销商”的真实情境开展铁铝电极电解氯化钠溶液的探究,进一步从电极材料的认识视角对电解原理认识模型进行修正。建模教学在建构化学知识的同时,促进学生的化学高阶思维能力和素养的有效发展。
关键词:建模教学;电解池放电顺序;高阶思维
文章编号:1008-0546(2021)10-0047-05中图分类号:G632.41文献标识码:B
doi:10.3969/j.issn.1008-0546.2021.10.011
《普通高中化学课程标准(2017年版)》提出的“模型认知”是化学学科的重要思想和方法[1],在教学中要引导学生构建思维模型,促进学生建模思维和建模能力的提升。霍伦(1996)[2]提出建模教学主要包括构建模型、评价模型、完善模型、应用模型,具体表现为先选择已构建的模型来解决问题;在新的情境下对已有的模型进行评价进而修正模型。新课标提倡“素养为本”的教学理念,倡导真实问题情境的创设,开展以化学实验为主的多种探究活动,重视教学内容的结构化设计,注重培养学科思维,其中培养学生解决陌生情境下不同复杂程度问题的能力,是“素养为本”化学课堂教学追求的重要目标。陌生情境下复杂问题的解决,需要学生具有较强的化学科学思维能力,尤其是高阶思维能力,其中化学高阶思维能力包括:概括关联的能力、解释说明能力、推断预测的能力、设计验证的能力及分析评价的能力等[3]。
一、内容分析
本节课主要选自人教版选修四第四章第三节《电解池》电解原理第二课时,“化学能与电能的相互转化”是贯穿第四章的主线。在原电池的学习中,学生已经了解自发的氧化还原反应通过原电池将化学能转化为电能,本节的核心概念是“对于非自发的氧化还原反应可以通过电解池实现由电能到化学能的转化”,本节的基本概念:电解池的基本要素、明确电解池的工作原理(包括电子导体回路、溶液中的离子行为、电极材料与电极反应、电极上放电顺序),电解池原理的内容结构图如图1。人教版教材的第一课时惰性电极电解CuCl2溶液承载着电解池的基本要素、溶液中的离子行为、电极反应等核心知识。本节课主要对电极上放电顺序及电极材料这两个基本概念从模型认知的视角进行建构,为下节课电解池的应用做知识铺垫。

二、基于模型建构的教学
1.“电解原理放电顺序”模型教学分析
通过回顾第一节课惰性电极电解氯化铜溶液归纳出电解池认识分析模型(溶液中存在哪些离子;通电时离子如何移动;产物、电极方程式),进阶到惰性电极电解饱和食盐产物的探究,从离子放电顺序的视角完善已有的电解池分析模型,再应用已有的模型去分析净水器推销商“科学实验”的真实情境时,学生发现已建立的分析模型不能适用,进而需要在原有的模型基础上通过探究金属活性电极电解饱和食盐水,进而发展学生电解池的分析的视角。通过回顾已有的电解池分析模型发展学生的概括关联、分析解释的高阶思维,在已有模型的基础上通过实验探究发展学生的推理预测、简单设计的高阶思维,将模型应用到真实情境中检验模型从而进行修正,发展学生的分析评价、系统探究的高阶思维,具体框架如图2。

3.教学重难点
从离子放电顺序和活性电极的两个视角发展电解池的分析模型。
4.突破教学重难点(教学策略)
在已有的模型基础上进行问题驱动和实验探究从而完善模型,在真实情境中应用模型进行系统探究和发展视角来修正模型。模型建构过程如图3所示。
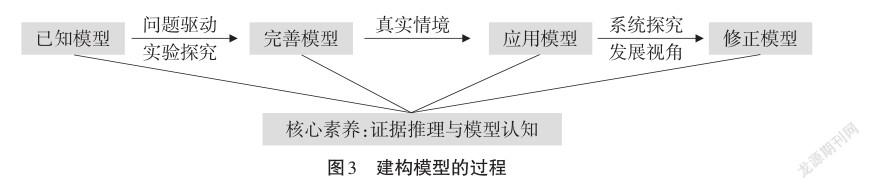
三、教学过程
1.教学设计流程图
本节课以“探究电解原理的放电顺序”为主线,以“惰性电极电解氯化钠溶液和铁铝电极电解氯化钠”为情境开展教学活动,具体流程如图4。
2.教学具体过程
环节一:回顾电解原理第一课时电解池分析认识模型
【回顾模型】第一节课我们通过惰性电极电解Cu? Cl2溶液的学习,从宏观到微观的视角归纳出了电解池反应的认知思维模型,请同学们进行回顾。
【学生回答】1.溶液有什么离子?2.通电后,离子如何移动?3.产物、电极反应
【提出问题】CuCl2溶液中除了Cl-、Cu2+其实还存在水电离的OH-、H+,通电时Cl-、OH-都向阳极移动,Cu2+、H+都向阴极移动,但是实验中H+和OH-都没有参与反应,那么如果利用上述实验的电解池装置来电解NaCl溶液,能否也得到金属Na?
设计意图:回顾第一课时电解CuCl2实验课本已建立的模型是还没考虑水中电离的OH-、H+,从已有的知识提出问题自然过渡到用惰性电极电解氯化钠溶液的探究,促进学生认识思路结构化。发展学生的概括关联能力。
环节二:通过惰性电极电解NaCl溶液,了解离子放电顺序,完善模型
【教师演示】惰性电极电解NaCl溶液
【收集证据】两个电极都产生了气泡
【学习任务】请同学们对惰性电极电解NaCl溶液的气体产物进行预测,并试着设置实验方案证明你们的预测。
【理论分析】根据实验结果思考以下问题:
1.NaCl溶液中存在哪些离子?
2.通电后,溶液中的离子如何移动?
3.结合证据,从得失电子、氧化还原反应的角度进行分析阴阳极可能的产物?
【学生讨论】
1.溶液总共四种离子Cl-、Cu2+、OH-、H+
2.Cl-、OH-移向阳极失电子;H+、Na+移向阴极得电子
【实验设计】对于阴极:基于有气泡放出的证据,可推测是H+放电,氢气的检验用点燃法和肥皂泡法;对于阳极:可能是Cl-失电子会变成氯气或是OH-失电子后必有一种元素化合价升高,推测产生的气体是氧气,氯气的检验可以用湿润碘化钾试纸;氧气检验用带火星木条。
【评价方案】引导学生对氢气检验方法(点燃法和肥皂泡法)进行评价:危险并难于成功。
【教师引导】水电离的H+得电子变成气体离开溶液体系,溶液体系会剩下大量的OH-,可通过间接检验OH-的存在(滴加酚酞)证明是氢离子放电变成氢气。
【学生实验】惰性电极电解NaCl溶液的产物检验(图5)。


【收集证据】阴极附近区域变红;阳极附近区域的湿润碘化钾试纸变蓝。
【证据分析】阴极是H+得电子变成氢气;阳极是Cl-失电子会变成氯气。
设计意图:引导学生从证据和氧化还原的理论两个角度进行产物的预测,可以减少探究的盲目性。对学生收集的证据及时提出任务教学,学生经过前面的学习,对理论分析部分以及阳极产物的检验能合作完成,知道氯气用湿润淀粉-KI试纸检验,氧气用带火星木条;而对于检验H2的方法,需要进行引导。发展学生推理预测、设计验证及分析解释的高阶思维能力,从而真正落实素养的发展。
【讨论总结】根据实验的结果,我们可以知道阴极:H+先于Na+放电;阳极:Cl-先于OH-放电,
【学习任务】你能解释不同离子的放电顺序为何不一样吗?
【理论分析】根据实验结果思考以下问题:
1.离子移动有何目的?
2.陽离子和阴离子能否放电与什么因素有关?
【学生讨论】离子移动的目的主要是得失电子,在阴极H+的得电子能力比Na+强,而得电子能力主要是反应氧化性的强弱;阳离子能否放电主要跟离子的氧化性有关;同理,阴离子能否放电主要跟离子的还原性有关。
【分析总结】离子放电顺序
阳极:阴离子——失电子(有还原性)
还原性强的离子优先放电:Cl->OH->含氧酸根离子(SO2-4等)
阴极:阳离子——得电子(有氧化性),氧化性强的离子优先放电:Cu2+>H+>Na+
【归纳推理】
阴离子放电(失电子)顺序:S2->I->Br->Cl->OH->SO2-4等
阳离子放电(得电子)顺序:Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+>K+
【完善模型】
在判断惰性电极电解池的阴极、阳极产物时我们要思考离子的放电顺序。
分析电解池反应的思维程序:
(1)溶液中存在哪些离子?
(2)通电时离子如何移动?
(3)离子放电顺序
(4)产物、电极反应
【讲解】经过探究学习,电解池装置电解NaCl溶液,是没办法得到金属Na。
设计意图:由惰性电极电解CuCl2的认识模型,迁移到电解NaCl溶液,通过分析电解NaCl溶液产物,从离子放电顺序的视角发展分析电解池的思维模型。由个别归纳推理出惰性电极的电解池一般的离子放电顺序。由于学生对离子的氧化性和还原性的比较有一定的认识,对于推理放电顺序的原因不是很难。发展学生的概括关联和分析解释的高阶思维能力。
环节三:应用模型,推销商的“科学实验
【新闻视频】成都周边一些消费者反映,卖净水器的推销商用电解仪放入饮用水出现了所谓的先变绿后变黄等现象(图6),并说这是“重金属”等有害物质,这种检测结果可信吗?

【资料卡片】推销商电解仪电极是铁棒和铝棒;自来水许多矿物质
【学生思考】观看新闻,结合资料卡片对新闻进行思考
【提出问题】已有分析电解池的模型是分析惰性电极电解模型,而对于分析金属活性电极的电解模型是否还适合呢?
【学习任务】采用控制变量法设置实验:相同的电解质溶液而不同的电极材料(改用活性电极)进行实验。
【思考和交流】从控制变量法的原理思考
设计意图:贴切的真实情境,将知识关联社会生活,感受学科化学的价值。引导学生根据实际需要提出探究课题,为了减少探究的盲目性,提供资料卡片并引导学生在提取原来的电解池分析模型时,发现原有的模型不适用,并引导学生确定探究任务“不同的电极材料电解相同的电解质”。
环节四:铁铝电极电解NaCl溶液,完善电解池认识分析模型,
【演示实验】铁铝电极电解NaCl溶液
【收集证据】阴极Al棒附近产生了无色气体;阳极Fe棒溶解且溶液周围先变绿色再变黄色
【追问】请同学们从理论分析和事实证据对产物进行推测及设置实验方案验证
【学生讨论】阳极Fe棒溶解且溶液周围变绿色,推测可能是电极Fe失去电子变成Fe2+,再被空气氧化成Fe3+,检验Fe3+可以用KSCN;阴极是产生无色气体,可能是来自水电离的H+得电子变成H2,可用酚酞间接检验是否有OH-即可证明是否是氢离子放电。
【实验验证】铁铝电极电解NaCl溶液的产物检验
【收集证据】阴极附近区域变红;阳极溶液变绿后再变黄,取阳极附近的溶液滴加KSCN溶液发现血红色。
【证据分析】说明阳极的Fe棒先于溶液离子失去电子变成Fe2+,Fe2+被空气氧化变成Fe3+。而Al棒连接在阴极,金属一般不会得到电子。
【完善模型】在判断电解池的阴极、阳极产物时我们先判断阳极是惰性还是活性电极,再思考离子的放电顺序。
【提出问题】现在你能识破推销商的“骗局”了吗?
【学生展示】小组进行铁铝电极电解自来水实验并解释说明原因。
设计意图:前面已经学习了Fe的化合物性质以及从离子放电顺序分析电解池原理,所以对于产物推断以及验证,学生能自主讨论交流完成,从离子的放电顺序和电极材料两个角度完善了电解池原理的认识,建构电解池的一般认识思路。回应情境,感受化学知识的价值,发展学生推理预测、设计验证及分析解释的高阶思维能力。
环节五:抗疫和“惰性电极电解氯化钠溶液”
【视频观赏】惰性电极电解氯化钠溶液可制备出抗疫的“一分子”——消毒液
【课后活动】写份小论文,谈谈为什么惰性电极电解氯化钠溶液可以制备消毒液?
设计意图:诊断与发展学生学科核心素养中社会责任水平及将化学成果应用于生产、生活的意识。本节课以电解氯化钠为主线,最后拓展惰性电极电解氯化钠溶液可制备出抗疫的“一分子”——消毒液,响应2020年抗疫的口号。
四、结语
建模教学重视认识视角和认识思路的形成,根据已有知识、理论和经验进行抽象、构建出初步模型,再经过验证、修正等若干操作表征研究对象的模型,丰富他们对化学反应原理的认识角度,提高他们对反应原理的认识深度,从而建立具有学科特质的化学认识视角和化学认识思路,进而发展学生的化学学科思维方式,真正落实从化学知识进阶到高阶思维能力再到素养发展的目标。另外培养学生解决陌生情境下问题的能力,是素養教学的重要目标,而陌生情境下复杂问题的解决,需要学生具有高阶思维能力。之所以基于建模教学可发展学生的化学高阶思维能力,是因为解决复杂问题的过程既是创造性地应用科学模型的过程,也是建构模型的过程。
参考文献
[1]中华人民共和国教育部.普通高中化学课程标准(2017年版)[S].北京:人民教育出版社,2018
[2]张晋,毕华林.模型建构与建模教学的理论分析[J].化学教育(中英文),2017,38(13):27-32
[3]郑长龙,孙佳林.“素养为本”的化学课堂教学的设计与实施[J].课程·教材·教法,2018,38(4):71-78

