双(α-呋喃甲酸)氧钒合成方法的改进及抗癌作用研究
李 雪,高丽辉,高安丽**,姜 婧,巨少英,余 娟
(1. 昆明贵金属研究所 稀贵金属综合利用新技术国家重点实验室,云南 昆明 650106;2. 昆明医科大学 生物医学工程研究中心,云南 昆明 650500)
在临床常用的70多种抗癌药物中,以顺铂为代表的铂类药物占有重要的位置,已广泛用于肺癌、卵巢癌、结肠癌等常见肿瘤的一线治疗,约占所有癌症化疗方案中的50%[1-4]. 尽管如此,目前铂类抗癌药物的临床应用还存在两大障碍:毒副反应和出现耐药性. 在化疗过程中,癌细胞对既往使用过的铂类药物不敏感、产生耐药性,而耐药性的产生降低药物的疗效,导致用药剂量的增加,这又加重了药物的毒副反应,最终造成化疗的失败[5-7]. 因此,寻找能克服或降低癌细胞耐药的新型无机抗癌药物一直是抗癌药物研究的重要方向之一.
钒是人体必需的微量元素,早在1985年加拿大科学家McNeill发现钒的化合物在葡萄糖的代谢过程中起着重要作用,具有多样化的生物学效应,尤其是类胰岛素效应[8]. 2005年由加拿大British Columbia 大学研制的有机钒抗糖尿病药物双(乙基麦芽糖酚)氧钒(BEOV)作为第一个钒类药物在英国进入Ⅰ期临床试验[9],2007年11月BEOV作为口服胰岛素调节剂在美国进入Ⅱ期临床试验[10-12].2008年北京大学王夔院士团队和南开大学闫世平教授团队等在这方面的研究也取得了重要进展[13].然而,国内外关于钒的抗癌作用的研究和报道较少. 1965年J Kieler等首次研究表明钒盐具有抗肿瘤作用[14],2000 年美国 Parker Hughes Institute 提出钒(Ⅳ)配合物和顺铂均能与核DNA相互作用的观点,研究表明它们的作用位点不同,顺铂通过共价键配位到DNA上嘌呤环的第7位氮原子上,而钒和核苷酸磷酸基团相互作用而打断Watson-Crick氢键[15-17]. 与此同时,美国的其他团队例如俄亥俄大学医学院内科学系合成并评价了一些钒的化合物,但均未发现优于顺铂的钒类化合物,研究进展相对比较缓慢[18-19].
双 (α-呋喃甲酸)氧钒(BFOV,图 1)为笔者项目组合成的一种新型钒配合物,它是以糠醛在人体内的代谢产物α-呋喃甲酸为配体的有机钒配合物,为非离子型配合物. 前期研究表明BFOV对四氧嘧啶和STZ诱导的1型糖尿病动物、高脂高糖+小剂量STZ诱导的2型糖尿病动物,均能明显降低其血糖、促进糖原合成和改善脂代谢紊乱,而且双(α-呋喃甲酸)氧钒的毒性明显低于国外正在临床试验的同类化合物 BEOV,且连续灌胃给予 20 mg·kg−1(有效剂量)后,大鼠出现毒副反应和钒在体内的积累明显低于BEOV,显示出一定的优越性[20-26].
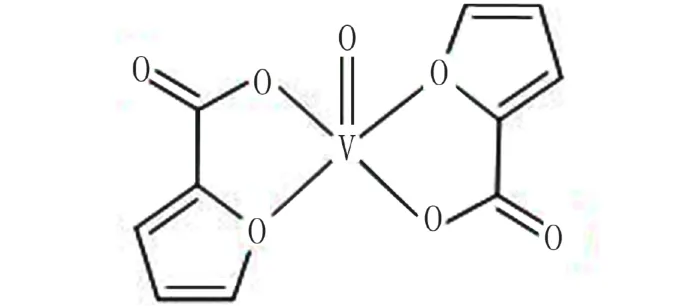
图 1 VO(C5H3O3)2(BFOV)的结构式Fig. 1 The structure of VO(C5H3O3)2 (BFOV)
基于双(α-呋喃甲酸)氧钒具有较好的水溶性和较低的毒副作用,我们在研究和评价其作为糖尿病药物的成药性时,开展了抗癌作用研究,并通过定量加入碳酸钡、检查反应终点和冷冻干燥除去溶剂(水)等手段对原来的合成方法进行改进,以提高产率和产品的纯度,满足生物学试验时静脉给药的要求. 本文将报告双(α-呋喃甲酸)氧钒合成的新方法、抗癌活性、特别是对顺铂耐药细胞株的活性以及对癌细胞的选择性和初步毒性.
1 实验部分
1.1 化学合成
1.1.1 仪 器 和 试 剂 紫 外 光 谱 用 岛 津 MPS 2 2000型紫外可见分光光度计测定. 核磁共振氢谱用BRUKER AM 2400超导核磁测定(四价钒为d1,属于顺磁性的化合物,会影响核磁测定,因此不采用核磁氢谱来解析其结构). 红外光谱用美国Nicolet 170 SXFT 2 IR 光谱仪测定,KBr压片法. 质谱用 VG AutoSpec 3000 质谱仪测定. 元素分析:C,H分析采用意大利Carlo 2 Erba1106型元素分析仪测定;V的含量采用经典的EDTA滴定法测定. 所有试剂均为市售A.R.级.
癌细胞株 A549、A549/DDP、SKOV3、SKOV3/DDP和肺正常上皮细胞株Beas-2B均购自美国ATCC. ICR 小鼠,雌雄各半,50 只,体重 18~22 g,由成都达硕实验动物有限公司提供,动物生产许可证号:SCXK(川)2008-24. AL204 电子天平:梅特勒−托利多仪器(上海)有限公司;GL-88B漩涡混合器:海门市其林贝尔仪器制造有限公司.
1.1.2 双(α-呋喃甲酸)氧钒的制备 称取 22.4 g(0.2 mol)α−呋喃甲酸,溶于 150 mL 水中,加入碳酸钡 (19.7 g, 0.1 mol),在 45 ℃ 下反应 5 h,得到无色的清亮溶液. 准确取储备的 1.0 mol/L VOSO4溶液102 mL(相当于 0.102 mol,过量 1%),与上述溶液在室温下混合并搅拌反应至用硫酸钠检查不到有游离的钡离子存在为止,这步反应一般需要3~4 h.过滤除去生成BaSO4,母液冷冻干燥得到绿色的双 (α-呋喃甲酸)氧钒晶状粉末约 30 g,产率 93%.经元素分析、红外光谱、质谱鉴定符合确定的结构式 . UV-vis(H2O)λmax(nm): 243(л→л*), 767 (2T2g→2Eg); IR (KBr, cm−1)ν: 1 630 (νas, COO― ), 1 383(νs,COO― ), 996 (V= O), 557(V― O); FAB-MS (m/z):289 (M+); 元素分析(w)理论计算 VO (C5H3O3)2•2H2O: C 36.86%, H 0.01%, V 15.65%; 实测 C 36.92%,H 0.03%, V, 15.69%. 样品中残留的钡采用电感耦合等离子发射光谱法(ICP-AES)测定,质量分数为8.5 mg/kg.
1.2 生物活性试验
1.2.1 双(α-呋喃甲酸)氧钒的抗癌作用的测定 以水为溶媒、以顺铂(cisplatin)为阳性对照药品,采用标准MTT法测定双(α-呋喃甲酸)氧钒对人非小细胞肺癌细胞株A549和人卵巢癌细胞株SKOV3生长的抑制作用,平行测定3次,药物与癌细胞的作用时间分别为48 h和72 h. 计算药物抑制癌细胞生长的半数质量浓度IC50. 采用同样的试验方法,测定双(α-呋喃甲酸)氧钒对耐受顺铂的人非小细胞肺癌细胞株A549/DDP、人卵巢癌细胞株SKOV3/DDP生长的抑制作用.
1.2.2 双(α-呋喃甲酸)氧钒毒性的测定
(1)对人正常肺上皮细胞的毒性测定. 以水为溶媒、以顺铂(cisplatin)为阳性对照药品,采用标准MTT法测定双(α-呋喃甲酸)氧钒对人肺支气管上皮细胞Beas-2B生长的抑制作用,计算半数抑制浓度IC50,平行测定3次,药物与细胞的作用时间为 72 h.
(2)对小鼠的急性毒性测定. 选择健康的昆明小鼠50只,雄雌各一半,体重在18~22 g,随机分为 5组,每组10只,给药前动物禁食约8 h,双(α-呋喃甲酸)氧钒(BFOV)用5%葡萄糖溶液溶解,动物按0.2 mL/10 g体重进行小鼠尾静脉给药,给药后连续观察14 d动物的中毒反应和死亡情况,并计算药物的半致死量LD10、LD50.
另外,选择健康的昆明小鼠50只,雄雌各一半,体重在18~22 g,随机分为5组,每组10只,给药前动物禁食约8 h,顺铂(cisplatin)用生理盐水溶解,动物按0.2 mL/10 g体重进行小鼠尾静脉给药,给药后连续观察14 d动物的中毒反应和死亡情况,并计算药物的半致死量LD10、LD50.
2 结果与讨论
2.1 双(α-呋喃甲酸)氧钒的制备采用如 1.1所述的方法合成出双(α-呋喃甲酸)氧钒,因为钡离子注射给药对动物和人均具有高毒性. 与文献[26]相比,本合成过程中增加了对反应终点的观察和钡残留量的控制. 同时,采用冷冻干燥技术,在低温下将溶剂(水)升华除去,以避免采用减压蒸馏时过高的温度使部分钒氧化成+5价. 改进后,产品的产率和纯度均有所提高,产率由原先的81%提高到了93%,产品中钡的残留量小于10 mg/kg.
2.2 双(α-呋喃甲酸)氧钒的抗癌活性双(α-呋喃甲酸)氧钒和顺铂对人肺癌细胞株A549和人卵巢癌细胞株SKOV3的生长均有很好的抑制作用,且呈现良好的量效关系和时效关系. 如表1的结果所示,在两个作用时间下,BFOV对SKOV3的半数抑制质量浓度IC50均小于顺铂,对A549的IC50与顺铂相当. 特别是它对耐受顺铂的A549和SKOV3(耐药指数约3~4)有更高的抑制活性,72 h作用时间的 IC50分别是 1.19 μmol/L 和 0.29 μmol/L,可以完全对抗癌细胞对顺铂耐药,结果显示可能存在与顺铂不一样的抗癌机制.
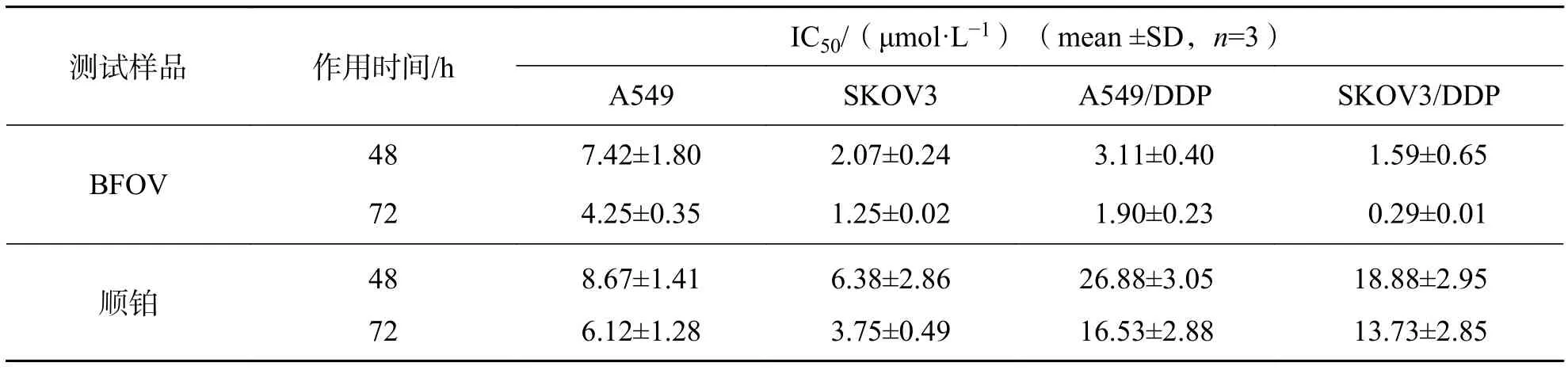
表 1 双(α-呋喃甲酸)氧钒(BFOV)抑制癌细胞生长的 IC50Tab. 1 The IC50 of bis (α-furanoic acid) vanadyl (BFOV) inhibiting cancer cell growth
2.3 双(α-呋喃甲酸)氧钒对肺癌细胞和正常肺细胞之间的选择性表2为双(α-呋喃甲酸)氧钒(BFOV)和顺铂对人肺正常上皮细胞(Beas-2B)生长的影响,BFOV和顺铂与Beas-2B作用72 h后半数浓度IC50分别为16.0 μmol/L 和2.61 μmol/L,BFOV对正常细胞的毒性小于顺铂,比较与对癌细胞的IC50可知,BFOV对癌细胞具有一定的选择性.

表 2 双(α-呋喃甲酸)氧钒(BFOV)抑制正常肺细胞生长的 IC50(t =72 h,n =3)Tab. 2 The IC50 of bis (α-furanoic acid) vanadyl (BFOV) inhibiting the growth of normal lung cells (t =72 h, n =3)
2.4 双(α-呋喃甲酸)氧钒的急性毒性表 3 为采用常规方法测定的双(α-呋喃甲酸)氧钒和顺铂对小鼠的急性毒性数据,从LD10和LD50数据来看,BFOV 的数据分别为 17.1 mg/kg 和 22.3 mg/kg,这两组数据分别均大于顺铂的对应值,说明静脉注射给药双(α-呋喃甲酸)氧钒的急性毒性小于顺铂.

表 3 双(α-呋喃甲酸)氧钒(BFOV)急性毒性Tab. 3 Acute toxicity of bis (α-furanoic acid) vanadyl (BFOV)
3 结论
本文提出了改进的双(α-呋喃甲酸)氧钒的合成方法,具有产率高且产品纯度好的优点. 双(α-呋喃甲酸)氧钒对人肺癌细胞A549和人卵巢癌细胞SKOV3有很强的抑制作用,对人卵巢癌SKOV3的抑制活性,明显高于顺铂,并且对耐受顺铂的肺癌细胞(A549/DDP)和卵巢癌细胞(SKOV3/DPP)也具有高的抑制活性. 同时,它对人正常细胞(Beas-2B)的毒性和对小鼠的急性毒性均小于顺铂,显示出一定的应用前景. 目前,双 (α-呋喃甲酸)氧钒作为抗癌药物的用途已获得国家发明专利授权(CN1035 99107B),下一步我们将在体内试验它的抗癌效果和研究其抗癌机制.

