CT引导下植入125I放射性粒子应用于胰腺癌治疗的临床价值研究*
1.重庆市巴南区人民医院放射科(重庆 401320)
2.陆军军医大学第一附属医院放射科(重庆 400038)
刘 颖1 冉林浩1 黄学全2,*
胰腺癌一种常见且恶性程度极高的消化道恶性肿瘤[1]。在我国,胰腺癌已成为我国人口死亡的十大恶性肿瘤之一[2-3]。多好发于41~70岁的中老年人,女性的发病率低于男性,但绝经后妇女的发病率与男性相仿[4]。胰腺癌的发生部位以胰头部位最为多见,约占70%。该病的病因尚未十分明确,但是首要的危险因素为吸烟,此处还有喝酒、高脂肪和高蛋白饮食、糖尿病、环境污染及遗传因素[5]。胰腺癌患者早期无明显症状,大多数患者就诊时已是进展期或晚期。患者晚期进行手术效果不佳,在放疗和化疗上的治疗效果也不是很理想,且预后较差[6]。目前对于胰腺癌的治疗,缺乏有效的治疗手段。放射性粒子植入是近年来临床医学上治疗恶性肿瘤的有效方法之一。在CT的引导下将放射性粒子直接放置在肿瘤内部,通过这些粒子在肿瘤内部发出的射线,达到杀死肿瘤细胞、截断肿瘤细胞扩散途径的目的。因此,本研究主要对CT引导下植入125I放射性粒子应用于胰腺癌治疗的临床价值进行了探究,现报道如下。
1 资料与方法
1.1 一般资料 选取本院2018年3月至2019年3月收治的60例胰腺癌患者,所有患者均经手术病理检查证实为胰腺癌。其中男性患者40例,女性患者20例;年龄40~80岁,平均年龄(50.48±9.08)岁。采用UICC肿瘤分期标准[7]进行分期,其中Ⅱ期20例,Ⅲ期21例,Ⅳ期19例。23例患者因腰腹部疼痛就诊,19例患者因腹部包块就诊,18例患者因其他原因就诊。
纳入标准:无其他严重疾病;肝肾功能正常;体内未安装心脏起搏器;无碘试剂过敏史;影像学资料和病理资料完整;无法手术切除或不愿意手术的患者;具有较好的依从性。
排除标准:有精神疾病或心血管疾病患者;患者未签署知情同意书;拒绝检查或未完成相关检查的患者;患有严重糖尿病患者。

表1 患者术前术后KPS积分变化[%(n)]
1.2 方法 仪器选用西门子16排螺旋CT和Pinpoint 穿刺引导系统。首先对患者进行CT扫描,患者平躺于扫描床,选取仰卧位。扫描完成后将图像传送到放射性粒子计算机治疗计划系统,进行三维立体数字化影像重组,勾画靶区。术前叮嘱患者前一天不要进食,术前12h口服导泻药。体表定位后,患者体位绝对要保持固定不变,保持自然呼吸状态,根据CT图像确定穿刺点后用标记笔标识。常规消毒铺巾,运用2%利多卡因进行局部麻醉。用注射针头再次CT扫描核实穿刺点位置和角度,根据注射针头导向角度和进针长度运用15cm或20cm长的18G穿刺针逐层进针到达靶部位。穿刺针远侧段到达肿块边缘5mm左右,释放第一粒粒子。按照治疗计划和布源设计路径,退针8~12mm再植粒子。操作完成后再次进行CT扫描确定粒子的位置。若扫描后显示粒子分布不均要及时补种。术后患者需要卧床休息且禁食不低于6h,并常规给予止血和抗生素治疗,治疗时间为2d。
1.3 观察指标 肿瘤疗效评估:患者术后3个月再进行CT复查,并采用WHO疗效评估标准。临床受益反应:采用KPS评分评价患者术前术后的生活质量,采用国际通用的数字分级法(NRS)评估患者术前术后的疼痛缓解程度。WHO疗效评估标准:CR(完全缓解),所有病灶均消失;PR(部分缓解),各病灶最大径之和减少50%以上;NC(无变化),各病灶最大两直径乘积之总和增大小于25%或减少小于50%;PD(进展),病灶最大径之和超过25%或有新病灶出现。NRS:0~10代表不痛程度的疼痛,0为无痛,1~3级为轻度疼痛,4~6级为中度疼痛,7~10级为重度疼痛。

图1 典型胰腺癌患者CT扫描图。1A:胰腺癌发生部位位于体尾部;1B:通过CT引导下穿刺针准确到达胰腺体尾部肿瘤内;1C患者术后CT增强扫描显示肿块明显变小,粒子聚集。
1.4 统计学方法 数据均采用SPSS 18.0软件进行统计分析,计数资料以百分率或构成比表示,并采用χ2检验;以P<0.05为差异具有统计学意义。
2 结 果
2.1 患者术前术后KPS积分变化 由表1可知,术后患者在营养、精神状态、睡眠时间等方面与术前相比明显改善,生活质量显著提高,与术前相比较差异有统计学意义(P<0.05)。
2.2 患者术前术后疼痛缓解情况 术后患者顽固性疼痛症状缓解明显,平均术后2~5d疼痛开始缓解。由表2可知,术前重度疼痛患者有29例,术后重度疼痛患者只有11例,与术前相比明显减少且比较差异有统计学意义(P<0.05)。
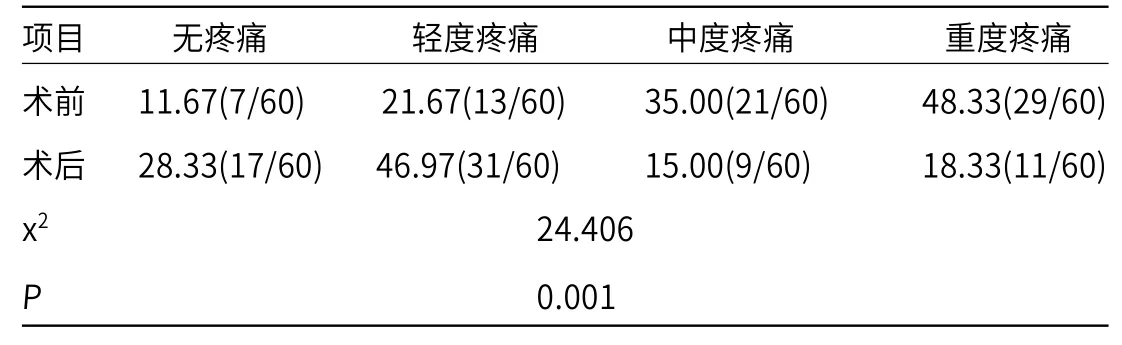
表2 患者术前术后疼痛缓解情况[%(n)]
2.3 治疗肿瘤效果 所有病例中完全缓解有11例,部分缓解有26例,无变化有15例,进展有8例。总有效率为61.66%,其中有7例患者因病情恶化死亡,4例患者因病灶全身多处转移死亡。典型病例患者,男性,72岁,粒子植入后3个月进行CT复查。
3 讨 论
胰腺癌作为消化道常见的恶性肿瘤,5年来生存率不超过1%,是预后最差的恶性肿瘤之一[8]。胰腺癌早期无明显症状,出现以上临床表现时大多数已经属于晚期,晚期患者通过手术切除得到根治的几率很低,治疗效果不佳[9]。近年来,CT引导下植入125I放射性粒子治疗肿瘤的方法得到广泛应用。
放射性粒子植入治疗肿瘤是指通过影像学引导技术将具有放射性的核素直接植入到肿瘤靶体积内或肿瘤周围,包括恶性肿瘤沿淋巴途径扩散的组织,通过放射性粒子源发出持续低能量的γ射线,使肿瘤组织遭受最大程度的辐射损伤和破坏,而正常组织不受损伤或仅受轻微损伤,达到治疗肿瘤的目的。125I放射性粒子持续低剂量率辐射,对周围正常组织没有损害,幅射距离短,对医生和家属也没有损害[10]。125I持续24h不停地杀灭肿瘤细胞,粒子作用时间长,可以长达180d。放射性粒子是一种微型粒子且是钛合金封装的,不会产生放射泄漏及治疗路径的污染,局部控制率高[11-12]。放射诱使肿瘤缩小,125I粒子密集,局部剂量自然增加,持续低剂量放疗,可改进肿瘤局部乏氧[13]。
近年来,有不少临床研究表明,放射性粒子植入治疗是一种安全且有效的治疗方法,对周围正常组织和脏器无明显损伤、患者全身也无明显不适反应等优点,是治疗恶性肿瘤的重要方法之一[14]。本研究中,60例胰腺癌患者,全部在CT引导下,植入125I放射性粒子进行治疗,结果显示,近期总有效率为61.66%,疼痛缓解的有效率达80.00%,且术后未出现严重的并发症。此外,在CT引导下植入125I放射性粒子的治疗需要注意:患者术前一天就要开始禁食,且术前12h要口服导泻药;术前对患者进行呼吸训练,在植入过程中保持自然呼吸状态,避免穿刺点出现差错;术前24h服用适量生长抑素,抑制胰液分泌,减少并发症的发生[15];在穿刺位置方面,原则上是不能穿过结肠,其中穿刺经胃是比经结肠安全的,经小肠穿刺也比经结肠安全;当出现黄疸时,首先要通过相应方法缓解黄疸症状,再植入125I放射性粒子进行治疗;利用CT检查明确胰腺肿块的正确位置、大小及其与周围血管的关系,确定进针的方向和深度;粒子植入后再马上进行CT扫描验证粒子分布是否均匀,必要时补充粒子,尽可能地减少靶面积的缺失。
综上所述,CT引导下植入125I放射性粒子治疗胰腺癌是安全可靠、有效、可重复的治疗,能够有效抑制肿瘤的生长和缓解患者疼痛,提高患者生活质量,值得广泛应用。

