PD-1/PD-L1免疫检查点抑制剂治疗不同BRAF基因型晚期结直肠癌的临床效果与安全性
章海斌,丁晓娇,王练,王子安
结直肠癌(CRC)是一种能够严重破坏人们身体健康的恶性肿瘤,且近些年患CRC的人数越来越多,因此结直肠癌已经成为一种常见的疾病。我国CRC的发病率与病死率均为世界最高且仍不断增长,其中我国CRC发病例数占全世界发病例数的18.6%,病死例数占全世界病死例数的20.1%[1]。随着精准治疗相关研究的进一步深入,研究者发现,Ras-Raf-MEK-ERK通路在CRC发生发展中起着重要调控作用,其中KRAS、NRAS及BRAF是该通路的重要组成部分,对细胞增殖、分化、基因表达、有丝分裂及细胞凋亡起调控作用[2]。其中BRAF基因位于7q34,长约190 kb,在绝大多数组织和细胞类型中,BRAF是MEK/ERK最为关键的激活因子。BRAF中起到重要作用的是有丝氨酸激酶通路中的丝氨酸—苏氨酸蛋白激酶,丝氨酸—苏氨酸蛋白激酶能够通过信号传导来调控细胞的生长、分化及凋亡[3]。对于具有MSI-H转移性的CRC来讲,在对该病症进行诊断和治疗时需要用到免疫检查点抑制剂,通过在实验室所进行的科学检验并对相关的临床表现进行大量的分析与总结,发现与程序性死亡蛋白受体-1相关的这类药物的效果明显。在经过大量的研究后发现PD-L1的表达与BRAF突变呈正相关,以及CD8+肿瘤浸润淋巴细胞在 BRAF突变的CRC中的表达率较高[4]。说明了免疫治疗方法能够有效治疗携带BRAF突变的CRC患者。本研究观察PD-1/PD-L1免疫检查点抑制剂用于不同BRAF基因型晚期CRC治疗的临床效果与安全性,现总结报道如下。
1 资料与方法
1.1 临床资料 回顾性分析2019年6月-2020年6月蚌埠医学院第一附属医院收治的CRC晚期接受PD-1/PD-L1单药免疫治疗患者57例的临床资料。纳入标准:(1)均为BRAF突变CRC晚期确诊患者,TNM分期为ⅢB期或Ⅳ期;(2)患者接受PD-1/PD-L1单药免疫治疗后所表现出的临床反应具有评价性;(3)患者预计生存期>3个月;(4)已接受BRAF突变基因检测;(5)存在可评估病灶。根据患者基因检测结果分为BRAF突变组(29例)和BRAF野生组(28例)。2组患者性别、年龄、ECOG评分、分期及转移部位等资料比较差异均无统计学意义(P>0.05),具有可比性。见表1。
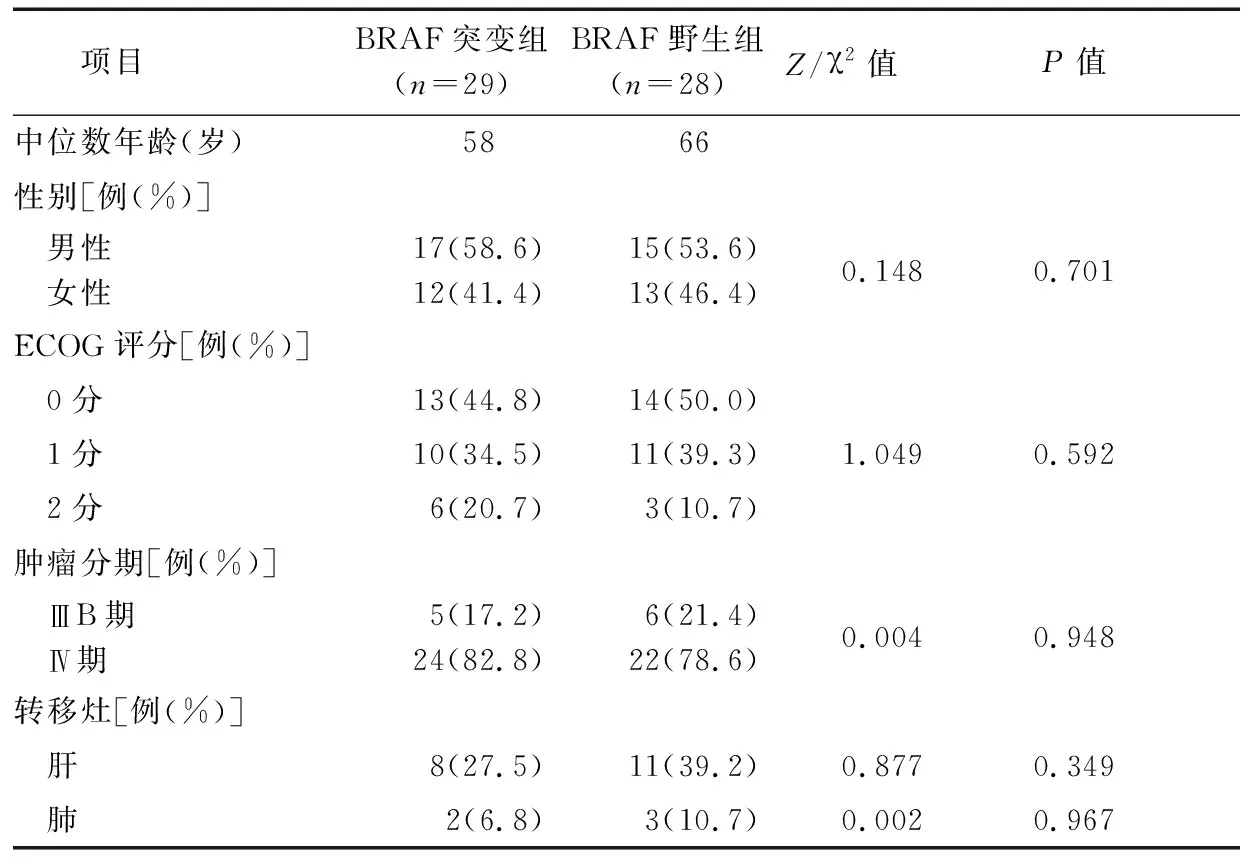
表1 2组晚期CRC患者PD-1/PD-L1免疫治疗基线特征比较
1.2 治疗方法 2组患者均予注射用卡瑞利珠单抗(苏州盛迪亚生物医药有限公司生产,国药准字S20190027)200 mg静脉注射,每次持续60 min,每2周1次,治疗周期时长为4周,每2个治疗周期进行1次疗效评价,持续至患者病情好转或难以耐受治疗。
1.3 观察指标与疗效评定标准 (1)近期疗效:于患者治疗前及每2个治疗周期后行影像学检查,参照实体瘤近期疗效评价(RECIST)对患者近期疗效进行评估,其中完全缓解(CR):可见的肿瘤病变完全消失,维持>4周;部分缓解(PR):肿瘤病灶的最大直径及其最大垂直横经的乘积缩小≥50%,其他病灶无增大,无新病灶出现,维持>4周;稳定(SD):肿瘤病灶的最大直径及其最大垂直横经的乘积缩小<50%,或增大≤25%,无新病灶出现,维持>4周;进展(PD):肿瘤病灶的最大直径及其最大垂直横经的乘积增大>25% 或新病灶出现。计算客观缓解率(ORR)与疾病控制率(DCR)。其中ORR=(CR+PR)/总例数×100%;DCR=(CR+PR+SD)/总例数×100%。(2)无进展生存期(PFS)。(3)不良反应:包括反应性毛细血管增生症、免疫性肺炎、免疫性肝炎、免疫性结肠炎、甲状腺功能减退等。
1.4 统计学方法 采用SPSS 22.0软件对数据进行统计分析。分类变量以频数/率(%)表示;连续变量以中位数形式表示;组间数据比较采用Wilcoxon秩和检验和χ2检验。无进展生存期数据分析采用Log-rank检验和Kaplan-Meier生存曲线法。双侧 α=0.05为统计学分析检验水准。
2 结 果
2.1 2组近期疗效比较 BRAF突变组ORR为27.6%、DCR为69.0%,BRAF野生组ORR为21.4%、DCR为53.5%,2组比较差异均无统计学意义(P>0.05)。见表2。
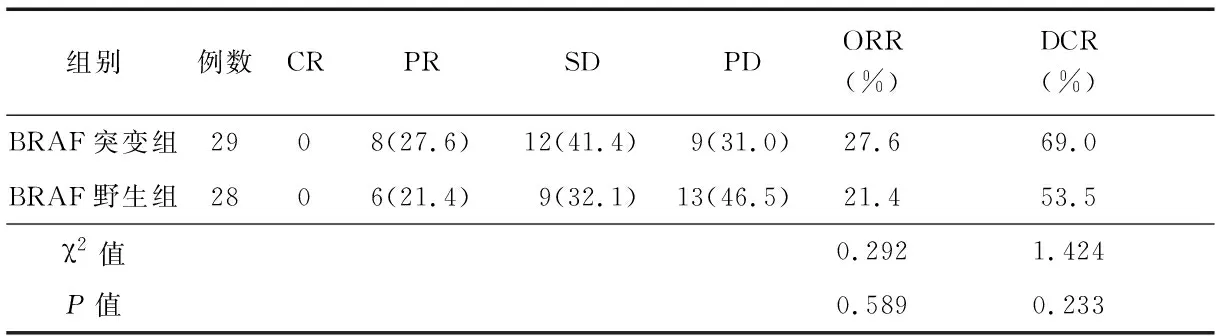
表2 2组患者近期疗效比较 [例(%)]
2.2 无进展生存期比较 BRAF突变患者中位PFS为4.2个月,BRAF野生组患者中位PFS为6.65个月,2组比较差异无统计学意义(P>0.05)。见图1。

图1 2组PFS的Kaplan-Meier生存曲线比较
2.3 不良反应比较 2组患者出现如反应性毛细血管增生症、免疫相关的肺、肝与结肠炎及甲状腺功能减退等不良反应,其中反应性毛细血管增生症发生率最高,且以1~2级为主,患者多可耐受。2组患者各级不良反应总发生率比较差异均无统计学意义(P>0.05)。见表3。
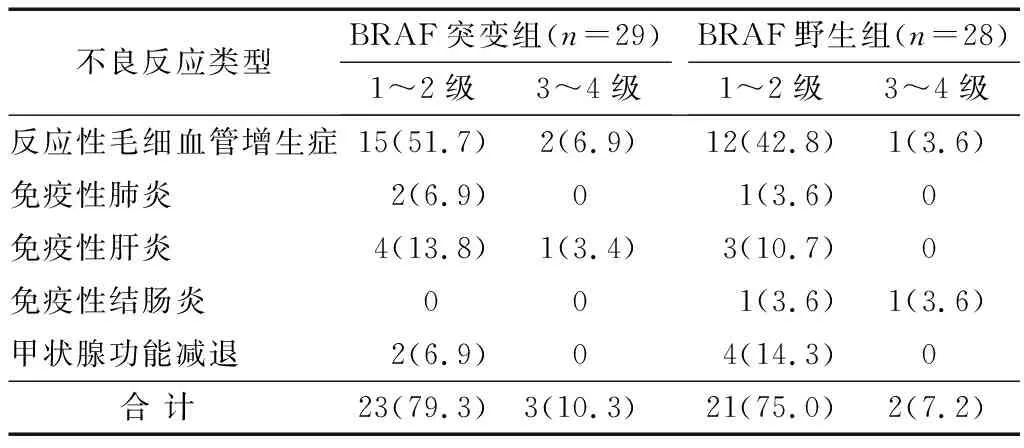
表3 2组患者不良反应比较 [例(%)]
3 讨 论
近年来,随着精准医疗的发展,BRAF突变的CRC治疗策略引起更多关注和思考,并且现如今在CRC的临床治疗上也将EGFR基因定为主要靶点。而且大量的实验得出BRAF突变与出现EGFR药物抵抗直接相关。对于BRAF突变型CRC患者,EGFR靶向抑制剂帕尼单抗和西妥昔单抗治疗效果差,且预后不良[5]。本研究旨在分析BRAF突变型CRC晚期患者在使用免疫检查点抑制剂单药方案治疗后的病情是否得到缓解及此治疗方案的安全性能否得到保证,这不仅有助于BRAF突变型CRC晚期患者的临床治疗,更可通过本研究印证晚期CRC患者免疫治疗的疗效及安全性稳定且不受BRAF表达状态的影响。
在CRC患者中,BRAF突变见占8%~10%。携带BRAF突变者常与MSI密切相关,预后差,且发病时肿瘤的分期无关。PETACC-3所研究的对象都是一些处于Ⅱ期或Ⅲ期的CRC患者,且在3 278例患者中选取1 403例患者来进行肿瘤组织的相关基因检测。对相关基因检测结果进行分析得出,当CRC患者的肿瘤组织的相关基因中所突变的基因是BRAF基因时,如在微卫星稳定(MSS)的CRC中,CRC患者的OS时间相对较短[6]。对此进行相关的研究,结果发现对于CRC患者,出现远处转移的分组中,携带BRAF突变型中位OS时间较BRAF野生型相比,BRAF野生型的OS时间几乎是携带BRAF突变型中位OS时间的2倍[7]。在MSS的CRC中,CRC患者如果携带来BRAF突变基因,就会有更高的癌症特异性死亡风险(HR=2.3,95%CI:1.3~4.0)。且有研究指出如患者为携带BRAF突变基因且微卫星高度不稳定的转移性CRC,则此类患者在进行一线化疗(以5-FU为基础的一线治疗,联合或不联合单克隆抗体)后,不仅患者的OS时间(14个月∶30个月,P<0.001)会大幅度缩短,且患者的无进展生存时间(3个月∶10个月,P<0.001)也会大幅度[8]。故当CRC患者到达晚期后,微卫星状态并不是影响患者预后的独立危险因素,而影响预后的独立危险因素是BRAF突变。这就意味着晚期CRC患者BRAF突变状态是影响治疗结果的重要因素。
程序性死亡受体-1(PD-1)是免疫抑制分子,当PD-1与它的配体PD-L1结合就能够启动T细胞的程序性死亡,这样就会使肿瘤细胞获得免疫逃逸。对CRC患者进行研究发现,表达为MSI-H型的CRC患者占全部患者的17%。而在表达为MSI-H型的CRC患者中,因为错配修复基因(MMR)胚系突变而导致患者表达为MSI-H型的CRC患者占25%,75%是由BRAF突变造成的[9]。Sergia等在CRC的研究中发现,MSI组的BRAF突变率为28%,而MSS组的BRAF突变率为7.5%,并且得出结论:MSS与MSI组CRC患者相比,MSS组CRC更难发生BRAF突变。BRAF野生型患者同时存在MSI-H表型的概率约为8%,而BRAF-mt CRC患者同时存在MSI-H表型的概率约为20%,由此可以看出抗PD-1/PD-L1治疗能使BFAF突变患者获益[10]。2018年NCCN指南推荐PD-1抑制剂纳武单抗和帕姆单抗可用于治疗转移性或不可切除的MSI-H型晚期CRC。现已被美国FDA批准应用于各类表现为MSI-H的恶性肿瘤[11]。患者普遍对免疫相关药物不会产生强烈的不良反应[12]。Brahmer等[13]进行了一项Ⅰ期临床试验(NCT00441337),旨在评估Nivolumab的安全性、耐受性、疗效和药代动力学特征。在39例研究对象中有14例是转移性BRAF突变型CRC患者,并且对这14例患者采取递增剂量治疗方式。在治疗过程中,多次使用均未发现致命性不良反应,患者耐受性良好。另一项多队列Ⅰb期临床试验对Pembrolizumab进行了安全性评估[14]。该研究收集了23例PD-L1阳性的CRC晚期患者的病例资料,并且这些患者的治疗方式为Pembrolizumab治疗,最后对患者进行疗效评估。观察发现有8例研究对象出现口腔炎及疲乏等轻度不良反应但无死亡病例。现已进入临床研究阶段。卡瑞利珠单抗是国产的重组人源化抗PD-1单抗,能够很好地用于霍奇金淋巴瘤的免疫治疗,也能够用于其他多种实体肿瘤的免疫治疗,希望在未来卡瑞利珠能够应用于肿瘤患者的临床治疗。
本研究通过回顾性分析临床实际患者病例数据来了解BRAF突变的转移性CRC患者以及野生型CRC晚期患者在使用免疫检查点抑制剂单药方案治疗后的病情是否得到缓解,以及这种治疗方案的安全性能否得到保证。研究结果表明PD-1/PD-L1免疫检查点抑制剂能够治疗BRAF突变型CRC晚期患者。但考虑到本研究为单中心回顾性分析研究,样本量较小,故研究数据与结果可能会受到影响而产生一定偏差,有待未来进一步开展大样本量的深入研究和求证。
综上所述,PD-1/PD-L1免疫检查点抑制剂用于不同BRAF基因型晚期CRC治疗的临床效果与安全性均值得肯定,值得临床进一步研究和推广应用。

