IL-PELD与MED治疗非极外侧型腰5/骶1椎间盘突出症的临床研究
刘佐忠,黄黎黎△,邵高海,李 波,屈一鸣,邓忠良
(1.重庆医科大学附属永川医院骨科 402160;2.重庆医科大学附属第二医院 400010)
腰椎间盘突出症(lumbar discherniation,LDH)是脊柱外科最为常见的疾病之一,约10%~18%[1]的患者需要手术治疗,目前经皮椎间孔镜下腰椎间盘髓核摘除术(percutaneous endoscopic lumber discectomy,PELD)及经后路显微内窥镜下腰椎间盘髓核摘除术(microendoscopic discectomy,MED)是治疗LDH最为微创的方式,也是临床上使用最为广泛的微创技术[2]。因高髂嵴、腰5横突肥大等原因,腰5/骶1椎间盘突出症通常经椎板间入路椎间孔镜(interlaminar percutaneous endoscopic lumber discectomy,IL-PELD)操作较为安全、方便。目前IL-PELD与MED在治疗非极外侧型腰5/骶1椎间盘突出症的临床疗效对照研究国内外报道较少。本研究将2016年10月至2018年12月永川医院骨科收治入院的非极外侧型腰5/骶1椎间盘突出症患者采用随机数字表法分为IL-PELD组与MED组,对临床疗效进行对照分析,为手术方式的选择提供参考。
1 资料与方法
1.1 一般资料
将62例单节段非极外侧型腰5/骶1椎间盘突出症患者,采用随机数字表法分为IL-PELD组(n=31)与MED组(n=31)。IL-PELD组男18例,女13例,平均年龄(42.6±5.4)岁;MED组男17例,女14例,平均年龄(43.8±5.2)岁。所有患者术前均行腰椎正侧位、动力位X线片,腰椎CT及MR检查。一般资料见表1。

表1患者的一般资料
1.2 纳入与排除标准
纳入标准:(1)非极外侧型腰5/骶1椎间盘突出症;(2)严格保守治疗3个月无效;(3)腰痛伴单侧下肢疼痛、麻木;(4)既往同节段无手术史;(5)年龄18~60岁。排除标准:(1)腰5/骶1椎间盘突出伴钙化;(2)复发性腰5/骶1椎间盘突出症;(3)合并腰椎失稳、椎管狭窄;(4)多节段椎间盘突出;(5)术前存在血液系统疾病等手术禁忌证。
1.3 手术方法
1.3.1IL-PELD组
患者取俯卧位,于胸前、腋下、腹股沟平面垫枕。手术床折叠成弓形,充分张开椎板间隙,C型臂透视定位腰5/骶1间隙进针点并标记,常规消毒铺巾,使用1%利多卡因于标记点开始对皮肤、深筋膜、腰5/骶1关节突内缘、黄韧带表面逐层麻醉。穿刺针穿刺透视定位满意后,退出针芯,置入导丝,以导丝为中心在皮肤做约0.8 cm切口,切开皮肤及深筋膜,沿导丝旋转置入扩张管道,安装工作通道。工作通道舌尖抵在腰5下关节突内缘黄韧带表面,退出扩张管道,置入内窥镜。射频电刀清理黄韧带表面的软组织并止血,用蓝钳咬开黄韧带。工作通道舌尖经破口处旋转进入椎管,在水压下辨别硬脊膜、神经根及突出的椎间盘组织,旋转工作通道,向内侧挤开神经根,显露突出椎间盘,摘除突出髓核组织。调整工作通道,于神经根肩部、腋部、硬膜囊腹侧探查是否存在突出、游离的髓核。减压完成后骶1神经根松弛、无卡压,射频电刀行纤维环成形、止血,确认无出血后,退出工作通道,缝合1针。
1.3.2MED组
患者气管插管+全身麻醉后,俯卧于手术床上,于胸前、腋下、腹股沟平面垫枕,使腹部悬空。C型臂透视定位腰5/骶1间隙进针点并做标记,术区消毒铺巾,标记处插入1.5 mm克氏针并固定,再次透视确定节段无误后,以克氏针为中心切开皮肤约2.0 cm,分离皮下、筋膜及肌肉至关节突周围。在克氏针引导下植入逐级扩张管道,最后安置工作通道并固定,连接显示器。清除视野内血凝块及肌肉组织,显露腰5椎板下缘,使用咬骨钳咬除腰5部分椎板下缘及骶1上关节突部分内缘,剔除黄韧带;显露骶1神经根及硬膜囊,神经剥离子上下分离椎管内的粘连后将神经根牵向对侧;显露前方的突出椎间盘,切除前方的髓核组织。探查骶1神经根松弛、未发现压迫。使用生理盐水冲洗切口并彻底止血,明胶海绵填塞,切口旁放置1根引流管,关闭切口,逐层缝合。
1.4 术后处理
两组患者术后24 h开始佩戴腰围下床活动,术后1个月避免久坐及剧烈活动,术后3个月内避免重体力劳动。
1.5 观察指标
比较两组患者手术时间、术中透视次数、术中失血量、切口大小、卧床时间、住院时间、术前VAS评分、术后VAS评分、ODI评分、JOA评分、并发症发生例数。
1.6 统计学处理
2 结 果
两组患者均顺利完成手术,无中转开放病例,所有患者均以门诊、微信或电话的方式至少随访12个月。IL-PELD手术时间、术中透视次数、并发症发生例数多于MED组(P<0.05),而术中失血量、术后卧床时间、住院时间少于MED组(P<0.05)。两组间末次随访腰痛及腿痛VAS评分(P腰痛=0.68、P腿痛=0.53)、JOA评分(P=0.86)、ODI评分(P=0.79)差异无统计学意义,见表2、3。
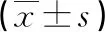
表2 IL-PELD组与MED组手术情况比较
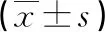
表3 IL-PELD组与MED组手术前后VAS、ODI、JOA评分比较
3 讨 论
由于高髂嵴、腰5横突肥大、腰5/骶1椎间孔狭窄、小关节增生等原因,腰5/骶1椎间盘突出症经椎间孔入路椎间孔镜下髓核摘除往往存在一定困难[3-4],2009年CHOI等[5]报道经髂骨入路建立通道行腰5/骶1节段椎间盘突出髓核摘除,但其穿刺要求高,术中需反复透视定位,并且容易引起髂骨骨折、损伤髂骨周围的动静脉,临床推广难度较大。而腰5/骶1椎板间隙较宽,研究[6-7]发现其高度9.95~13.24 mm,宽度25.75 ~31.89 mm,椎间孔镜工作通道仅为7.5 mm,为行IL-PELD的天然解剖间隙。RUETTEN等[8]和CHOI等[9]分别于2006年报道采用IL-LELD法行腰5/骶1节段腰椎间盘突出症近期临床效果良好。因IL-PELD经腰5/骶1椎板间隙进入,其操作入路与 MED相同,但在治疗非极外侧型腰5/骶1节段腰椎间盘突出症方面,哪种手术方式更具优势目前报道较少。本研究通过临床对照实验,分析两种手术方式在手术时间、术中出血量、VAS评分等方面的优缺点,为临床选择手术方式提供参考。
本研究中两组患者性别、年龄、病程、术前VAS评分、术前ODI评分、术前JOA评分差异无统计学意义(P>0.05),两组间一般资料具有齐同可比性。在术后1年的随访时间里,两组患者的腰痛及腿痛VAS评分、ODI评分、JOA评分较术前明显改善,并且两组间差异无统计学意义,表明两种手术方式均可取得良好的临床效果,与相关研究[10-12]报道一致。
然而在手术时间、术中透视次数方面,IL-PELD多于MED,差异有统计学意义(P<0.05),考虑主要原因为IL-PELD术中需要多次透视定位,术中操作空间较小(工作通道约7.5 mm),需要反复转动工作通道,查看神经根、硬膜囊与椎间盘的位置关系。并且年龄较大的患者,椎间盘退变往往较重,突出髓核组织呈小碎块状,髓核钳又小,需要多次夹取髓核碎片后才能达到神经根减压,导致整个手术所需时间较长。MED在行后路髓核摘除过程中,操作空间较大(工作通道约1.5 cm),视野开阔,即使是小碎块状的髓核组织也很容易取出。本研究结果与俞云龙等[11]报道一致。
在并发症方面,早期开展IL-PELD过程中出现2例硬脊膜破裂,未出现神经根损伤、术后感染、下肢肌力及感觉异常等并发症。在纳入研究的MED组患者术后均未出现并发症。在随访的1年时间里两组病例均未出现椎间盘突出症术后复发。术中硬脊膜破裂主要发生于剪开黄韧带的过程中,特别对于巨大的椎间盘突出,硬脊膜及神经根被顶向背侧,紧贴黄韧带,损伤的风险更大,术中需要逐层剪开黄韧带,在破开黄韧带后使用神经探勾向上下方适当的分离与硬脊膜之间的粘连,再经黄韧带破口处置入通道到达椎管。
在术中失血量、术后卧床、住院时间方面,IL-PELD优于MED组,考虑主要原因为MED需要切除部分腰5下关节突及骶1部分上关节突内缘,骨创面渗血,而IL-PELD不需要切除骨质或切除很少,并且水介质压力下可以起到止血的作用,故MED术中出血量较多。同时MED切除部分骨质,手术切口较长,伤口内创面较大,术后患者因疼痛等原因,故卧床及住院时间较长[13]。
在IL-PELD组中,3例中央型椎间盘突出患者,相对于旁中央型突出类型手术时间更长、出血量更多,虽然最终VAS评分、ODI评分及JOA评分差异无统计学意义,但是术后腰腿痛缓解更慢,恢复正常生活所需时间更久。CHEN等[14]认为与中央型椎间盘突出往往较大,而工作通道仅7.5 mm,很难到达椎管中央,突出的髓核取出困难有关。而MED则可以咬除较多的骨质,工作通道宽,视野广,减压相对更加充分[15]。但是在后期的随访过程中,MED的腰痛VAS评分更高,考虑与术中过多咬除骨质,腰椎失稳、退变有关。
IL-PELD与MED治疗非极外侧型腰5/骶1椎间盘突出症均可取得满意的临床效果,但是IL-PELD出血量更少、创伤更小、术后卧床及住院时间更短,退变不严重的非极外侧腰5/骶1椎间盘突出值得推荐。而MED术中出血量、透视次数更少,对于中央型椎间盘突出及退变严重的巨大非极外侧腰5/骶1椎间盘突出值得推荐。MED术中尽量少切除关节突关节,减少远期腰痛的发生。应术前充分评估,选择恰当的手术方案,达到最佳治疗效果。

